hemijski element sa simbolom Pu i atomskim brojem 94 From Wikipedia, the free encyclopedia
Plutonij je hemijski element sa simbolom Pu i atomskim brojem 94. U periodnom sistemu on se nalazi u grupi aktinoida (7. perioda, f-blok) i ubraja se u tranuranijske elemente. Plutonij je vrlo otrovni, radioaktivni teški metal. Dobio je ime po patuljastoj planeti Plutonu. Prema svom rednom broju, on je najteži element koji se nalazi u prirodi. Međutim, u prirodi se nalazi samo u tragovima unutar veoma starih stijena. Veće količine ovog elementa dobijaju se vještački, pretežno u atomskim centralama i reaktorima. Kao jedan od malobrojnih hemijskih elemenata podložnih fisiji, igra veoma važnu ulogu za proizvodnju nuklearnog oružja. Naprimjer, osnovni reaktivni materijal u atomskoj bombi bačenoj 9. augusta 1945. na Nagasaki bio je plutonij. Ovaj element nastaje tokom rada nuklearnih reaktora iz uranijskih šipki nuklearnog goriva.
 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Plutonij u periodnom sistemu | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Hemijski element, Simbol, Atomski broj | Plutonij, Pu, 94 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Serija | Aktinoidi | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Grupa, Perioda, Blok | Ac, 7, f | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Izgled | srebrenasti metal | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Zastupljenost | 2 · 10−20[1] % | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Atomske osobine | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Atomska masa | 244,0642 u | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Atomski radijus (izračunat) | 151 (-) pm | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Kovalentni radijus | 187 pm | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Van der Waalsov radijus | - pm | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Elektronska konfiguracija | [Rn] 5f67s2 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Broj elektrona u energetskom nivou | 2, 8, 18, 32, 24, 8, 2 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 1. energija ionizacije | 584,7 kJ/mol | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Fizikalne osobine | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Agregatno stanje | čvrsto | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Kristalna struktura | monoklinska | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Gustoća | 19816 kg/m3 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Magnetizam | paramagnetičan ( = 6,2 · 10−4)[2] | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Tačka topljenja | 912,5 K (639,4 °C) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Tačka ključanja | 3509 K (3230 °C) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Molarni volumen | 12,29 · 10-6 m3/mol | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Toplota isparavanja | 325 kJ/mol | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Toplota topljenja | 11,48[1] kJ/mol | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Brzina zvuka | 2260 m/s pri 293,15 K | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Specifična toplota | 130 J/(kg · K) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Specifična električna provodljivost | 6,8 · 105 S/m pri 293 K | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Toplotna provodljivost | 6,74[1] W/(m · K) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Hemijske osobine | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Oksidacioni broj | 3, 4, 5, 6, (7) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Elektrodni potencijal | −2,031 V (Pu3+ + 3e− → Pu) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Elektronegativnost | 1,28 (Pauling-skala) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Izotopi | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Sigurnosno obavještenje | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Oznake upozorenja
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Obavještenja o riziku i sigurnosti | R: / S: / | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Ostala upozorenja | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Radioaktivnost | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
 Radioaktivni element | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Ako je moguće i u upotrebi, koriste se osnovne SI jedinice. Ako nije drugačije označeno, svi podaci dobijeni su mjerenjima u normalnim uvjetima. | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||

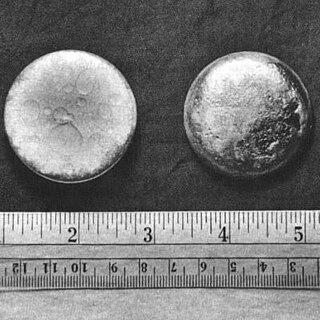
Plutonij su otkrili američki naučnici Glenn T. Seaborg, J. W. Kennedy, E. M. McMillan, Michael Cefola i Arthur Wahl. Oni su 14. decembra 1940. izveli eksperiment u ciklotronu, bombardirajući metu od uranija 238U atomima deuterija dobivši tako izotop 238Pu. Pri tom eksperimentu, najprije je napravljen uzorak 238U u obliku oksida U3O8 u tankom sloju na ploči od bakra. U ovoj reakciji emitirana su dva neutrona. U kratkom međuvremenu, nastao je neptunij kao međuproizvod a koji se odmah raspao na 238Pu. Nedvosmisleni dokaz o dobijanju elementa 94 dao je Arthur Wahl 23/24. februara 1941. godine.[4][5]
Drugi izotop plutonija dobijen je bombardovanjem brzim neutronima:
Novootkrivenom elementu dali su ime u martu 1942. godine po, u to vrijeme, najudaljenjenijoj otkrivenoj planeti Plutonu, a koji je opet dobio ime po istoimenom božanstvu iz rimske mitologije: ...nazvan po planeti koja slijedi nakon Neptuna, a u aspektu užasavajućeg djelovanja plutonijske atomske bombe daleko više mu odgovara izvođenje iz imena Plutona, božanstva podzemlja.[6] Prema tome, tri dotad najteža poznata elementa, uranij, neptunij i plutonij dobili su imena prema istoimenim planetama: Uranu, Neptunu i Plutonu. Prva mjerljiva količina plutonija od oko 4 µg dobijena je u augustu/septembru 1942. kada ga je izolirala grupa naučnika Burris B. Cunningham, Michael Cefola i Louis B. Werner.[7] Otkriće je držano u tajnosti tokom Drugog svjetskog rata. Sa prvom proizvodnjom plutonija u većem obimu otpočelo se u okvirima američkog projekta "Manhattan". Prva eksplozija atomske bombe kojoj je svjedočilo čovječanstvo bio je test "Trinity", čija je osnova bio plutonij 239Pu, kao i za bombu Debeljko (engleski: Fat Man) koja je u augustu 1945. razorila japanski grad Nagasaki. Joseph Hamilton je izvodio testove na dobrovoljcima, davajući im plutonij, a zbog ogromne otrovnosti ovog elementa danas su takvi testovi zabranjeni.
Čak i prije otkrića plutonija, u Njemačkoj je Carl Friedrich von Weizsäcker nagovijestio da je u nuklearnim reaktorima moguć nastanak novog elementa eka-renija (tj. 239Eka Re).[8] Osim njega, Friedrich Georg Houtermans je također 1942. predvidio postojanje teoretsko postojanje nekog transuranijskog elementa u svom tajnom izvještaju. Međutim u okvirima nacističkog uranijskog projekta, prema današnjim saznanjima, do kraja Drugog svjetskog rata nije došlo do sinteze plutonija.[9]
Pri normalnim uslovima temperature i pritiska, plutonij je srebrenasto-sjajni teški metal, veoma velike gustoće (19,86 g/cm3[10]). Kao i svi aktinoidi, on također postoji samo u vidu radioaktivnih izotopa. On se zagrijava sam od sebe, tako da naprimjer 100 grama plutonija emitira oko 0,2 vata toplote (odnosi se na izotop 239Pu).[11] U poređenju s drugim metalima, plutonij je vrlo slab provodnik toplote i električne struje. Metal se kristalizira nezavisno od temperature u ukupno šest alotropskih modifikacija. One se jednim dijelom znatno razlikuju po svojoj gustoći. Na sobnoj temperaturi stabilna modifikacija α-Pu je monoklinska. Kod plutonija pri višim temperaturama javlja se vrlo rijedak slučaj anomalije gustoće, jer ona raste pri prelasku iz δ' modifikacije u ε modifikaciju. Pri njegovom topljenju, slično kao kod vode, gustoća mu raste.[12] Istopljeni plutonij ima najvišu viskoznost od svih elemenata u tečnom stanju.[13] Međutim, i pored neuobičajeno visoke magnetne susceptibilnosti za metale i tendencije usmjeravanju pri niskim temperaturama, plutonij ne pokazuje usmjeravanje u širokim rasponima temperature pa se stoga treba svrstavati kao paramagnetičan.[12] Ipak, tačna mjerenja ometa stalno odavanje toplote uzrokovano radioaktivnim raspadom plutonija 239Pu. Iz istog razloga nemoguće je postići temperature plutonija bliske apsolutnoj nuli.
| Opis faze |
Stabilan u temperaturnom području |
Gustoća (temperatura) | Kristalni sistem | Bravaisova rešetka | Prostorna grupa |
|---|---|---|---|---|---|
| α-Pu[14] | 0 K – 395 K | 19,77 g/cm3 (293 K) | monoklinski | primitivna | P21/m (br. 11) |
| β-Pu[15] | 395 K – 479 K | 17,7 g/cm3 (395 K) | monoklinski | centrirana po bazi | I2/m (br. 12 poz. 3) |
| γ-Pu[16] | 479 K – 592 K | 17,14 g/cm3 (479 K) | ortorompski | plošno centrirana | Fddd (br. 70) |
| δ-Pu[17] | 592 K – 730 K | 15,9 g/cm3 (592 K) | monoklinski | centrirana po bazi | Cm (br. 8) |
| δ'-Pu[18] | 730 K – 749 K | 16,0 g/cm3 (730 K) | tetragonalni | prostorno centrirana | I4/mmm (br. 139) |
| ε-Pu[19] | 749 K – 914 K | 16,5 g/cm3 (749 K) | kubični | prostorno centrirana | Imm |
| tečni[2] | 914 K – 3503 K | 16,63 g/cm3 (914 K) | — | — | — |
Osim navedenih, poznate su i visokotlačne modifikacije, koje se dobiju iz α-Pu pri pritisku iznad 40 GPa, a kristaliziraju se u prostornoj grupi P63.[20]

Plutonij je neplemeniti, veoma reaktivni metal. Izložen zraku, brzo reagira s kisikom i vlagom. Pri tome metal postaje mat i prevlači se tamnim, plavo-crnim slojem oksida, dok dužim stajanjem na zraku stvara se tamniji, sivo-zeleni, praškasti sloj oksida koji lahko skida.[21] Pri zagrijavanju, metal reagira sa većinom nemetala i vodom. Međutim na sobnoj temperaturi, plutonij ne napadaju ni bazični rastvori niti voda. U koncentriranoj dušičnoj kiselini on nije rastvorljiv zbog pasivizacije svoje površine.[11] Plutonij se rastvara u hlorovodičnoj kiselini i dušičnoj ali uz dodatak fluorida. U tom slučaju, ioni fluorida poništavaju i onemogućavaju pasiviziranje metala koje se inače javlja napadanjem čiste dušične kiseline. Hemijske osobine plutonija uglavnom su slične kao i kod ostalih aktinoida. Kao i kod većine ovih elemenata, njegove hemijske osobine su pod znatnim utjecajem njegove snažne radioaktivnosti, a zbog zagrijavanja metala i emitiranja jakog radioaktivnog zračenja, njegove veze sa drugim elementima vrlo lahko pucaju. Ovaj element može graditi cijeli niz spojeva u kojima se može nalaziti u oksidacijskim stanjima od +3 do +7, što znači da plutonij zajedno s neptunijem gradi najviša oksidacijska stanja među svim aktinoidima. Najstabilniji je u oksidacijskom stanju +4. U vodenim rastvorima, ioni plutonija imaju karakteristične boje. Tako naprimjer ion Pu3+ je ljubičast, ion Pu4+ smeđ, PuVO2+ roze boje, PuVIO22+ narandžast, a PuVIIO23+ zelen.[22]
Do danas je izmjereno i ispitano 20 izotopa i 15 nuklearnih izomera plutonija, čiji maseni brojevi se kreću od 228 do 247.[23] Vremena poluraspada se kreću od 37 · 10−12 sekundi za izomer 236m1Pu do oko 80 miliona godina za izotop 244Pu. "Najdugovječniji" izotopi sa vremenima poluraspada dužim od 11 dana imaju masene brojeve između 236 i 244. Jedini izuzetak među njima je 243Pu čije vrijeme poluraspada iznosi kraće od 5 sati.[23] Neki od izotopa se smatraju početnim tačkama za određene radioaktivne lance raspada.
Plutonij je posljednji, doduše izuzetno rijetki, element u periodnom sistemu za koji je poznato da se može pronaći u prirodi. Sa udjelom od 2 · 10−19% (po težini)[1][25] on je jedan od najrjeđih elemenata u Zemljinoj kori. U nalazištima uranija može nastati plutonij u vrlo malim količinama apsorpcijom prirodno otpuštenih neutrona iz uranija. Procjenjuje se da na 140 milijardi atoma uranija može nastati jedan atom plutonija. Američki hemičar D. F. Peppard je 1951. iz koncentrata uranijeve rude izdvojio jedan mikrogram izotopa 239Pu. Za tako dobijeni mikrogram plutonija bilo je neophodno 100 tona rude.[26]
Najduže živući izotop plutonija, 244Pu, datiran u vrijeme nastanka Sunčevog sistema, pronađen je u mineralu bastnesitu, koji je dobio ime po mjestu pronalaska, rudniku Bastnäs u Švedskoj. Uz pomoć vrlo precizne analitike, uspjelo se dokazati prisustvo ovog izotopa u tragovima. Međutim, ove količine su tako neznatne da su pronađene tek 1971. godine, odnosno mnogo godina nakon vještačkog dobijanja plutonija u nuklearnim reaktorima.[24][27]
U prirodnom nuklearnom reaktoru Oklo u Gabonu kao i u susjednom nalazištu uranijske rude, poznato je da se tamo tokom nekoliko milenija odvijala nuklearna fisija kao lančana reakcija ali u prirodnom okruženju. U Oklou za oko 1,5 do 2 milijarde godina do danas nastalo je od 2 do 4 tone 239Pu putem sakupljanja fisibilnih neutrona na, tada vrlo česti, izotop uranija 238U. U pojedinim dijelovima nalazišta Oklo, dolazilo je i do direktne fisije 239Pu, što je značajno utjecalo na cjelokupni proces nuklearne fisije. Oko jedne trećine ukupno raspadnutog uranija 235U ima izvor u alfa-raspadu plutonija 239Pu. Ostatak nastalog plutonija se u međuvremenu potpuno raspao.
Plutonij nastaje pri eksplozijama nuklearnih bombi kao i u atomskim reaktorima putem transmutacije uranija. Međutim, tako vještački dobijeni plutonij posjeduju nuklearne sile i neke od visokorazvijenih država koje imaju izgrađene nuklearne elektrane, a procjenjuje se da te države imaju nekoliko stotina tona plutonija, između ostalih Rusija oko 180 tona a SAD oko 90 tona.[28]
Između 1945. i 1980. nadzemnim nuklearnim testovima ispušteno je u okolinu od tri do pet tona antropogenog plutonija,[27] čiji tragovi se i danas mogu pronaći u mnogim dijelovima svijeta. Osim toga, određene količine plutonija su emitirane kroz brojne nuklearne nesreće kao i u drugim nenamjernim događajima, kojima je uzrok čovjek:
Proces nastajanja plutonija nezaobilazno počinje u nuklearnim centralama koje pogoni izotopska smjesa bogata uranijem 238U. Pri tom dio korištenog 238U prelazi u 239Pu putem zahvata jednog neutrona i naknadnim beta raspadom.
Dodatni neutron dovodi, u većini slučajeva, do cijepanja jezgra, ali djelimično nastaje i izotop plutonija 240Pu. Pošto je taj izotop dosta teško fisibilan, dolazi do još jednog zahvata neutrona i nastanka izotopa 241Pu, koji se opet vrlo lahko cijepa. Međutim, ne cijepaju se svi atomi, tako da se proces obogaćivanja može nastaviti dobijajući izotop 242Pu pa i teže od njega. Ipak, izotop 243Pu ima dosta kratko vrijeme poluraspada pa je daljnji zahvat neutrona koji vodi do cijepanja atoma, ili vrlo rijetko, do nastanka 244Pu, gotovo zanemariv. Dakle, obogaćivanje plutonija u ovom procesu praktično je gotovo nastankom 243Pu te vodi preko beta raspada do izotopa americija 243Am.
Svaka od ovih faza nuklearne reakcije zahtijeva određeno vrijeme, pa se u jezgrima reaktora tokom vremena minjea relativna količina i udio izotopa. Brzina kojom se odvijaju ove nuklearne reakcije zavisi od brzine rasprostiranja neutrona. Zbog toga što se najveći dio lahko cjepivih izotopa zaista i iscijepa te ne pređe u druge izotope, nastankom svakog takvog cjepivog izotopa opada i mogući prinos (efikasnost) procesa obogaćivanja.
Lakši izotop 238Pu ciljano se dobija po potrebama. On nastaje zahvatom više neutrona iz izotopa uranija 235U. Pri tome prvo nastaje jezgro uranija 236U u pobuđenom stanju, a koje ima vrijeme poluraspada od samo 120 nanosekundi i cijepa se uz vrlo visoku vjerovatnoću. Osim toga, pobuđena jezgra 236U mogu preći u stabilno osnovno stanje putem emisije gama zraka. Putem daljnjeg zahvata neutrona i β-raspada nastaje neptunij 237Np. Nakon određenog vremena tokom kojeg djeluje beta zračenje, neptunij, koji se sastoji gotovo isključivo iz 237Np, se izdvaja iz šipki nuklearnog goriva. Neptunij se može ponovno vratiti u reaktor u obliku nuklearnih šipki od čistog neptunija i izložiti neutronskom zračenju. Pri tome on zahvatom neutrona prelazi u 238Np a koji se raspada na 238Pu uz beta zračenje.

Tako obrađene gorive šipke također sadrže i teže izotope plutonija. Osim toga, neke atome neptunija pogađaju i neutroni energija iznad 6,27 MeV, pri čemu nastaju i manje količine plutonija 236Pu. On se dalje raspada preko tzv. torijevog niza čime nastaje izotop talija 208Tl, poznat kao veoma snažan emiter gama zraka. Međutim, ako 239Pu pogode brzi, odnosno neusporeni neutroni i pri tome ga razbiju, prosječni broj novonastalih i otpuštenih neutrona po jednom atomskom jezgru je posebno visok. U takvom reaktoru, teoretski, mnogo više uranija 238U može se prevesti u novi plutonij 239Pu nego što će ga se istovremeno "potrošiti" putem raspada. Takva vrsta reaktora naziva se brzi oplodni reaktor odnosno "brza oplodnja". Ipak u praksi je do danas postignuta maksimalna stopa konverzije od 0,7 tako da danas ne postoji brzi oplodni reaktor koji bi se mogao komercijalno iskorištavati u industrijskom obimu.
Nakon iskorištenja u reaktoru, plutonij zajedno sa proizvodima cijepanja atoma i neupotrebljivim ostacima nuklearnog goriva, preostaje u gorivim šipkama. Takozvanim PUREX procesom iz tih ostataka se može izdvojiti plutonij, kao i potrebni uranij, u postrojenjima za preradu potrošenog nuklearnog goriva. Najprije se materijal rastvori u dušičnoj kiselini te se plutonij i uranij izdvajaju pomoću tri-n-butil fosfata, dok se proizvodi cijepanja atoma i drugi nepoželjni ostaci odbacuju. Godišnje se tako preradi oko 20 tona plutonija, pretežno u obliku izotopa 239Pu.[32]
Prodaja ili transport nuklearnog materijala (poput plutonija 239Pu i 241Pu) kao i materijala koji su potrebni za njegovo dobijanje, državama koje ne posjeduju nuklearno oružje zabranjeno je po članu 3. ugovora o zabrani širenja nuklearnog naoružanja pod kontrolom IAEA.[33] U nekim državama poput Njemačke na snazi je poseban zakon o rukovanju i posjedovanju nuklearnog materijala. On, između ostalog, regulira pod kojim uslovima se nuklearni materijal može posjedovati ili nabavljati u Njemačkoj.[34]
Biološke funkcije plutonija nisu poznate. Neka istraživanja i ispitivanja se koncentriraju na djelovanja mikroba sa plutonijem, koja za cilj imaju sanaciju i dekontaminiranje njegovih skladišta i okoline.[35] Otkriveno je da neke enterobakterije iz roda Citrobacter mogu istaložiti plutonij(IV) iz vodenog rastvora u svoje ćelijske zidove pomoću aktivnosti fosfataze te ga povezati u lantan-fosfatne komplekse.[36]
Seamless Wikipedia browsing. On steroids.
Every time you click a link to Wikipedia, Wiktionary or Wikiquote in your browser's search results, it will show the modern Wikiwand interface.
Wikiwand extension is a five stars, simple, with minimum permission required to keep your browsing private, safe and transparent.