Коронавірусна хвороба 2019
гостра респіраторна хвороба, яку спричинює коронавірус SARS-CoV-2 З Вікіпедії, вільної енциклопедії
Коронаві́русна хвороба 2019[40][41] (англ. coronavirus disease 2019, абревіатура COVID-19 затверджена як офіційна скорочена назва[42]) — інфекційна хвороба, яка вперше виявлена у людини в грудні 2019 року в місті Ухань, Центральний Китай. Хвороба почалася як спалах, що розвинувся у пандемію. Причиною хвороби став коронавірус SARS-CoV-2[43], циркуляція якого в людській популяції до грудня 2019 року була невідомою.
Пандемію цієї хвороби Всесвітня організація охорони здоров'я (ВООЗ) визнала надзвичайною ситуацією в галузі міжнародної охорони здоров'я та внесла заходи з боротьби проти неї до тимчасових рекомендацій згідно з Міжнародними медико-санітарними правилами 2005 року[44]. Щоб уникнути стигматизації, пов'язаної з географічним регіоном, де виникли перші випадки захворювання, а також із расовою приналежністю чи певною етнічною групою, ВООЗ затвердила офіційну назву «коронавірусна хвороба 2019 (COVID-19)».
5 травня 2023 року ВОЗ оголосила що зараз коронавірусна хвороба 2019 є встановленою та постійною проблемою суспільної охорони здоров'я, яка більше не є надзвичайною ситуацією в галузі охорони здоров'я міжнародного значення.[45][46]. За час з грудня 2019 року до серпня 2023 року в усьому світі було зареєстровано понад 760 мільйонів випадків хвороби і 6,9 мільйона смертей, але фактична кількість вважається більшою.[47]
Етіологія
Узагальнити
Перспектива
Родина Coronaviridae (CoV, коронавіруси) включає дві підродини, 5 родів, 23 триби та приблизно 40 відомих видів. Багато з цих вірусів спричинюють захворювання у ссавців і птахів, можуть передаватися від тварин до людей. Коронавіруси людини (hCoV) були вперше описані в 1965 році. Відомі коронавіруси людини 229E, NL63, OC43, HKU1, й зоонозні за походженням MERS-CoV і SARS-CoV переважно належать до роду бетакоронавірусів. Наприкінці грудня 2019 року в Ухані (Китай) вперше виявлено новий патогенний бетакоронавірус людини, який отримав назву SARS-CoV-2. Він є третім коронавірусом людини, який імовірно прийшов за останні два десятиліття від тваринного джерела, став загалом сьомим із відомих людських коронавірусів.
Геномні дослідження
Порівнювання повнорозмірної послідовності геному SARS-CoV-2 та інших доступних геномів бетакоронавірусів показали, що у нього найтісніший зв'язок із кажанним штамом ВАРС BatCov RaTG13, гомологічність досягає 96 %, за іншими даними — 98 %. Із SARS-CoV (збудником тяжкого гострого респіраторного синдрому / SARS / ТГРС) гомологічність сягає 79 %, з вірусом MERS-CoV, причиною близькосхідного респіраторного синдрому — 50 %[48].
Існують заяви стосовно штучного походження цього збудника, але деякі науковці та дослідницькі організації це спростовують, стверджуючи, що він має безперечно тваринне походження[49]. ВООЗ заявила, що усі наявні докази свідчать про те, що SARS-CoV-2 має тваринне джерело. Багато дослідників змогли вивчити геномні особливості цього вірусу і виявити, що немає підтвердження того, що SARS-CoV-2 є лабораторною конструкцією. Побудований вірус демонстрував би поєднання відомих елементів у геномних послідовностях — а це не так[50]. Науковці Центрів з контролю та профілактики захворювань у США (CDC) проаналізували геном SARS-COV-2, отриманого від першого пацієнта в США, який захворів 24 січня 2020 року, зробивши висновок, що послідовність майже ідентична послідовностям, про які повідомляли китайські науковці[51].
Досліджено ступінь молекулярної дивергенції між SARS-CoV-2 та іншими коронавірусами. Хоча виявлено лише 4 % варіабельності геномних нуклеотидів між SARS-CoV-2 та SARS-CoV відносно кажанного RaTG13, різниця у нейтральних ділянках становила 17 %, що дозволяє припустити, що розбіжність між двома вірусами значно більша, ніж раніше оцінювалось. Усі коронавіруси мають специфічний спосіб проникнення в клітини хазяїна — за допомогою особливого білка на зовнішніх шипах. Відбулося утворення нових варіацій функціональних ділянок у рецептор-зв'язуючому домені (RBD) шипа, що спостерігається у SARS-CoV-2 та вірусу панголіну SARSr-CoV, геном якого на 90 % збігається з геномом SARS-CoV-2. Було зроблено висновок, що це, ймовірно, спричинено мутаціями та природним добором, проте не рекомбінацією. Вияснено, що структура шипів у вірусів панголіну і SARS-CoV-2 збігається на 99 %, а ось ступінь подібності зовнішніх шипів у кажанного і SARS-CoV-2 становить всього 77 %. Зроблено висновок, що після переходу SARS-CoV-2 від кажанів до людини приблизно вдесятеро збільшилася частка мутацій нуклеотидів РНК G в U.[52][53] Припускається, що кажанний і панголіновий віруси могли в організму якоїсь тварини на одній із тваринних ферм Китаю утворити SARS-CoV-2, який із цією або цими тваринами потрапив до ринку в Ухані. Також повідомляється про новий коронавірус, який виявлений у кажанів, позначається як RmYN02. Він ідентифікований за допомогою метагеномічного аналізу зразків від 227 кажанів, зібраних у провінції Юньнань у Китаї в період із травня по жовтень 2019 року. Зокрема, RmYN02 має 93,3 % ідентичності нуклеотидів із SARS-CoV-2 за шкалою повного геному вірусу та 97,2 % ідентичності за геном 1ab, за яким він є найближчим родичем SARS-CoV-2 серед повідомлених на середину 2020 року. При цьому RmYN02 виявив низьку ідентичність послідовності (61,3 %) до SARS-CoV-2 в домені, що зв'язує рецептор (RBD), і не може зв'язуватися з ангіотензинперетворювальним ферментом 2 (ACE2). Аналогічно SARS-CoV-2, RmYN02 характеризувався введенням декількох амінокислот у місці стику S1 і S2 субодиниць білка шипа. Це дає вагомі докази того, що подібні події вставки можуть відбуватися природним шляхом у бетакоронавірусів тварин[54]. У вересні 2021 року у підковоносного кажана з печери у провінції В'єнтьян на заході Лаоса знайдено коронавірус, який є генетично ближчим до Sars-CoV-2, ніж вірус RaTG13, знайдений у Китаї в 2013 році, що вважався попередником SARS-CoV-2. Вірус названо Banal-52, і він має 96,8 % ідентичності нуклеотидів із SARS-CoV-2 за шкалою повного геному вірусу, тоді як RaTG13 — 96,1 %[55].
Першовідкривач ВІЛ Нобелівський лауреат, вірусолог Люк Монтаньє стверджував, що пандемія коронавірусу 2019 року була створена людиною в лабораторії і це може бути результатом спроби створити вакцину проти ВІЛ-інфекції. За його словами, «наявність елементів ВІЛ і малярійного плазмодія в геномі коронавірусу є дуже підозрілими, і такі характеристики вірусу не могли виникнути природним шляхом»[56].
Філогенетичні оцінки стверджують, що циркуляція SARS-CoV-2 серед людей і, відповідно, пандемія COVID-2 почалася приблизно в період 6 жовтня — 11 грудня 2019 року. 198 ділянок геному SARS-CoV-2 станом на липень 2020 року зазнали мутацій. Виявлені мутації можуть вказувати на постійну адаптацію SARS-CoV-2 до його людського хазяїна[57].
Головні мутаційні лінії SARS-CoV-2
SARS-CoV-2, як й інші віруси, в ході еволюції набуває мутації. Ті з них, які допомагають вірусам краще розмножуватися і поширюватися, зберігаються в геномі, інші ж еволюція відкидає. Таким чином з'являються нові варіанти SARS-CoV-2. Дослідження раніше показували, що у SARS-CoV-2 мутації з'являються приблизно раз у два тижні. У більшості випадків вірус передається або знищується до того, як встигає почати мутувати. Це означає, що ймовірність того, що SARS-CoV-2 буде мутувати в організмі пацієнта, не дуже велика. Проте проведені у 2021 році дослідження показали, що у фокус уваги авторів ранніх досліджень потрапляли тільки успішні мутації, а ті, що не дозволяли вірусу довго виживати в організмі пацієнта, просто не враховувалися. Якщо взяти до уваги такі мутації, то швидкість зміни геному SARS-CoV-2 може бути вище, ніж вважали раніше — на 49-67 %[58].
6 листопада 2020 року ВООЗ повідомила, що з червня 2020 року в Данії, регіон Північна Ютландія, виявлено 214 випадків захворювання людей коронавірусною хворобою 2019, що спричинили штами вірусу, з яких 12 є унікальними, пов'язаними з норками. Вісім із цих людських випадків чітко пов'язані з вирощуванням норок. Клінічні прояви, тяжкість і передача інфекції серед інфікованих аналогічні іншим штамам SARS-CoV-2, що циркулюють. Проте цей штам, названий варіантом «кластера 5», має комбінацію мутацій, що раніше не спостерігалися, і їхнє значення уточняється[59].
Чергова мутація SARS-CoV-2 виявлена у Великій Британії у вересні 2020 року. VOC-202012/01 / B.1.1.7 ідентифікований шляхом вірусного геномного секвенування. Цей варіант містить 23 нуклеотидні заміни і не є філогенетично пов'язаним із вірусною лінією SARS-CoV-2, що циркулювала у Сполученому Королівстві на момент виявлення цього мутаційного варіанту. Як і звідки виник SARS-CoV-2 VOC 202012/01, незрозуміло. Цей варіант визначається наявністю діапазону з 14 мутацій, що призводить до змін амінокислот і трьох делецій. Деякі з цих мутацій можуть впливати на передачу вірусу у людей. Ця нова вірусна лінія поширилася у 2020 році у країні й витіснила там інші мутаційні лінії. Наслідки цього вивчені, зрештою не виявлено збільшення летальності чи тяжкості хвороби, хоча не виключено підвищення рівня контагіозності від відомого до цього поширення пандемії 1:1,5 (від одного зараженого заражаються 1,5 людини) до 1:1,7. Загалом 1108 випадків зараження цим варіантом виявлено у країні станом на 13 грудня 2020 року. Більшість випадків хвороби, коли був ідентифікований цей варіант, мали місце у людей віком до 60 років. Новий варіант ідентифікований станом на 30 грудня ще у 31-й країні / території, включаючи Австралію, Данію, Італію, Ісландію та Нідерланди[60][61]. ЄвроCDC оцінила ймовірність поширення цього варіанту, що викликає занепокоєння, в Європейському Союзі як дуже високу через підвищену передачу, що призвело до збільшення кількості випадків захворювання. Це, в свою чергу, призвело до вищого рівня госпіталізації та летальності серед усіх вікових груп, але особливо для осіб старшого віку та тих, хто мають супутні захворювання[62]. Отримані результати порівняння кількості випадків смерті померлих не з категорій ризику від первинної лінії коронавірусу, що циркулювала з початку пандемії, і від B.1.1.7 показало розбіжність, що становило 1,64 (95 % довірчий інтервал 1,32-2,04). У цій порівняно низькій групі ризику це означає збільшення смертності з 2,5 до 4,1 на 1000 виявлених випадків[63].
18 грудня 2020 року влада ПАР оголосила про виявлення нового варіанту SARS-CoV-2, який швидко поширився в трьох провінціях Південної Африки. Там назвали цей варіант 501Y.V2 через мутацію N501Y. Хоча SARS-CoV-2 VOC 202012/01 із Великої Британії також має мутацію N501Y, філогенетичний аналіз показав, що 501Y.V2 з Південної Африки — це інша мутаційна лінія вірусу. Починаючи з 16 листопада 2020 року виявлено, що цей новий варіант SARS-CoV-2 значною мірою замінив інші вірусні лінії SARS-CoV-2, які циркулювали у провінціях Східного Капського мису, Західної Капської провінції та Квазулу-Натал. Хоча одержані дані геномного дослідження показали, що варіант 501.V2 швидко витіснив інші лінії коронавірусу, що циркулюють у Південній Африці, і попередні дослідження показали, що цей варіант пов'язаний із більшим вірусним навантаженням, підвищенням активності передачі. Загалом не знайдено чітких доказів того, що новий варіант пов'язаний з тяжчим клінічним перебігом захворювання або гіршими наслідками.
ВООЗ анонсувала нову систему назв для мутаційних ліній / штамів SARS-CoV-2. З 1 червня 2021 року ВООЗ використовує літери грецької абетки для тих штамів, які раніше називали британським, південноафриканським, індійським тощо. Для:
- британського (вересень 2020) GR/501Y.V1 / B.1.1.7 обрали літеру «Альфа» (грец. Ά),
- для південноафриканського (травень 2020) GH/501Y.V2 / B.1.351 — «Бета» (грец. Β),
- для пізнього бразильського (листопад 2020) GR/501Y.V3 / P.1 — «Гамма» (грец. Γ),
- для індійського (жовтень 2020) G/452R.V3 / B.1.617.2 — «Дельта» (грец. Δ),
- для раннього американського (березень 2020) GH/452R.V1 / B.1.427/B.1.429 — «Епсилон» (лат. Έ),
- для раннього бразильського (квітень 2020) GR / P.2 — «Зета» (грец. Ζ),
- для всесвітньо поширеного (грудень 2019) G/484K.V3 / B.1.525 — «Ета» (грец. Ή),
- для філіппінського (січень 2021) GR / P.3 — «Тета» (грец. Θ),
- для пізнього американського (листопад 2020) GH / B.1.526 — «Йота» (грец. Ί),
- для ще одного індійського (жовтень 2020) G/452R.V3 2 / B.1.617.1 — «Каппа» (грец. Κ),
- для перуанського (грудень 2020) GR/452Q.V1 / C.37 — «Лямбда» (грец. Λ),
- для колумбійського (січень 2021) GH / B.1.621 — «Мю» (грец. Μ),[64]
- для південноафриканського (листопад 2021) GR/484A / B.1.1.529. — «Омікрон» (грец. Ο)[65].
Це зроблено для того, щоб спростити найменування і подолати стигму довкола країн походження мутаційних ліній[66][67]. Також виявлений «безіменний варіант» (англ. Unnamed variant) B.1.617.3. У США запропонували його вважати таким, «що викликає інтерес», тоді як ВООЗ так не вважає. Вперше цей варіант був ідентифікований в Індії в жовтні 2020 року і має ту саму батьківську лінію, що і «Дельта». Останній випадок був зареєстрований у США в квітні 2020 року, і в усьому світі зараз він становить <0,5 % усіх випадків зараження. Може мати властивості, що дозволяють ухиляються від антитіл, як це є у варіантів «Ета» і «Каппа»[68].
На червень 2021 року «Дельта» класифікований CDC як варіант, який «представляє інтерес», тобто має генетичні маркери, пов'язані зі зниженням нейтралізації антитілами, створеними в результаті перенесеного захворювання або внаслідок вакцинації, зменшенням ефективності лікування, труднощами специфічної діагностики, збільшенням заразливості та тяжкості хвороби. Він виник наприкінці минулого року в Індії, загалом зареєстрований вже повсюдно. Абсолютно очевидно, що його заразливість вище, щонайменше ніж у «Альфа», бо на відміну від нього йде більша реплікація у структурах носа, через що у клінічній картині хвороби переважає нежить зі значним виділенням внаслідок цього коронавірусу у довкілля. Його вірусне навантаження в організмі людини в тисячі разів більше від такого при зараженні варіантами «Ета» і «Альфа». Пік захворюваності реєструється у молодих людей 12-20 років[69]. Велике британське національне дослідження виявило більший ризик госпіталізації та невідкладної інтенсивної допомоги для пацієнтів, інфікованих варіантом «Дельта», порівняно з «Альфа». Результати свідчать про те, що ураження варіантом «Дельта» у невакцинованих популяціях призводить до більшого навантаження на медичні служби, ніж при ураженні варіантом «Альфа»[70]. Станом на кінець 2021 року хвороба, яку продовжує спричиняти цей варіант, призводить до щоденної смерті в середньому до 1300 громадян США[71].
Продовжується спостереження за поширенням нового субваріанту «Дельта-плюс». Варіант «Дельта» наприкінці 2021 року був домінуючим варіантом у світі. Але зокрема у Великій Британії останні офіційні дані свідчать про те, що 6 % випадків зумовлено субваріантом «Дельта-плюс» (Y.4.2), що містить мутацію, яка може дати переваги виживанню вірусу. Ця мутація K417N впливає на білок-шип, необхідний вірусу для зараження клітин, і це є основною мішенню для мРНК та інших вакцин.
Є вже вагомі свідчення, що варіант «Омікрон» здатний заражати людей у 70 разів швидше, ніж попередні варіанти. Його коефіцієнт заразності досягає 3,5, тоді як у варіанту «Дельта» — 0,85. Проте масштаб його відтворення є удесятеро меншим, ніж у початкового варіанту SARS-CoV-2. Припускають, що «Омікрон» буде спричиняти менш тяжкий перебіг хвороби, проте цей дуже заразний варіант хоч і може бути менш хвороботворним, здатен інфікувати набагато більше людей і може спричинити більше випадків серйозного перебігу хвороби та летальних наслідків. З цієї причини і беручи до уваги попередні дослідження про здатність «Омікрону» частково обходити вакцинний імунітет та спричинити повторні випадки захворювання коронавірусною хворобою 2019, загальна загроза від нього, ймовірно, дуже значна[72]. Виявлено, що цей варіант має більше 30 мутацій у S-білку вірусу, 15 з яких знаходяться у рецепторзв'язувальному домені. Через це він позбавлений можливості ефективного зв'язування з рецепторами, уникає дії нейтралізуючих антитіл до інших варіантів SARS-CoV-2. Чимраз більше даних про те, що він поступається тяжкістю клінічного перебігу іншим варіантам, проте компенсує це полегшеною передачею, що веде до швидкого наростання захворюваності. Навіть удвічі менш вірулентний варіант може завдати набагато більших збитків, якщо він до того ж поширюється в кілька разів швидше. Три чверті перших випадків, спричинених варіантом «Омікрон» у США було зареєстровано серед вакцинованих або вже перехворілих. У Данії, де ведеться один із найкращих у світі епіднагляд за варіантами, частка таких випадків була такою ж. В інших регіонах світу цей показник становив 80 % або вище. Припускається, що саме ті, хто не захищений вакцинацією, будуть набувати імунітет від зустрічі з відносно менш небезпечним варіантом SARS-CoV-2. Його швидке зростання, ймовірно, відбувається за рахунок поширення серед уже захищених, вакцинованих людей. Проговорена думка, що цей варіант поширюється в популяції не замінивши повністю циркуляцію варіанту «Дельта», а отже йдуть паралельно 2 хвилі пандемії, чого не спостерігалось від початку її. Накопичені певні дані свідчать, що вакциновані та особливо щеплені люди виявляються досить добре захищеними від тяжкого перебігу коронавірусної хвороби 2019, спричиненого варіантом «Омікрон», але від зараження — ні. При двох дозах вакцини AstraZeneca захист від зараження дорівнює нулю. Для двох доз вакцини Pfizer — становить лише 30 %. Тому, як припускають епідеміологи, багато щеплених людей заражаються. Є припущення, що перехресний імунітет між варіантами «Омікрон» і «Дельта» дуже низкий через високий рівень дивергенції. Також припускається, що імунітет, отриманий внаслідок хвороби, яку спричинив варіант «Омікрон», не буде захищати від ураження, яке спричинює варіант «Дельта» тою ж мірою, як і ранні варіанти[71]. Виявлений субваріант «Омікрону» (якому дана неофіційна назва стеалс-Омікрон англ. stealth Omicron) BА.2 на відміну від того BА.1, що нині масово циркулює в світі, не просто поширюється швидше, а також може спричинити тяжчий клінічний перебіг і, схоже, здатний перешкодити деяким засобам, які є для лікування та профілактики, зокрема препаратам моноклональних антитіл, показують нові дослідження[73][74].
Чергова мутація виявлена французькими науковцями на чолі з Дідьє Раулем у пацієнтів із коронавірусною хворобою 2019 у госпіталі Форкальк'є, що в департаменті Альпи Верхнього Провансу. Ними виявлено 12 хворих, які заразилися від нульового пацієнта, що до цього приїхав із Камеруна. Цей варіант зареєстрований під назвою B.1.640.2 у мережі GISAID (Глобальна ініціатива щодо обміну даними про пташиний грип). Для того, щоб дізнатися, чи є він більш інфекційним чи спричинює тяжчий перебіг, необхідно провести ретельний епідеміологічний нагляд[75]. У варіанта виявлено 46 мутацій і 37 делецій, що привели до 30 амінокислотних замін. 14 із цих замін і 9 делецій розташовані в спайковому білку SARS-CoV-2 порівняно з первинним варіантом його. Це є, за думкою науковців, ще одним прикладом непередбачуваності появи варіантів SARS-CoV-2, а також їх впровадження в певну географічну зону з-за кордону[76]. Проте ВООЗ заявила, що з 22 листопада 2021 року спостерігає за цим варіантом, не відмічає його широкого поширення — досі його виявлено лише у зразках, взятих від 20 осіб і лише один із них виявлений у грудні 2021 року. ВООЗ надала йому найнижчий за загрозливістю статус «варіант під наглядом» (VUM)[77][78]
Повідомлено про виявлення на Кіпрі нового варіанту «Дельтакрон», який має походження від варіанту «Дельта» з деякими мутаціями, притаманному варіанту «Омікрон», продовжується його вивчення[79].
Варіант Omicron XE є рекомбінантним варіантом Omicron BA.1, оригінального варіанту Omicron та Omicron BA.2. Він має 3 мутації, яких немає у варіанту Omicron BA.1 або BA.2, є ще заразнішим та найпоширенішим у США та більшості країн. Отримані дані свідчать, що варіант Omicron XE за своєю здатністю до легкого поширення нагадує варіант BA.2 та не являє серйозної загрози виникнення швидких або масових спалахів. Рекомбінантні штами добре описані для багатьох інших вірусів і рідко бувають пов'язані з тяжчими випадками. Перші виявлені випадки хвороби, спричиненої Omicron ХЕ, зареєстровані у Великій Британії наприкінці січня 2022 року і в травні 2022 року на їх долю припадало менше 1 % від усіх випадків у цьому регіоні, основним залишався варіант Omicron BA.2 як у Сполученому Королівстві, так і в усьому світі. Виявляли цей варіант також в Таїланді та Індії. Дослідження вказують на ефективність вакцин проти цього варіанту вірусу. Оскільки варіанти Omicron BA.1 і BA.2 є стійкими до деяких моноклональних антитіл, ці препарати, ймовірно, будуть неефективними і проти Omicron XE. Паксловід та молнупіравір, за деякими даними, зберігають ефективність проти цього варіанту вірусу для амбулаторної терапії[80][81].
Ідентифіковано ще два субваріанти SARS-CoV-2 — «Омікрон» BA.3 і BA.4, але даних про їх клінічні особливості та можливість передачі від людини до людини поки що не прояснені. BA.3 має 13 мутацій у спайк протеїні та вперше був ідентифікований в Південній Африці наприкінці 2021 року. Варіанти BA.4 і BA.5 (або B.1.1.529), були підтверджені в Південній Африці та США. Вони мають потенціал для уникнення поствакцинального імунітету і захисту від попередньої інфекції, що є наслідком мутацій. Варіанти «Омікрону» BA.4 і BA.5 виявляються ще заразнішими, ніж BA.2 (Стелс). Випадки захворювання в Південній Африці збільшуються, незважаючи на те, що 90 % населення були вакциновані або хворіли раніше, що ще більше підтверджує прогноз, що цим варіантам не запобігають наявні антитіла.
Новий підваріант «Омікрону», який вперше ідентифікований в Індії в травні 2022 року, ВА.2.75 (Кентавр) виявлено також у США та ще декількох країнах. Його особливістю є ще більша здатність ухилятися від імунітету, ніж це роблять інші варіанти вірусу. Поки що його розглядають як варіант, який викликає інтерес, тому що його заразність, формування ступеню тяжкості клінічного перебігу захворювання і відхилення від імунітету ще вивчаються. Ряд експертів вважають, що наявні 9 додаткових мутацій Кентавра дозволять йому захищатися від природного та штучного імунітету.
Виявлено кілька рекомбінантних форм вірусу, які включають генетичний матеріал Дельта-Омікрон і BA.1-BA.2. Отримані дані свідчать про те, що вони не мають вищий рівень передачі та тяжчі наслідки, ніж вихідні штами.
Культуральні особливості
Виділення вірусу проводять за допомогою різних клітинних ліній, таких як епітеліальні клітини дихальних шляхів людини, Vero E6 і Huh-7. Цитопатичні ефекти спостерігаються через 96 годин після інокуляції.
Білки та ферменти вірусу
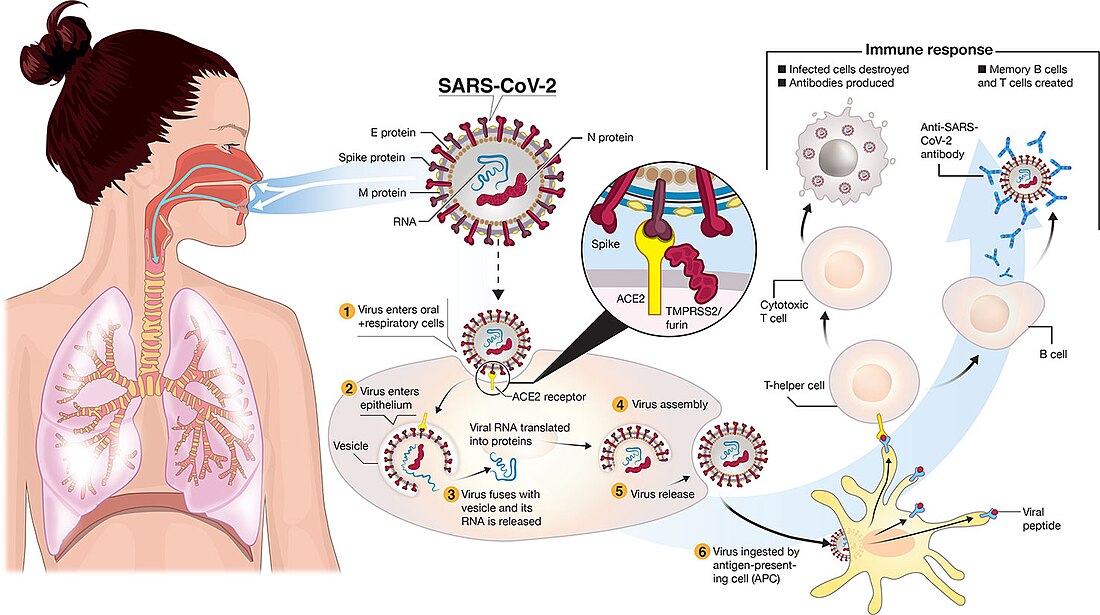
Як й інші коронавіруси, SARS-CoV-2 має чотири структурні білки, відомі як S (шип), E (оболонка), M (мембрана) та N (нуклеокапсид). N білок утримує РНК, а білки S, E і M разом створюють вірусну оболонку.
Подібно до SARS-CoV і MERS-CoV, геном SARS-CoV-2 кодує неструктурні білки (такі як основна 3-хімотрипсин-подібна протеаза, папаїн-подібна протеаза, РНК-геліказа і РНК-залежна РНК-полімераза), структурні білки (глікопротеїни) і допоміжні. Чотири неструктурні білки є ключовими ферментами в життєвому циклі коронавірусу, а поверхневі глікопротеїни необхідні для здійснення зв'язування коронавірусу з рецепторами на поверхні чутливих клітин, внаслідок чого він проникає у клітину.
3-хімотрипсин-подібна протеаза (англ. coronavirus 3CL hydrolase enzyme) являє собою кристалічну структуру з високою роздільною здатністю. Вона необхідна вірусу для дозрівання. Вважається, що це багатообіцяюча мета для виявлення низькомолекулярних препаратів, які б гальмували розщеплення вірусного поліпротеїну та запобігали поширенню хвороби. Виявлено дуже високу ідентичність послідовності амінокислот (96 %) між основною протеазою SARS-CoV-2 і такою в SARS-CoV.
SARS-CoV-2 виробляє щонайменше три фактори вірулентності, які сприяють вивільненню нових віріонів із клітин-хазяїв та інгібують імунну відповідь[82].
Морфологічні особливості
SARS-CoV-2 має певну мінливість форми — від круглої до овальної. Кожен віріон SARS-CoV-2 має діаметр 50–200 нанометрів.
Детальніші відомості з цієї теми ви можете знайти в статті SARS-CoV-2.
Епідеміологічні особливості
Узагальнити
Перспектива
Джерело та резервуар
Після роботи в лютому 2021 року місії ВООЗ до Китаю по вивченню можливого джерела появи SARS-CoV-2 у людській популяції, до якої входило 14 експертів із 10 країн, заявлено, що вислизання вірусу з біологічної лабораторії в Ухані є «надзвичайно малоймовірним», і найімовірніше, він скочив до людини від тваринного джерела, тому розглядається кілька теорій того, як хвороба вперше потрапила до людей. Повідомлено, що віруси, які зберігаються в уханській лабораторії та інших подібних лабораторіях в інших місцях, генетично занадто відрізняються від вірусу SARS-CoV-2, щоб бути його ймовірними родоначальниками. Експерти вважають, що інтродукція через посередника-хазяїна є найімовірнішим шляхом, який потребуватиме додаткових досліджень. Вважається, що цей коронавірус виник у кажанів, перш ніж передаватися людям через інші види диких тварин, таких, як панголіни чи бамбукові щури, що вважаються екзотичними делікатесами у Китаї. Команда ВООЗ не підтримала тверджень уряду Китаю, що вірус вперше з'явився в зовсім іншій країні, позиціонуючи Італію, Індію та США як можливих кандидатів, але не виключила того, що заморожені продукти могли допомогти поширенню цього коронавірусу в усьому світі, що потребує подальшого ґрунтовного вивчення. Американський уряд заявив, що не прийме висновки ВООЗ, не перевіривши їх самостійно[83]. Також існує думка, що цей коронавірус було створено штучно, а згодом спеціально піддано молекулярній обробці аби він виглядав так, ніби еволюціонував природно від кажанів[84]
Первинним джерелом і резервуаром інфекції підозрюються кажани, змії та ще невідомі тварини, від яких збудник потрапив поки що нез'ясованим шляхом до людей. Так є інформація про панголінів як можливе джерело. Вони вживаються в їжу в Китаї. Однак це припущення піддано дискусії[85][86][87]. За аналогією з іншими зоонозними коронавірусними хворобами, як то тяжкий гострий респіраторний синдром (SARS / ТГРС) чи близькосхідний коронавірусний респіраторний синдром (БКРС) припускається, що передача можлива від тварин до людини через безпосередній близький контакт із живою твариною або через певні продукти, зокрема верблюже молоко, як це дискутується при БКРС. Це відбулося ймовірно на ринку тварин і морепродуктів в Ухані, хоча деякі китайські науковці це спростовують. Дані свідчать про те, що людина, заражена SARS-CoV-2, може заразити інших ссавців, включаючи собак, котів і норок. Однак залишається невиясненим, чи будуть ці заражені ссавці джерелом для стійкої передачі людям[88]. Подальші дослідження показали, що норки часто інфікуються в результаті контакту з інфікованими людьми і можуть бути резервуаром SARS-CoV-2, передаючи вірус один одному і людині. Інфікована людина далі може передавати цей вірус у популяції. Данія, Нідерланди, Швеція, Іспанія, Італія та Сполучені Штати Америки повідомили ВООЗ про виявлення SARS-CoV-2 у вирощуваних норок[59]. Люди у перебігу пандемії є повноцінним джерелом і резервуаром коронавірусної хвороби 2019. У листопаді 2020 року було зареєстровано 349 випадків серед людей, пов'язаних із вирощуванням норок, що було більше порівняно з 200 випадками у жовтні 2020 року. З червня 2020 року загалом 644 людини, пов'язані з вирощуванням норок, дали позитивні результати в ПЛР. Крім того, зафіксовано щонайменше 338 випадків серед людей, які працювали із шкурками норок, на шести заводах і двох невеликих підприємствах, що свідчить про те, що існує підвищений ризик зараження у людей, які займаються землеробством, вибракуванням та обробкою норок. Станом на 1 грудня 2020 року постраждало 289 норкових ферм, що становить приблизно 20 % усіх норкових ферм Данії[89].
Спостереження 8 випадків спільного перебігу коронавірусної хвороби 2019 і близькосхідного коронавірусного респіраторного синдрому свідчить про відсутність конкуренції між збудниками цих хвороб і про спільність шляхів передачі цих захворювань[90].
Механізм і фактори передачі
Встановлено, що SARS-CoV-2 інтенсивно поширюється в людській популяції без залучення тваринного джерела практично виключно від людини до людини як антропоноз за допомогою повітряно-крапельного механізму передачі вірусу через аерозольні, переважно великодисперсні (› 5 мкм), виділення з дихальних шляхів, які швидко падають на землю через силу тяжіння, як правило, в межах 1-2 метрів від людини-джерела. Також існує думка, що передача можлива через дрібнодисперсні аерозолі (≤ 5 мкм), які швидко випаровуються у повітрі, залишаючи після себе ядра аерозолю, що є досить маленькими та легкими, щоб залишитися суспендованими у повітрі годинами (аналогічно пилу), що дає гіпотетично можливість зараження в приміщенні навіть вже за відсутності джерела інфекції, однак це дискутується. Потрібні подальші дослідження, щоб визначити, чи можна виявити життєздатний SARS-CoV-2 у зразках повітря з помешкань, де не виконуються ніякі медичні процедури, що генерують аерозолі та яку роль дрібнодисперсні аерозолі можуть грати в передачі SARS-CoV-2[88].
Показано, що реплікація SARS-CoV-2 у людини досить тривала, корелює з тяжкістю захворювання і навіть на 20-й день хвороби може бути активною. В аерозолізованій формі виживає понад 3 години в експериментальних умовах, але це механічне утворення аерозолів навряд чи імітує справжній клінічний сценарій[91]. Серії випадків, в яких були оцінені тісні контакти з пацієнтами з підтвердженим COVID-19, повідомляють, що зараження відбулося лише у близько 5 % контактів. Однак навіть ця низька швидкість не розподіляється рівномірно серед близьких контактів, а змінюється залежно від тривалості та інтенсивності контакту. Ризик найвищий серед членів домогосподарств, у яких швидкість передачі становить від 10 % до 40 %. Тісний, але менш стійкий контакт, наприклад, обмін їжею, дає близько 7 %, тоді як передача між людьми під час покупок у магазинах — 0,6 %. Люди, заражені SARS-CoV-2, можуть виробляти як великодисперсні аерозолі (краплі), так і дрібнодисперсні аерозолі, але більшість цих виділень не заражають інших людей. Ця закономірність здається стосується тільки тих респіраторних виділень, які швидше падають на землю у вузькому радіусі від зараженої людини, і не тих дрібнодисперсних аерозолів із вірусами, що залишаються суспендованими годинами у повітрі на рівні обличчя, де їх може вдихнути будь-хто. Винятком може стати тривале потрапляння інфікованої людини в погано провітрюване приміщення, що дозволяє інакше накопичувати незначну кількість аерозолів, що містять віруси. На користь дрібноаерозольної передачі начебто свідчать задокументовані випадки спалахів серед учасників хору, відвідувачів ресторанів та офісних працівників, які перебували в закритих приміщеннях. Однак, виходячи із загальновідомої передачі SARS-CoV-2, ці випадки є швидше винятком, ніж правилом. Крім того, важко визначити заднім числом усі потенційні взаємодії між людьми, які могли статися до, під час та безпосередньо після цих контактів. Не можна недооцінювати потенційну здатність коронавірусів широко та швидко поширюватися серед груп у закритих середовищах за допомогою декількох шляхів: на основі експериментів, що використовували мічені фаги, показано, що віруси можуть поширюватися від однієї забрудненої коронавірусами дверної ручки або від забруднених рук лише однієї зараженої людини до здорових людей і обладнання в усій офісній будівлі впродовж кількох годин.
Кількість людей, яких заражає одна хвора на коронавірусну хворобу 2019 людина, оцінюється від 2 до 3. Так само відбувається при грипі й це зовсім відрізняється від тих хвороб, де йде поширення через дрібнодисперсні аерозолі, зокрема як при кору, де кількість заражених близька до 18. Враховуючи, що більшість хворих із коронавірусною хворобою 2019 заразні близько 1 тижня, кількість заражень від 2 до 3 є досить невеликою, враховуючи велику кількість контактів, які більшість людей мають за звичайних обставин життя впродовж 7 днів. Або кількість SARS-CoV-2, необхідна для спричинення хвороби, значно більша, ніж при кору, або дрібнодисперсні аерозолі не є домінуючим шляхом передачі. Наявні на 2024 рік дані рандомізованих досліджень і мета-аналізів свідчать про те, що передача на основі дрібнодисперсних аерозолів все-таки не є переважним шляхом передачі SARS-CoV-2.[92].
Аерозолі, що утворюються при стисканні грудної клітки та спробах вентиляції у пацієнтів із зупинкою серця, можуть призвести до зараження збудниками повітряно-крапельних інфекцій, в тому числі й SARS-CoV-2. Відповідно, тимчасові міжнародні вказівки з реанімації обмежили базове забезпечення життєдіяльності рятувальниками непрофесіоналами лише стисненням грудної клітки та використанням автоматизованого зовнішнього дефібрилятора під час пандемії коронавірусної хвороби 2019[93]
Ступінь активності цього механізму визначається як в'ялий, не такий активний як під час грипу. Потужним джерелом інфекції стали діти, у яких переважає безсимптомна форма. Індекс контагіозності доходить до 50 %, тоді як при кору досягає 95 %. Для оцінки контагіозності епідеміологи використовують математичні формули з чіткими та прийнятними припущеннями для обчислення показника заразливості. З цією метою обчислюється «базовий показник відтворення» (R0), і він вказує на очікувану кількість випадків, які безпосередньо заражаються від одного джерела інфекції в популяції (при тому, що до цієї хвороби, як вважається, мають бути чутливі всі). При SARS / ТГРС та БКРС цей показник приблизно дорівнює 2, що вказує на те, що кожна заражена людина може ефективно заразити в середньому двох людей при близькому контакті. Різні дослідження показують коливання цього показника в широких межах — 1,95[94], 2,2[95], 3,28[96] аж до 6,47[97]. Така різниця обчисленого базового показника відтворювання пояснюється тим, що використовувалися різні методи обчислення та проводилися розрахунки в різний час пандемії[48]. Проведені дослідження показують, що активна передача коронавірусу майже в половині випадків обумовлена безсимптомними поширювачами[98]. З появою варіанту «Омікрон» індекс контагіозності збільшився, проте не досягає такого рівня як при кору[99]
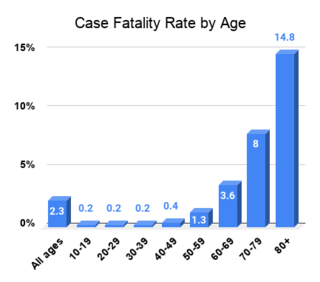
Виявлені показники летальності — 1,0 % серед дорослих у віці 50–59 років, 3,5 % серед 60–69 років, 12,8 % серед 70–79 років і 20,2 % серед 80 років і старше. Серед тяжкохворих, як повідомляється, летальність досягає 50 % серед дорослих у віці 40–49 років і 87,5–100 % серед тих, хто старше 70 років. Точний рівень загальної летальності в світі невідомий — хоча деякі моделі, що містять легкі та безсимптомні випадки, оцінюють його у 0,5-1 %[91].
Не виключається можливість зараження через потрапляння аерозолів на кон'юнктиви[100], хоча ймовірним отут є зараження внаслідок торкання пальцями до повік, які забруднили виділення від хворого, або потирання їх, а потім несвідоме перенесення вірусу забрудненими пальцями до губ і надалі вдихання у дихальні шляхи.
Виявлено, що більші концентрації вірусу у підтверджених випадках виділяються з дихальних шляхів на ранніх стадіях захворювання, а з перебігом хвороби концентрація вірусу різко знижується. Передачі сприяє тривалий тісний контакт із хворим в одному приміщенні, відстань до 1-2 м. Факторами передачі можуть бути харчові продукти та предмети побуту, що контаміновані (забруднені) SARS-CoV-2. Наразі не виявлено доказів того, що SARS-CoV-2 може передаватися іншими механізмами передачі інфекції через сечу, кал, кров, грудне молоко[88]. Проте не виключається трансплацентарна передача вірусу від матері до плода через білок NRP1[101].
Сприйнятливість, фактори ризику
Поки що достеменно не визначено ступінь сприйнятливості. Досліджується питання того, чи захищають від коронавірусної хвороби 2019 антитіла до людських коронавірусів, які є у 80 % людей у світі. Виявлено, що Т-клітини перехресно-реактивної пам'яті, які з'являються у людей через захворювання протягом життя незоонозними коронавірусними інфекціями, здатні певною мірою захистити тих осіб, що контактували з хворими на підтверджену коронавірусну хворобу 2019[102]. Найуразливішим контингентом наразі вважаються курці[103], у них за результатами численних проведених метааналізів передбачається частий тяжкий перебіг[104]; особи чоловічої статі, люди азійської етногрупи, похилого віку[105] й особи з тяжкими фоновими хворобами (цукровий діабет, есенціальна артеріальна гіпертензія тощо) і значними зрушеннями в імунній системі, люди старші 60-65 років. Завданням профілактики є захист людей з цих категорії ризику, адже їх кількість досягає багатьох сотень мільйонів осіб на Землі[106]. Великий ризик мають медичні працівники, особливо лікарі, що безпосередньо і тривалий час контактують із хворими, в них він увосьмеро більший, ніж у звичайного населення. Виявлено часте внутрішньолікарняне інфікування як медичних працівників, так і пацієнтів, які перебували з іншими респіраторними захворюваннями в лікарні. Тривалість імунітету після перенесеної хвороби невідома. ВООЗ виступила із заявою, що хоча уряди деяких країн припускають, що виявлення антитіл до SARS-CoV-2 може послужити основою для «імунного паспорта» або «сертифіката відсутності ризику», наразі немає доказів того, що люди, які одужали від коронавірусної хвороби 2019 і мають антитіла до коронавірусу, захищені від повторної інфекції[107].
Розглядаються фактори, що можуть сприяти зараженню і тяжкості клінічного перебігу коронавірусної хвороби 2019. Зокрема досліджується вплив у різних країнах вакцинації людей БЦЖ на зменшення рівня захворюваності та летальності[108][109], різних факторів довкілля на летальність[110][111][112][113][114][115]. Зокрема проведене дослідження порівняння між картографічним рівнем забруднення повітря оксидом азоту (NO2) в тропосфері регіонів і рівнем летальності від коронавірусної хвороби 2019 там. Результати застосування просторового аналізу показали, що із 4443 випадків смертей 3487 (78 %) були у п'яти регіонах, розташованих на півночі Італії та центральній Іспанії. Крім того, в тих самих п'яти регіонах спостерігаються найвищі концентрації NO2 у поєднанні із сталими низхідними потоками повітря, що запобігає ефективному розпорошенню забруднення повітря. Отримані результати на думку автора свідчать про те, що тривалий вплив NO2 може бути одним із найважливіших факторів високого рівня смертей від COVID-19 у цих регіонах та, можливо, у всьому світі[116]. Дослідження, проведені в Китаї, не показали зв'язку температури довкілля з кількістю захворілих, робиться висновок, що немає жодних доказів того, що кількість випадків COVID-19 може знизитися, коли погода стане теплішою[110]. Дослідження іранських науковців виявило, що наростання випадків захворювання відбувається швидко в густонаселених районах при слабкому вітрі, високій вологості та низькому рівні сонячного опромінення[111]. Дослідження турецьких науковців також свідчать про роль вітру та температурних показників у збільшенні захворюваності в 9-ти містах Туреччини[112]. Підозрюється, що повсюдно поширений забруднювач повітря твердими частками, який називається PM2.5, може бути учасником природного відбору вірусу SARS-CoV-2 з подальшою появою його варіантів[117].
Метааналіз даних серед жінок репродуктивного віку виявив, що відносно грипу порівняно з коронавірусною хворобою 2019 вагітність пов'язана із семикратно більшим ризиком госпіталізації, проте меншим ризиком потрапляння до відділення інтенсивної терапії та меншим ризиком смерті[118]. Загальна кількість померлих вагітних від коронавірусної хвороби 2019 є малою[119]. Клінічні особливості перебігу коронавірусної хвороби у вагітних включають гарячку та кашель, проте значно рідше, ніж у хворих невагітних жінок. Ятрогенні передчасні пологи є основним несприятливим акушерським результатом. Поточні дані не свідчать про можливість вертикальної передачі коронавірусу в третьому триместрі вагітності[120].
Генетичне дослідження визначило кластер генів у хромосомі 3 людини як предиктор ризику дихальної недостатності при коронавірусній хворобі 2019. На основі проведеного нового дослідження, яке включало 3199 госпіталізованих пацієнтів виявило, що це основний генетичний фактор ризику тяжкої форми та госпіталізації. Було показано, що ризик несе геномний сегмент ~ 50 кб, який успадковано від неандертальців, і який мають у XXI столітті близько 50 % людей у Південній Азії та 16 % людей у Європі, тоді як серед жителів Центральної Африки і Східної Азії такого геномного сегмента майже немає[121][122].
Науковці британського Центру вірусних досліджень Університету Глазго провели дослідження і пояснили, чому частина населення планети може виявитися несприйнятливою до коронавірусної хвороби 2019. На їхню думку, за це відповідає мутація в гені OAS1. Внутрішньоклітинний противірусний захист може не тільки створювати природний імунітет до SARS-CoV-2, але і пригнічувати реплікацію вірусів, тобто знижувати тяжкість захворювання. На основі скринінгу експресії генів, стимульованих інтерфероном, виявлено, що OAS1 через РНКазу L сильно інгібує SARS-CoV-2. Йдеться про пренілірований ген, до білку якого приєднана одна молекула жиру. У госпіталізованих пацієнтів експресія пренілірованого OAS1 асоціювалася із захистом від тяжкого перебігу хвороби, що свідчить про те, що цей противірусний захист є основним компонентом захисної противірусної відповіді. Якщо ж OAS1 не є пренілірованим, то він фактично не реагує на SARS-CoV-2 і не може надіслати сигнали імунній системі[123].
Дослідження Техаської медичної асоціації США показали, що:
Ризик зараження
- найбільший ризик зараження звичайних людей (9 балів) виникає:
- під час відвідування бару;
- релігійної служби, в якій бере участь більше 500 людей;
- похід на спортивне змагання на стадіоні.
- Трохи менше вони оцінили ризик зараження (8 балів за їхньою градацією) для:
- відвідування велелюдного музикального концерту;
- парку розваг;
- обіду в їдальні чи ресторані всередині;
- тренування у спортзалі.
- У 7 балів оцінено ризик зараження під час:
- обіймів чи рукостискання;
- гри у футбол;
- гри у баскетбол;
- польоті в літаку;
- участі у поховальній церемонії;
- харчування в ресторані на зовнішньому майданчику,
- перебуванні у перукарні.
- У 6 балів ризику оцінено:
- відвідування родичів похилого віку в їхніх помешканнях;
- плавання у громадському басейні;
- тижнева праця в офісному приміщенні;
- контакт з дітьми в школі, дитячому таборі або щоденний догляд за ними.
- У 5 балів ризику оцінено:
- покупки на пошті;
- похід на пляж;
- відвідування місця, де готують барбекю;
- їда в чужому будинку.
- У 4 бали оцінено:
- перебування впродовж однієї години на дитячому майданчику;
- похід до ділового центру міста;
- відвідування бібліотек чи музеїв;
- очікування прийому у лікаря;
- перебування в готелі більше двох ночей.
- У 3 бали дослідники оцінили:
- гру в гольф;
- прогулянку, заняття бігом чи їзду на велосипеді;
- похід до продуктових магазинів і ринків.
- У 2 бали оцінено ризик:
- проживання в кемпінгу;
- гри в теніс;
- перекачування бензину;
- отримання їжі з ресторану на винос.
Найнижчий ризик при відкриванні поштового листа — 1 бал.[124][125]
Патогенез
Узагальнити
Перспектива
Дослідження патогенезу коронавірусної хвороби 2019 широко проводяться у світі, але отримані результати часто суперечливі, мають попередній характер. Поки що не є зрозумілим, чому деякі пацієнти реагують на Sars-Cov-2 занадто слабо, а інші навпаки занадто сильно. Чи Т- і В-клітинна відповідь у периферичній крові показує міру імунних процесів у дихальній системі, куди потрапляє Sars-Cov-2. Не прояснено, чи є корисними або шкідливими імунні реакції при цій хворобі[126].
Патофізіологія індукованого гострого респіраторного дистрес-синдрому при цій хворобі: у пацієнтів спостерігається інтенсивна дисфункція ендотелію з тромбозапальним станом. Виявлено багато механізмів порушення регуляції легеневої перфузії: скасування гіпоксичної легеневої вазоконстрикції, надмірної легеневої вазоконстрикції; і мікротромбоз або макротромбоз, що призводить до збільшення мертвого (не дихаючого) простору легень. Легеневий мікротромбоз і пошкодження ендотелію, що призводить до невідповідності вентиляції перфузії, гіпоксемії та розширенню судин[127].
Взаємодія з рецепторами ангіотензин-перетворюючого ферменту II і ураження легень
Дослідження показали, що SARS-CoV-2 використовує для потрапляння в клітини-мішені ті самі рецептори ангіотензин-перетворюючого ферменту II (АПФ) ACE2, що і збудник тяжкого гострого респіраторного синдрому SARS-Cov[128]. Ґрунтуючись на загальнодоступній базі даних, найсучаснішій одноклітинній RNA-секвенуючій техніці, проаналізовано профіль експресії РНК ACE2 у здорових легенях людини. Результат вказує на те, що рецептори вірусу сконцентровані в невеликій частці альвеолярних клітин типу II (АТ2), основна функція яких — синтез у пластинчатих тілах сурфактанта. Виявлено, що ця популяція АТ2 також сильно експресувала багато інших генів, які регулювали розмноження та передачу вірусів.
Існуюча артеріальна гіпертензія є відомим фактором ризику розвитку тяжкого перебігу коронавірусної хвороби 2019. Аномальна активація ангіотензинових рецепторів підвищує рівень ангіотензину II і сприяє тяжким проявам. Інгібітори рецепторів ангіотензину-ІІ є основою антигіпертензивної терапії, сучасна медична практика у 2021 році не рекомендує зменшувати їх прийом для захисту хворих на гіпертонічну хворобу. Навпаки, існують клінічні дані, що підтверджують сприятливий ефект їх у пацієнтів з артеріальною гіпертензією в розпал пандемії, хоча точний механізм цього неясний. Є припущення, що вони зменшують ступінь тяжкості коронавірусної хвороби 2019, сприяючи формуванню комплексу ACE2-AT1R на поверхні клітини, де AT1R опосередковує основні вазопресорні ефекти ангіотензину II. Припускається, що взаємодія між ACE2 та AT1R перешкоджає зв'язуванню SARS-CoV-2 з ACE2, тим самим дозволяючи ACE2 перетворювати ангіотензин II на корисніший ангіотензин I, який має судинорозширювальну та протизапальну активність[129].
Вагітність є фактором ризику сприйнятливості та несприятливих наслідків при грипі та тяжких формах ГРВІ, при цьому поточні дані суперечать тому, що інфекція SARS-CoV-2 під час вагітності є тяжчою, ніж у загальній популяції, з відносно низьким рівнем смертності матерів і плодів чи новонароджених. Вірусне навантаження може призвести до зменшення доступних рецепторів АПФ-2, посилюючи таким чином патологічне звуження судин (вазоконстрікцію), фіброз, запалення та тромботичні процеси. Припускається, що нормальний стан вагітності із сильно експресованими рецепторами АПФ-2 призводить до значного розширення судин (вазодилатації) та протизапальної реакції на інфекцію SARS-COV-2. Таким чином, така регуляція рецепторів АСЕ-2 під час вагітності насправді може бути захисною[130].
Сидячий спосіб життя збільшує ризик госпіталізації із приводу коронавірусної хвороби 2019 незалежно від інших чинників. Існує достатня кількість статистичних даних, які показують, що фізичні вправи запобігають тяжкому перебігу цієї хвороби. Стверджується, що інтенсивні фізичні навантаження через гіпоксію крові збільшують експресію трансмембранного ангіотензинперетворюючого ферменту 2 (tACE2) в ендотелії судин, збільшуючи ризик розвитку тяжкого перебігу, особливо у нетренованих осіб. З іншого боку, вправи помірної інтенсивності збільшують у крові концентрацію розчинного ангіотензинперетворюючого ферменту 2 (АПФ2), який чинить захист при зараженні SARS-CoV-2 і може запобігти ускладненням[131].
Цитокіни та інші фактори запалення
Певну роль у виникненні тяжких уражень у деяких хворих ймовірно відіграє збільшення рівня цитокінів. Вторинний гемофагоцитарний лімфогістіоцитоз (sHLH) є недостатньо розпізнаваним патофізіологічним синдромом надмірного запалення, що характеризується фульмінантною та фатальною гіперцитокінемією. Виникає поліорганний збій. У дорослих найчастіше це відбувається при вірусних інфекціях і у понад 40 % випадків сепсису. Профіль цитокінів, що корелює з тяжкістю захворювання на коронавірусну хворобу 2019, характеризується у 50 % випадків вкрай тяжкого клінічного перебігу цієї хвороби підвищенням рівнем інтерлейкінів IL-2, IL-7, гранулоцит-колоніального стимулюючого фактору, гамма-інтерферон індуцибельного протеїну 10, моноцитарного гемоатрактанту протеїну 1, макрофагального запального протеїну 1-α і фактору некрозу пухлини-α. Разом із тим виникає значна лейкопенія[132]. Постійно високий рівень трьох цитокінів (CXCL10, CCL7 та антагоніст рецепторів IL-1) був пов'язаний із збільшенням вірусного навантаження, порушенням функції легень, пошкодженням їх та смертю[133][134]. Виявлено кілька ознак, притаманних хворим із тяжким клінічним перебігом: високий рівень системних цитокінів чи хемокінів, як то IL-6, CXCL8, CXCL9 і CXCL10, зрушення індукції та синтезу інтерферону I-го типу. Все це здатне впливати на Т-клітинну відповідь[126].
Хоча основна маса цитокінів, вироблення яких стимулює SARS-CoV-2, є значущими у процесі посилення запалення, але, ймовірно, вони не мають важливого значення для виведення (кліренсу) вірусу. Ймовірно, вірусний кліренс переважно залежить від таких цитокінів, як IL-15, інтерферони типу I та гамма-інтерферону[135]. Виявлене значне підвищення рівня білка галектіна-9 у плазмі крові, кореляцію його концентрації та рівня прозапальних цитокінів[136].
Однак наразі є думки, що сучасних даних недостатньо для встановлення точної ролі та обсягу нерегульованих цитокінових відповідей у хворих на коронавірусну хворобу 2019. Видається, що порівняно з іншими причинами ГРДС, при коронавірусній хворобі 2019 клінічний перебіг характеризується нижчими рівнями цитокінових реакцій. Слабко визначений патофізіологічний суб'єкт як «цитокіновий шторм», який виникає через неадекватну реакцію макрофагів. Йому бракує чіткого біологічного підґрунтя, що може лише ще більше збільшити невизначеність щодо того, як найкраще сприйняти патогенез цієї хвороби і ускладнення ГРДС. Показово, що піковий рівень IL-6 у плазмі крові у пацієнтів, у яких розвинувся ГРДС після лікування Т-клітинами химерних антигенних рецепторів, становив приблизно 10000 пг / мл, що майже в 1000 разів вище, ніж при тяжкому клінічному перебігу коронавірусної хвороби 2019. Проявами підвищеного рівня медіаторів у передбачуваній бурі цитокінів, найімовірніше, є дисфункція ендотелію та системне запалення, що призводить до гарячки, тахікардії, тахіпное та артеріальної гіпотензії. Це сполучення симптомів вже давно входить до поняття «синдром системної запальної відповіді». Хоча термін «цитокінова буря» викликає драматичні образи і привертає увагу загальних і наукових засобів масової інформації, сучасні дані не дають змоги повноцінно його використовувати. Поки нові дані не встановлять інше, зв'язок цитокінової бурі з коронавірусною хворобою 2019 може бути не що інше, як «буря в стакані»[137].
За думкою Інституту здоров'я США у пацієнтів із коронавірусною хворобою 2019 може бути підвищений рівень прозапальних і протизапальних цитокінів, що раніше називалося «синдромом вивільнення цитокінів» або «цитокіновим штормом», хоча це неточні терміни. Зрештою вживання цих термінів при коронавірусній хворобі 2019 є помилковим, оскільки величина збільшення цитокінів у пацієнтів із цією хворобою є меншою порівняно з такою у хворих на багато інших тяжких захворювань, як от при сепсисі[138].
Пролактин
Зниження рівня пролактину в крові у пацієнтів з ожирінням та у дорослих чоловіків підвищує сприйнятливість і тяжкість коронавірусної хвороби 2019. Є думки, що курці сигарет, діти та вагітні через підвищення рівня пролактину мають низький ризик зараження SARS-CoV-2[139]. Проте різні дослідження показали, що секреція пролактину пригнічена у хронічних курців сигарет[140]. Хронічний вплив нікотину пригнічує секрецію пролактину шляхом активації нікотинових рецепторів нейронів дофаміну, вивільняючи його як фактор інгібітору пролактину. Виявлено, що нікотин може зменшити експресію гена пролактину в клітинних лініях гіпофіза пацюків[141]. Рівень пролактину нижчий у курців порівняно з некурцями. Крім того, виявлено значне зниження концентрації пролактину у жінок, які палять під час вагітності та годують груддю[142].
Однак деякі інші дослідження показали, що секреція пролактину збільшується після паління. Незважаючи на захисний ефект паління від SARS-CoV-2, він є значним фактором ризику бактеріальних і вірусних інфекцій. Повідомлялося, що курці удвічі більш схильні до розвитку пневмонії та 5 разів — до грипу. Показане, що куріння пов'язане з тяжчим перебігом коронавірусної хвороби 2019, більшим ризиком потрапляння в реанімацію та більшою летальністю. Курці частіше потребують госпіталізації порівняно з некурцями[143]. Деякі дослідження показали, що базальні концентрації пролактину подібні у людей з ожирінням і нормальною вагою, тоді як інші показали наявність високих рівнів або ж низьких у людей з ожирінням. Однак хронічне запалення, порушення імунної відповіді, зміна мікрофлори кишки, висока експресія ACE2, резистентність до інсуліну, гіперглікемія, надлишок жиру, стійкість до лептину та зниження адипонектину роблять пацієнтів з ожирінням сприйнятливими до коронавірусної хвороби 2019[144]. Хоча вагітні мають високий рівень пролактину, вони сприйнятливіші до SARS-CoV-2 порівняно із загальною популяцією. Повідомлено, що вагітні та невагітні мають практично однакову сприйнятливість[145].
Запалення судин і коагулопатичні зрушення
Значну роль у патогенезі хвороби відіграють зміни коагулопатійного характеру, запалення ендотелію судин, що призводить часто до тромбоемболічних ускладнень. Наразі відомо, що SARS-CoV-2 використовує для проникнення в клітину рецептор ангіотензинперетворювального ферменту-2, що є на клітинах легеневих альвеол, обумовлюючи пошкодження легень. Цей рецептор є також на ендотеліоцитах, які вистилають кровоносні судини багатьох органів. Доведено, що SARS-CoV‑2 може безпосередньо інфікувати епітеліоцити кровоносних судин людини in vitro. Пряме ураження ендотеліоцитів SARS-CoV-2 чи їхнє опосередковане ушкодження імунними клітинами, цитокінами і вільними радикалами може призвести до вираженого порушення функції ендотелію. Ендотелій судин вважається активним паракринним, ендокринним та автокринним органом, що бере активну участь у регуляції тонусу кровоносних судин і підтримці їхнього гомеостазу. Ендотеліальна дисфункція, що розвивається при цій хворобі, спричинює порушення мікроциркуляції, вазоконстрикцію з подальшою ішемією органів, запаленням і набряком тканин, прокоагуляцію. Ендотеліїт може зумовити системні порушення мікроциркуляції в різних судинних руслах, їхні клінічні наслідки у хворих із коронавірусною хворобою 2019. Дисфункція ендотелію диктує необхідність використання відповідного лікування для нормалізації можливостей ендотелію під час боротьби з реплікацією збудника, особливо терапії протицитокіновими препаратами, інгібіторами АПФ і статинами. Таке стратегічне направлення особливо актуальне для захворілих, які мають вагомі фактори ризику дисфункції ендотелію (артеріальна гіпертензія, цукровий діабет, ожиріння та серцево-судинні захворювання, паління). Дисфункція ендотелію і хронічне запалення йдуть з гіперкоагуляцією, супроводжуються підвищенням рівня фібриногену, зниженням процесів фібринолізу й антикоагуляції, що й зумовлює зрештою утворення тромбів[146].
Не виключається, що частково в цій ситуації діє механізм системного розладу через відкладання в дрібних кровоносних судинах IgA і компонента системи комплементу, як це відбувається при геморагічному васкуліті[147]. Розтини померлих показали, що у легенях відбуваються тяжке ураження ендотелію, пов'язане з вірусом SARS-CoV-2 та порушенням мембран ендотеліальних клітин; поширений судинний тромбоз із мікроангіопатією та оклюзією альвеолярних капілярів; значне утворення нових судин через механізм, який називається інтуссептичним ангіогенезом, що в цілому робить хворобу тяжчою ніж грип. Розвивається часто атипова пневмонія[148][149], яка маніфестується при тяжкому перебігу наприкінці 1-го тижня хвороби, на 2-му тижні, але з переважанням циркуляції світі дельта варіанту SARS-CoV-2, іноді вже на 3-й добі хвороби.
Брадикінін
Висунута гіпотеза про можливу дію при коронавірусній хворобі 2019 на кровоносні судини великої кількості брадикініну, який активно виробляється під впливом SARS-CoV-2. Дослідники на основі розрахунків суперкомп'ютера в Oak Ridge National Lab у Тенессі зробили висновок, що SARS-CoV-2 запускає механізм активізації клітин, що експресують АСЕ2 навіть у тих структурах, де в нормі таких клітин мало і їхня активність мінімальна. Це призводить до викиду великої кількості брадикініну, що спричинює універсальне ураження кровоносних судин багатьох органів (легені, кишка, серце тощо) з виходом у простір навколо судин рідини, що створює набряк. Брадикінін збільшує проникність гематоенцефалічного бар'єра, що на думку дослідників саме призводить до частих при цій хворобі порушень роботи головного мозку, психотичних розладів. Дослідники вважають, що зміни цитокінів не є головними при коронавірусній хворобі 2019, а в кращому випадку, вони є додатковим фактором до дії брадикінину.[150][151].
Триптофан і серотонін
Дефіцит серотоніну погіршує гіпоксемію та пригнічує гіпоксичне звуження судин легень, що призводить до посилення тяжкості захворювання. У хворих на коронавірусну хворобу 2019 виявлено дефіцит триптофану, через те, що АПФ2, який є ключовим фактором всмоктування триптофану з їжі, значно зменшується у пацієнтів, тому що SarS-CoV-2 використовує АСЕ2 як рецептор для входу в клітини-мішені. Дефіцит триптофану призводить до дефіциту серотоніну у таких пацієнтів, оскільки триптофан є попередником його синтезу. Крім того, у пацієнтів може знизитися рівень протизапального мелатоніну (синтезованого з серотоніну) та нікотинаміду аденіндінуклеотиду, що виробляється з ніацину, попередником якого є триптофан. Селективні інгібітори зворотного захоплення серотоніну можуть не дуже допомогти у виправленні дефіциту його під час хвороби, адже їхня ефективність значно знижується, коли в організмі недостатньо триптофану. Тому тільки збільшення його концентрації під час хвороби здатне покращити її перебіг[152].
Ураження органів та інших систем організму
Легені
Оксидативний стрес грає важливу роль у патогенезі коронавірусної хвороби 2019, збільшуючи наслідки цитокінових зрушень, посилюючи згортання крові та гіпоксію, що спричинює пошкодження тканин і органну недостатність. SARS-CoV‑2 здатний порушити рівновагу між ядерним фактором транскрипції NF‑κB, що задіяний в експресії цитокінів, і активацією Nrf2, що експресує антиоксидантні ферменти. Виникає перехресний зв'язок між цитокіновими зрушеннями і оксидативним стресом. Ці зміни здатні грати важливу роль у виразності симптомів у хворих. Таким чином модель патогенезу коронавірусної хвороби 2019 йде з первинним ураженням легень і пізньою гематологічною, тканинною гіпоксемією та мітохондріальною дисфункцією внаслідок оксидативного стресу.
Основними ланками патоморфології і патогенезу інтерстиціальної пневмонії при коронавірусній хворобі 2019 є дизрегуляторна активація системи моноцитарних фагоцитів, поява генералізованого тромбозу на рівні мікроциркуляторного русла, прогресуючий внутрішньоальвеолярний та інтерстиціальний легеневий фіброз.
У відповідь на проникнення SARS-CoV‑2 під час ексудації та проліферації превалює Т‑клітинний імунітет. При зміни їх на фіброз загальна кількість Т‑лімфоцитів різко знижується, тоді як клітини гуморального імунітету ще не з'являються. Переважання CD8+ Т‑лімфоцитів-супресорів над CD4+ Т‑лімфоцитами-хелперами, ймовірно, пов'язане з механізмами автоімунного пошкодження[146]. Лімфопенія у хворих може свідчити як про гіперактивацію і міграцію лімфоцитів до легень, так й про апоптоз і супресію Т-лімфоцитів. Аналіз РНК-послідовностей верхніх дихальних шляхів у них виявив, що в разі тяжкого клінічного перебігу хвороби рівень цитотоксичних Т-лімфоцитів значно знижується порівняно з таким у хворих із середньотяжким перебігом[126].
Пошкодження легень через безпосереднє ураження SARS-CoV‑2 і цитокінами ендотелію судин та клітин альвеол і міжальвеолярних перегородок призводить до появи рентгенологічного симптому «матового скла» формування інтерстиціальної пневмонії, активації фіброзоутворення, а також зниження функції легень[146].
Особливостями дифузного альвеолярного ураження є 3 фази патоморфогенезу інтерстиціальної пневмонії при коронавірусній хворобі 2019:
- фульмінантна (блискавична) — до 10 діб; відповідає ексудативній і проліферативній стадіям гострого респіраторного дистрес-синдрому, хоча є заперечення, що при цій хворобі формується цей синдром (принаймні спочатку), а йде особлива пневмонія[153][154][155][156];
- персистувальна — 11-20-та доба; відповідає проліферативній стадії гострого респіраторного дистрес-синдрому;
- фібротична — знайдена у хворих, які померли на 21-45-ту добу; відповідає стадії організації гострого респіраторного дистрес-синдрому[146].
Звичайними проявами в госпіталізованих хворих є дихальна недостатність, сухий кашель, задишка й зміни легень при комп'ютерній томографії у вигляді помутніння та / або ущільнення у вигляді «матового скла». Під час гострої фази переносимість фізичного навантаження не можна оцінювати за допомогою стандартних тестів, як тест із 6-хвилинною ходьбою[146].
Під час поширення дельта-варіанту Sars-Cov-2 пневмонія виникає й розвивається досить швидко на 3-4-й день у окремих хворих, які ймовірно отримали велику дозу збудника. У таких випадках пневмонія перебігає іноді без підвищення прозапальних маркерів, зокрема, СРБ. Зазвичай при такому клінічному перебігу характерна відразу висока температура тіла, виражений інтоксікаційний синдром. Це може призводити до падіння сатурації вже на 4-5-й день від початку хвороби[157].
Є спостереження, що поширеність хронічного обструктивного захворювання легень (ХОЗЛ) значно нижча, ніж інших супутніх хвороб серед пацієнтів із коронавірусною хворобою 2019. Таке ж спостерігалося і спостерігається з іншими коронавірусними хворобами, як то тяжкий гострий респіраторний синдром і близькосхідний коронавірусний респіраторний синдром, але не є при інших ГРВІ, як то грип та респіраторно-синцитіальна інфекція. Обговорюється, що однією із загальноприйнятих причин низького рівня ХОЗЛ серед пацієнтів із коронавірусною хворобою 2019 є використання інгаляційних кортикостероїдів або бронходилататорів, які можуть захистити від коронавірусу. Інша можлива причина — це те, що легені у такого хворого можуть не сприяти тяжкому перебігу коронавірусної хвороби 2019. ХОЗЛ спричинює закупорки слизом великих і дрібних дихальних шляхів, що може перешкоджати проникненню SARS-CoV-2 у глибші відділи легень — альвеоли. Таким чином, SARS-CoV-2 може локалізуватися лише у верхніх дихальних шляхах людей із ХОЗЛ, спричинюючи легкі або безсимптомні форми, що не потребують медичної допомоги. Навіть якщо SARS-CoV-2 досягне альвеол, клітини в них, ймовірно, піддаються тяжкому стресу ендоплазматичного ретикулуму і сильно пошкоджуються там, що не дає підтримувати ефективну реплікацію вірусу[158].
Серцево-судинна система
SARS-CoV‑2 здатний вплинути на серцево-судинну систему численними шляхами, він ускладнює вже наявні серцево-судинні хвороби або ж зумовлює розвиток нових. У таких пацієнтів описано багато випадків серцевих хвороб, їхніх ускладнень, включаючи серцеву недостатність, особливо у госпіталізованих хворих, і кардіоміопатію. Припускається, що вона розвивається внаслідок прямої дії вірусу та / чи токсичних ефектів цитокінів, що утворюються під час перебігу хвороби. У численних пацієнтів під час гострої фази захворювання розвивається тромботичний стан, який може призвести до тромбоемболії легеневої артерії, утворення тромбів у коронарних судинах і загострення ішемічної хвороби серця. Найбільшому ризику наражаються пацієнти із серцево-судинними факторами ризику, тобто чоловіки, хворі на цукровий діабет, артеріальну гіпертензію й ожиріння, ті, у яких є фонові серцево-судинні хвороби[146].
Нервова система
Значне системне запалення, пов'язане із вродженим імунітетом, що провокується зв'язуванням спайкового білка SARS-CoV‑2 S1 з експресувальними АПФ-2-клітинами, нейросудинною дисфункцією ендотелію, пошкодженням гематоенцефалічного бар'єра потенційно спричинює розвиток ускладнень центральної нервової системи[146].
Цитокіни здатні збільшувати проникність гематоенцефалічного бар'єру, забезпечуючи проникнення вірусу в мозок. Потрапляючи до ЦНС вірус може інфікувати астроцити й мікроглію, активуючи каскад нейрозапалення та нейродегенерації через вивільнення фактора некрозу пухлини, цитокінів та інших медіаторів запалення[146].
Є непрямі механізми залучення мозку, які включають:
- порушення регуляції цитокінів — доведено, що прозапальні, як то інтерлейкін-6 і фактор некрозу пухлин, пов'язані з розвитком енцефаліту на тлі цитокінового шторму;
- міграцію імунних клітин із периферії за механізмом «троянського коня», що спричинює запалення у нервових клітинах і вірус-індуковану невропатію;
- автоімунну агресію;
- гіпоксичну травму через безпосередній вплив SARS-CoV‑2 на дихальний і серцево-судинний центри довгастого мозку. Гіпоксія головного мозку спричинює активацію анаеробного метаболізму, через що й виникає набряк мозку, знижується мозковий кровоток, підвищується внутрішньочерепний тиск, розвиваються неврологічні та психіатричні прояви;
- тромботичну мікроангіопатію, що спричинює продукування антитіл проти кардіоліпіну, ушкодження мозку за участю антифосфоліпідних антитіл[146].
Є припущення, що розвиток агевзії пов'язаний з дією SARS-CoV-2 на відповідні центри у головному мозку. Цей коронавірус можливо спричинює ураження ядер деяких черепних нервів, з чим і, зокрема, пов'язують агевзію.
Також SARS-CoV‑2 може спричинити тяжкі ураження мозку (інсульти, енцефаліти тощо) у пацієнтів, які страждають неврологічними розладами, включаючи параною і галюцинації[159]. Спостерігаються й численні поведінкові відхилення, які свідчать про ураження головного мозку[160] За аналогією з іншими коронавірусними хворобами науковці прогнозують довгострокові наслідки запалення головного мозку у окремих хворих[161]. Магнітно-резонансна томографія виявила у низки пацієнтів високий ступінь ураження білої речовини головного мозку, проте питання чи це ураження, яке спричинює власне SARS-CoV-2, чи гіпоксія через пошкодження судин достеменно не вивчене[162]. Отримано підтвердження, що SARS-CoV‑2 може провокувати розвиток ще й енцефалопатії (незапального судинного ураження паренхіми мозку), менінгіту, гострого дисемінованого енцефаломієліту, судомних нападів, нейром'язових розладів як то синдром Гієна — Барре, полінейропатія, парези, атаксія. Частими неврологічними симптомами, які супроводжують коронавірусну хворобу 2019, є запаморочення, головний біль, порушення свідомості[146].
Ураження формених елементів крові
- «Еритроцитарна ланка»
Ураження SARS-CoV-2 асоціюється зі зниженням рівня кисню в крові навіть у пацієнтів без гіпоксії. Ця розбіжність ілюструє необхідність пояснення того, чи впливає вірус прямо чи опосередковано на еритропоез. Виявлено значно більшу кількість попередників еритроцитів — клітин CD71+ у циркуляції крові пацієнтів із коронавірусною хворобою 2019. Виявлено, що ці клітини мають виразні імунодепресивні властивості. Виявлено сильну негативну кореляцію між кількістю цих клітин зі співвідношеннями Т- і В-клітин у пацієнтів із коронавірусною хворобою 2019. Збільшення клітин CD71+ негативно корелювало з рівнем гемоглобіну. Субпопуляції еритроїдних клітин CD45+, CD71+ — клітин, що експресують ACE2, TMPRSS2, CD147 та CD26 можуть бути інфіковані SARS-CoV-2. У свою чергу, попередня обробка їх дексаметазоном суттєво зменшила експресію ACE2 / TMPRSS2 і згодом знизила їх зараженість SARS-CoV-2[163].
- «Тромбоцитарна ланка»
У пацієнтів із коронавірусною хворобою 2019 спостерігається вторинна імунна тромбоцитопенія, яка також називається імунною тромбоцитопенічною пурпурою або вторинним гемофагоцитарним лімфогістіоцитозом. Патогенез такої тромбоцитопенії при ураженні SARS-CoV-2 достеменно невідомий. Рідкісні випадки протромботичної імунної тромбоцитопенії, індукованої вакцинами на основі аденовірусів проти коронавірусної хвороби 2019 пов'язані з аутоантитілами, які націлені на фактор тромбоцитів 4 (PF4). Для пояснення етіології такої тромбоцитопенії у хворих вивчають потенційну участь гемофагоцитарних гістіоцитів, націлених на тромбоцити, атакованих аутоантитілами, що узгоджується зі спостережуваними аутоантитілами PF4 при вакцинальних реакціях[164].
Печінка
Виявлене у хворих із тяжким перебігом підвищення активності амінотрансфераз свідчить про розвиток щонайменше реактивного гепатиту. Загалом Sars-Cov-2 безпосередньо не чинить цитолітичної дії на гепатоцити, проте спричинений універсальний ендотеліїт ймовірно й породжує ураження паренхіми печінки. З'явилися припущення, що виявлені у березні -квітні 2022 року декілька 82 випадків у дітей гепатиту невиясненого походження з тяжким перебігом, що спостерігалися в Шотландії, Англії, Ірландії та Іспанії, де були виключені ураження відомими гепатотропними вірусами та печінковими отрутами, можуть бути спричинені спільною дією Sars-Cov-2 і аденовірусами[165].
Нирки
Ураження нирок наразі пов'язують з тим, що виникає індукований SARS-CoV-2 неадекватний імунний цитоліз через «бунт макрофагів», хоча це активно дискутується.
Обговорюється питання про те, що виникаюча поліорганна недостатність зумовлена не сепсисом, який нечасто приєднується при коронавірусній хворобі 2019, а універсальним ураженням судин в органах, яке спричинює SARS-CoV-2.
Шкіра
Летальність
На початку пандемії серед захворілих у Китаї згідно з даними Китайського Центру з контролю та запобігання хворобам (дослідження на більше ніж 70 тисяч уражених) у понад 80 % випадків хвороба перебігала без ускладнень, у 13,8 % випадків спостерігався тяжкий перебіг і лише 4,7 % випадків — критичний, загалом рівень летальності від Covid-19 становив 2,3 %. Найвищий рівень смертей серед пацієнтів із підтвердженим діагнозом — у людей, яким понад 80 років. Серед тих, хто помер, більше було чоловіків (2,8 %), ніж жінок (1,7 %)[167]. Однак подальший перебіг пандемії коронавірусної хвороби 2019 вніс коректив у гіпотезу про переважну ураженість осіб монголоїдної раси. Загалом під час подальшого поширення вірусу середня летальність сягнула 6,3 %[168].
Згідно з висновками ВООЗ, летальність при зараженні SARS CoV становила 10 %, а при MERS CoV досягає 36 %[169][170][171].
Упродовж останніх трьох місяців 2020 року, упродовж 2021 року спостерігається збільшення кількості померлих хворих із тяжким перебігом коронавірусної хвороби 2019 серед осіб молодших 60-ти років внаслідок циркуляції варіанту «Дельта». Нерідко вони не мають обтяжливого анамнезу.
Станом на 21 червня 2021 року летальність серед підтверджених випадків хвороби в світі дорівнює 1,89 %[172]. Згідно з подальшими спостереженнями з початком циркуляції варіанту «Омікрон» летальність не зростає[173]
Можливий зв'язок тяжкості уражень із групами крові
Не виключається можливість зв'язку тяжкості клінічного перебігу коронавірусної хвороби 2019 із групами крові людини. Ідентифіковано кластер генів 3p21.31 як локус генетичної чутливості у пацієнтів із дихальною недостатністю та підтверджено потенційне залучення до системи груп крові АВО. Генетичні дослідження свідчать, що наявність у людей групи крові O меншою мірою пов'язана з ризиком розвитку Covid-19, порівняно з людьми, у яких група крові A. Біологічні механізми, що лежать в основі цих знахідок, можуть мати відношення до групи АВО як такої, наприклад, через вироблення нейтралізуючих антитіл проти пов'язаних із білками N-гліканів або з іншими біологічними ефектами як то стабілізація фактора Віллебранда[174].
Формування імунітету
Розвиток імунітету до збудника через природно придбану інфекцію є багатоетапним процесом, який зазвичай відбувається впродовж 1-2 тижнів. Організм реагує на будь-яку вірусну інфекцію негайним неспецифічним процесом, в якому макрофаги, нейтрофіли та дендритні клітини сповільнюють прогресування вірусу і навіть можуть запобігти виникненню маніфестної хвороби. В організмі також утворюються Т-клітини, які розпізнають та усувають ті клітини, що заражені вірусом, створюючи клітинний імунітет. За думками деяких науковців існує ймовірність того, що такий неспецифічний захист від SARS-CoV-2 мають до 30-50 % людей[175]. Як показують лабораторні дослідження, нові мутаційні лінії SARS-CoV-2, ймовірно, не ухиляються від Т-клітин[176]. Ця неспецифічна відповідь супроводжується адаптивним вже специфічним процесом, коли організм виробляє антитіла (імуноглобуліни), які специфічно зв'язуються із SARS-CoV-2, створюється гуморальний імунітет. Ця комбінована адаптивна відповідь може видалити SARS-CoV-2 з організму, і якщо вона досить сильна, може запобігти прогресуванню до тяжкої форми або повторному зараженню тим же вірусом. Реагування Т-клітин пов'язують з адекватною роботою залози тимуса, яка з віком піддається інволюції, через що рівень клітинного імунітету падає. З цим пов'язується нездатність літніх людей адекватно реагувати на інфікування SARS-CoV-2, внаслідок чого він на ранньому етапі не знешкоджується, а далі прогресують запальні зміни з розвитком неадекватних реакцій у першу чергу в легенях. Ключове запитання поки ще не розв'язане і полягає в тому, чи може сформуватись захисна Т-клітинна пам'ять після інфекції SARS-CoV-2 або вакцинації. Специфічну протикоронавірусну імунну пам'ять було виявлено у CD4-T-лімфоцитів у 100 % осіб, що одужали, та CD8-T-лімфоцитів у 70 % таких осіб. Також виявлені реакції Т-клітинної пам'яті на більшість білків SARS-CoV-2, не тільки на білок шипа, а й на нуклеопротеїн і мембранний білок вірусу. Чи цього достатньо для захисного імунітету і скільки він триватиме, поки не вияснено. Розв'язати це питання можна вивчаючи не тільки клітинну, але й гуморальну імунну пам'ять у хворих, які одужали[126].
Вважається, що імунна гуморальна відповідь є вирішальною для елімінації цитопатичних вірусів з організму і є основною складовою імунної пам'яті, що перешкоджає повторному зараженню. Довгостроковий захист досягається за рахунок індукції плазматичних клітин і В-клітин пам'яті. SARS-CoV-2 спричинює стійку B-клітинну відповідь, що показує швидка універсальна поява вірусоспецифічних IgM-, IgG- і IgA-антитіл, нейтралізуючих антитіл класу IgG у перші 7-10 днів після зараження. Як правило виявляються антитіла, що зв'язують внутрішній протеїн N і зовнішній глікопротеїн S SARS-CoV-2. Більшість досліджень гуморальної ланки імунітету при коронавірусній хворобі 2019 показують, що люди, які одужали від хвороби, мають антитіла проти вірусу. Незважаючи на ознаки успішної нейтралізуючої дії противірусних антитіл, вищі їхні титри можуть асоціюватись із тяжчим клінічним перебігом хвороби, що підтверджується спостереженнями часів епідемії тяжкого гострого респіраторного синдрому, коли титри нейтралізуючих антитіл були значно вищими у померлих пацієнтів у порівнянні з тими, які одужали. Це провокує побоювання, що противірусні антитіла можуть сприяти погіршенню внаслідок антитілозалежного посилення інфекції, що може бути спричинено переносом вірусу в клітину через Fc-фрагмент імуноглобулінів[126]. Однак деякі з цих людей мають дуже низький рівень нейтралізуючих антитіл у крові, що свідчить про те, що клітинна ланка імунітету може бути у них вирішальною для видужання. Люди, заражені будь-яким з інших коронавірусів, можуть виробляти антитіла, що, як вважається, здатні перехресно реагувати з антитілами, що утворюються у відповідь на коронавірусну хворобу 2019[107]. Тривалість гуморальної відповіді після перенесеної хвороби наразі обговорюється. Є свідчення того, що рівень імуноглобулінів класу G швидко знижується особливо після перенесення хвороби з легким перебігом, тоді як є міркування, що у клітинах імунної пам'яті створюється пул, що швидко реагує виробленням антитіл надалі при новому зараженні[177].
З'явилися припущення, що імунітет після перенесеної хвороби, навіть в легкій формі, іноді може бути тривалим, навіть довічним[178][179]. Отримано результати досліджень у 52238 осіб, що свідчать про те, що вакцинація була пов'язана зі значно нижчим ризиком зараження SARS-CoV-2 серед тих, хто раніше не інфікувався і отримав вакцинацію, ніж серед тих, хто раніше хворів та отримав вакцинацію. Жоден з 1359 людей, які раніше хворіли та не вакцинувалися, не мали повторного захворювання протягом усього дослідження[180].
Було показано, що люди, які перехворіли на тяжкий гострий респіраторний синдром у 2003 році, мають через 17 років антитіла до SARS-CoV-1, збудника цієї хвороби, що є дуже близьким до SARS-CoV-2. У гострій фазі хвороби рівні антитіл швидко досягають піку, який створюється не тривало живучими плазматичними клітинами. А надалі вступають у дію тривало живучі клітини імунологічної пам'яті, що виробляють антитіла в тих, хто видужав від коронавірусної хвороби 2019, як наразі відомо й упродовж 6-11 місяців від зараження. Рівні цих антитіл знижуються через шість місяців, але залишаються більш-менш постійними на рівні приблизно від 10 до 20 відсотків від максимального значення реакції на гостру інфекцію або вакцинацію. Клітини імунологічної пам'яті забезпечують довгострокову продукцію цих антитіл на рівні 10-20 % від рівня гострої фази, що забезпечує стабільний захист. Такі клітини зберігаються протягом багатьох років, ймовірно, усе життя[181][182].
Клінічні прояви
Узагальнити
Перспектива
Класифікація
Наразі виділяють наступні клінічні варіанти перебігу захворювання:
- неускладнені випадки з наявністю неспецифічних симптомів (легкий перебіг);
- пневмонія без дихальної недостатності (середньотяжкий перебіг);
- пневмонія з ознаками дихальної недостатності (тяжкий перебіг);
- критичне захворювання, яке включає появу:
- гострого респіраторного дистрес-синдрому (ГРДС);
- поліорганної недостатності;
- тромботичних проявів;
- сепсису;
- септичного шоку;
Легкий перебіг захворювання
Інкубаційний період триває від 2 до 14 днів, хоча є свідчення, що може досягати і 20 днів. Багато випадків зараження усіма варіантами не супроводжуються взагалі появою симптомів. Легка форма типово проявляється невисокою гарячкою до 38 °C, кашлем, ринітом та / або закладанням носу. Пацієнти з легким перебігом захворювання можуть також скаржитися на біль у горлі, головний біль, міалгії та нездужання, спотворення нюху (дизосмія), смаку (дизгевзія) та / або втрату нюху (аносмія), смаку (агевзія). У пацієнтів з легким перебігом відсутні ознаки зневоднення, сепсису, задишка або утруднене дихання з відчуттям стискання за грудниною, збільшення частоти дихальних рухів, наявність мокротиння або кровохаркання, нудота, блювання та / або діарея, немає змін психічного стану — сплутаності свідомості, млявості[183]. Літні та імуносупресивні пацієнти можуть мати атипові симптоми.
Аносмія є відносно частим симптомом, який виявляється у певної кількості пацієнтів[184], у низці досліджень до 82 % безсимптомних пацієнтів[185]. Нюхові проблеми зазвичай зустрічаються при у початковому періоді хвороби, у молодому віці, серед жінок, при легкому перебігу хвороби, хоча й іноді трапляються у хворих з тяжчими формами клінічного перебігу[186]. Ймовірною причиною втрати нюху є потрапляння вірусу до допоміжних клітин нюхового епітелію[en][184]. Разом із тим, це не є достатніми для пояснення зворотної аносмії та агевзії, які швидко усуваються. Крім того, залишається невідомою причина порушення хімічних відчуттів у деяких хворих. Є припущення, що пацієнти страждають від дефіциту триптофану, оскільки АПФ2, ключовий елемент у процесі всмоктування триптофану з їжі, значно зменшується у пацієнтів, оскільки SarS-CoV-2 використовує АСЕ2 як рецептор для входу в клітини-мішені. Дефіцит триптофану призводить до дефіциту серотоніну у таких пацієнтів, оскільки триптофан є попередником його синтезу. Такий дефіцит серотоніну може пояснити аносмію, агевзію, враховуючи той факт, що він є важливим нейромодулятором у нюхових нейронах, клітинах смакових рецепторів і транзиторних рецепторних потенційних каналах, які беруть участь у нюхальному та вкусовому процесі[152].
Зміна циркуляції в світі варіантів SarS-CoV-2 призвела до того, що переважаючий з літа 2021 року варіант «Дельта» спричинює захворювання з переважанням нежиттю, значної ринореї і зменшенням випадків аносмії та авгезії відносно того, як це спостерігалося до цього періоду. Хвороба, яку спричинює варіант «Омікрон», має короткий інкубаційний період до 5 днів, відсутність змін нюху та смаку, і переважання легкого перебігу.
Обстеження хворих з легким і середньотяжким ураженням класичним штамом SarS-CoV-2 показало наявність у них перламутрової везикулярної енантеми на піднебінні на відміну від уражень тими варіантами, що з'явились у циркуляції пізніше[187].
Середньотяжкий перебіг
Пацієнти з таким перебігом не мають ознак дихальної недостатності. Їх турбують такі ж скарги, як і в хворих із легким перебігом. Проте на 1-му тижні хвороби частим проявом, не властивим легкому перебігу, є гарячка з підвищенням температури тіла вище від 38 °C. Суб'єктивно міальгії та артралгії у цих хворих сприймаються значно виразніше і більше, ніж у хворих із легким перебігом. Кашель може бути з мокротинням, при аускультації вислуховуються вологі хрипи. З'являється утруднення та прискорення дихання. Головним у діагностиці є виявлення на комп'ютерній томографії вогнищ запалення в легенях, як правило, дрібних за розміром. Сатурація при такому перебігу не менше ніж 92 %[183].
Тяжкий перебіг (тяжка пневмонія)
Характерним є поява наприкінці 1-го тижня, протягом 2-го тижня пневмонії. Початок часто з високої за рівнем температури тіла гарячки та інтоксикації. При тяжкій пневмонії у підлітків або дорослих є гарячка або підозра на респіраторну інфекцію, плюс частота дихання до 30 вдихів / хвилину, виражена дихальна недостатність або <90 % на спонтанному диханні в приміщенні. Дитина з кашлем або утрудненням дихання плюс хоча б одне з наступних:
- центральний ціаноз або <90 %;
- виражена дихальна недостатність (наприклад, хрипи, напруження грудної клітки);
- ознаки пневмонії із загальними небезпечними проявами: відмова від грудного годування та пиття, млявість чи непритомність, судоми.
Можуть бути й інші ознаки пневмонії: участь допоміжних м'язів у диханні, часте дихання (кількість вдихів / хвилину): при віці <2 місяців — 60 і більше; 2–11 місяців — 50 і більше; 1–5 років — 40 і більше.
Домінування з початку літа 2021 року варіанту «Дельта» SARS-CoV-2 призвело до деяких змін клінічного перебігу. Зокрема відзначається нерідкий розвиток тяжкого перебігу з виразною інтоксикацією вже за 4-5 днів від початку хвороби з відповідним раннім формуванням пневмонії і швидким падінням сатурації.
Критичний перебіг хвороби
Проявляється появою нових симптомів або погіршенням респіраторних симптомів, що були до того, появою гострого респіраторного дистрес-синдрому (ГРДС) упродовж одного тижня від початку коронавірусної хвороби 2019.
Критеріями гострого респіраторного дистрес-синдрому (критичної форми при коронавірусній хворобі 2019) визнані[188]:
- задишка з частотою дихання більше 30 вдихів / хвилину;
- гіпоксемія (за результатами пульсоксиметрії);
- дані комп'ютерної томографії грудної клітки з наявністю мультичасткових інфільтратів або міжчасткової легеневої інфільтрації, не пояснена плевральним випотом, колапсом частки або легені або вогнищами, що прогресувала більше ніж на 50 % упродовж 24 — 48 годин. Дихальна недостатність у такій ситуації не повністю пояснюється серцевою недостатністю або можливим перевантаженням введеною рідиною.
Синдром поліорганної недостатності
Небезпечна для життя дисфункція органів, спричинена порушенням імунної відповіді пацієнта на підозрювану чи доказану інфекцію, що супроводжується поліорганною недостатністю (також мультисистемний запальний синдром). Розвивається при критичному перебігу коронавірусної хвороби 2019. Ознаки такої дисфункції органів:
- змінений психічний стан,
- утруднене або часте дихання,
- низьке насичення киснем,
- зниження діурезу,
- тахікардія,
- слабкий пульс,
- холодні кінцівки або артеріальна гіпотензія,
- зміна забарвлення шкіри,
- лабораторні докази коагулопатії, тромбоцитопенії, ацидозу, високий рівень лактату або гіпербілірубінемія.
Спостерігається при сепсисі, проте може зустрітися й при інших тяжких захворюваннях. Як припускається, виникає при коронавірусній хворобі 2019 через надмірний рівень імунного запалення, «бунт макрофагів».
Шок
У дорослих зберігається артеріальна гіпотензія, незважаючи на адекватність введення рідини, існує нагальна потреба у вазопресорах для підтримки середнього артеріального тиску ≥65 мм рт. ст. та рівня лактату в сироватці крові> 2 ммоль / літр. Наразі є думки, що такий шок не виникає тільки через сепсис із септичним шоком, а є результатом виникнення тяжкої поліорганної недостатності через надмірне вірусне й імунне запалення, внаслідок чого ефективність гемодинаміки як центральної, так і периферичної пропадає.
Післякоронавірусний (постCOVID-19) синдром
Цей синдром (англ. The post-COVID-19 syndrome / Long-haul syndrome) характеризується тривалим нездужанням, головним болем, генералізованою втомою, проблемами зі сном, випаданням волосся, розладом запаху, зниженням апетиту, тривалими артралгіями, задишкою, болем у грудях та когнітивною дисфункцією. До 80 % пацієнтів відчувають тривале нездужання після коронавірусної хвороби 2019, яке може зберігатися протягом місяців після гострої інфекції, і майже половина пацієнтів повідомляє про зниження якості свого життя. Ці довгострокові ефекти відбуваються в таких масштабах, що можуть перевищити існуючий потенціал охорони здоров'я, особливо в країнах із низьким і середнім рівнем доходу населення[189].
Пацієнти можуть страждати тривалими нейропсихологічними проявами у різних сферах пізнання. Загадковою особливістю синдрому є те, що він не прогнозується початковою тяжкістю захворювання. Він часто уражає тих, хто хворів легко та середньотяжко, молодих людей, які не потребували дихальної підтримки або інтенсивної терапії. Післякоронавірусний синдром, імовірно, є результатом різноманітних патогенетичних механізмів. Постійні респіраторні прояви пов'язані з незакінченою пневмонією. Неврологічні симптоми пов'язані з мікро- та / або макросудинною тромботичною хворобою. МРТ головного мозку через 3 місяці після зараження продемонструвала мікроструктурні зміни у 55 % пацієнтів. Крім того, особливості ураження головного мозку пов'язані з енцефалітом та аутоантитілами до тканини мозку, а також серйозною церебральною вазоконстрикцією. Мікроваскулярна тканина мозку експресує рецептори АПФ-2, а «псевдовіріони» SARS-CoV-2 можуть зв'язуватися з мікросудинним ендотелієм, спричиняючи церебральне мікросудинне запалення та згортання там крові. Особливості післякоронавірусного синдрому збігаються з особливостями міалгічного енцефаломієліту / синдрому хронічної втоми. Спостерігалася подібність між синдромом активації тучних клітин і післякоронавірусним синдромом, і багато хто з науковців вважає його варіантом синдрому активації тучних клітин. Ці клітини присутні в головному мозку, особливо в середній частині гіпоталамуса, де вони розташовані навколо судин поблизу нервових закінчень. Після стимуляції тучні клітини вивільняють прозапальні медіатори, як то гістамін, триптазу, хемокіни та цитокіни, що може призвести до нервово-судинного запалення. «Туман мозку», когнітивні порушення та загальна втома, про які повідомляється в перебігу післякоронавірусного синдрому, ймовірно пов'язані із запаленням нервової та судинної систем. Імовірно, у хворих, які отримували неадекватне і надмірне протизапальне лікування під час гострої фази коронавірусної хвороби 2019, набагато частіше розвивається післякоронавірусний синдром. Подібно до пацієнтів, які одужали від сепсису, тривале порушення імунітету з підвищеними про- та протизапальних цитокінів може сприяти розвитку післякоронавірусного синдрому. Невідома кількість хворих, які одужали від пневмонії при коронавірусній хворобі 2019, у яких розвинеться фіброз легень, що пов'язаний з обмеженням рухової активності під час хвороби. Цих пацієнтів слід направити до пульмонолога, який має досвід у лікуванні фіброзу легень. Антифібротична терапія може дати ефект у цих хворих. Є міркування, що блокатор серотонінових рецепторів ципрогептадин може зменшити ризик легеневого фіброзу[146][190][191].
Поки що немає чіткого узгодженого всіма науковцями визначення посткоронавірусного (постCOVID-19) синдрому. У клінічних настановах Національного інституту охорони здоров'я та вдосконалення медичної допомоги Великої Британії (NICE) «Лікування довгострокових наслідків COVID-19» (NG188) використовуються такі клінічні визначення для первинної хвороби та тривалої коронавірусної хвороби 2019 залежно від часу, коли вони виникли та впродовж якого зберігаються:
- гостра коронавірусна хвороба 2019 — ознаки та симптоми захворювання зберігаються до 4 тижнів;
- тривала коронавірусна хвороба 2019 із симптомами — ознаки та прояви зберігаються 4-12 тижнів;
- пост-COVID-синдром — ознаки та прояви розвиваються під час або після коронавірусної хвороби 2019, зберігаються понад 12 тижнів і не пояснюються альтернативними діагнозами[146].
Американське товариство з інфекційних захворювань (IDSA) вирізняє «тривалу коронавірусну хворобу 2019», «пост-COVID-синдром» і «пост-гострий COVID-синдром». Поняття «хронічного» або «тривалого» перебігу будь-якої інфекційної хвороби включає персистенцію збудника. Інші коронавіруси мають властивість тривалий час зберігатися в нервовій системі, ймовірно SARS-CoV-2 також схильний до цього. Якщо патологічні зміни після перенесеної хвороби зберігаються, але збудника при цьому вже не знаходять, то йдеться про наслідки хвороби, яке має називатися посткоронавірусним синдромом. Гарвардська вища медична школа створила поняття «далекобійник» (англ. post-COVID long-hauler), — будь-яка людина, з підтвердженою коронавірусною хворобою 2019, яка не повернулася до свого рівня здоров'я й функціонування через 6 місяців після перенесеного захворювання. За різними даними, «далекобійниками» стають від 10 до 50 % хворих, які перенесли коронавірусну хворобу 2019[146].
Розрізняють дві групи таких пацієнтів:
- ті, які мають незворотні ушкодження серця, легень, нирок чи головного мозку, що впливають на їх здатність жити повноцінним життям;
- ті, в кого тривають серйозні клінічні прояви, незважаючи на відсутність помітних ушкоджень цих органів.
Якою б не була природа змін, що пов'язані із тривалим збереженням клінічних проявів або появою нових після перенесеного гострої коронавірусної хвороби 2019, їхня наявність потребує реабілітаційних заходів[146].
Встановлено, що в осіб, які перенесли коронавірусну хворобу 2019, через 2 тижня після клінічного одужання концентрація цитокінів у сироватці крові, включаючи відповідні деякі інтерлейкіни, вища порівняно з групою контролю, що свідчить про подовження запалення[192][193].
Ендотеліїт (запалення ендотелію) є одним із головних патологічних процесів, що виникає під час коронавірусної хвороби 2019. Є докази прямого інфікування SARS-CoV‑2 ендотеліальних клітин і спричиненого цим дифузного ендотеліїту. Ураження ендотелію кровоносних судин через гіперімунну реакцію ушкодження цитокінами та вільними радикалами зумовлює розвиток системного «тліючого» запалення під час посткороновірусного синдрому[146].
Після перенесеної коронавірусної хвороби 2019 у хворих через ураження ендотелію судин на 25 % збільшується ризик тромбоемболій. Виявляється стійкий спазм кровоносних судин (вазоконстрикція). Через ураження міокарда часті аритмії і на 22 % збільшується ризик інфаркту міокарда. Спостерігаються порушення кровопостачання (перфузії) та ішемічні зміни в міокарді[146].
У багатьох хворих формується виразний астенічний синдром, який значною мірою знижує їхню якість життя й істотно зменшує працездатність. У таких пацієнтів тривалий час може йти запалення низької інтенсивності в головному мозку, знижується приток крові до нього, приєднується автоімунне ушкодження цього органу або відбувається поєднання цих аномалій. Накопичення прозапальних цитокінів, які проходять через гематоенцефалічний бар'єр, у ЦНС може сформувати дисрегуляцію центральних структур і породити вегетативну дисфункцію (гарячка, порушення циклу сну, когнітивні проблеми, швидка втомлюваність). Після перенесення гострої фази коронавірусної хвороби 2019 потрібен обов'язковий моніторинг дихальної функції, стану кардіальної, нервової системи і психічних функцій, а ще синдромально-патогенетичний підхід до реабілітації хворих, спрямований першочергово на знешкодження системного фонового запалення, покращення функції ендотелію та зниження астенічних проявів[146].
Виявлено відносно високу частоту когнітивних порушень через кілька місяців після того, як пацієнти заразилися SARS-CoV‑2. Серед них переважали порушення виконавчої діяльності, швидкості обробки інформації, вільного володіння категоріями, ураження пам'яті та запам'ятовування. Ця закономірність узгоджується з ранніми повідомленнями, що описують дисекзекутивний синдром після коронавірусної хвороби 2019, і має значні наслідки для професійних, психологічних і функціональних результатів. Відомо, що певні групи населення, як то люди похилого віку, можуть бути особливо сприйнятливі до когнітивних порушень після тяжкої хвороби. Проте й у відносно молодих людей виявлено часту когнітивну дисфункцію кілька місяців після одужання. Результати цього дослідження загалом збігаються з результатами досліджень стосовно інших вірусних хвороб, як то грипу[194].
Діагностика
Узагальнити
Перспектива
Визначення випадку коронавірусної хвороби 2019 (COVID-19)
- Підозрілий випадок:
- 1. Пацієнти з тяжкою гострою респіраторною інфекцією (гарячкою, кашлем і стан яких потребує госпіталізації), та без будь-якого іншого етіологічного чинника, який би міг повністю пояснити клінічні прояви, і які за 14 днів до появи симптомів відповідали принаймні одному із наступних критеріїв:
- тісний контакт з підтвердженим або ймовірним випадком коронавірусної хвороби 2019;
- або
- перебували в районах із відомою суспільною передачею COVID-19.
- 2. Пацієнти з будь-яким гострим респіраторним захворюванням та наявністю хоча б одного з наступних критеріїв протягом попередніх 14 днів:
- перебував у контакті із підтвердженим або ймовірним випадком COVID-19;
- працював або відвідував заклад охорони здоров'я, де проходили лікування пацієнти з підтвердженою або ймовірною COVID-19.
- Епідеміологічно пов'язаний випадок — це такий підозрілий випадок, коли ще не проведено адекватного лабораторного обстеження, але який мав контакт з іншим лабораторно підтвердженим випадком COVID-19 за 14 днів до появи симптомів у себе.
- Ймовірний випадок: пацієнт із підозрою на коронавірусну хворобу 2019, результат лабораторного дослідження якого на SARS-CoV-2 є сумнівним або, що отримав позитивний результат на загальний для всіх бетакоронавірусів антиген (панкоронавірусний антиген), а також у нього відсутні лабораторні підтвердження наявності інших (некоронавірусних) респіраторних патогенів.
- Підтверджений випадок — людина з лабораторно підтвердженою коронавірусною хворобою 2019, незалежно від наявності або прояву клінічних ознак і симптомів.
Важливо зазначити, що визначення випадків різняться залежно від країн і регіонів територій, що постраждали від захворювання, і це, в свою чергу, вплинуло на реакцію на охорону здоров'я. При визначенні випадків важливо, щоб національні рекомендації враховували віковий розподіл населення та наявність супутніх захворювань, включаючи серцево-судинні захворювання, цукровий діабет і рак, що збільшує ризик розвитку тяжких та / або критичних захворювань та ризик смерті[91].
Визначення контакту
Контактний/а — це особа, яка відповідає будь-якому з наступних критеріїв:
- надання прямої медичної допомоги пацієнтам із коронавірусною хворобою 2019 — медичний працівник або інша особа, яка надавала медичну допомогу або проводила догляд за хворим на неї навіть за умови використання відповідних засобів індивідуального захисту;
- працівники лабораторій, які обробляють зразки з дихальних шляхів отримані від хворих на коронавірусну хворобу 2019 або працівники патологоанатомічних / судово-медичних бюро / відділень, які безпосередньо розтинали тіла і проводили процедури, які можуть призводити до утворення інфекційного аерозолю (застосування операційної кісткової пилки, центрифуги, аспіраційного обладнання тощо), в тому числі брали зразки для проведення лабораторного дослідження навіть за умови використання відповідних засобів індивідуального захисту;
- робота з медичними працівниками, зараженими SARS-CoV-2, відвідування пацієнтів або перебування в одному приміщенні з пацієнтом із коронавірусною хворобою 2019;
- особа, яка мала прямий фізичний контакт із хворим на COVID-19 (зокрема, через рукостискання);
- особа, яка мала незахищений контакт без використання засобів індивідуального захисту із слизовими виділеннями з дихальних шляхів хворого на COVID-19 (зокрема, перебування поблизу від такого пацієнта під час кашлю, чи доторкування руками до використаних серветок);
- особа, що контактувала із хворим або кількома на відстані до одного метру протягом 15 хвилин і більше, без використання відповідних засобів індивідуального захисту або при підозрі на їх неправильне використання (зокрема, при порушенні цілісності рукавичок);
- спільна робота або навчання в безпосередній близькості з пацієнтом із коронавірусною хворобою 2019;
- подорож разом із пацієнтом із коронавірусною хворобою 2019 у будь-якому транспорті, при контакті в літаку в межах двох сидінь (у будь-якому напрямку) з хворим, контактами вважаються супутники подорожі та члени екіпажу, які обслуговували в салоні літака, де знаходився хворий, якщо тяжкість симптомів (наприклад, частий кашель) або переміщення особи вказують на більшу зону ризику зараження, пасажири, які сидять у всій секції, або всі пасажири літака;
- проживання в одному домогосподарстві з хворим на коронавірусну хворобу 2019 упродовж 14 днів після виникнення симптомів у цього хворого.
Клінічна діагностика
Оцінка неспроможності органів (SOFA) коливається в межах від 0 до 24 і включає бали, пов'язані з 6 системами організму:
- дихальна (гіпоксемія, визначена низьким рівнем PaO2 / FiO2);
- згортання крові (низький рівень тромбоцитів);
- печінка (поява жовтяниці, високий рівень білірубіну);
- серцево-судинна (артеріальна гіпотензія);
- центральна нервова система (низький рівень свідомості, визначений за шкалою Глазго);
- ниркова (знижений діурез або високий вміст креатиніну).
Синдром визначається збільшенням послідовної оцінки SOFA на ≥2 бали.

Інструментальна діагностика
Для діагностики атипової пневмонії при коронавірусній хворобі 2019 проводиться рентгенографія легень та комп'ютерна томографія (КТ).
Рентгенографія є доступним методом, адже навіть у лежачого пацієнта її можна зробити за допомогою переносного рентгенівського апарату. Але вона часто не показує зміни у хворих із нетяжкою пневмонією. На рентгенологічних знімках у самих тяжких випадках відзначається двосторонні рентгенологічні затемнення в обох легенях, що демонструється появою світлого забарвлення на тлі притаманній рентгенологічній картині нормальній темній паренхіми легень.
КТ грудної клітки показує двостороннє ураження. Відзначаються вогнища ущільнення паренхіми типу «матового скла». Цей метод дає можливість визначення кількісного ураження паренхіми легень у відсотках. КТ-контроль у тих хворих, в яких було діагностовано пневмонію на початку хвороби, слід проводити не раніше ніж за 2-3 місяці. Навіть тоді у частини хворих спостерігаються зміни по типу «матового скла», характерні для гострої пневмонії. Через технічну складність проведення рентгенографії та КТ у хворих, що знаходяться на штучній вентиляції легень, рекомендується для контролю стану легень застосовувати ультразвукову діагностику (УЗД) за допомогою переносних апаратів, яка до цього в діагностиці ураження легень у рутинній клінічній практиці використовувалася нечасто через застосування рентгенографії та КТ. Наявність переважно підплевральних уражень дає перевагу використанню УЗД[195][196].
Загальнолабораторна діагностика
Перелік діагностичних обстежень при госпіталізації в Україні включає обов'язкову ЕКГ, клінічний аналіз крові, клінічний аналіз сечі, біохімічний аналіз крові, визначення рівня глюкози крові[197].
У госпіталізованих пацієнтів із пневмонією відмічено лейкопенію або лейкоцитоз, лімфопенію, тромбоцитопенію, підвищену активність аланінамінотрансферази (АЛТ) та аспартатамінотрансферази (АСТ). У пацієнтів, які перебували на лікуванні у відділенні інтенсивної терапії, додатково відзначалися відхилення в лабораторних показниках, які можуть бути обумовлені розвитком клітинного імунодефіциту, активацією коагуляції, пошкодженням міокарда, порушенням функції печінки і нирок. Виявлено статистично достовірне збільшення кількості нейтрофілів із прогресивною лімфопенією, підвищення рівня D-димеру як маркеру легеневих тромбозів, сечовини і креатиніну сироватки крові, прокальцитоніну (поліпептиду, який є неактивним попередником кальцитоніну)[198], С-реактивного білка, який є чітким маркером тяжкості перебігу коронавірусної хвороби 2019 (його рівні вище 100 мкг / мл при будь-якому захворюванні є ознакою фульмінантного запалення та пов'язані з поганим прогнозом захворювання),[199], і феритину, інтерлейкінів 6, 8 і 10[127]. Проте є дослідження, що припускають менше значення використання рівнів D-димеру для виключення легеневих тромбозів серед пацієнтів, госпіталізованих із коронавірусною хворобою 2019, чи їх обмежену клінічну користь[200].
Специфічна лабораторна діагностика

Полімеразна ланцюгова реакція і методи отримання матеріалу для неї
Відбираються зразки з верхніх і нижніх дихальних шляхів для тестування на SARS-CoV-2 за допомогою ПЛР (в режимі реального часу — rRT-PCR), яка є одним із видів тестів на ампліфікацію нуклеїнових кислот (Nucleic acid amplification tests або NAAT). За необхідності проводиться підтверджуюче секвенування нуклеїнової кислоти[201]. Матеріал для дослідження відбирають медичні працівники, одягнені в засоби індивідуального захисту. Виявлення РНК SARS-CoV-2 проводиться всім пацієнтам з підозрою на коронавірусну хворобу 2019, а також контактним особам. Для дослідження береться матеріал, отриманий при взятті мазка з носоглотки (щонайменше на глибину 3 см у носових ходах) і ротоглотки, промивні води бронхів, отримані при фібробронхоскопії (бронхоальвеолярний лаваж), ендотрахеальний, назофарингеальний аспірат, мокротиння. Від пацієнтів із механічною вентиляцією легень можна збирати тільки зразки виділень із нижніх дихальних шляхів[202]. При збиранні зразків матеріалу з верхніх дихальних шляхів використовуються вірусні тампони[203] та вірусні транспортні носії. Не слід під час взяття мазка торкатися ніздрів або мигдаликів. У пацієнта з підозрою на коронавірусну хворобу 2019, особливо з пневмонією або тяжкими респіраторними проявами, один зразок із верхніх дихальних шляхів є недостатнім, і рекомендується взяття додаткових зразків із верхніх дихальних і з нижніх дихальних шляхів, останнім надається перевага. Один позитивний тест підтверджується другим тестом ПЛР, який визначає інший ген SARS-CoV-2. Одиничний негативний тест на виявлення SARS-CoV-2 (особливо, якщо це зразок із верхніх дихальних шляхів) або позитивний результат дослідження щодо виявлення іншого респіраторного збудника не виключає коронавірусної хвороби 2019. Якщо існує обґрунтована підозра на інфікування, слід перевірити інший зразок за допомогою первинного та вторинного ПЛР. Виявлення РНК за допомогою ПЛР не обов'язково свідчить про те, що він зберігає здатність до реплікації чи спричинити надалі хворобу[88].

У госпіталізованих пацієнтів з підтвердженою коронавірусною хворобою 2019 необхідно повторно взяти зразки з верхніх та нижніх дихальних шляхів для визначення змін кількості коронавірусу — вірусного кліренсу. Забір зразків має проводитися щонайменше кожні 2 — 4 дні, поки у пацієнта, що клінічно одужав, не буде досягнуто інтервал не менше 24 годин між двома наступними один за одним негативними результатами (обидва зразки з верхніх дихальних шляхів і з нижніх дихальних шляхів, за умови, якщо обидва були зібрані). Всі зразки слід зберігати при температурі 2-8 °C до 48 годин після збору. Для обробки та доставки через 48 годин рекомендується зберігання зразків при температурі -70 °C. Дослідження слід проводити щонайменше у боксах біологічної безпеки II класу. Лабораторії проводять тестування на ПЛР стосовно SARS-CoV-2 самостійно та у співпраці зі спеціалізованими лабораторіями у випадках неоднозначних чи сумнівних результатів. Робити забір зразків крові, сечі та випорожнень для проведення обстеження хворого на SARS-CoV-2 методом ПЛР не рекомендується.
Повідомлено про створення швидкого тесту ампліфікації нуклеїнових кислот (Nucleic acid amplification tests або NAAT) за допомогою ПЛР, який дає результат через 5 хвилин від початку дослідження. Тест проводиться на основі приладної спеціальної швидкої ізотермічної системи для якісного виявлення інфекційних захворювань. Це дозволить клініцистам приймати клінічні рішення, засновані на доказах, безпосередньо під час візиту пацієнта[204][205].
З міркувань біологічної безпеки CDC не рекомендує проводити виділення SARS-CoV-2 на культурах клітин у звичайних лабораторіях. Це дослідження можливо проводити лише у боксах біологічної безпеки II класу.
Імунохроматографічні дослідження
Впроваджено швидкий імунохроматографічний тест для якісного виявлення антигенів (нуклеокапсидного білка) SARS-CoV-2 (CITO TEST COVID-19 Ag) у мазках з носоглотки осіб з підозрою на коронавірусну хворобу 2019 в гостру фазу хвороби впродовж 5-7 днів після появи перших симптомів[206]. Чутливість методу досягає 90 %, точність 97 %. Результати можуть бути отримані за 15-20 хвилин[207].
Розроблені експрес-тести на основі імунохемілюмінесцентного аналізу для виявлення антитіл класів IgM та IgG[208][209]. На основі імунохемілюмінесцентного іммуноаналізу бічного потоку можливе швидке якісне роздільне виявлення анти-SARS-CoV-2 IgG та IgM у зразках цільної крові людини, сироватки крові або плазми. Цей метод може бути застосований у польових (не лабораторних) умовах. Важливо зазначити, що на ранніх стадіях хвороби (3-7 день) ці антитіла можуть бути в концентрації нижче межі виявлення для цього тесту. Ці тести не підтверджують наявність коронавірусної хвороби 2019, а є орієнтовними. Американський інститут здоров'я не рекомендує використовувати цей тест для діагностики гострої фази коронавірусної хвороби 2019[210].
Імуноферментний аналіз
Також в Україні розроблені і впроваджені методи виявлення антитіл класів IgM та IgG у лабораторному режимі в імуноферментному аналізі (ІФА), вони є точнішими за експрес-тести, але також не є підтверджуючими наявність коронавірусної хвороби 2019[211]. Наявність у крові людини антитіл класу IgM свідчить про можливість гострої стадії коронавірусної хвороби 2019, тоді як IgG — про період видужання. Впроваджено й дослідження в крові антитіл класу IgA, наявність яких у підвищеній кількості відбувається в гострому періоді хвороби.
Специфічне обстеження супутніх хвороб і станів
Бажане обстеження для виявлення ко-інфекцій з іншими респіраторними вірусами, такими як збудники грипу A і B, пташиного грипу, респіраторно-синцитіальний вірус, віруси парагрипу, аденовіруси, ентеровіруси (зокрема, EVD68), метапневмовірус людини та ендемічний коронавірус людини БКРС / MERS (тобто ізоляти HKU1, OC43, NL63 та 229E). Зразки також слід перевірити на бактеріальні збудники, зокрема Legionella pneumophila (збудник легіонельозу), які спричинюють тяжкі респіраторні ураження. Для встановлення причини пневмонії також рекомендовано застосування класичної (звичайної) ПЛР, зі зворотною транскрипцією (ЗТ-ПЛР), мультиплексною ПЛР на 19 вірусних і 7 бактеріальних збудників, ПЛР із детекцією продукту ампліфікації в реальному часі. Це є перспективним для виявлення таких збудників, як M. pneumoniae і C. pneumoniae, а також респіраторних вірусів.
Через можливий розвиток сепсису та вторинної бактеріальної пневмонії в деяких випадках тяжкого перебігу COVID-19 збір зразків для лабораторної діагностики не повинен відкладати початок антимікробної терапії. Слід проводити бактеріологічний посів крові для виділення культури бактерій, а також посів мокротиння, в ідеалі перед початком антибактеріальної терапії.
Систематичний скринінг венозних тромбоемболій у хворих із коронавірусною хворобою 2019 не рекомендується, але має бути підвищений рівень обізнаності відносно можливого розвитку венозної тромбоемболії під час госпіталізації. Слід звернути увагу на такі клінічні ознаки, як пастозність (припухлість) нижньої кінцівки, гіпоксемію, різке погіршення дихання, гостру правошлуночкову недостатність чи розширення правого шлуночка за даними ехокардіоскопії, проблеми з катетером тощо, судоми у нижніх кінцівках особливо вночі, які можуть бути через тромбоз глибоких вен. Візуалізація повинна бути виконана у всіх випадках підозри на венозну тромбоемболію[212].
Лікування
Узагальнити
Перспектива
Зауважте, Вікіпедія не дає медичних порад! Якщо у вас виникли проблеми зі здоров'ям — зверніться до лікаря. |
Тактика лікування починаючи з 2023 року заснована на якнайранньому підтвердженні діагнозу і негайному призначенні за умови відсутності дихальної недостатності ефективних противірусних засобів особам, які мають фактори ризику:
- вік > 60 років
- існуючі неінфекційні захворювання (включаючи артеріальну гіпертензію, цукровий діабет, серцево-судинні захворювання, хронічні захворювання легенів, цереброваскулярні захворювання, деменцію, психічні розлади, хронічну хворобу нирок, ожиріння, рак)
- імунодефіцит (включаючи ВІЛ-інфекцію, імуносупресивне лікування ревматоїдного або іншого аутоімунного захворювання)
- нещеплені проти COVID-19.
- у вагітних або нещодавно вагітних жінок додатковими факторами ризику є: похилий вік матері (>=35 років), ожиріння, хронічні захворювання та характерні для вагітності розлади (наприклад, гестаційний діабет і прееклампсія/еклампсія).[213]
Показання до госпіталізації
Госпіталізація показана хворим з підозрою або підтвердженою коронавірусною хворобою 2019 при:
- середньотяжкому (нетяжка пневмонія) і тяжкому перебігу, коли є аускультативні ознаки пневмонії та / чи дихальної недостатності (збільшення частоти дихальних рухів вище фізіологічної норми, кровохаркання, показник SpO2 при вимірюванні пульсоксиметром ≤ 92 %) за наявності рентгенологічно підтвердженої пневмонії;
- наявність клініко-інструментальних даних гострого респіраторного дистрес-синдрому;
- наявність клініко-лабораторних даних сепсису та / чи септичного шоку;
- наявність клініко-лабораторних даних іншої, окрім дихальної, органної / системної недостатності;
- пацієнти, незалежно від тяжкості стану, які належать до групи ризику розвитку ускладнень: тяжкий перебіг артеріальної гіпертензії, декомпенсований цукровий діабет, ниркова недостатність, тяжка хронічна патологія дихальної та серцево-судинної систем, тяжкі алергічні хвороби, цереброваскулярні захворювання в фазі декомпенсації, аутоімунні захворювання, онкологічні захворювання;
- хворі незалежно від тяжкості стану, в яких відзначається гарячка вище 38°С, що погано піддається корекції (короткочасне, не більше ніж на 1-1,5 години зниження температури тіла на тлі вживання жарознижувальних препаратів, з подальшим її підвищенням).
Особам, які звернулися за екстреною медичною допомогою телефоном, диспетчер цієї служби проводить опитування відповідно до алгоритму пошуку особи з підозрою на коронавірусну хворобу 2019. Якщо під час опитування відсутні показання до виїзду бригади, то пацієнту надаються відповідні рекомендації. Якщо вони наявні, то до такої особи виїжджає бригада у засобах індивідуального захисту, проводить обстеження, встановлює попередній діагноз та ступінь тяжкості захворювання і наявність показань до госпіталізації. Пацієнтам, які не мають таких, надаються поради по самоізоляції та наголошується на необхідності звернення до сімейного лікаря (а за відсутності сімейного лікаря — до регіональної чи національної гарячої лінії COVID-19). Пацієнти, у яких є показання до госпіталізації, транспортуються бригадою екстреної медичної допомоги у визначений для приймання таких хворих регіональний заклад охорони здоров'я.
Особливості оцінки лікування недоказаними лікарськими препаратами
Науковці застерігають від надмірного оцінювання деяких препаратів у лікуванні коронавірусної хвороби 2019. Вони відмічають, що подання інформації про те чи інше дослідження відбувається з недоліками через:
- зосередження уваги на результатах одного дослідження без зв'язку з іншими;
- відсутність визнання того, що окремі дослідження рідкісно призводять до остаточних висновків;
- надмірний акцент на якісь результати, без вказівки на певні обмеження;
- повідомлення, які засновані на неповних чи нерецензованих звітах[214].
Новини звітів про окремі дослідження мають бути фактичними та звітуючими про основні результати та абсолютні ризики, визначати сукупність пацієнтів і підкреслювати обмеження у валідності та узагальненості. Вони також повинні включати думки інших незалежних експертів у цій галузі, які не мають конфлікт інтересів. Висновки цих експертів повинні бути контекстними, включати порівняння з результатами інших досліджень, перевагу, яку слід надати (або не надати) поточним порівняно з іншими дослідженнями, і як зазвичай таке лікування вивчається для цього захворювання[214].
Обґрунтування пробного призначення ймовірних етіотропних і патогенетичних препаратів
У зв'язку з відсутністю доказового специфічного лікування пацієнтам із підозрою або підтвердженою COVID-19, яким ніщо інше (патогенетичні засоби, киснева неінвазивна підтримка) не допомогло і стан пацієнта наближається до критичного, можливе застосування неліцензованих методів лікування або препаратів поза прямих їх показань до застосування за фармакологічною інструкцією (out-of-treatment treatment або off lable drug use), за рішенням консиліуму та згоди самого пацієнта. Така можливість використовується й при ситуації з такими інфекційними хворобами, які мають тяжкі наслідки, несподіваний тяжкий ефект для пацієнта, часто відбуваються в рамках надзвичайної ситуації світового масштабу. Тоді ВООЗ може застосувати відповідний протокол. Етично запропонувати окремим пацієнтам експериментальні втручання в екстрених випадках поза клінічними випробуваннями («співчутливе використання»), за умови:
- що не існує доведеного ефективного лікування;
- неможливо негайно розпочати клінічні дослідження;
- пацієнт або його законний представник дав усвідомлену згоду;
- і невідкладне використання втручання контролюється, а результати документуються та своєчасно передаються широкій медичній та науковій спільноті.
Рішення запропонувати пацієнтові недоведене або експериментальне лікування приймається виключно лікарем і пацієнтом, але повинно відповідати національному законодавству. Там, де можливо і здійснено можливість лікування в рамках клінічного випробування, це слід робити, якщо пацієнт не відмовиться брати участь у дослідженні[215][216].
Через відсутність доказових схем лікування клінічний підрозділ ВООЗ продовжує збирати клініцистів в усьому світі двічі на тиждень у режимі телеконференції (COVID-19 Clinical Network) для обміну знаннями та досвідом лікарів, які лікують пацієнтів з COVID-19, і висвітлює оперативні виклики та технічні питання, що виникають.
Засоби і заходи, що використано під час пандемії
Засоби і заходи.
Наразі препарати з можливою етіотропною та патогенетичною дією, які використано при лікуванні коронавірусної хвороби 2019, скомпоновано у класифікацію видів лікування[216][217]:
- неспецифічні противірусні препарати — інтерферони, імуноглобулін, інтерлейкін-2;
- антивірусні препарати широкого спектра дії — фавіпіравір, рибавірин, тріазавірин, уміфеновір, софосбувір+даклатасвір, софосбувір+ледіпасвір, уміфеновір+рибавірин, сіяньпін, нітазоксанід, галідесивір, молнупіравір;
- антиретровірусні препарати — ASC09, азвудін, данопревір, дарунавір, дарунавір+кобіцистат, лопінавір+ритонавір, ремдесивір, данопревір+ритонавір, нілма, ASC09+ритонавір, клевудин;
- інші противірусні препарати — балоксавіру марбоксил, озельтамівір, BLD-2660;
- антивірусні комбінації (коли йде поєднання противірусних препаратів різних фармакологічних груп) — інтерферон альфа+лопінавір, уміфеновір+інтерферон альфа, лопінавір+ритонавір+рибавірин+інтерферон бета1, ASC09F+озельтамівір, ритонавір+озельтамівір, лопінавір+ритонавір+сіяньпін, лопінавір+ритонавір+інтерферон бета1, нірматрелвір+ритонавір;
- протималярійні препарати — хлорохін, гідроксихлорохін, дигідроартемізинін, мефлохін, GNS561 (аналог хлорохіна)
- протималярійні + антибіотики — гідроксихлорохін + азитроміцин;
- антибіотики + протималярійні + моноклональні антитіла — азитроміцин+гідроксихлорохін+тоцилізумаб;
- антибіотики — канаміцин, цефтріаксон, левофлоксацин або моксифлоксацин, піперацилін+тазобактам, цефтароліна фозарміл, амоксицилін+потассіум клавунат, оритаванцин, стандартний курс макролідів, тейкопланін, далбаванцин, азитроміцин, мерафлоксацин[218];
- антипаразитарні — сураміна содіум, левамізол, сенікапок, ніклозамід, нітазоксанід, івермектин;
- протималярійні + антипаразитарні — гідроксихлорохін+івермектин;
- протигрибкові — ітраконазол;
- неспецифічні протизапальні препарати — метилпреднізолон, ціклозонід, дексаметазон, будесонід+формотерол, гідрокортизон, інші глюкокортикостероїди, преднізон;
- протизапальні — колхіцин, пікліденосон, ебселен, фенретинід, пікліденозон, буцілламін;
- імуносупрессанти — фінголімод, лефлуномід, талідомід;
- 10 % нормальний імуноглобулін людини;
- інгібітори тирозинкінази — джакотініба гідрохлорід, руксолітиніб, нінтеданіб езілат, іматиніб мезілат, акалабрутиніб, баріцитиніб, фостаматініб;
- неспецифічні протизапальні + імуносупресанти — метилпреднізолон+такролімус;
- інгібітори протеаз — камостата мезілат;
- моноклональні антитіла — адалімумаб, бевацизумаб, камрелізумаб, екулізумаб, маврілімумаб, меолізумаб, PD-1 mAb, сарілумаб, тоцилізумаб, меплазумаб, адамумаб+тозумаб, іксекізумаб, ніволумаб, IFX-1, леронлімаб (PRO 140), клазікізумаб, бамланівімаб разом з етесевімабом, сотровірімаб, касиривімаб разом з імдевімабом, регданвімаб, ланаделумаб;
- противірусні + моноклональні антитіла — фавіпіравір+тоцилізумаб;
- противірусні + протималярійні — дарунавір+кобіцистат+гідрооксихлорохін, фавіпіравір+хлорохіна фосфат;
- імуномодулятори — CD24, анакінра;
- інгібітори ангіотензинових рецепторів — лозартан, рекомбінантний людський ангіотензинконвертуючий фермент 2 (rhACE2), телмісартан, валсартан, каптоприл, Renin-Angiotensin-System-Blockade;
- протиаритмічні — аміодарон;
- альфа-адреноблокатори — празозин;
- блокатори кальцієвих каналів — верапаміл;
- вазоділятатори — ангіотензин 1-7;
- кардіопротектори — аспірін+клопідогрель+ривароксабан+аторвастатин+омепразол;
- антикоагулянти — еноксапарину содіум, ривароксабан, тинзапарин;
- антивірусні + антагістамінні препарати — ебастин+інтерферон альфа;
- ненаркотичні анальгетики (NSAID) — ібупрофен, напроксен;
- муколітики — ацетилцистеїн, бромгексину гідрохлорид;
- антидепресанти — флувоксамін;
- інші препарати — авіптаділ (вазоактивний інтестінальний пептид), бісмута потассіума цитрат (блокатор SARS-CoV1-гелікази), дипіридамол, пірфенідон (препарат, що застосовується при ідіопатичному фіброзі легень), поліінозинна-поліцитіділічна кислота (polyinosinic-polycytidylic acid), rhG-CSF, тимозин, траніласт, улінастатин, вітамін С, содіума аесцінат, тетранандрін, ліпоєва кислота ін'єкційна, PUL-042 розчин для інгаляцій, носкапін, Т89 (поліпшує сатурацію крові киснем), напроксен+лансопразол, нейрокінін-1 антагоніст, дефероксамін, рабепразол, з'єднання амінокислот, транексамова кислота, розчин, що виділяє оксид азоту, хлорид цинку, селінексор, розчин для ін'єкцій Т3, куркумін С3, берберин, піридостигмін, даларгін, фебуксостат, вазегепант, дапагліфлозин, абатацепт, апрепітант;
- вакцини — БЦЖ, рекомбінантна нова коронавірусна вакцина аденовірусного вектора (Recombinant Novel Coronavirus (2019-nCOV) Vaccine (Adenovirus Vector), bacTRL-Spike vaccine, ChAdOx1 nCoV-19 vaccine, CIGB 2020 vaccine);
- не ліки:
- розширена терапія медичними продуктами (Advanced Therapy Medicinal Products) — аерозоль vMIP (вірусний макрофагальний запальний білок), анкілозавр (Ankylosaurus — M1 макрофагальна ціль), інактивована анти-2019-nCoV плазма реконвалесцентів / тих, хто видужав[219], інактивована анти-2019-nCoV-2 плазма реконвалесцентів, лікувальна плазма, мезенхімальні стовбурові клітини крові, стовбурові клітини людської менструальної крові, імуноглобулін від пацієнтів, що вилікувалися, інактивована вакцина проти мікобактерій, мезенхімальні стовбурові клітини, атомізовані екзосоми мезенхімальних стовбурових клітин, мРНК-1273, NK-клітини (природні кілери), ін'єкція білка рекомбінантного цитокіну, регулювання кишкової мікрофлори, антитіла від хворих, що видужали від коронавірусної пневмонії, мононуклеарні[220] клітини пуповинної крові, мезенхімальні стовбурові клітини пуповинної крові (hucMSC), мезенхімальні стовбурові клітини Вортона Джеллі, стовбурові клітини зубної пульпи людини, сарграмостім (Rhu GM-CSF), рекомбінантний суперскладений інтерферон (rSIFN-co), алогенна мезенхімальна терапія стовбуровими клітинами (HBadMSC), мезенхімальні стовбурові клітини кісткового мозку;
- перегрупована метаболомічна[221] група — з'єднана амінокислота;
- захисні пристрої — під час гастрофіброскопії саморобна «гастроскопічна маска», медична маска, респіратор N95;
- засоби інфекційного контролю — пропофоловий наркоз, поширена екстубація та післяопераційна стратегія «кровообіг — індуковане дихання», анестезія севофлураном;
- реабілітація — легенева реабілітація за допомогою затіненого екрана телевізора, тренування з реабілітації легень, реабілітація з дистанційним моніторингом, освіта пацієнтів;
- інгаляції газу — вдихання оксиду азоту, застосування концентратору кисню, застосування водно-кисневого небулайзеру, вдихання водню, використання постійного позитивного тиску в дихальних шляхах;
- респіраторна підтримка — високопотокова киснева терапія за допомогою носових канюль (HFNC), з зубцями, для дорослих і дітей; киснева маска з оксигенацією (SMO), високопотокова киснева (безканюльна) носова оксигенація, мішок і клапан, висококонцентрований, для дорослих, нестерильний, одноразовий; маска Вентурі, із замком O2 і насосно-компресорними трубами для дітей і дорослих; постуральне позиціювання (на животі);
- життєва підтримка — ниркова замісна терапія (гемодіаліз), штучна печінкова терапія, озонована аутогемотерапія, екстракорпоральна мембранна оксигенація (ECMO), цитосорб-терапія, одноразовий гемоперфузійний картридж HA330;
- мікробіотичне[en] (мікрофлорове) втручання — пробіотики, комбіновані порошкові пробіотики бета-глютену Newgen, промиті трансплантаційні мікробіоти, регулювання кишкової мікрофлори;
- медичні прилади — ультра короткохвильова електротерапія, інспіраторні тренування, експіраторні тренувальні апарати;
- промивання ротової порожнини — повідон-йодин, перекис водню, Німа екстракт (Azadirachta indica);
- навчання — навчання носінню маски.
Етіотропна терапія
Етіотропних препаратів із дією на SARS-CoV-2 станом на 2024 рік створено і випробувано вже багато. У травні 2021 року група науковців з Інституту Гріффіта штату Квінсленд (Австралія) повідомили, що вони створили перший етіотропний препарат проти SARS-COV-2 зі 100 % ефективністю, проте дослідження були проведені тільки на мишах, а отже потребують перевірки ефективності на людях[222].
ВООЗ вважає, що етично запропонувати окремим пацієнтам експериментальні втручання в екстрених випадках поза клінічними випробуваннями, за умови, що не існує перевіреного ефективного лікування; неможливо негайно розпочати клінічні дослідження; пацієнт або його законний представник дав усвідомлену згоду; і невідкладне використання втручання контролюється, а результати документуються та своєчасно передаються широкій медичній і науковій спільноті[223].
У зв'язку із тим, що варіант «Дельта» Sars-CoV-2, певний час домінував у світі, спричинючи виражений із самого початку інтоксикаційний синдром із високою гарячкою через вірусемію, іноді — раптове і раннє зниження сатурації, триваліший перебіг хвороби, наразі рекомендується раннє призначення деяких противірусних препаратів[157]. Ймовірна етіотропна противірусна терапія має бути призначена якнайшвидше після встановлення діагнозу, особливо групам ризику, через що бажано їх одразу госпіталізувати.
Препарати
Лопінавір / Ритонавір
Детальніші відомості з цієї теми ви можете знайти в статті Лопінавір/Ритонавір.
Ремдесивір
Через зміни в клінічному перебігу хвороби, пов'язані з широким поширенням дельта-варіанту Sars-CoV-2, вважається потрібним раннє призначення ремдесівіра, що призводить до зниження вірусного навантаження, яке від початку є дуже високим. Призначення препарату полегшує перебіг хвороби. Ремдесівір залишається найкращим препаратом наразі для цілей зменшення вірусного навантаження в хворого[157][224].
Детальніші відомості з цієї теми ви можете знайти в статті Ремдесивір.
Галідесивір
Детальніші відомості з цієї теми ви можете знайти в статті Галідесивір.
Фавіпіравір
Детальніші відомості з цієї теми ви можете знайти в статті Фавіпіравір.
Ринтатолімод
Детальніші відомості з цієї теми ви можете знайти в статті Ринтатолімод.
Хлорохін і гідроксихлорохін
Детальніші відомості з цієї теми ви можете знайти в статті Хлорохін.
Детальніші відомості з цієї теми ви можете знайти в статті Гідроксихлорохін.
Баріцитиніб
Детальніші відомості з цієї теми ви можете знайти в статті Баріцитиніб.
ВООЗ 14 січня 2022 року заявили, що препарат «настійно рекомендовано для пацієнтів із тяжким або критичним перебігом коронавірусної хвороби 2019»[225].
Азвудин
Детальніші відомості з цієї теми ви можете знайти в статті Азвудин.
Препарат азвудин закінчує III фазу клінічних випробувань у Китаї як пероральний засіб для лікування коронавірусної хвороби 2019. Частина випробувань цієї фази проходить в Бразилії та Російській Федерації. Дослідницька група університету Хенаню повідомила, що вони готові випустити його на внутрішній ринок вже у грудні 2021 року. Це препарат проти ВІЛ, який діє як інгібітор зворотної транскриптази. Він показав хорошу противірусну активність на клітинному та тваринному рівні[226].
Данопревір
Детальніші відомості з цієї теми ви можете знайти в статті Данопревір.
Арбідол
Детальніші відомості з цієї теми ви можете знайти в статті Арбідол.
Івермектин
Дослідження показали, що препарат, який було створено для лікування деяких гельмінтозів і шкірних паразитарних хвороб, зменшує у клітинних культурах розмноження SARS-CoV-2 у 5000 разів. Через це його було застосовано в лікуванні різних клінічних форм коронавірусної хвороби 2019 і введено в ряд протоколів лікування[227].
Івермектин діє шляхом інгібування ядерних транспортних білків альфа / бета-1 клітин організму, які є частиною ключового внутрішньоклітинного транспортного процесу, що використовують віруси для свого укорінення і поширення, пригнічуючи противірусну реакцію організму. Ймовірно, основа його активності в широкому спектрі дії, встановлену in vitro проти вірусів, що спричинюють гарячку денге, хворобу Зіка, ВІЛ-інфекцію та жовту гарячку[228]. Але ВООЗ рекомендувала застосування івермектину при коронавірусній хворобі 2019 тільки в межах клінічних досліджень тому, що фармакокінетичні та фармакодинамічні досліди свідчать, що досягнення плазмової концентрації, необхідної для противірусної ефективності, виявленої in vitro, потребує введення доз, що в 100 разів перевищують дози, дозволені для використання у людей. Разом з тим показано в дослідженні, що летальність була нижчою серед тих пацієнтів, які отримували івермектин, ніж серед пацієнтів групи звичайного догляду (АБО 0,27; Р = 0,03). Визначається, що користь від івермектину виявлена для пацієнтів з тяжким перебігом захворювання. Не було виявлено різниці для груп середньої тривалості перебування в лікарні або пацієнтів з механічною вентиляцією, яких успішно екстубували (36 % у групі івермектину проти 15 % у групі звичайного догляду; P = 0,07)[229].
Разом з тим було проведене подвійне сліпе, плацебо-контрольоване дослідження ескалації дози івермектину. Воно показало, що івермектин, як правило, добре переноситься при вищих за звичайні дози та частому призначенні під час лікування коронавірусної хвороби 2019[230]. В іншому дослідженні було також показано, що івермектин асоціювався з нижчою летальністю під час лікування COVID-19, особливо у пацієнтів, які потребували вищого вмісту кисню при вентиляційній підтримці[231].
Сучасні метааналізи досліджень івермектину з усього світу показують переконливу тенденцію до потужних переваг препарату проти SARS-CoV-2. Івермектин, розроблений у 1975 році, призвів до викорінення «пандемії» паразитарних хвороб на багатьох континентах і його першовідкривачі, Вільям Кемпбелл і Ōмура Сатоші здобули Нобелівську премію з фізіології або медицини у 2015 році[232]. Проте Агентство з контролю за харчовими продуктами та ліками США (Food and Drug Administration, FDA) та американське медичне товариство FLCCC (Front Line Covid-19 Critical Care Alliance) рекомендують продовжувати його використання лише у межах клінічних досліджень, адже самовільне його вживання пацієнтами у вигляді ветеринарних препаратів призвело у деяких випадках до небажаних наслідків. Його препарати для тварин сильно відрізняються від препаратів для людей. Ліки для тварин часто мають високу концентрацію і такі надмірні дози можуть бути дуже токсичними для людини[233].
Британська група по розробці рекомендацій щодо івермектину нещодавно провела ґрунтовну розробку рекомендацій по лікуванню ним з використанням стандартних керівних принципів, яких дотримується ВООЗ. Була створена технічна робоча група, яка зробила систематичний огляд і метааналіз. Вона прийшла до висновку, що достовірні докази впливу івермектину на виживання є переконливими, і рекомендувала беззастережно прийняти його для використання в профілактиці та лікуванні коронавірусної хвороби 2019[234].
Нітазоксанід
Саліциланіліди
Дослідження показали, що один з саліциналідів[235] під номером 11 показав у дослідженнях на мишах як високу протикоронавірусну активність, яка проявляється всередині вірусу, що здатне реалізуватися проти усіх варіантів SARS-CoV-2. так і протизапальні властивості, знижуючи рівень інтерлейкіну-6[236].
Плітідепсин
Повідомлено, що препарат плітідепсин (аплідин), який має обмежене клінічне схвалення, володіє противірусною активністю (IC90 = 0,88 нМ) у 27,5 разів потужнішим, ніж ремдесивір проти SARS-CoV-2 in vitro, з обмеженою токсичністю в культурі клітин. Він є представником класу сполук, відомим як дидемніни. Противірусна активність плітидепсину щодо SARS-CoV-2 опосередковується через інгібування відомого цільового eEF1A, що є ключовим для розмноження та поширення коронавірусу. Продемонстровано ефективність лікування плітідепсином in vivo на двох моделях мишей з інфекцією SARS-CoV-2 із зменшенням реплікації коронавірусу в легенях на два порядки за допомогою цього профілактичного лікування. Результати вказують на те, що плітідепсин є перспективним терапевтичним кандидатом для противірусної терапії коронавірусної хвороби 2019[237]
Молнупіравір
Головний медичний радник Білого дому, доктор Ентоні Фаучі заявив, що Управління з питань харчових продуктів та медикаментів США якомога швидко перегляне дані про новий препарат проти коронавірусної хвороби 2019 компанії «Merck and Ridgeback Biotherapeutics» для видачі можливого дозволу на екстрене використання. Компанія заявили, що їх пероральний противірусний препарат молнупіравір (MK-4482, EIDD-2801, торгова назва Лагевріо[238]) зменшив ризик госпіталізації або смерті невакцинованих пацієнтів із легким або помірним клінічним перебігом хвороби приблизно на 50 %. У третій фазі клінічного дослідження MOVe-OUT, в якому брали участь 775 учасників, які приймали або молнупіравір або плацебо, вісім осіб, які отримували плацебо, померли протягом 29 днів. Ніхто з учасників, які приймали молнупіравір, не помер. Ці дані були оприлюднені у пресрелізі компанії і поки що не підтверджені незалежними рецензіями. США погодилися придбати 1,7 млн курсів препарату. Заявлено, що уряд США має можливість придбати ще більші дози, якщо препарат буде схвалений[239]. Молнупіравір показав зниження ризику госпіталізації та/або смерті в усіх ключових підгрупах; на ефективність не впливали терміни появи симптомів або основний фактор ризику. Крім того, виходячи з доступних даних секвенування вірусів (приблизно у 40 % учасників), препарат продемонстрував постійну ефективність щодо варіантів SARS-CoV-2 «Гамма», «Дельта» та «Мю». «Merck and Ridgeback Biotherapeutics» очікує виготовити 10 мільйонів курсів лікування до кінця 2021 року, а більше доз очікується в 2022 році.[240]. Велика Британія першою у світі схвалила цей препарат для лікування коронавірусної хвороби 2019. Клінічні випробування довели, що він приблизно вдвічі знижує ризик госпіталізації та смерті при цій хворобі. Ліки схвалило британське Агентство з контролю за лікарськими засобами та виробами медичного призначення (MHRA). Уряд країни вже замовив 480 тис. курсів препарату, які мають надійти до кінця 2021 року.[241]. «Merck» підписала угоду, що дозволить виробляти та продавати молнупіравір у вигляді дженериків[242].
Паксловід
Американська компанія «Pfizer» заявила, що створений її фахівцями препарат паксловід, якій діє проти SARS-CoV-2, при коронавірусній хворобі 2019 знижує на 89 % ризик смерті й госпіталізації серед дорослих пацієнтів із категорій ризику. Він діє як інгібітор протеази 3CL, що блокує фермент, необхідний цьому коронавірусу для розмноження. Представник «Pfizer» заявив, що компанія достроково припинила клінічні випробування препарату, оскільки початкові результати вже були дуже позитивні. Заявлено, що компанія подала результати проміжних випробувань свого препарату до регуляторного органу з питань лікарських засобів у США Агентства з контролю за харчовими продуктами та ліками (Food and Drug Administration, FDA) задля отримання дозволу на екстрене використання, що було надано. Уряд Великої Британії замовив 230 тисяч доз цього препарату[243]. Паксловід (PF-07321332; ritonavir) на основі проміжного аналізу фази 2/3 EPIC-HR (оцінка інгібування протеази для коронавірусної хвороби 2019 у пацієнтів високого ризику) рандомізованого подвійного сліпого дослідження негоспіталізованих дорослих пацієнтів, які мають високий ризик переходу хвороби у тяжку форму, показав гарний результат — до 28 дня не було зареєстровано жодної смерті у групі пацієнтів, які отримували PAXLOVID™, порівняно з 10 смертями у групі пацієнтів, які отримували плацебо. Статистична значущість цих результатів була високою (p<0,0001). Одночасне застосування нірматрелвіру з низькою дозою ритонавіру допомагає уповільнити метаболізм або розпад PF-07321332 (ці 2 компоненти й складають препарат PAXLOVID™), щоб він залишався активним в організмі упродовж тривалішого періоду часу у вищих концентраціях, щоб допомогти боротися з вірусом[244]. «Pfizer» підписала угоду, що дозволить виробляти та продавати цей свій препарат у 95 бідніших країнах, куди ввійде й Україна, як держава із нижчими за середній світовий рівень доходами[242].
Етіотропне лікування супутніх станів і коінфекцій
Рекомендовано призначення впродовж першої години після надходження пацієнта за наявності ознак сепсису емпіричного лікування проти ймовірних збудників, які могли стати причиною розвитку його. Також за підозри на зараження вірусом грипу, ця емпірична терапія повинна включати інгібітори нейрамінідази, які мають активність проти вірусу грипу: озельтамівіру фосфат, занамівір, перамівір і балоксавіру марбоксил.
Патогенетична терапія
Протизапальна терапія при настанні імунопатологічної фази коронавірусної хвороби 2019 має призначатися поступово, проте в разі відсутності ефекту або ж погіршення стану у тяжких хворих роздуми про корекцію лікування не мають тривати більше 24-48 годин.
За наявності помірної гарячки доцільно її не зменшувати через нестійкість коронавірусу до підвищеної температури тіла. У разі поганої переносимості гарячки або її надмірності (збільшення температури тіла вище 40 °C, погане індивідуальне самопочуття навіть при нижчих цифрах) бажано у помірних дозах вживати жарознижувальні засоби (щоб температура тіла не падала нижче 38 °C) перевагу надаючи парацетамолу. Його слід приймати не більше 1 г на прийом і не більше 3 г на добу. Слід уникати використання високих доз ібупрофену (≥2,4 г на добу) у хворих з неконтрольованою артеріальною гіпертензією, застійною серцевою недостатністю, ішемічною хворобою серця, захворюванням периферичних артерій та / чи судинними захворюваннями центральної нервової системи.
Моноклональні антитіла
Інгібітори інтерлейкіну-6 (IL-6) можуть полегшити тяжке ураження легеневої тканини, яке спричинює вивільнення цитокінів у пацієнтів з тяжкими проявами коронавірусної хвороби 2019. 6 липня 2021 року видано рекомендації ВООЗ про застосовування антагоністів інтерлейкіну-6 пацієнтам із тяжким чи критичним перебігом коронавірусної хвороби 2019 разом із кортикостероїдами. Дослідження, скоординовані ВООЗ в партнерстві з Королівським і Університетським коледжами Лондона, Брістольською університетом і Фондом охорони здоров'я Гая і Сент-Томаса, показало, що введення інгібіторів інтерлейкіну-6, а також кортикостероїдів знижує ризик смерті на 17 % в порівнянні з використанням тільки кортикостероїдів, а ризик штучної вентиляції легень (ШВЛ) знижується на 21 %[245][246].
Сарілумаб
Детальніші відомості з цієї теми ви можете знайти в статті Сарілумаб.
Тоцилізумаб
Детальніші відомості з цієї теми ви можете знайти в статті Тоцилізумаб.
Сотровірімаб / Сотровімаб
Детальніші відомості з цієї теми ви можете знайти в статті Сотровірімаб.
14 січня 2022 року ВООЗ заявило, що цей препарат «умовно рекомендований для лікування легкого або середнього ступеня тяжкості коронавірусної хвороби 2019 у пацієнтів, які мають високий ризик госпіталізації»[225].
Маврілімумаб
Детальніші відомості з цієї теми ви можете знайти в статті Маврілімумаб.
Екулізумаб
Детальніші відомості з цієї теми ви можете знайти в статті Екулізумаб.
Регданвімаб
Детальніші відомості з цієї теми ви можете знайти в статті Регданвімаб.
Інші препарати та комбінації моноклональних антитіл
- Бамланівімаб і етесевімаб. У лютому 2021 року Агентство з контролю за харчовими продуктами та ліками США (Food and Drug Administration, FDA) видало дозвіл на екстрене застосування комбінації моноклональних антитіл — бамланівімаба і етесевімаба для лікування дорослих і дітей з легким і середньотяжким клінічним перебігом коронавірусної хвороби 2019, підтвердженої позитивним результатом ПЛР і ризиком тяжкого перебігу захворювання. Комбінація може вводитися лише в тих медичних закладах, в яких можливе лікування тяжкої інфузійної реакції, як то анафілаксії, за необхідності. У клінічних дослідженнях одноразова внутрішньовенна інфузія бамланівімаба і етесевімаба значно знизила кількість госпіталізацій і смертей упродовж 29 днів спостереження, в порівнянні з плацебо. Безпека і ефективність цієї експериментальної терапії для лікування коронавірусної хвороби продовжує оцінюватися. Бамланівімаб і етесевімаб зв'язуються з різними сайтами S — білка збудника. Моноклональні антитіла не дозволені для пацієнтів, які потребують кисневої підтримки, через те, що вони можуть бути пов'язані з гіршими клінічними результатами[247][248]. 25 червня 2021 року Управління з продовольства і медикаментів (FDA) відізвало рекомендацію застосування цих препаратів для лікування коронавірусної хвороби 2019 в США. До цього їх було дозволено для лікування хворих із середньотяжким перебігом, у яких прогнозувалось погіршення стану. У США наразі циркулюють варіанти Sars-Cov-2, що викликають занепокоєння, а ці препарати, що вводяться разом, не дозволені до застосування у штатах і на територіях, що підлягають юрисдикції США, і в яких останнім часом виявлена стійкість до цих ліків, що перевищує 5 %. Про що і йдеться у рекомендаціях з лікування коронавірусної хвороби 2019, виданих Управлінням з продовольства і медикаментів[249]. Хоча 25 червня 2021 року розповсюдження бамланівімабу плюс етесевімабу в США було призупинено через збільшення загальної частоти двох варіантів SARS-CoV-2, що викликають занепокоєння та циркулюють по всій країні: гамма і бета-варіанти. В останні місяці дельта-варіант став переважним, що циркулює у всіх штатах. Оскільки комбінація бамланівімабу плюс етесевімабу зберігає активність проти дельта-варіанта, який має мутації L452R та T478K. Продемонстровано, що сприйнятливість до бамланівімабу плюс етесевімабу зберігається в лабораторних дослідженнях. Тому станом на 2 вересня 2021 року використання та розповсюдження цих моноклональних антитіл проти SARS-CoV-2 було відновлено у всіх штатах і територіях юрисдикції США. У лабораторних дослідженнях цей варіант також виявився сприйнятливим до касирівімабу разом з імдевімабом і до сотровімабу, тому ці моноклональні антитіла продовжують також рекомендуватися для лікування хворих із середньотяжким перебігом, у яких прогнозується погіршення стану. Оскільки циркулюючі резистентні варіанти SARS-CoV-2 швидко змінюються, використання та розповсюдження бамланівімабу плюс етесевімабу або інших моноклональних антитіл може бути обмежене в районах із підвищеною частотою циркуляції варіантів, що помітно знизили сприйнятливість in vitro до цього режиму[250].
- Касиривімаб та імдевімаб. У лютому 2021 року Агентство з контролю за харчовими продуктами та ліками США (Food and Drug Administration, FDA) видало дозвіл на екстрене застосування комбінації моноклональних антитіл — касиривімаба та імдевімаба для лікування дорослих і дітей з легким і середньотяжким клінічним перебігом коронавірусної хвороби 2019, підтвердженої позитивним результатом ПЛР і ризиком тяжкого перебігу захворювання. Комбінація може вводитися лише в тих медичних закладах, в яких можливе лікування тяжкої інфузійної реакції, як то анафілаксії, за необхідності. Дозування для дорослих та педіатричних пацієнтів (віком від 12 років і старше, вагою не менше 40 кг) становить 1200 мг касиривімабу та 1200 мг імдевімабу. Їх вводять разом по одному внутрішньовенно впродовж щонайменше 60 хвилин. Їх слід вводити разом одразу після отримання позитивних результатів безпосереднього вірусного тестування та впродовж 10 днів після появи клінічних проявів. Безпека касиривімабу та імдевімабу заснована на аналізі спостереження 799 амбулаторних хворих у R10933-10987-COV-2067, рандомізованому, подвійному сліпому, плацебо-контрольоване клінічному дослідженні серед амбулаторних дорослих пацієнтів з легкими та середньотяжкими проявами коронавірусної хвороби 2019. Показано, що у клітинах культури Vero E6, препарати нейтралізували SARS-CoV-2 (ізолят USA-WA1 / 2020) зі значеннями 0,006 мкг / мл і 0,005 мкг / мл відповідно. Антитілозалежна клітинно-опосередкована цитотоксичність та антитілозалежний клітинний фагоцитоз оцінювалися за допомогою клітин-мішеней Jurkat, що експресують білок SARS-CoV-2. Комбінація касиривімабу та імдевімабу опосередковувала цитотоксичність з ефекторними клітинами природних кілерів людини[251].
- Продовжується дослідження інших моноклональних антитіл. Виявлено, що моноклональне антитіло SARS2-38 націлене на ту частину S-білка коронавірусу, яка мало змінюється внаслідок мутацій, і на яку не діють інші антитіла. Тому воно може працювати проти найпоширеніших сьогодні варіантів SARS-CoV-2[252].
3 вересня 2021 року Колегія з рекомендацій щодо лікування коронавірусної хвороби 2019 рекомендувала використовувати моноклональні антитіла проти SARS-CoV-2 для лікування легкого та середньотяжкого клінічного перебігу хвороби та для постконтактної профілактики інфекції SARS-CoV-2 у осіб, які мають високий ризик прогресування до тяжкого перебігу. Колегія запропонувала надання пріоритету лікуванню хвороби над постконтактною профілактикою. Пріоритет перед вакцинованими особами, які, як очікується, мають адекватну імунну відповідь має належати невакцинованим або частково вакцинованим особам, які мають високий ризик розвитку тяжкого перебігу хвороби; вакцинованим особам, від яких не очікується адекватної імунної відповіді (як то особи з ослабленим імунітетом)[253].
Показано у проведеному дослідженні, що введення в домашніх умовах громадськими інтегрованими парамедиками препаратів моноклональних антитіл створило важливу основу пацієнтам з високим ризиком прогресування коронавірусної хвороби 2019 для запобігання від звернення до департаменту невідкладної допомоги та потреби госпіталізації[254].
Очищення крові від надмірної кількості цитокінів та інших медіаторів запалення
Агентство з контролю за харчовими продуктами та ліками США (Food and Drug Administration, FDA) видало дозвіл на екстрене використання пристрою очищення крові для лікування пацієнтів віком 18 років або старше з підтвердженою коронавірусною хворобою 2019, які прийняті до реанімаційного відділення з підтвердженою або неминучою дихальною недостатністю. Дозволений пристрій працює за рахунок зменшення кількості цитокінів та інших медіаторів запалення, які контролюють імунну відповідь, шляхом фільтрації крові та повернення відфільтрованої крові пацієнту[255].
Аскорбінова кислота (вітамін C)
Детальніші відомості з цієї теми ви можете знайти в статті Вітамін C.
Кверцетин
Детальніші відомості з цієї теми ви можете знайти в статті Кверцетин.
Оксид азоту
Детальніші відомості з цієї теми ви можете знайти в статті Оксид азоту.
Колхіцин
Детальніші відомості з цієї теми ви можете знайти в статті Колхіцин.
Внутрішньовенна дезінтоксикаційна терапія
Проводиться з обережністю у пацієнтів з тяжкою пневмонією без ознак шоку, тому що агресивне внутрішньовенне введення розчинів може погіршити оксигенацію, особливо в умовах обмеженої можливості проведення штучної вентиляції легень.
Ставлення до глюкокортикостероїдів
Глюкокортикостероїди збільшують тривалість перебування вірусів в організмі, таким чином затримуючи терміни запалення. Їхня здатність пригнічувати імунітет призводить до зниження захисних властивостей та поширення вірусів по органах в організмі. Дослідження застосування глюкокортикостероїдів у лікуванні грипу, респіраторно-синцитіальної інфекції, близькосхідного коронавірусного респіраторного і тяжкого гострого респіраторного синдрому показали підвищення ризиків смерті серед осіб, які їх отримували, збільшення тривалості перебування у відділенні інтенсивної терапії, а також ризиків виникнення вторинних бактеріальних чи грибкових інфекцій. Виявлено маніфестацію цукрового діабету та аваскулярного некрозу як ускладнень терапії глюкокортикостероїдами[256].

Проте 16 червня 2020 року представник проведених у Великій Британії рандомізованих досліджень у хворих на коронавірусну хворобу 2019 поінформував у пресрелізі, що отримано попередні результати, які свідчать, що препарат дексаметазон може врятувати життя пацієнтам, які критично хворіють. Для пацієнтів, що під'єднані до ШВЛ, таке лікування зменшило летальність приблизно на третину, а для пацієнтів, які потребують лише неінвазивної кисневої підтримки, летальність була скорочена приблизно на одну п'яту. Користь спостерігалася лише у пацієнтів, які тяжко хворіли на COVID-19, і не спостерігалася у пацієнтів із легшими клінічними формами. ВООЗ привітала результати клінічних випробувань і чекатиме повного аналізу даних, в тому числі, отримання позитивних рецензій на це дослідження[257].
Дослідження американських науковців з Нью-Йорка стосовно дії глюкокортикостероїдів при коронавірусній хворобі 2019 показало, що їх результати корелюють з британським дослідженням RECOVERY, і свідчать про те, що для оптимального застосування цих препаратів потрібний відбір хворих за певними клінічними і лабораторними показниками. Зокрема показано, що терапія ними в перші 7 днів хвороби неефективна у всіх групах хворих і не призводить до якого-небудь позитивного ефекту, бо вони здатні придушити власний захист організму в період активного розмноження SARS-CoV-2 і нанести, тим самим, шкоди в перший тиждень хвороби. Якщо в дебюті захворювання їх призначати, це надає вірусу можливості необмеженої реплікації, а при Дельта і Омікрон варіантах вірусне навантаження в сотні разів вище за таке у попередніх варіантів. Усі подальші ураження є індукованими великою кількістю SARS-CoV-2.
Отримані дані, що тест на С-реактивний білок може допомогти лікарям ухвалити рішення про призначення глюкокортикоїдних гормонів. Якщо у пацієнта цей білок підвищувався до ≥200 мг / л, то застосування цих гормонів (як то метилпреднізолон, преднізолон, дексаметазон) показало зменшення на 77 % ризику потрапляння на ШВЛ чи смерті. Тоді як рівень С-реактивного білку сягав ≤100 мг / л, то ризик потрапити на ШВЛ чи померти збільшувався майже втричі при застосуванні цих гормонів. Зроблено також висновок, що небажано використовувати глюкокортикоїди в ранній фазі хвороби, тому що це може привести до несподіваних результатів: затримки коронавірусу в організмі, бактеріальної чи грибкової суперінфекції[258]. Дослідження RECOVERY проводиться з березня 2020 року, 6 липня припинено набір хворих, оскільки кількість залучених склало близько 6000 осіб, дані вивчені у 94 % пацієнтів у 175 лікувальних закладах. Воно показало, що всі пацієнти на будь-якій респіраторній підтримці потребують призначення дексаметазону, і він істотно знижує ризик смерті. Але у пацієнтів без респіраторної підтримки це дослідження не показало ніяких переваг застосування дексаметазону. Виявлено, що призначення дексаметазону краще допомагає чоловікам і особам віком менше 70 років. Найбільший ефект отримано у пацієнтів, в яких або не було цукрового діабету або був, але з невисокими рівнями глюкози крові ≤7,8 ммоль / л. Альтернативним предиктором призначення дексаметазону може служити рівень D-димеру >3 мкг / мл чи тропонінів >0,1 нг / мл[259]. Рандомізоване дослідження показало, що найкращою дозою є 6 мг дексаметазону на добу, у порівнянні з цією дозою призначення 12 мг дексаметазону статистично не зменшило кількість днів життя без надання життєвої підтримки упродовж 28 днів[260].
Станом на 2021 рік вважається, що «це реагуюча на глюкокортикостероїди хвороба. При цьому час призначення є критичним. Занадто рано не можна, проте й не занадто пізно»[190].
Інгібітори ангіотензин-перетворюючого ферменту і блокатори ангіотензинових рецепторів 1-го типу
Наразі не виявлено передумов для збільшення ураження легенів SARS-CoV-2 на тлі вживання препаратів для лікування серцево-судинних захворювань — інгібіторів ангіотензин-перетворюючого ферменту і блокаторів ангіотензинових рецепторів 1-го типу. Від застосування цих препаратів для лікування есенціальної гіпертензії в передбаченні гіпотетичного зараження SARS-CoV-2 не слід відмовлятися, як і непотрібно починати їх приймати без наявності показань з боку серцево-судинної системи задля можливої, але непідтвердженої, профілактичної дії для розвитку тяжких уражень легень під час коронавірусної хвороби 2019[261]. Застосування блокаторів ангіотензинових рецепторів 1-го типу (сартанів) і, меншою мірою, інгібіторів ангіотензин-перетворюючого ферменту збільшує вміст ангіотензину 2 в крові, і він починає зв'язуватися з більшою кількістю АТ-2 рецепторів. Як наслідок, доступність цих рецепторів для SARS-CoV-2 теоретично може зменшуватися[262]. Одночасно сартани можуть блокувати надмірну активацію АТ-1 рецепторів, яка, ймовірно, відбувається в умовах хвороби і є шкідливою для організму. Блокатори ангіотензинових рецепторів 1-го типу збільшують кількість ангіотензин-перетворюючого ферменту 2-го типу, що розщеплює ангіотензин-2 з утворенням ангіотензину 1-7. Останній здатен розширювати й легеневі судини. Оскільки одним із механізмів гострого ушкодження легень є зв'язування SARS-CoV-2 з ангіотензин-перетворюючим ферментом 2-го типу зі зменшенням утворення ангіотензину 1-7, терапія сартанами, теоретично, має перешкоджати цьому[263].
Ікатібант
Детальніші відомості з цієї теми ви можете знайти в статті Ікатібант.
Циклоспорин
Детальніші відомості з цієї теми ви можете знайти в статті Циклоспорин.
Сироватка крові перехворілих
Китайські лікарі пропонують застосувати для лікування введення сироватки крові, отриманої від перехворілих, яка має містити захисні антитіла проти SARS-CoV-2. Проте ВООЗ закликала ставитися до такого лікування з обережністю, адже таке лікування важко стандартизувати, оскільки різні перехворілі виробляють різну кількість протикоронавірусних антитіл і для того, щоб отримати лікувальну дозу треба взяти кров від багатьох реконвалесцентів, що є як морально, так і технічно проблемно. До того плазму необхідно зберігати з великими пересторогами[264]. Управління з контролю продовольства і медикаментів США (Food and Drug Administration, FDA) 23 серпня 2020 року дала дозвіл на застосування плазми перехворілих[265]. Начебто американське дослідження показало зниження летальності на 35 % серед осіб молодше 80 років через місяць після початку лікування плазмою на ранньому етапі хвороби. Такі попередні результати були опубліковані нещодавно. Це дослідження ще не пройшло наукове рецензування. Однак інші науковці критично назвали таку заяву грубим перебільшенням попередніх результатів дослідження, проведеного престижною клінікою Mayo Clinic. У дизайні цього дослідження не проведено вкрай важливе порівняння з пацієнтами, які не отримували плазму перехворілих[266]. Станом на 2021 рік не рекомендується використовувати низького і високого титру реконвалесцентну плазму для лікування хворих на коронавірусну хворобу 2019, що не мають ослабленого імунітету, не потребують кисневої підтримки, тих пацієнтів, хто знаходиться на ШВЛ за винятком участі клінічних випробуваннях[267]
Згідно з новим переглядом протоколу лікування хворих в Україні дозволено застосування при тяжких формах реконвалесцентної плазми (сироватки крові перехворілих), що містить нейтралізуючі антитіла класу IgG проти SARS-CoV-2 у високих титрах[197].
Гіпербарична оксигенація
Детальніші відомості з цієї теми ви можете знайти в статті Гіпербарична медицина.
Інтенсивна терапія
Критеріями критичного стану хворих, які потребують лікування у відділення інтенсивної терапії або реанімації, є[188]:
- гостра дихальна недостатність;
- септичний шок;
- інша органна недостатність, яка вимагає госпіталізації до відділення інтенсивної терапії.
Всім лежачим пацієнтам з тяжким перебігом хвороби здійснюється профілактика загальних ускладнень. Згідно з розрахунками 5 % хворих на коронавірусну хворобу 2019 знадобиться інтенсивна терапія.
Киснева вентиляція легень
Згідно з розрахунками 14 % хворих на коронавірусну хворобу 2019 потребують кисневої підтримки. У хворого може продовжуватися порушення дихання або гіпоксемія, навіть коли кисень доставляється через маску для обличчя з резервуарним мішком. Гіпоксемічна дихальна недостатність при гострому респіраторному дистрес-синдромі зазвичай є наслідком невідповідності внутрішньолегеневої вентиляції та перфузії / шунту і зазвичай потребує механічної вентиляції. Кисень з високим потоком через носові катетери / неінвазивна (за допомогою маски) вентиляція застосовується лише у деяких пацієнтів з гіпоксемічною дихальною недостатністю. Пацієнти, які отримували неінвазивну вентиляцію, мають високий ризик неефективності лікування, і пацієнтів, які отримували цей вид лікування, необхідно ретельно моніторувати стосовно можливого погіршення клінічного стану. Пацієнти, які отримують неінвазивну вентиляцію, повинні знаходитись у контрольованих умовах за наявності досвідченого персоналу, здатного застосувати ендотрахеальну інтубацію, якщо стан пацієнта гостро погіршиться або не покращиться після короткого випробування (близько 1-ї години). При цьому слід враховувати, що доказових рекомендацій щодо неінвазивної вентиляції не існує, а повідомлення про результати застосування цього методу у пацієнтів з ТГРС та БКРС обмежені. Неінвазивна вентиляція наразі не рекомендована при тяжкому клінічному перебігу грипу чи ГРВІ іншої етіології. У хворого на коронавірусну хворобу 2019 може тривати порушення дихання або гіпоксемія, навіть коли кисень подається через маску для обличчя з резервуарним мішком зі швидкістю потоку 10-15 л/хв, що, зазвичай, є мінімальним потоком, необхідним для підтримки інфляції мішка (FiO2 0,60-0,95). Пацієнти з гемодинамічною нестабільністю, поліорганною недостатністю (як при сепсисі) або порушенням психічного стану не повинні отримувати неінвазивну вентиляцію. Припускається, що новіші технічні системи реалізації цього методу з герметичним інтерфейсом не створюють широкої дисперсії повітря, що видихається, і тому вони мають низький ризик передачі збудників через повітря.
Ендотрахеальна інтубація проводиться для забезпечення інвазивної (штучної) вентиляції легень (ШВЛ). Показаннями для інтубації та переводу на ШВЛ є рефрактерна до неінвазивної підтримки гіпоксемія SpO2 менше 84 %, порушення свідомості, психомоторне збудження, задишка більше 45 дихань/хвилину із залученням допоміжних м'язів вдиху. Перевірку толерантності до неінвазивної респіраторної підтримки проводять оксигенацією 100 % O2 протягом п'яти хвилин через маску для обличчя з резервуарним мішком, клапанною маскою тощо[212]. Через те, що вона в цій ситуації проводиться хворому у тямі, який починає інстинктивно цьому опиратися, а також для забезпечення синхронізації з респіратором та досягнення цільових об'ємних показників (об'єм вдиху, pH крові тощо) проводиться глибока седація. Слід використовувати протоколи відлучення, що включають щоденну оцінку готовності хворого до спонтанного дихання. Також звести до мінімуму безперервну або періодичну седацію, орієнтуючись на конкретні кінцеві точки титрування (легка седація, якщо не протипоказана), або з щоденним перериванням седації. Пацієнтам із вираженим ГРДС рекомендується інвазивна вентиляція у положенні на животі більше 12 годин на день міняючи положення тіла кожні 3-4 години. Але слід уникати невиправданого відключення пацієнта від апарату штучної вентиляції, що призводить до небажаних наслідків, зокрема до ателектазу. Необхідно застосовувати вбудовані катетери для відсмоктування секрету дихальних шляхів і затискання ендотрахеальної трубки, коли потрібно відключення (наприклад, при переведенні на транспортну вентиляцію). Респіраторна підтримка проводиться із забезпеченням нормального газообміну (PaO2 в межах 60-75 мм рт. ст., SaO2 — 90-93 %). Тримати пацієнта слід у напівлежачому положенні (підйом голови в ліжку 30-45º). Починати кисневу терапію слід зі швидкістю 5 л / хвилину та регулювати швидкість потоку для досягнення цільового значення SpO2≥93 % у дорослих і SpO2≥92-95 % у вагітних. Діти з екстреними ознаками (утруднене чи відсутнє дихання, ГРДС, генералізований ціаноз, шок, кома або судоми) повинні отримувати кисневу терапію під час реанімаційних заходів до досягнення SpO2 ≥94 %[212].
Достовірні результати видужання деяких хворих з легеневими проблемами отримані при застосуванні методу екстракорпоральної мембранної оксигенації (штучні легені). Але метод є технічно складним і дуже кошторисним, через що його застосування є обмеженим.
Підтримувальна терапія у тяжких хворих
Для зменшення частоти пролежнів слід перевертати пацієнта з тяжкими проявами кожні дві години. Для зменшення гіподинамії необхідно активно мобілізувати хворого на початку хвороби, коли це безпечно. Для профілактики стресових виразок шлунко-кишкової системи, кровотеч з них слід якнайшвидше перейти на ентеральне (через рот) харчування (протягом 24–48 годин після надходження хворого в стаціонар). Застосовують блокатори H2-гістамінових рецепторів або інгібітори протонної помпи пацієнтам із факторами ризику таких ускладнень.
Антитромботична терапія
Задля зменшення ризику венозної тромбоемболії слід вводити гепарин з низькою молекулярною вагою (˂ 12 тис. дальтон) або звичайний гепарин (молекулярна вага в межах 12-16 тис. дальтон) 5000 одиниць підшкірно двічі на день в осіб без протипоказань. Тим, у кого є протипоказання, необхідно застосовувати механічну профілактику — переривчасті пневматичні компресійні пристрої.
Згідно зі звітом, опублікованим Національним центром здоров'я США, повна доза антикоагуляції низькомолекулярними чи нефракційними гепаринами перевершує низькі профілактичні дози в зменшенні потреби у кисневій підтримці, летальності у пацієнтів з коронавірусною хворобою 2019. Результати отримані на підставі трьох взаємопов'язаних клінічних випробувань REMAP-CAP, ACTIV-4 і ATTACC, що вивчають безпеку і ефективність повної дози антикоагуляції для лікування середньотяжких і тяжких форм клінічного перебігу, у порівнянні зі звичною нижчою дозою[268]. У ще одному рандомізованому клінічному дослідженні HEP-COVID показано, що терапевтична доза низькомолекулярних гепаринів зменшила рівень тромбоемболій та смерть від них порівняно зі стандартною тромбопрофілактикою звичайним гепарином серед стаціонарних пацієнтів із дуже підвищеним рівнем D-димеру. Ефект від лікування не спостерігався у пацієнтів із відділень реанімації[269].
Опубліковано результати відкритого багатоцентрового рандомізованого контрольованого дослідження (MICHELLE), яке показало, що розширена антикоагуляція низькими дозами ривароксабану після госпіталізації із приводу коронавірусної хвороби 2019 може знизити ризик венозної тромбоемболії без погіршення ризику кровотечі у пацієнтів із групи високого ризику, виписаних на амбулаторне лікування[270].
Лікування сепсису та септичного шоку
Детальніші відомості з цієї теми ви можете знайти в статті Сепсис.
Детальніші відомості з цієї теми ви можете знайти в статті Септичний шок.
Ведення вагітних із коронавірусною хворобою 2019
Вагітним із підозрою або підтвердженою хворобою проводиться терапія з урахуванням стандартів ведення вагітності. Використання досліджуваних терапевтичних препаратів поза межами клінічного дослідження розглядається на основі індивідуального аналізу ризику та корисності на основі потенційної користі для вагітної та безпеки для плода після консультації досвідчених акушерів за рішенням консиліуму. Рішення щодо екстрених пологів і припинення вагітності розглядається та ґрунтується на багатьох чинниках: вік гестації, стан вагітної та стабільність плоду, після мультидисциплінарних консультацій з акушерами, неонатологами та фахівцями з інтенсивної терапії. Не змінюють стандартного антикоагулянтного режиму під час вагітності та після пологів. У вагітних із підтвердженою коронавірусною хворобою 2019 без тяжких проявів не слід застосовувати тромбопрофілактику, якщо не призначено інше. Вагітним із вираженими проявами (висока гарячка, тривале вимушене положення тощо) призначається тромбопрофілактика. Для госпіталізованих вагітних із підтвердженою коронавірусною хворобою 2019, але за відсутності симптомів, проводиться стандартне оцінювання ризику для тромбопрофілактики в акушерстві. Якщо виявлено венозну тромбоемболію, лікування антикоагулянтами продовжують упродовж щонайменше 6 тижнів після пологів і щонайбільше 3 місяці. Профілактика венозних тромбоемболій у породіль з підтвердженою коронавірусною хворобою 2019 розглядається на основі індивідуального оцінювання ризику. Якщо передпологова профілактика не проводилась, післяпологова теж не проводиться за умов безсимптомного перебігу чи наявності помірних симптомів коронавірусної хвороби 2019 у випадку, якщо пологи були неускладненими й відсутні акушерські показання для післяпологової профілактики венозних тромбоемболій. Якщо проводилась передпологова профілактика через наявність коронавірусної хвороби 2019, слід продовжувати її впродовж 14 днів. Тоді потребу в ній необхідно повторно оцінити відповідно до співвідношення ризик-користь (тяжкості перебігу коронавірусної хвороби 2019 та інших факторів ризику)[212].
Амбулаторне лікування в країнах світу
Амбулаторне лікування в США
У США відсутній загальний для країни протокол лікування хворих на коронавірусну хворобу 2019 через непевність доказового лікування, проте у різних штатах, медичних закладах впроваджені локальні протоколи. Одним з таких, який часто застосовується в практиці, є протокол Східновірджинської медичної школи (EVSM), згідно з яким при лікуванні вдома хворих зі слабкими клінічними проявами рекомендується:
- Івермектин у добовій дозі з розрахунку 50—200 мкг / кг, приймати щодня, розділивши добову дозу на два прийоми;
- Вітамін С у добовій дозі 500 мг, розділивши її на два прийоми, і кверцетин у добовій дозі 250—500 мг, розділивши її на 3 прийоми ;
- Вітамін D3 2000 — 4000 од / добу;
- Комплекс вітамінів групи В;
- Цинк 75-100 мг / добу;
- Мелатонін 6-10 мг на ніч (оптимальна доза не визначена);
- Аспірин ASA 81-325 мг / добу (якщо до нього немає протипоказань);
- Флувоксамін 2 рази на день 10-14 діб.
У пацієнтів рекомендується моніторинг за допомогою домашньої пульсоксиметрії. Зниження сатурації нижче 94 % повинне спонукати до госпіталізації[271]
Амбулаторне лікування в Україні
Пацієнтам з підозрою на коронавірусну хворобу 2019, із легкою та середньої тяжкості клінічними формами захворювання, які не мають показань до госпіталізації, рекомендовано лікувати в амбулаторних умовах. Також включаючи ті ситуації, коли стаціонарна допомога недоступна, або у випадку інформованої відмови від госпіталізації потрібне надання медичної допомоги в амбулаторних домашніх умовах[183].
Рішення відносно лікування в амбулаторних умовах має прийняти лікар з надання первинної медичної допомоги після клінічної оцінки стану пацієнта та безпеки його домашнього середовища, провівши опитування. Так можуть лікуватися лише пацієнти, що не мають супутніх серйозних хронічних захворювань, таких як хвороби легень чи серця, ниркової недостатності, первинних та вторинних імунодефіцитів, алергологічної та автоімунної патології, які зумовлюють підвищений ризик розвитку ускладнень. Переводити на амбулаторне лікування слід одужуючих пацієнтів, які вже не потребують цілодобового нагляду. Обґрунтування рішення про лікування в амбулаторних умовах вноситься до форми первинної облікової документації[183].
У випадку звернення пацієнта до лікаря первинної медичної допомоги (сімейний лікар, страховий тощо) за допомогою засобів дистанційного зв'язку той має провести оцінювання стану хворого відповідно до класифікації за ступенем тяжкості клінічного перебігу захворювання. Якщо пацієнт має легкі прояви клінічного перебігу захворювання, то лікар дає рекомендації щодо самоізоляції, лікування у разі погіршення стану. Якщо ж у пацієнта тяжкий клінічний перебіг захворювання, то лікар дає рекомендацію виклику екстреної медичної допомоги за номером 103 або сам викликає бригаду екстреної медичної допомоги[183].
Пацієнти, яких залишають на амбулаторному лікуванні, та спільно проживаючі з ними особи мають бути поінформовані щодо:
- необхідності повноцінного дотримання особистої гігієни;
- основних заходів і засобів з профілактики інфікування інших мешканців;
- безпечності догляду;
- необхідності обмежень побутових контактів;
- методів зв'язку із медичним персоналом (наприклад, мати номер телефону, за яким потрібно телефонувати у разі погіршення стану);
- способів транспортування пацієнта до амбулаторно-поліклінічного закладу в разі потреби (зокрема, визначення часу і входу до закладу).
У разі появи клінічних проявів у контактної особи медичні працівники оцінюють її клінічний стан і приймають рішення щодо необхідності госпіталізації чи доцільності амбулаторного лікування. У разі ухвалення рішення про необхідність госпіталізації, здійснюється комплекс заходів, спрямованих на обмеження подальшого поширення хвороби[183].
Рекомендації зі стаціонарного лікування в інших країнах
У США
Нетяжкий перебіг
Стаціонарним хворим з нетяжким клінічним перебігом (нетяжка пневмонія) згідно з локальним протоколом Східновірджинської медичної школи (EVSM) призначаються:
- Івермектин у добовій дозі із розрахунку 150—200 мкг / кг розділивши її на 2 прийоми;
- Вітамін С у добовій дозі 500 мг перорально, розділивши її на 4 прийоми та кверцетин у добовій дозі 250—500 мг, розділивши її на 3 прийоми на день;
- Вітамін D3 20 000 — 60 000 мо разова пероральна доза. Кальцифедіол 200—500 мкг є альтернативою. Потім 20000 мо D3 (або 200 мкг кальцифедіолу) щотижня щоденно до виписки з лікарні;
- Вітаміни комплексу групи В;
- Цинк 75-100 мг / добу;
- Мелатонін 10 мг на ніч (оптимальна доза не визначена);
- Еноксапарин 60 мг на день;
- Метилпреднізолон 40 мг кожні 12 годин на годину; збільшення до 80 мг кожні 12 годин, якщо є погана реакція на лікування.
Переведення до відділення інтенсивної терапії при погіршанні хвороби, посиленні респіраторних ознак та артеріальній десатурації[271].
У схемі лікування, яке пропонує Американський інститут здоров'я, рекомендується у випадку середньотяжкого перебігу без необхідності кисневої підтримки застосування ремдесивіру 200 мг в/в в перший день, та з 2 по 5-й день по 100 мг, тоді як введення дексаметазону не вважається потрібним[272].
Тяжкий перебіг
Для лікування хворих з тяжким клінічним перебігом у стаціонарі (реанімаційні відділення) при гіпоксії, що вимагає кисневого постачання ≥ 4 л / хв. Основне лікування (гасіння «цитокінового шторму») включає:
- метилпреднізолон 80 мг навантажувальна доза, потім по 40 мг кожні 12 годин щонайменше впродовж 7 днів та / або до переведення з реанімаційного відділення. У пацієнтів з поганою реакцією дозу слід збільшити до 80-125 мг двічі на добу. В оновлених рекомендаціях Американської асоціації інфекціоністів (IDSA) з лікування коронавірусної хвороби 2019 у госпіталізованих пацієнтів із тяжким клінічним перебігом, яким не можна призначити кортикостероїди через протипоказання, рекомендаційна група асоціації пропонує використовувати ремдесивір разом з баріцитинібом, а не лише один ремдесивір, хоча й констатує, що це є умовною рекомендацією, з низькою достовірністю доказів[273][274].
- аскорбінова кислота (вітамін С) 3 г в/в — цю дозу вводити 4 рази на добу щонайменше 7 днів та / або до переведення з реанімаційного відділення.
- повна антикоагуляційна терапія (при надходженні до реанімаційного відділення та підключення до ШВЛ) еноксапарином, тобто 1 мг/кг поділивши дозу на 2 рази за добу. Коригування дози за кліренсом креатиніну <30 мл / хв. Гепарин пропонується при кліренсі <15 мл / хв.
- Ретельна назофарингеальна санація.
Завчасне припинення прийому аскорбінової кислоти та кортикостероїдів, ймовірно, призведе до ефекту повернення проявів — синдрому відміни[271].
Продовжується застосування тих базових препаратів, які використовуються при лікуванні на амбулаторному етапі, додається до них аторвастатин по 80 мг / добу[271].
Додаткове лікування включає:
- плазмоферез — цей метод слід враховувати у пацієнтів з прогресуючою недостатністю оксигенації, незважаючи на терапію кортикостероїдами. Пацієнтам може знадобитися до 5 сеансів видалення плазми.
- ще більші дози кортикостероїдів; болюсно (струмінно в/в) 250—500 мг / добу метилпреднізолону.
- половинна доза рекомбінантного тканинного активатору плазміногену (rTPA).
- EKMO[271].
Респіраторна підтримка ґрунтується на максимальному відтермінуванні ШВЛ. Здійснюється неінвазивна респіраторна підтримка за допомогою носової канюлі з низьким рівнем потоку кисню 1-6 літрів за хвилину. При наростанні дихальної недостатності використовується носова канюля високого рівню потоку, що дає змогу:
- досягнути дозвільної гіпоксемії (насиченість O2> 86 %);
- титрування FiO2 на основі результатів насиченості киснем пацієнта;
- здійснювати потік кисню від 60 до 80 л / хв;
- провести пробу інгаляційного флолану (епопростенол);
- досліджувати ефективність спроб самостійного дихання у співпраці з пацієнтом[271].
У разі неможливості подальшого проведення неінвазивної респіраторної підтримки через погіршення стану хворого здійснюється інвазивна механічна вентиляція легень, як включає:
- об'єм дихання близько 6 см³ О2/ кг маси тіла;
- найнижчий тиск витіснення та позитивний тиск на кінці видиху (англ. positive end-expiratory pressure / PEEP);
- седацію пацієнта, щоб уникнути самоекстубації;
- інгаляційний флолан (епопростенол).
Стосовно позиції на животі хворого під час інвазивної респіраторної підтримки, то однозначності в цьому питанні не існує, однак це слід враховувати у тих, у кого співвідношення PaO2 / FiO2 <150[271].
Рятівна терапія включає:
- вкрай високі дози кортикостероїдів — 120—250 мг метилпреднізолону кожні 6-8 годин;
- продовження видалення плазми крові;
- половинна доза рекомбінантного тканинного активатору плазміногену (rTPA), якщо до цього він не вводився[271].
Обговорюється питання про застосування екстреної трансплантації легень.
Слід моніторувати:
- при надходженні: СРБ, натрій-діуретичний пептид В-типу, тропоніни, феритин, рівень тромбоцитів, співвідношення нейтрофіли-лімфоцити у периферичній крові, D-димер і рівень магнію.
- щодня продовжувати визначати: СРБ, феритин, D-димер та тромбоцити. СРБ і феритин є предикторами тяжкості захворювання, хоча показники феритину, як правило, відстають від показників СРБ.
- у пацієнтів, які отримують внутрішньовенно вітамін С, глюкометри здатні показати фальшиво високі значення глюкози в крові. Тому для визначення справжнього рівня глюкози в крові рекомендується застосування лабораторних методів[271].
Після зникнення необхідності в інтенсивній терапії застосовуються:
- еноксапарин 40-60 мг підшкірно щодня;
- метилпреднізон 40 мг на добу, надалі повільно знижується доза;
- вітамін С 500 мг 2 рази на добу;
- мелатонін 3-6 мг на ніч[271].
Супровід після виписки з лікарні включає:
- розширену тромбопрофілактику у пацієнтів високого ризику;
- лікування і профілактику посткоронавірусного синдрому;
- оцінка можливості подальшого прийому ГКС або припинення (моніторуючи СРБ);
- вживання Омега-3 жирних кислот;
- аторвастатин 40 мг щодня;
- мелатонін;
- полівітаміни, в яких входить комплекс групи В і вітамін D[271].
У схемі лікування, яке пропонує Американський інститут здоров'я, рекомендується у випадку тяжкого перебігу з необхідністю мінімальної кисневої підтримки застосування ремдесивіру 200 мг в/в в перший день, та з 2 по 5-й день по 100 мг, тоді як введення дексаметазону не вважається доцільним. Пацієнти, які до того отримували дексаметазон або інший кортикостероїд (преднізон, метилпреднізолон чи гідрокортизон) через наявність фонового захворювання, повинні продовжувати цю терапію. Лікування ремдесивіром може бути продовжено до 10 днів, якщо до 5-го дня не спостерігається значного клінічного поліпшення. За наявності більшого рівня кисневої підтримки (тобто тим пацієнтам, яким потрібен додатковий кисень, але не потрібна доставка його за допомогою пристрою з високим потоком, неінвазивної вентиляції, інвазивної механічної вентиляції або екстракорпоральної мембранної оксигенації) рекомендується призначення разом із ремдесивіром дексаметазону 6 мг внутрішньовенно або внутрішньовенно один раз на день протягом 10 днів або до виписки з лікарні, або іншими кортикостероїдами в еквівалентних дозах. У разі швидкого розвитку запалення, прогресування дихальної недостатності до необхідності ШВЛ та проведення ЕКМО також застосовується дексаметазон або інші кортикостероїди у великих дозах, внутрішньовенно вводяться або тоцилізумаб 8 мг/кг маси тіла або баріцитиніб. Можливе введення замість тоцилізумаба сарілумаба та тофацитиніба замість баріцитиніба[272].
Додаткові заходи лікування
Велике значення слід приділяти проблемам ментального здоров'я і психічної резистентності, особливо у дітей та осіб із категорій ризику. Зважаючи на руйнівну дію хвороби, включаючи соціальне дистанціювання, яке домінує в нашому повсякденному житті під час пандемії, важливо, щоб люди перевіряли один одного, дзвонили та спілкувались у відеочаті та були чутливими до унікальних потреб психічного здоров'я. Занепокоєння та страхи слід визнати, а не ігнорувати, а краще зрозуміти та вирішити, щоб це робили люди, громади та уряди[275].
Застереження стосовно деяких методів лікування
З початку пандемії коронавірусної хвороби 2019 численні продукти, що містять діоксид хлору[en] або його похідні, продаються самостійно або в поєднанні з іншими продуктами, з помилковими твердженнями, що вони можуть вилікувати коронавірусну хворобу 2019 та інші супутні недуги. Через це ВООЗ і її американське представництво не рекомендує перорально або парентерально використовувати продукти на основі діоксиду хлору або гіпохлориту натрію пацієнтам із підозрою на або діагностованою коронавірусною хворобою 2019 чи для чогось іншого. Немає жодних доказів ефективності цих сполук, і вживання або вдихання таких продуктів може спричинити серйозні несприятливі наслідки для здоров'я людини. Рекомендується населенню уникати вживання продуктів, що містять діоксид хлору або супутні речовини (гіпохлорит натрію, хлорне вапно тощо), А про весь маркетинг таких «чудодійних» продуктів з лікувальною метою слід повідомляти владі[276].
Група науковців з різних наукових закладів кількох країн вивчила поширення неправдивої інформації при коронавірусній хворобі 2019 у 87 країнах на 25 мовах з грудня 2019 року до квітня 2020 року. Результати дослідження виявили 2311 випадків надання неправдивої інформації. З 2276 звітів, для яких було доступне оцінювання текстів, 1856 були помилковими (82 %). Серед усіх категорій невірної інформації, яку відстежено, чутки була найпоширенішими. Більшість таких чуток стосувалися хвороби, передачі та летальності від COVID-19, заходів профілактики. Були неправдиві повідомлення про вживання в їжу часнику, утримання горла постійно вологим, необхідність уникати гострої їжі, що допомагає запобігти захворюванню. З'явилися чутки, що розпилення хлору може запобігти зараженню коронавірусом. З'явилися так звані методи лікування, такі як «диво мінеральні розчини», які передбачали змішування розчину хлориду натрію з лимонною кислотою. Або пиття алкоголю для підвищення імунітету. Інші повідомлення були для лікування пити чай та коров'ячу сечу чи гній в Індії, верблюжу сечу з хлорним вапном у Саудівській Аравії. Використавши такого роду фейкову інформацію, як вияснили науковці, 800 людей померло, 5 876 осіб було госпіталізовано і 60 повністю втратило зір, випивши метанол (метиловий спирт) як начебто ліки проти коронавірусної хвороби 2019. У Стамбулі більше 30-ти людей померло від вживання чистого спирту «для запобігання зараженню коронавірусом»[277].
Протокол лікування хворих в Україні
2.04 2020 року затверджено протокол надання медичної допомоги для лікування коронавірусної хвороби. Через те, що на момент затвердження протоколу відсутнє специфічне противірусне лікування коронавірусної хвороби 2019, а в світі проводиться понад 350 клінічних досліджень різних лікарських засобів, включаючи дослідження SOLIDARITY, співавтором якого є ВООЗ, у клінічний протокол внесено інформацію щодо лікарських препаратів, що рекомендовані офіційним органом Сполучених Штатів Америки, країн — членів Європейського Союзу, Великої Британії, Швейцарської Конфедерації, Японії, Австралії, Канади, Китайської Народної Республіки, Держави Ізраїль для лікування коронавірусної хвороби 2019, що зареєстровані з іншими показаннями або не зареєстровані в Україні, але застосовуються для лікування окремих груп пацієнтів з коронавірусною хворобою 2019 у цих країнах, що регламентується Законом України від 30 березня 2020 року № 539-IX «Про внесення змін до деяких законів України щодо забезпечення лікування коронавірусної хвороби (COVID-19)». Протокол ставить за мету реалізацію порядку призначення та застосування лікарських засобів для лікування груп пацієнтів із підтвердженою коронавірусною хворобою 2019 при середньотяжкому, тяжкому, критичному клінічному перебігу. При госпіталізації здійснюються для оцінки клінічного стану хворого та визначення можливості застосування зазначених у протоколі лікарських засобів з огляду на наявність індивідуальних протипоказань та взаємодію препаратів. Призначення лікарських засобів здійснюється за умови отримання інформованої згоди від пацієнта. Призначення цих препаратів не передбачено для застосування на амбулаторному етапі, без нагляду кваліфікованого лікаря. У протоколі розглянуто експериментальне етіологічне і патогенетичне лікування із застосуванням гідроксихлорохіну, хлорохіну, лопінавіру / ритонавіру, і, у вкрай тяжких випадках, фавіпіравіру, ремдесивіру та тоцилізумабу.
14 липня 2020 року МОЗ України внаслідок роботи робочої групи виключило лопінавір / ритонавір з протоколу лікування хворих на коронавірусну хворобу 2019 і змінило використання в ньому гідроксихлорохіну чи хлорохіну, припинивши їх призначення при тяжких формах у дорослих і у дітей, але залишивши для лікування хвороби у групах ризику, при середньотяжких формах у стаціонарі та постекспозиційній профілактики під наглядом лікаря. Залишено для лікування тяжких форм хвороби фавіпіравір, ремдесивір, тоцилізумаб[278].
17 вересня 2020 року МОЗ України після висновків робочої групи уточнило в протоколах лікування коронавірусної хвороби 2019 порядок застосування антипіретичних препаратів парацетамола та ібупрофена, застосування системних глюкокортикостероїдів перорально чи внутрішньовенно. У протоколи введена можливість використання при тяжкому перебігу або критичному стану дексаметазону чи інших, таких як гідрокортизон, метилпреднізолон чи преднізон. Доза дексаметазону 6 мг один раз/добу є еквівалентною з позиції глюкокортикоїдного ефекту 150 мг гідрокортизону (50 мг кожні 8 годин), 40 мг преднізону, 32 мг метилпреднізолону (8 мг кожні 6 годин або 16 мг кожні 12 годин). Уточнено характер антикоагулянтної терапії в лікуванні хворих на коронавірусну хворобу 2019. Передбачається дві схеми призначення антикоагулянтів. Перша застосовується у госпіталізованих пацієнтів і після виписки. Друга у хворих, які лікуються амбулаторно[212].
20 листопада 2020 року МОЗ України після висновків робочої групи дозволило в протоколах лікування коронавірусної хвороби 2019 використання 10 % нормального імуноглобуліну людини у хворих з тяжким перебігом захворювання. У пацієнтів з такою клінічною формою, в яких відбувається наростання інтоксикаційного синдрому, дихальної недостатності, разом з негативною лабораторною динамікою: прогресуюче підвищення рівня С-реактивного білка понад 50 Од, наростаюча абсолютна лімфопенія, підвищення рівня ферритину та інтерлейкіну 6 (ІЛ-6) є доцільність застосування внутрішньовенно 10 % імуноглобуліну людини нормального в дозі 0,8-1,0 г/кг один раз на добу впродовж 2-х діб від початку погіршення стану. Курсова доза становить 1,6-2,0 г/кг ідеальної маси тіла<[279].
Антикоагулянтна терапія
У госпіталізованих пацієнтів і після їхньої виписки не застосовується у хворих з високим ризиком кровотечі (зокрема, при низькому рівні тромбоцитів, недавніх значних кровотечах, після діалізу тощо). При надходженні пацієнта в лікарню слід врахувати ризики венозних тромбоемболій при діагностиці основної хвороби та впродовж усього періоду госпіталізації, а для пацієнтів з високим ризиком венозної тромбоемболії — впродовж 4-6 тижнів. Хворі, що до захворювання на коронавірусну хворобу 2019 отримували антикоагулянтну терапію з приводу фонових хвороб (фібриляція передсердь, венозна тромбоемболія, штучні клапани серця тощо), слід її продовжувати. Перехід на терапевтичну дозу замість пероральної антикоагулянтної терапії (антагоністи вітаміну К чи прямі пероральні антикоагулянти) відбувається у тяжкохворих, пацієнтів із шлунково-кишковими захворюваннями, із запланованими інвазивними процедурами, з нестабільними результатами дослідження міжнародного нормалізованого відношення (МНВ) та / чи за наявності взаємодій між лікарськими засобами[212].
Низькомолекулярні гепарини визнано препаратами вибору для фармакологічної профілактики тромбозів у хворих, що мають фактори високого ризику розвитку венозних тромботичних ускладнень (активний перебіг онкологічних хвороб; венозна глибока тромбемболія, епізод якої був раніше; ліжковий режим більше 3-х діб; встановлена раніше тромбофілія; значна травма чи операція раніше; вік 70 років і старше; серцева та / чи дихальна недостатність; інфаркт міокарда; інсульт; фонова ревматична хвороба; ожиріння з індексом маси тіла рівним чи більшим 30 кг/м2; застосування гормональної терапії). Для пацієнтів, що не перебувають у відділеннях інтенсивної терапії, рекомендується низька профілактична доза низькомолекулярних гепаринів, тоді як для хворих, що знаходяться у відділеннях інтенсивної терапії, рекомендуються високі профілактичні дози їх. Хворим, у яких розвивається чи розвинулася венозна тромбоемболія під час госпіталізації з коронавірусною хворобою 2019, рекомендовано лікування терапевтичними дозами низькомолекулярних гепаринів. Їх не слід застосовувати у пацієнтів з вираженою дисфункцією нирок, для яких нефракціонований гепарин може розглядатися на основі якнайретельнішої оцінки ризик / користь і у хворих на гепарин-індуковану тромбоцитопенію. У них фондапаринукс (2,5 мг 1 раз підшкірно) розглядається як альтернативне лікування. За наявності протипоказань до гепаринової профілактики венозної тромбоемболії, потрібно використовувати переміжну пневматичну компресію нижніх. Не доцільно регулярно змінювати режим антикоагулянтного лікування на основі рівнів D-димеру, тому що результати можуть варіювати залежно від використовуваного методу. Але підвищення рівня D-димеру є підозрілим на розвиток венозної тромбоемболії і має спонукати проведення візуалізації венозної тромбоемболії кінцівок. Також не рекомендується проводити систематичний моніторинг антикоагулянтної терапії за допомогою визначення рівнів анти-Xa[280] за винятком випадків застосування низькомолекулярних гепаринів у лікувальних дозуваннях. Проте за можливості слід визначити анти-Xa при підозрі на накопичення гепарину, і, відповідно, при підвищеному ризику виникнення кровотечі у пацієнтів з низькою або надмірною вагою тіла, нирковою недостатністю, за наявності геморагічного діатезу[212].
По закінченню лікування в стаціонарі і при продовженні його амбулаторно пацієнтам, які проводили хронічну терапевтичну пероральну антикоагулянтну терапію слід повернутися до неї і відновити повноцінний режим її застосування. У тих пацієнтів, у яких терапевтична антикоагулянтна пероральна терапія до цього не проводилася, але які отримували тромбопрофілактику на час госпіталізації, пропонується продовжити її в дозі для еноксапарину по 4000 анти-Ха MO один раз на добу впродовж двох тижнів. Дозу інших низькомолекулярних гепаринів як то надропарин, дальтепарин і беміпарин, які зареєстровані в Україні, потрібно визначати згідно з їхніми інструкціями для медичного застосування. Якщо є чинники ризику венозних тромбозів та емболій, а саме: перебування під час захворювання на коронавірусну хворобу 2019 у відділенні інтенсивної терапії чи реанімації, тромбофілія в анамнезі, ожиріння, тютюнокуріння, застосування високих доз естрогенів, тривала іммобілізація, хронічна серцева та дихальна недостатність, вік старший за 70 років, активний раковий процес, сімейний анамнез венозної тромбоемболії та / або серйозне оперативне втручання за останні 3 місяці, пропонується розширена тромбопрофілактика впродовж 4-6 тижнів після виписки зі стаціонару. Щоб зменшити контакт з медичними працівниками, по поверненню додому, можна розглянути питання переходу з низькомолекулярних гепаринів на прямі пероральні антикоагулянти, якщо пацієнт потребує подовження антикоагулянтної терапії, пероральний прийом препаратів можливий, немає порушення функції нирок. У негоспіталізованих хворих якщо їх стан дозволяє, потрібно стимулювати розширення фізичної активності для зниження ризику венозної тромбоемболії, надати їм інформацію, щоб вони знали про її ознаки та симптоми. При підозрі на венозну тромбоемболію хворий має бути направлений на відповідне діагностичне тестування. Упродовж очікування його результатів можна почати відповідну антикоагулянтну терапію, якщо підозра є достатньо великою, а ризик кровотечі — низьким. Якщо низькомолекулярні гепарини слід приймати вдома, потрібно заохочувати самостійне їх введення пацієнтами, аби уникнути контакту з медичними працівниками. Тривалість профілактики у негоспіталізованих пацієнтів (коли постійна антикоагулянтна терапія не потрібна) рекомендується впродовж 14 днів. Після цього доцільність пролонгації має бути переглянута.[212].
У хворих з підтвердженою коронавірусною хворобою 2019, які не мають симптомів або мають незначні симптоми, тобто при легкій формі, рекомендується не проводити профілактичну антикоагулянтну терапію. Всі діти, які госпіталізовані для лікування коронавірусної хвороби 2019, проходять обстеження при поступленні, а потім щоденно на можливість виникнення тромбозів. Рекомендується після госпіталізації моніторувати щоденно клінічний аналіз крові з підрахунком тромбоцитів, дослідження фібриногену, протромбінового часу, D-димеру. Усім дітям з підтвердженою хворобою, які мають ризик тромбозу, слід починати за необхідності його профілактику. Рішення про початок такої терапії у дитини приймається комісійно за участі дитячих інфекціоністів, гематологів і спеціалістів з невідкладної терапії. За наявності показань до тромболітичної терапії рекомендується використати низькомолекулярний чи нефракційний гепарин, спираючись на наявний досвід по застосуванню препаратів гепарину у дітей. Не рекомендовано застосування пероральних антикоагулянтів прямої дії через обмежені дані щодо їхнього застосування у дітей під час коронавірусної хвороби 2019. Терапевтична антикоагулянтна терапія рекомендується тим хворим дітям, що отримували її за різних причин перед госпіталізацією, з гемодинамічно нестабільною тромбоемболією легеневої артерії, загрозою виникнення тромбозу глибоких вен кінцівок чи підозрою на венозну тромбоемболію. Призначення антикоагулянтних препаратів дітям має бути персоніфіковане[212].
Застосування ремдесивіру
У разі ймовірності розвитку критичного перебігу з метою профілактики гострого дистрес-синдрому переважно впродовж 1-го тижня клінічних проявів можливе призначення ремдесивіру в перший день — навантажувальна доза у 200 мг один раз на добу (в/в упродовж 30-120 хв), з другого дня — підтримувальна доза 100 мг один раз на добу (також в/в упродовж 30-120 хв). Тривалість лікування — 5 днів для тих хворих, які не потребують ШВЛ чи ЕКМО. За відсутності ефекту від 5-денного призначення, чи якщо пацієнт перебуває на ШВЛ чи ЕКМО — курс лікування має бути 10 днів. Перед початком та щодня впродовж введення ремдесивіру у дорослих хворих рекомендовано визначати розрахункову швидкість клубочкової фільтрації. Його не слід застосовувати пацієнтам із розрахунковою швидкістю клубочкової фільтрації <30 мл/хв. Препарат необхідно застосовувати хворим з порушеннями функцій печінки виключно в тих ситуаціях, коли потенційна користь перевищує можливий ризик. Препарат не слід застосовувати пацієнтам, у яких активність АЛТ у сироватці крові більше, ніж уп'ятеро перевищує верхню межу норми. Необхідно негайно припинити введення препарату хворим, у яких активність АЛТ більше, ніж уп'ятеро перевищує верхню межу норми після лікування ремдесивіром. Прийом можна відновити тільки тоді, коли активність АЛТ менше, ніж уп'ятеро перевищує верхню межу норми[279][281].
Застосування фавіпіравіру
У разі відсутності ремдесивіру можна застосувати фавіпіравір. У перший день — навантажувальна доза по 1600 мг 2 рази на добу, надалі — по 600 мг 2 рази на добу впродовж 5-14 днів[279][281].
Застосування тоцилізумабу
При загрозі критичного перебігу і швидкого прогресування хвороби (інтерстиціальна пневмонія з гострою недостатністю дихання, прогресування її, необхідність підключення до неінвазивної або інвазивної вентиляції, наявність позалегеневих уражень органів) через гіперімунний цитоліз (лейкопенія та/або лімфопенія в клінічному аналізі крові; підвищений рівень С-реактивного білку; підвищений рівень ІЛ-6, ІЛ-2) можливе призначення тоцилізумабу не раніше 7-го дня від початку клінічних симптомів або з урахуванням рентгенологічних змін з розрахунку 4-6 мг/кг, рекомендована доза 400 мг, введення дози впродовж 1 години на 100 мл 0,9 % фізіологічного розчину. Повторне введення не рекомендується враховуючи невизначеність доказів додаткової користі[282].
Найбільший ефект від введення препарату прогнозується у пацієнтів до 60 років, що мають гарячку 38ºС та вище, швидку тенденцію до зниження сатурації і підвищений рівень С-реактивного білку вп'ятеро та вище. Введення тоцилізумабу пацієнтам старшим 60 років, без суттєвого підвищення температури тіла (у межах до 37,5ºС), абсолютним рівнем лімфоцитів 0,5х109/л та нижче на момент введення має здійснюватися з ретельним оцінюванням користь/шкода[279][281].
Протипоказання до призначення тоцилізумабу є:
- підвищення активності АСТ/АЛТ >5 раз вище норми;
- кількість нейтрофілів <500;
- кількість тромбоцитів < 50 000;
- сепсис, що не спричинений SARS-CoV-2;
- підвищений рівень прокальцитоніну >2 рази;
- наявність фонових станів, що можуть призвести до негативного прогнозу, ускладнений дивертикуліт, піодермія, негативний результат імуносупресивного лікування.[281]. Оскільки тоцилізумаб пригнічує утворення С-реактивного білку, зниження його рівня у пацієнта не потрібно враховуватися як ознака клінічного покращення[282].
10 % нормальний імуноглобулін людини
У пацієнтів з критичним перебігом хвороби, що супроводжується зростанням інтоксикаційного синдрому та дихальної недостатності, негативною лабораторною динамікою: прогресуючим підвищенням рівня С-реактивного білка >50 Од, прогресуванням абсолютної лімфопенії, збільшенням рівня ферритину та ІЛ-6 (якщо доступне їх визначення) можливе застосування 10 % імуноглобуліну людини нормального для внутрішньовенного введення в дозуванні 0,8-1,0 г/кг один раз на добу впродовж 2 діб від початку погіршення стану. Курсова доза становить 1,6-2,0 г/кг ідеальної маси тіла. Кратність і швидкість введення визначаються лікарем залежно від стану хворого. Добова доза може бути скоригована задля неперевищення максимального добового об'єму інфузійного лікування[281].
Обов'язковим при цьому є контроль стану системи згортання крові та діурезу, особливо у хворих з надлишком маси тіла. Через лікування препаратами імуноглобуліну може виникнути тромбоз. Особливо це можливе при ожирінні, атеросклерозі в анамнезі, порушенні серцевого викиду, артеріальній гіпертензії, цукровому діабеті з наявністю ангіопатій і випадків тромбозу, при набутій чи спадковій тромбофілії, тяжкій гіповолемі, при підвищеній в'язкості крові, літньому віці, тривалій іммобілізації, станах гіперкоагуляції, венозному чи артеріальному тромбозі в анамнезі, застосуванні естрогенів, використанні постійних центральних судинних катетерів. Тромбоз може виникнути навіть у разі відсутності цих факторів ризику[281].
Необхідно провести загальну оцінку в'язкості крові у хворих з ризиком підвищення її, включаючи таку, що пов'язана з кріоглобулінемією, хіломікронемією голодування, значно підвищеним рівнем тригліцеридів чи моноклональною гамопатією. Для хворих з ризиком виникнення тромбозів слід вводити 10 % імуноглобулін у мінімальних дозах і з мінімальною швидкістю введення. Перед застосуванням препарату слід переконатися у належному рівні насичення організму рідиною (гідратації) хворого[281].
Використання плазми реконвалесцентів
Для раннього специфічного лікування коронавірусної хвороби 2019 лише для пацієнтів, які мають лабораторно підтвердження хвороби, тяжкий чи критичний перебіг її або мають прогностичні предиктори прогресу до тяжкого чи критичного стану можливе використання плазми крові тих, хто видужав від коронавірусної хвороби 2019. Ця плазма містить нейтралізуючі антитіла класу IgG проти SARS-CoV-2 у високих титрах. Оптимальним вважається введення цієї плазми на початку хвороби до появи власних антитіл, а найефективнішим — у перші 72 години від появи перших клінічних проявів. Разова доза плазми для трансфузії становить 200 мл, але може бути й більшою (до 500 мл), якщо лікуючий лікар дійде висновку, що трансфузія більшого об'єму є доцільною. Залежно від тяжкості хвороби чи толерантності до вливань таким чином можливе повторне введення однієї чи двох доз по 200 мл. Протипоказаннями до введення плазми реконвалесцентів є тривалість хвороби більше 14 днів на момент розглядання рішення; наявність в анамнезі алергічних реакцій на кров чи продукти плазми; виявлений дефіцит IgA (рівень IgA слід перевіряти перед переливанням, оскільки рівень IgA не повинен бути менше нижньої межі норми); клінічні стани, при яких збільшення внутрішньосудинного об'єму може бути шкідливим для хворого як то при декомпенсованій застійній серцевій недостатності. Побічні ефекти застосування р плазми реконвалесцентів можуть включати легку гарячку; алергічні реакції, що включають у рідкісних випадках сироваткову хворобу; гостре посттрансфузійне ураження легень. З метою його уникнення слід надавати перевагу використанню плазми, забраної від донорів-чоловіків або тих донорів-жінок, які ніколи не були вагітними (враховуючи й відсутність абортів). Слід враховувати потенційний ризик передачі гемоконтактного інфекційного захворювання від донора[281].
Легкий перебіг
Згідно з протоколом МОЗ України слід надати захворілому інформацію щодо повноцінного харчування та відповідної регідратації. Можливе застосування жарознижувальних засобів (парацетамол, ібупрофен тощо) при гарячці та болю. При застосуванні ібупрофену в низьких дозах до 1200 мг на добу не спостерігається збільшення ризику серцево-судинних тромбозів[281].
Середньотяжкий перебіг
При лікуванні амбулаторно діють ті ж неспецифічні рекомендації як і при легкому перебігу. Не рекомендується використання системних кортикостероїдів для лікування тих хворих, що не потребують кисневої підтримки. Антибактерійні засоби протипоказані та призначаються виключно за наявності лабораторно підтвердженої супутньої бактеріальної інфекції або при обґрунтованій підозрі на неї. При виникненні утруднення дихання рекомендується якнайдовше бути в положенні «лежачи на животі», тому що це допомагає розкрити альвеоли, що спалися, та підвищити рівень кисню в крові[281].
Якщо пацієнта госпіталізовано, то призначаються низькомолекулярні гепарини, якщо це не протипоказано[281]. Слід розглянути можливість застосування ремдесивіру або фавіпіравіру, як противірусних препаратів прямої дії, не тільки для госпіталізованих, а й за можливістю амбулаторних хворих із груп ризику з легким і середньотяжким перебігом. В окремих випадках у відділеннях, що мають досвід застосування стандартного гепарину, можливо розглянути тривале інфузійне його введення під контролем активованого часткового тромбопластинового часу[283].
Тяжкий перебіг
Здійснюється оптимальна підтримуюча терапія в лікарняній палаті чи відділенні / палаті інтенсивної терапії. Надається обов'язково киснева підтримка, призначаються системні кортикостероїди перорально чи внутрішньовенно залежно від клінічної ситуації. Якщо ефекту від терапевтичних доз їх немає можуть бути розглянуті вищі дози системних кортикостероїдів відповідно до інструкції для медичного застосування[282]. Можливе застосування ремдесивіру, 10 % імуноглобуліну людини нормального,[281].
Критичний перебіг
Здійснюється оптимальна підтримуюча терапія виключно у відділенні або палаті інтенсивної терапії. Проводиться механічна вентиляція легень. Призначаються низькомолекулярні гепарини, якщо це не протипоказано. Системні кортикостероїди призначаються тільки внутрішньовенно. Проводиться спеціальна профілактика та лікування гострого респіраторного дистрес-синдрому:
- рекомендується вентиляція легень у положенні на животі впродовж >12 годин на день змінюючи положення тіла кожні 3-4 години;
- пропонується вищий PEEP замість нижчого. Титрування PEEP вимагає врахування переваг (зменшення ателектазів і поліпшення стану альвеол) проти ризиків (кінцеве перенапруження вдиху, що призводить до ураження легень і вищого опору легеневих судин);
- використовується поміркована рестриктивна стратегія внутрішньовенних інфузій, головний ефект якої полягає у скороченні тривалості вентиляції;
- рекомендується уникати відключення пацієнта від ШВЛ, що призводить до втрати PEEP, збільшення ателектазу. Пропонується використовувати вбудовані катетери для відсмоктування секрету з дихальних шляхів і затискання ендотрахеальної трубки, коли потрібно відключення від ШВЛ для необхідного транспортування пацієнта[281].
Антимікробні засоби не діють на коронавірус, тому протимікробна терапія повинна застосовуватися у хворих з коронавірусною хворобою 2019 виключно за наявності підтвердженої бактеріальної коінфекції, себто після отримання позитивного бактеріологічного дослідження крові та / або мокротиння. Проте враховуючи те, що результатів дослідження треба чекати кілька днів, антибіотики, за певних показань, можуть призначатися емпірично. З лабораторних показників окрім позитивних результатів бактеріологічного дослідження найінформативнішим вважається рівень прокальцитоніну в крові, якщо він у нормі, показання до антибіотикотерапії, як правило, відсутні. Менш інформативними є лейкоцитоз та зсув лейкоцитарної формули вліво, що часто відбувається на тлі цитокінових зрушень[281].
Правила виписування хворого зі стаціонару
Рішення про виписку приймає лікар, що лікує хворого, на підставі відсутності або зменшення клінічних ознак захворювання, стійкої тенденції до нормалізації загальнолабораторних показників (клінічного аналізу крові, С-реактивного білку, АЛТ, АСТ, сечовини, креатиніну). Якщо у хворого, попри відсутність клінічних і лабораторних ознак активного інфекційного процесу ПЛР показує позитивний або сумнівний результат (імовірно визначаються залишки РНК коронавірусу), хворий може бути виписаний додому на самоізоляцію зі спостереженням сімейного лікаря. Тестування ПЛР з метою ухвалення рішення про виписку пацієнта починається не раніше 5-го дня клінічного поліпшення перебігу хвороби. Згідно з уточненими настановами ВООЗ хворі, що перенесли коронавірусну хворобу 2019 і не мають клінічних симптомів, але тривалий час у них позитивні результати тестування в ПЛР, імовірно не є заразними і не здатні передати коронавірус здоровим людям, тому їхнє виписування зі стаціонару можливе[284]. Пацієнти, які відповідали визначенню підтвердженого випадку коронавірусної хвороби 2019 вважаються не контагіозними після 10 днів лікування, якщо методом ПЛР у них не визначаються фрагменти РНК збудника (негативний результат); за відсутності клінічних проявів гострого респіраторного захворювання впродовж 3 днів рахуючи з 10 дня від дати появи симптомів без лабораторного обстеження[207].
Реабілітація осіб з посткоронавірусним (постCOVID-19) синдромом
Групою експертів реабілітаційного центру Міністерства оборони в Стенфорд-холі (Велика Британія) розроблено документ–консенсус, який містить загальні рекомендації реабілітації та лікувальної корекції такого синдрому для цільової групи активних людей:
- схема реабілітаційного лікування має бути індивідуалізованою відповідно до потреб особи з урахуванням фонових хвороб;
- реабілітація має бути спрямована на полегшення симптомів, поліпшення психологічного стану, фізичної форми та якості життя;
- хворі мають періодично обстежуватися під час реабілітації;
- вони повинні отримувати всебічну інформацію про свій стан і про можливості відновлення після перенесеної ними хвороби[146].
Підходи до кардіологічної реабілітації у хворих, які перенесли коронавірусну хворобу 2019, згідно з Консенсусом Stanford Hall включають:
- кардіологічні ускладнення потрібно передбачати в усіх осіб, які перенесли цю хворобу, незалежно від тяжкості клінічного перебігу. У них слід виявити кардіологічні симптоми й порушення серцевої функції. За потреби варто проконсультувати пацієнта у фахівця та здійснити поглиблене обстеження.
- період фізичного і психічного спокою після перенесеної хвороби здатний зменшити ризик виникнення постінфекційної серцевої недостатності та міокардиту.
- за наявності у пацієнта кардіологічних проблем слід розробити спеціальні персоналізовані реабілітаційні програми, що ґрунтуются на оцінці наявних ускладнень, зрушень і життєвих потреб пацієнта[146].
Основні напрямки корекції посткоронавірусної астенії включають:
- оптимізацію медикаментозного лікування та ранній відхід від застосування препаратів із катаболічними властивостями як то дексаметазон;
- організацію оптимального як за кількісними показниками, так і за збалансованістю складу харчування;
- психологічну підтримку як в родині, так і у професійній діяльності;
- виявлення та контроль водно-електролітних і метаболічних порушень;
- моніторування та корекцію порушень при супутніх захворюваннях (артеріальна гіпертензія, цукровий діабет, тощо);
- профілактику розладів метаболізму — кетоацидозу (при голодуванні, цукровому діабеті);
- компенсацію внутрішньоклітинного енергетичного дефіциту;
- ліквідацію триваючого системного запалення[146].
Імовірними напрямками лікування триваючого системного запалення є:
- зниження рівня цитокінів і медіаторів, зменшення проникності гематоенцефалічного бар'єра;
- корекція порушення функції ендотелію;
- збільшення ефективності роботи власних антиоксидантних систем організму[146].
Підходи до неврологічної реабілітації хворих, які перенесли коронавірусну хворобу 2019, за Консенсусом Stanford Hall включають:
- усіх потрібно обстежити на наявність будь-яких неврологічних проявів, що можуть виявлятися під час активної фази хвороби чи протягом декількох тижнів після неї. Рекомендується провести пошук когнітивних порушень для пацієнтів групи ризику — після реанімації або із залишковими когнітивними порушеннями;
- необхідно запевнити хворих, що незначні неврологічні прояви, як то головний біль, запаморочення, втрата смаку або ж нюху, сенсорні порушення, найімовірніше, минуть при мінімальному медичному втручанні, а неврологічні прояви легкого чи середнього ступеня тяжкості зрештою будуть повністю знівельовані;
- тяжкі прояви потенційно здатні спричинити серйозні порушення, суттєво змінити якість життя, тому для якнайбільшого одужання хворим із помірними або тяжкими неврологічними проявами рекомендується мультидисциплінарна реабілітація стаціонарного типу[146].
Принципи легеневої реабілітації в хворих, які перенесли коронавірусну хворобу 2019, згідно з Консенсусом Stanford Hall:
- респіраторні ускладнення являють собою порушення і функціональні обмеження певного ступеня вираженості, загалом, але не тільки, через зниження функції дихання.
- рекомендується своєчасне первинне оцінювання стану хворого, проведення якого напряму залежить від ступеня дисфункції, нормокапнічної дихальної недостатності, фізичного та психічного стану хворого.
- на початку реабілітації необхідно розглянути вправи низької інтенсивності, зокрема для хворих, які потребують подальшої кисневої терапії. Разом з цим слід контролювати життєво важливі показники, такі, як частота скорочень серця, пульсоксиметрія, артеріальний тиск. Поступове підвищення фізичних навантажень має бути скореговане з вираженістю клінічних проявів хворого[146].
Напрямками дихальної реабілітації є нівелювання проявів задишки, зменшення занепокоєння та боротьба з депресією, запобігання дисфункції дихання, зниження частоти настання інвалідності, збереження функції дихання в максимальному обсязі, покращення якості життя[146].
Рекомендації з реабілітації респіраторних функцій включають фізичні вправи:
- аеробні, тобто ходьба і швидка ходьба, біг підтюпцем, плавання тощо, починаючи з низькоінтенсивних, поступово підвищуючи інтенсивність і збільшуючи тривалість;
- силові тренування — прогресивні з ваговими навантаженнями;
- тренування дихання при задишці, хрипах, труднощах із відходженням харкотиння потрібно проводити за допомогою тренувальної дихальної техніки, яка призведе до поліпшення відходження мокроти, регулювання ритму дихання, збільшення активності грудної клітки та мобілізації дихальних м'язів[146].
Дослідження, що оцінюють варіанти лікування післякоронавірусного синдрому є нечисленними. Рекомендації I-RECOVER Protocol for the treatment of the «Long-haul Syndrome» щодо управління довгостроковими наслідками не містять конкретних настанов відносно лікування. Загалом, хоча лікування має бути індивідуальним, деякі методи можуть відігравати певну роль у лікуванні цього розладу. Лікування першої лінії включає:
- Преднізон 60 мг на добу, потім зменшується, залежно від клінічної відповіді.
- Івермектин відіграє певну роль у лікуванні. Рекомендується доза 0,2 мг / кг на день протягом 5 днів; повторний курс для тих, хто погано реагує або мав рецидив після припинення лікування. Протизапальні властивості івермектину можуть опосередковувати цю користь.
- Омега-3 жирні кислоти 4 г на день. Вони відіграють важливу роль у вирішенні запалення, стимулюючи вироблення резольвіну.
- Лютеолін 100—200 мг на добу чи кверцетин 250 мг на добу (або змішані флаваноїди). Вони мають протизапальні властивості широкого спектру. Ці природні флавоноїди інгібують опасисті клітини і, як було продемонстровано, зменшують нейрозапалення.
- Фамотидин 20-40 мг на день як блокатор гістаміну-2 в розгортанні синдрому порушення тучних клітин.
- Мелатонін 2–5 мг повільного вивільнення на ніч зберігаючи основні засади гігієни сну.
- Вітамін D3 1000-3000 од / добу та вітамін С 500 мг два рази на день.
- Функціональна реабілітація за допомогою легких дихальних вправ з темпом відповідно до індивідуальних можливостей.
- Модифікація поведінки та психологічна підтримка сприяють покращенню загального самопочуття та психічного здоров'я[190].
Лікування другої лінії включає:
- Повторити терапію першої лінії, включаючи кортикостероїди та івермектин, доза якого збільшується до 0,4 мг / кг на добу протягом 5-10 днів.
- Аторвастатин 40 мг на добу (який збільшує стез резольвіну).
- Флувоксамін, особливо у тих, хто має нейрокогнітивні проблеми. Слід починати з 25 мг на добу, повільно збільшуючи дозу до 50-100 мг на день. Слід уважно стежити за реакцією, тому що підлітки та молоді люди, яким призначають флувоксамін, можуть відчувати гостру тривожність, яку повинно контролювати, щоб запобігти рідкісній ескалації до самогубства або жорстокої поведінки.
- Необов'язково: якій-небудь блокатор H1-гістамінових рецепторів III покоління (за наявності синдрому активації тучних клітин).
- Необов'язково: монтелукаст 10 мг / добу (за наявності синдрому активації тучних клітин)[190].
Реабілітація осіб із посткоронавірусним синдромом в Україні
В Україні в квітні 2021 року створено протокол надання реабілітаційної допомоги хворим на коронавірусну хворобу 2019 та реконвалесцентам. Створений протокол вводить поняття «мультидисциплінарна реабілітаційна команда», в яку запропоновано включити ряд медичних спеціалістів. Її має очолити лікар фізичної та реабілітаційної медицини, який є відповідальним за організацію роботи цієї команди, виконання індивідуального реабілітаційного плану та інших завдань, що покладені на команду. Протокол затверджує алгоритм надання такої реабілітаційної допомоги, забезпечення доступу до мультидисциплінарних послуг для оцінювання проявів фізичного та психічного здоров'я, проведення подальших тестувань і досліджень. Їх має проводити лікар з відповідними фаховими навичками та досвідом, з належною підтримкою різних спеціалістів, беручи до уваги різноманітність проявів, що виявляються. Медичні працівники повинні володіти низкою спеціальних навичок, мати досвід у лікуванні синдрому втоми та респіраторних проявів включаючи задишку. Реабілітаційні заходи для хворих з тяжким перебігом вкрай потрібні у гострому періоді, мають необхідність у реабілітації як під час перебування в лікарні, так і після виписки. Потреби щодо реабілітації відрізняються залежно від періоду реабілітації, особливостей перебігу хвороби, фонової патології. За протоколом міждісциплінарна команда може включати, але не обмежується спеціалістами наступних фахів:
- медична реабілітація;
- фізична терапія;
- ерготерапія;
- терапія мови і мовлення (логопедія, логосенсорика);
- клінічна психологія та психіатрія.
Професійний і кількісний склад команди напряму залежить від особливостей обмеження повсякденних функцій особи, якій потрібна реабілітація, а також від специфіки закладу, відділення, підрозділу, де має здійснюватися реабілітація.
Реабілітація госпіталізованих хворих має починатись у стаціонарі і тривати до ухвалення рішення про виписку їх додому[285].
Потреби в реабілітації у хворих на коронавірусну хворобу 2019 і в реконвалесцентів поділяються на:
- порушення комунікації;
- порушення ковтання;
- порушення легеневої функції;
- фізичне виснаження та слабкість;
- обмеження повсякденної діяльності;
- тривога і депресія;
- делірій та інші когнітивні порушення (пам'яті, уваги, мови, виконавчих функцій, свідомості)[285].
Пацієнти, які перехворіли з наявними порушеннями легеневої функції, через 6–8 тижнів по виписці з медичного закладу мають пройти комплексну програму легеневої реабілітації, що відповідає міжнародним стандартам (Quality Standards for Pulmonary Rehabilitation in Adults, 2014; British Thoracic Society guideline on pulmonary rehabilitation in adults, 2013; American Thoracic Society, Assembly on Pulmonary Rehabilitation «Guidance for re-opening pulmonary rehabilitation programs», 2020). Їм слід оцінити потребу в кисні в стані спокою та при фізичних навантаженнях у госпіталізованих перед випискою їх з лікарні. Надалі лікар, що буде займатися реабілітацією, має вирішити, яка потреба в амбулаторній реабілітації під час фізичних навантажень і повсякденній діяльності. Чи необхідне для цього пацієнта короткотривале застосування оксигенотерапії короткими періодами 10-20 хвилин при транзиторній гіпоксемії або виникненні стійкої, або ж довготривала оксигенотерапія більше 15 годин на день у хворих на хронічну гіпоксемію в домашніх умовах. Лікар має визначити дату наступного оцінювання потреби в кисні. Ці призначення мають бути відображені в індивідуальному реабілітаційному плані[285].
Хворі із втратою маси та / чи функції м'язів нижньої кінцівки через 6–8 тижнів по виписці з медичного закладу мають бути направлені для участі в програмах реабілітації, спрямованих на збільшення сили м'язів. Вид вправ, особливості тренувань і тривалість програми фізіотерапії визначається потребами хворого. Пацієнтів слід заохочувати здійснювати фізичні вправи низької та помірної інтенсивності вдома, тоді як фізичні вправи високої інтенсивності не рекомендуються. Це слід робити в перші 6–8 тижнів по виписці з лікарні, якщо не здійснювалося формальне оцінювання під час виконання фізичних вправ із визначенням сатурації при навантаженні[285].
Хворого слід перевести у реабілітаційне відділення, якщо є обмеження життєдіяльності після виписки з інфекційного відділення. У випадку відсутності потреби в цілодобовому спостереженні та реабілітації високої інтенсивності хворий має бути направлений до амбулаторних програм реабілітації або таких на базі громади, що доступні на місцевому рівні. Слід обрати варіанти, що містять найменшу кількість проблем для участі, за можливості скористатися послугами з телемедичної реабілітації. Хворих слід забезпечити освітніми та інформаційними матеріалами для самостійної підтримки під час реабілітації, особливо за недоступності реабілітаційного сервісу. Оцінку потреб хворого у необхідності реабілітації слід здійснювати у формі самозвіту за шкалою Post-COVID-19 Functional Status (PCFS), як частини первинної консультації, щоб спромогтися виявити усі посткоронавірусні прояви. Самозвіт потрібно застосувати лише разом із клінічним оцінюванням. Терміни проведення оцінювання за PCFS-шкалою визначаються категоріями осіб, що підлягають реабілітації:
- на першому прийомі в медичному закладі після гострої коронавірусної хвороби 2019;
- через 4-8 тижнів від першого прийому в медичному закладі;
- через 6 місяців від першого прийому в медичному закладі[285].
Хворих з симптоматичною коронавірусною інфекцією 2019 або з підозрою на посткоронавірусний синдром, що мають тяжкі психічні прояви чи ризикують завдати собі шкоду або ж спричинити самогубство, потребують негайного скерування на консультацію до психіатра. Слід дотримуватись відповідних національних рекомендацій щодо осіб, які мають тривогу, емоційні розлади або інші психічні прояви. Необхідно вирішити який напрямок вибрати: психотерапію, якщо ці люди мають загальні прояви легкої тривоги та депресії, або психіатричну службу, якщо у них є складніші потреби[285].
Профілактика
Узагальнити
Перспектива

Активний епідеміологічний пошук випадків здійснюється шляхом лабораторного тестування на SARS-CoV-2 серед осіб, які відповідають критеріям підозрілого випадку, або в рамках диференціальної діагностики у пацієнтів з вірусною пневмонією та / чи тяжкими проявами гострої респіраторної хвороби.
Під час міжнародних поїздок слід уникати тісного контакту з хворими людьми. Намагатися не торкатися очей, носа і рота немитими руками. Часто мити руки з милом і водою не менше 20 секунд, особливо після відвідування туалету, перед їдою, після кашлю та чхання. Якщо мило і вода недоступні, необхідно використовувати дезінфікувальний засіб для рук на спиртовій основі з вмістом спирту не менше 60 %. Наразі визначено, що внаслідок зараження достатньо великої кількості людей в осередках, багато з них можуть бути джерелом інфекції не маючи симптомів і не розуміючи того, що вони здатні поширювати SARS-CoV-2, тому в багатьох країнах світу було вирішено носити маски всім людям за межами домівки. Згідно з оновленими рекомендаціями із запобігання коронавірусній хворобі 2019, які видали Центри з контролю та профілактики захворювань у США (CDC), особа, яка носить маску, захищає від SARS-CoV-2 не лише оточуючих, але й себе. Наголошено, що багато наукових досліджень засвідчили користь режиму загальнообов'язкового носіння масок[289]. Дослідження показали, що поєднання масок та поліпшення їхнього прилягання, надають більший захист від будь-яких респіраторних заражень. Носіння тканинної маски разом із медичною захищає від 91 % частинок із повітря, яке видихається, і 85 % частинок із повітря, що виділяється під час кашлю. Медична маска без модифікацій блокувала близько 42 % частинок із повітря, що видихається, і 56 % частинок, що потрапляють назовні під час кашлю[290].
За аналогією з профілактикою інших коронавірусних інфекцій рекомендується обробка контамінованих металевих, пластикових, скляних поверхонь протягом 1 хвилини 70 % етанолом, 0,2 % розчином перекису водню або 0,1 % гіпохлориту калію. Інші дезінфікувальні засоби менш ефективні[291].
Захист медичних працівників
Усі медичні працівники, які безпосередньо надають медичну допомогу пацієнтам з COVID-19, контактують з їхніми біологічними матеріалами, мають застосовувати засоби індивідуального захисту від інфекційного захворювання. Медичним працівникам, а також тим, хто забезпечує життєдіяльність ізольованих чи підозрюваних, слід захищати себе за допомогою:
- Рукавички для огляду, з нітрилу, без порошку, нестерильні. Повинні мати довгі манжети, що сягають значно вище зап'ястя, в ідеалі, до середини передпліччя. (згідно з державними стандартами України це ДСТУ EN 455-І:2014 і ДСТУ EN 165233-1:2018[292]).
- Щиток для лиця, зроблений з прозорого пластику, що забезпечує хорошу видимість як для користувача, так і для пацієнта, з регульованою смугою, яка міцно прикріплюється навколо голови і щільно прилягає до чола, стійкий до запотівання, повністю покриває сторони і довжину обличчя, багаторазовий — виготовлений з міцного матеріалу, який можна очистити та дезінфікувати (згідно з державними стандартами України це ДСТУ EN 166:2017[292]). При нетривалих чи епізодичних контактах допускається застосування одноразових засобів захисту обличчя типу маски хірургічної, з високою стійкістю до рідини, гарною повітропроникністю, внутрішні та зовнішні поверхні повинні бути чітко визначені, структурована конструкція, яка не змінює форми при використанні, зокрема, у формі каченяти-дзьоба чи чашки.
- Окуляри захисні, що добре прилягають до шкіри обличчя, гнучка рамка з ПВХ, яка легко вписується в контури обличчя рівномірним тиском, закриває очі та навколишні ділянки, вміщує окуляри для корекції зору, прозору пластикову лінзу із захистом від запотівання та подряпин, регульовану смугу для міцного закріплення, щоб не загубилися під час діяльності, непряма вентиляція для уникнення запотівання, багато- (з можливістю знезараження) або одноразові (згідно з державними стандартами України це ДСТУ EN 166:2017[292]).
- Халат одноразового використання, стійкий до рідини, завдовжки до середини литок, щоб покрити верх черевиків, світлих відтінків для кращого виявлення можливих забруднень, з петлями для пальця / пальців або еластичною манжетою для закріплення рукавів (згідно з державними стандартами України це ДСТУ EN 13795:2004, ДСТУ EN 14126:2008, ДСТУ EN 13034:2017, ДСТУ EN 14605:2017[292]). Для захисту працівників лабораторій застосовуються водонепроникні лабораторні костюми із захистом від інфекційних агентів (ДСТУ EN 14126:2008). Також під час пандемії використовують одноразові або багаторазові захисні комбінезони типу Chemsafe C1, AllSet, Tyvek тощо.

Виконувати медичні процедури слід у добре провітрюваному приміщенні, зокрема, з доступним надходженням повітря до нього в обсязі не менше ніж 160 літрів / секунду на пацієнта[293][294] або із забезпеченням мінімум 12-кратним обміном повітря за годину в приміщенні з негативним тиском або із застосуванням механічної вентиляції. При цьому слід використовувати протиаерозольні респіратори:
- сертифікований Національним інститутом США з охорони праці промисловий гігієнічний респіратор N95;
- сертифікований Європейським союзом респіратор FFP2 чи FFP3 або будь-який інший еквівалентний респіратор.
Згідно з державними стандартами України це ДСТУ EN 149:2017[292]. При використанні таких одноразових респіраторів обов'язково проводиться перевірка герметичності — якісний чи кількісний фіт-тест. Ці респіратори здатні захистити від дрібнодисперсних аерозолів, надати максимальний захист від твердих та рідких аерозолів при концентрації не нижче 12 гранично допустимих концентрацій (ГДК).
Після закінчення процедури діагностичного відбору зразків, клінічного обстеження хворого або підозрілого на коронавірусну хворобу 2019, лікувальних дій медичний працівник з метою недопущення інфікування має зняти та утилізувати засоби індивідуального захисту, які він одягав перед проведенням обстеження, в одній із послідовностей: або рукавички, захисні окуляри або щиток, ізоляційний (захисний) халат, респіратор; або ізоляційний (захисний) халат разом із рукавичками, захисні окуляри або щиток, респіратор. Після зняття та утилізації засобів індивідуального захисту слід обов'язково провести гігієну рук. Заходи безпеки, направлені на запобігання передачі, як контактні, так і крапельні, мають тривати до тих пір, поки у пацієнта будуть проявлятися симптоми, тобто до закінчення періоду контагіозності.
Тестування методом ПЛР проводити кожні 5 днів медичним працівникам, які безпосередньо надають медичну допомогу хворим на коронавірусну хворобу 2019 або проводять догляд за хворими на неї в умовах стаціонару, працівникам лабораторій, які обробляють зразки з дихальних шляхів отримані від таких хворих, працівникам патологоанатомічних, судово-медичних бюро, які безпосередньо беруть участь у розтині тіла, в тому числі — у взятті зразків секційного матеріалу.
ВООЗ ініціювала проведення міжнародного багатоцентрового дослідження оцінки факторів ризику коронавірусної хвороби 2019 у медичних працівників. Медичні працівники з підтвердженим діагнозом набираються як група дослідження, тоді як інші медичні працівники, які перебувають у тій самій установі охорони здоров'я без зараження, набираються до контрольної групи (вибірка щільності захворюваності). Набір випадків здійснюється за допомогою доступного шаблону збору даних Go.Data. ВООЗ координує це дослідження, яке, безсумнівно, призведе до ґрунтовнішого аналізу потенційних факторів[295].
ВООЗ 24 грудня 2021 року опублікувала оновлені правила для медпрацівників, що включають рекомендацію використовувати респіратор чи медичну маску на додаток до іншого особистого захисту, при вході до приміщення, де перебуває хворий із підтвердженим чи підозрюваним діагнозом коронавірусної хвороби 2019[296].
Особливості захисту медичних працівників в Україні
З фізіолого-гігієнічних засад праця медичного персоналу в Україні в умовах подолання пандемії коронавірусної хвороби 2019 відповідно до критеріїв «Гігієнічної класифікації праці за показниками шкідливості та небезпечності факторів виробничого процесу, важкості та напруженості праці»[297] за умовами роботи належить до небезпечної (екстремальної) — 4-го класу. Ризик небезпеки згідно з індексом розвитку професійної хвороби для цього класу робіт перевищує 1, тоді як такий індекс при проведенні робіт у шкідливих умовах (клас 3) становить 0,05-1,0, допустимих (клас 2) — менше 0,05; оптимальних (клас 1) — 0. Зрештою ризик розвитку як професійної хвороби COVID-19 у медичного персоналу, навіть працюючого у спеціальних засобах індивідуального захисту, є надзвичайно високим і ймовірним.
Документи МОЗ України і ДС України з питань праці зазначили, що лабораторно підтверджені випадки інфікування коронавірусною хворобою 2019 медичних та інших працівників, що виконують професійні обов'язки в умовах підвищеного ризику зараження, підлягають розслідуванню як випадки гострого професійного захворювання відповідно до вимог «Порядку розслідування та обліку нещасних випадків, професійних захворювань та аварій на виробництві», затвердженого постановою Кабінету Міністрів України від 17 квітня 2019 року № 337. Таким чином лабораторно підтверджений професійно зумовлений випадок коронавірусної хвороби 2019 у медичного працівника обліковується як гостре професійне захворювання «Коронавірусна хвороба COVID-19» із відшкодуванням усіх передбачених чинним законодавством збитків для випадку професійного захворювання[298].
Запобігання зараженню при амбулаторному контакті
Якщо пацієнта залишають лікуватися амбулаторно вдома, то його слід розмістити у добре провітрюваному приміщенні. Необхідно обмежити кількість доглядачів пацієнта, в ідеалі призначається одна людина не з категорій ризику. Відвідування пацієнта забороняються. Члени домогосподарств мусять перебувати в іншій кімнаті або, якщо це неможливо, дотримуватися відстані не менше 1 м від хворої людини. Винятком вважається мати, що годує грудьми: враховуючи переваги грудного вигодовування та незначну роль грудного молока в передачі інших респіраторних вірусів, мати може продовжувати годувати грудьми, водночас вона повинна носити медичну маску (ДСТУ EN 14683:2014), коли вона знаходиться поруч із дитиною, і дотримуватися ретельної гігієни рук перед тісним контактом із дитиною. Їй слід також застосувати й інші гігієнічні заходи. Потрібно обмежити рухливість пацієнта та мінімізувати його загальний простір. Загальні приміщення, зокрема кухня та ванна кімната, мають добре провітрюватися. Доглядач пацієнта повинен носити медичну маску, що щільно прилягає до обличчя, коли знаходиться в одній кімнаті з ним. Під час використання маски її не слід чіпати. Якщо маска намокне або забрудниться виділеннями, її потрібно негайно змінити. Застосовуються одноразові маски. Це має бути медична / хірургічна маска, з високою стійкістю до рідини, гарною повітропроникністю, внутрішні та зовнішні поверхні якої повинні бути чітко означені, структурованої конструкції, що не змінює форми при використанні. Згідно з результатами проведеного дослідження, особи, що доглядали хворого на коронавірусну хворобу 2019, який був без маски, і самі одягали при цьому маску з тканини, заразилися вже за 20 хвилин. Якщо мали хірургічну маску, цей термін збільшився до 30 хвилин, а при носінні добре підігнаних респіраторів N95, чи KF94, або ж KN95, цей час збільшився до 2,5 годин. Він ще більше продовжувався, якщо пацієнт також був у масці[299].
Після зняття маски необхідно провести гігієнічну обробку рук.
ВООЗ, яка на початку пандемії не вітала застосування масок серед населення, переконуючи, що немає достатньо доказів, аби стверджувати, що здорові люди повинні носити маски, змінила свій погляд на цю проблему і заявила, що здоровим людям рекомендується носити «тканинну — тобто немедичну маску» у районах, де існує ризик передачі захворювання, тому що люди можуть бути сильно заразними для оточуючих за кілька днів до того, як у них з'являться симптоми хвороби. Інші люди передають вірус, але у них самих симптоми хвороби так і не з'являться. Отож, там де безпечна відстань неможлива, слід прикривати обличчя тканинними масками. Представник ВООЗ заявила, що її нові рекомендації зумовлені останніми дослідженнями і організація радить урядам країн заохочувати громадськість носити маски[88][300]. Проведений аналіз багатьох наукових досліджень показав значне зниження захворюваності коронавірусною хворобою 2019 при носінні масок і фізичному дистанціюванні[301].
Слід проводити гігієнічну обробку рук після будь-яких контактів із хворим або його найближчим оточенням. Гігієну рук також необхідно застосовувати до і після приготування їжі, перед вживанням її, після туалету, кожного разу, коли руки забруднюються. Якщо на руках відсутнє помітне забруднення, можна витерти руки засобом на основі спирту. Руки при помітному забрудненні слід мити з милом і водою. Для осушування бажано використовувати одноразові паперові рушники для рук. Якщо немає, слід використовувати виділені рушники з тканини та замінити їх, коли вони стануть вологими.
Пацієнтам слід пояснити засади гігієни дихання, що потрібно прикривати рот і ніс під час кашлю або чхання за допомогою медичних масок, тканинних масок, тканин або згинанням ліктя з подальшою гігієнічною обробкою рук. Необхідно відмовитися від багаторазового використовування матеріалів для покриття рота або носа або відповідним чином очищувати їх після використання (наприклад, прання хусток, використовуючи звичайне мило або миючий засіб і воду). Слід уникати прямого контакту з біологічними рідинами організму, зокрема пероральними, дихальними виділеннями та випорожненнями пацієнта. Використовуються одноразові рукавички для надання догляду за ротовою порожниною або диханням та при поводженні з фекаліями, сечею та іншими відходами. Застосовується гігієнічна обробка рук до і після зняття рукавичок. Рукавички, тканини, маски та інші відходи хворих осіб або доглядальників за хворими, слід розміщувати в окремому контейнері в приміщенні, де знаходиться хвора людина, до вивезення цих відходів.
Необхідно уникнути інших видів можливого потрапляння виділень хворих або забруднених предметів у безпосереднє оточення здорових. Не слід користуватися спільно зубними щітками, цигарками, посудом, напоями, рушниками, мочалками або постільною білизною. Посуд після використання слід мити з милом або миючим засобом і водою; використовувати повторно, а не викидати. Щодня слід дезінфікувати поверхні, такі як тумбочки, покривала та інші меблі для спальні звичайним побутовим дезінфікувальним засобом, що містить розведений розчин хлорного вапна (1 частина розчину хлорного вапна на 99 частин води). Необхідно дезінфікувати поверхні ванної та туалету принаймні один раз на день звичайними побутовими дезінфікувальними засобами, що містять розведений розчин хлорного вапна у тій же пропорції. Слід прати одяг, постільну білизну, рушники для ванни та рук хворих людей, використовуючи звичайне мило та воду для прання чи машинне прання при температурі 60–90 °C загальним побутовим миючим засобом, та ретельно висушувати. Забруднену білизну необхідно викидати у мішок для білизни. Не дозволяється струшувати забруднену білизну. Слід уникати прямого контакту шкіри та одягу із забрудненими матеріалами. Необхідно використовувати одноразові рукавички та захисний одяг при обробці поверхонь, одягу чи білизни, забруднених біологічними рідинами хворого. Потрібно дотримуватися гігієни рук до і після зняття рукавичок.
Особи з проявами хвороби повинні залишатися вдома до тих пір, поки не буде доведено відсутність її на підставі клінічних та / або лабораторних результатів — два негативних ПЛР-тести з інтервалом не менше 24 годин. Усі члени домогосподарства вважаються контактними, а їхнє здоров'я слід контролювати.
Дії медичного працівника за появи симптомів коронавірусної хвороби 2019 у контактної особи
Слід повідомити заклад охорони здоров'я, який виділено для лікування таких хворих, що контактна особа з симптомами направлена до їхнього закладу. Під час транспортування пацієнт повинен носити, якщо це дозволяє його стан, медичну маску. Слід при цьому уникнути громадського транспорту, якщо це можливо; викликати екстрену медичну допомогу або перевезти хворого на приватному транспортному засобі та, якщо можливо, відкрити вікна під час транспортування. Пацієнту слід порадити, якщо дозволяє його стан, завжди дотримуватись етикету гігієни дихання та гігієни рук; стояти або сидіти на відстані від 1 м або більше від інших, під час транспортування і перебування в закладі охорони здоров‘я. Належну гігієнічну обробку рук слід робити й іншим контактним особам та доглядальникам. Будь-які поверхні, які під час транспортування забруднилися виділеннями або рідинами пацієнта, повинні бути очищені та дезінфіковані звичайними побутовими засобами.
Вакцинація
Для специфічної профілактики хвороби з початку пандемії створено декілька вакцин, які застосовуються в різних регіонах світу.
Можливий вплив вакцинації БЦЖ на запобігання розвитку коронавірусної хвороби 2019
Деякі науковці наголосили, що вакцинація проти туберкульозу за допомогою вакцини БЦЖ, яка була розроблена на початку XX століття, може захистити від тяжкого перебігу коронавірусної хвороби 2019.
Детальніші відомості з цієї теми ви можете знайти в статті БЦЖ.
Медикаментозна профілактика коронавірусної хвороби 2019
У світі багато країн запровадили таку профілактику для запобігання зараження хворобі. Зокрема для цієї мети американська Східновіргінська медична школа (EVSM) пропонує у своєму протоколі:
- підтримуюча імунна терапія:
- вітамін С у добовій дозі 500 мг перорально, розділивши її на два прийоми і кверцетин у добовій дозі 250 мг, розділивши її на 3 прийоми;
- вітамінні комплекси групи В;
- препарати омега-3 ненасичених жирних кислот;
- препарати цинку 30-50 мг / добу;
- мелатонін із повільним вивільненням починаючи з 0,3 мг і збільшуючи дозу при задовільній реакції до 2 мг перед сном;
- вітамін D3 1000-3000 од / добу;
- щотижневий прийом івермектину по 150—200 мкг / кг двічі на тиждень для післяконтактної профілактики усім людям чи хронічно в групах високого ризику;
- полоскання ротоглотки 2 рази на день антисептичною рідиною з цетилпіридинієм хлоридом не ковтаючи, 1 % розчином повідон/йоду або лістерином з ефірними оліями[271].
Американський інститут здоров'я повідомив, що 16 вересня 2021 року Управління з контролю за харчовими продуктами та лікарськими засобами США розширило вказівки щодо дозволу на екстрене використання моноклональних антитіл проти SARS-CoV-2 бамланівімабу плюс етесевімабу з метою постконтактної профілактики інфекції SARS-CoV-2 для окремих осіб. Казирівімаб плюс імдевімаб також можуть бути використані для цього показання[302]
Цілі в боротьбі з пандемією коронавірусної хвороби 2019
Узагальнити
Перспектива
Стратегічні цілі ВООЗ:
- перервати передачу людини від людини, включаючи зменшення вторинних випадків серед близьких контактів хворих, та у медичних працівників, запобігаючи посиленню передачі та подальшому міжнародному поширенню. Цього можна досягти за допомогою комбінації заходів системи охорони здоров'я, таких, як швидке виявлення випадків, їхня клінічна діагностика та лікування, ідентифікація контактів і спостереження за ними, профілактика та контроль цього з боку закладів охорони здоров'я, здійснення заходів з охорони здоров'я мандрівників, підвищення обізнаності серед населення та запобігання ризикового спілкування;
- швидко виявляти, ізолювати та доглядати пацієнтів, включаючи надання їм оптимізованої допомоги;
- виявити і розшифрувати найважливіші невідомі фактори для оцінки клінічної тяжкості, ступеня ризику передачі, варіантів лікування, прискорення розвитку специфічної діагностики, терапії та вакцинації;
- донести до всієї громадськості інформацію про критичні ризики, події, протидіяти дезінформації;
- мінімізувати соціальний та економічний вплив через багатогалузеві партнерства[303].
Ерадикація коронавірусу Sars-Cov-2 і, відповідно, коронавірусної хвороби 2019 наразі не стоїть в ерадикаційних планах ВООЗ, що включать такі хвороби як поліомієліт, фрамбезію, дракункульоз, малярію, кір, епідемічний паротит, краснуху, лімфатичні філяріїдози та цистицеркоз. Згідно з науковими критеріями, для того, щоб хворобу можна було б ерадикувати, вона повинна бути епідеміологічно вразливою для атаки, тобто важко поширюватися і легко діагностуватися, або хвороба повинна приводити до довічного імунітету тих, хто виживає. Також необхідна можливість ефективного втручання, такого як вакцинація або використання ліків, щоб зупинити хворобу. Крім того, необхідні докази, що хвороба вже була переможена в якомусь конкретному регіоні, що підтверджувало б можливість позбавлення від неї в ширшому масштабі. Зусилля по викоріненню такої повинні бути доступними і мало витратними. У довгостроковій перспективі повне зникнення захворювання повинно мати значну перевагу в порівнянні з його постійним контролем. Коронавірусна хвороба 2019 легко поширюється, періодично спалахує навіть у благополучних до того регіонах, проблемно діагностується, імунітет поки є непроясненим, ефективних етіотропних ліків не створено, вакцинація також має певні проблеми[304].
Прогнозовані наслідки пандемії
Узагальнити
Перспектива
Пандемія значно вплинула як на якість надання медичної допомоги, так і на доступ до неї. Часте використання дистанційного обстеження хворих, спрямоване на мінімізацію ризику захворювання, призвело до затримки виявлення тяжких декомпенсованих станів у хворих із різними хронічними захворюваннями та пізньою діагностикою гострих випадків. В усьому світі медичні установи спостерігали зменшення кількості пацієнтів, які зверталися за невідкладною медичною допомогою у зв'язку із серйозними захворюваннями[305]. Страх зараження не дозволяв пацієнтам звертатися за плановою медичною допомогою та обстеженнями[306]. За оцінками ВООЗ, через пандемію рівень планових щеплень у світі знизиться на 20 мільйонів[307].
Глобальний фонд — неприбуткове державно-приватне партнерство для боротьби з ВІЛ, туберкульозом і малярією. Він виділяє 4 мільярди доларів на рік на місцеві зусилля в більш ніж 100 країнах і відстежує прогрес у боротьбі з цими хворобами. У його звіті показано, що під час пандемії цей прогрес гальмується, оскільки кількість тестів на ВІЛ впала зі 134 мільйонів у 2019 році до 104 мільйонів у 2020 році. На 4,5 % менше матерів із ВІЛ-інфекцією отримували ліки під час вагітності, щоб запобігти передачі новонародженим. Загалом у 2020 році на 1 мільйон людей менше проходило тести на туберкульоз або лікування в порівнянні з 2019 роком — зниження, яке може призвести до розвитку та поширення туберкульозу з множинною лікарською стійкістю, згідно зі звітом. Прогрес у боротьбі з малярією також зупинився: кількість тестів зменшилась приблизно на 4 %, а лікування — на 0,5 %[308].
Дослідження показали, що внаслідок поширення пандемії на африканський континент виникли проблеми у профілактиці найтяжчого варіанту малярії — тропічної, яка обумовлює до 98 % летальності від малярії. В Африці південніше Сахари реєструється найбільша кількість випадків зараження. Основним методом профілактики є хіміотерапія, яка передбачає вживання деяких препаратів, які у багатьох регіонах і країнах Африки люди отримують, приходячи у відповідні медичні центри. Через побоювання зараження SARS-CoV-2 значно зменшилася циркуляція населення і походи за отриманням цих профілактичних препаратів. Разом із тим зменшено фінансування інших профілактичних заходів. Така ситуація відбувається й в Індії. Все це може призвести до збільшення захворюваності та летальності від тропічної малярії, що зведе нанівець усю профілактичну діяльність упродовж останніх декількох десятиліть[309][310][311].
Імуносупресія, яку спричинює малярія, також спостерігалася у багатьох випадках коінфекцій, значно інгібуючи імунну відповідь на іншу хворобу, зокрема, на сальмонельоз. Також показано, що імуномодуляція, яку спричинює малярія, захищає від тяжких проявів деяких респіраторних вірусних захворювань. Діти, госпіталізовані з діагнозом грипу та малярії, мали меншу ймовірність дихальних розладів, ніж ті, що страждали лише на грип. Коінфекція з малярією може придушити вироблення легеневих цитокінів і зменшити дифузію клітинних запальних компонентів до легень, що призведе до зменшення клінічних симптомів і запалення, як було виявлено під час респіраторних вірусних інфекцій на мишачій моделі. Однак у цій моделі спостерігалося порушення вірусного контролю, що призвело до посилення передачі вірусів іншим тваринам. Подібна динаміка може спостерігатися під час коінфекції плазмодія — SARS-CoV-2. Імуносупресія від малярійного плазмодія здатна призвести до м'якших проявів коронавірусної хвороби 2019, але одночасно потенційно збільшити або зберегти на високому рівні вірусне навантаження, що може посилити передачу SARS-CoV-2 в популяції[309].
Коронавірусна хвороба 2019 індукує гіперкоагулянтний стан через порушення багатьох патогенетичних факторів. Клінічно цей стан проявляється високою швидкістю венозної тромбоемболії та артеріальних тромботичних ускладнень (включаючи легеневу емболію та інсульт). Тромбоцитопенія є ще однією потенційною особливістю коронавірусної хвороби 2019. Малярія також асоціюється з гіперкоагулянтним станом, а тромбоцитопенія розвивається у 60–80 % випадків малярії. Хоча кровотечі та тромботичні ускладнення спостерігаються зрідка, зустрічаючись лише у тяжких випадках малярії, що супроводжуються коагулопатією, але вони асоціюються з високою летальністю. Лізис активованих тромбоцитів разом із тканинним фактором, що виділяється з пошкоджених клітин ендотелію судин, сприяє гіперкоагулянтному стану аналогічно гіпотетичному механізму пошкодження при коронавірусній хворобі 2019. Зроблено аргументоване припущення, що коінфекція малярія + коронавірусна хвороба 2019 може призвести до ще більшого розвитку коагулопатії та тяжчого клінічного перебігу, ніж за наявності лише однієї з них[309].
Коінфекція паразитарними хворобами, що поширені у країнах Африки, Азії та Південної Америки, може призвести до зміни тяжкості клінічних проявів коронавірусної хвороби 2019, що може призвести до зниження розвитку імунітету і збільшення вірусних навантажень. При хворобі Шагаса у 20-30 % пацієнтів молодого та середнього віку розвивається кардіоміопатія. Для цих людей коінфекція з коронавірусною хворобою 2019 може бути вкрай небезпечною для життя. Для вагітних і дітей з кишковими гельмінтозами коронавірусна хвороба 2019 може стати смертельною через притаманну деяким гельмінтозам анемію[309].
Хронічне недоїдання є відносно поширеним серед дітей в Африці на південь від Сахари, а також у деяких регіонах Латинської Америки та Азії. Встановлено, що преальбумін, маркер білкової гіпотрофії, нижчий у пацієнтів із коронавірусною хворобою 2019, у яких розвинувся ГРДС, ніж у тих, у кого це не відбулося. Хоча нижчий преальбумін може бути маркером інших тяжких захворювань, імуносупресія, пов'язана з недоїданням, яка передує зараженню SARS-CoV-2, може посилити тяжкість коронавірусної хвороби 2019. Вважається, що недоїдання призвело до надмірної летальності як при пандемії іспанського грипу 1918 року, так і при пандемії H1N1 2009 року. Поєднання недоїдання і тяжкої коронавірусної хвороби 2019 може збільшити частку тяжких прогнозів, особливо у дітей[309].
Разом з тим показано, що під час ізоляції при пандемії коронавірусної хвороби 2019 ризик зараження гарячкою денге зменшився приблизно на 9,1 %. Заявлено, що мобільність людей може відігравати важливу роль в епідеміології денге[312].
Передбачається, що надмірне і неконтрольоване використання антибіотиків у перебігу коронавірусної хвороби 2019 здатне призвести до значного збільшення кількості випадків антибіотиконечутливого кандидозу та інших грибкових хвороб, як то мукормікозу[313][314], тому що в генезі коронавірусної хвороби 2019 підвищується сприйнятливість пацієнтів до мукормікозу через збільшення вірулентності грибів, де вирішальну роль відіграє недостатність синтезу мелатоніну[315]. Також передбачається формування стійких до антибіотиків бактерій дихальних шляхів.
Див. також
- Пандемія коронавірусної хвороби 2019
- Коронавірусна хвороба 2019 в Україні
- SARS-CoV-2
- Експериментальне лікування коронавірусної хвороби 2019
- Вакцина проти COVID-19
- Коронавірусна інфекція
- Тяжкий гострий респіраторний синдром
- Близькосхідний коронавірусний респіраторний синдром
- Твіндемія
- Постковідний синдром
Примітки
Джерела
Посилання
Wikiwand - on
Seamless Wikipedia browsing. On steroids.