From Wikipedia, the free encyclopedia
As actinas[2] son unha familia de proteínas globulares que forman os microfilamentos, un dos tres compoñentes fundamentais do citoesqueleto das células dos organismos eucariotas. A actina pode encontrarse como monómero en forma libre, denominado actina G, ou formando parte de polímeros lineares denominados microfilamentos ou actina F, que son esenciais para funcións celulares tan importantes coma a mobilidade e a contracción da célula durante a división celular. En vertebrados, identificáronse tres grandes grupos de isoformas da actina, chamadas alfa, beta, e gamma. As alfa encóntranse nos tecidos musculares, e son un dos constituíntes principais do aparato contráctil do músculo. As beta e as gamma coexisten na maior parte dos tipos celulares como compoñentes do citoesqueleto, e como mediadores da mobilidade celular interna.
| Actina | |||||||||
|---|---|---|---|---|---|---|---|---|---|
 Modelo de fitas da actina G.PDB 1j6z. Represéntanse no centro activo o ADP e o catión divalente, e un ión calcio en complexo (esfera verde).[1] | |||||||||
| Identificadores | |||||||||
| Símbolo | Actin | ||||||||
| Pfam | PF00022 | ||||||||
| InterPro | IPR004000 | ||||||||
| PROSITE | PDOC00340 | ||||||||
| SCOPe | 2btf / SUPFAM | ||||||||
| |||||||||
A importancia da actina reflíctese na elevada porcentaxe que esta proteína supón no contido proteico total da célula e en que a súa secuencia está moi conservada, é dicir, que cambiou moi pouco ao longo da evolución, polo que se pode dicir que a súa estrutura foi optimizada. Presenta dúas características peculiares: é un encima que hidroliza ATP, a molécula enerxética biolóxica, e faino de maneira moi lenta, e ademais é a proteína que establece máis interaccións con outras proteínas de todas as coñecidas, o que lle permite realizar as máis variadas funcións, que afectan a case todos os aspectos da vida celular. A miosina é un exemplo de proteína que se une á actina. Outro exemplo é a vilina, que pode entrelazar a actina en feixes ou ben cortar os filamentos de actina, dependendo da concentración do catión calcio no medio.[3]
A actina, ao formar microfilamentos nun proceso dinámico proporciona unha andamiaxe que lle dá á célula a posibilidade de remodelar a súa forma rapidamente en resposta á súa contorna ou a sinais enviados polo organismo, por exemplo, aumentando a superficie celular para a absorción ou dando soporte á adhesión das células para formar tecidos. Sobre esta andamiaxe poden ancorarse outros encimas, orgánulos como os cilios, e dirixirse a deformación da membrana plasmática para permitir a endocitose ou a citocinese. Tamén pode producir movemento, por ela mesma ou axudada por motores moleculares. Dese xeito contribúe a procesos como o transporte intracelular de vesículas e orgánulos e á contracción muscular, ou a migración celular, importante no desenvolvemento embrionario, curación de feridas ou na invasividade do cancro. A orixe evolutiva desta proteína pode rastrearse nas células procariotas, nas cales existen equivalentes. Por último, é importante no control da expresión xénica.
Hai moitas doenzas que teñen a súa base en alteracións xenéticas en alelos dos xenes encargados da produción de actina ou das súas proteínas asociadas, e é tamén esencial no proceso de infección dalgúns microorganismos patóxenos. As mutacións nos distintos xenes de actina presentes en humanos ocasionan miopatías, variacións no tamaño e a función cardíaca e xordeira. Os compoñentes do citoesqueleto tamén teñen relación coa patoxenicidade de bacterias intracelulares e virus, especialmente en procesos relacionados coa evasión da resposta do sistema inmune.[4]
A actina é unha das proteínas máis abundantes nos eucariotas e está presente por todo o citoplasma.[3] Nas fibras musculares representa o 20% en peso da proteína celular total e, noutras células animais, oscila entre o 1 e o 5%. Porén, non existe un único tipo de actina, senón que os seus xenes codificantes forman unha familia multixénica (familia que, en plantas, comprende máis de 60 elementos, entre xenes e pseudoxenes e, en humanos, máis de 30).[5] Isto significa que a información xenética de cada individuo posúe instrucións para xerar variantes da actina (denominadas isoformas) que posuirán funcións lixeiramente distintas. Deste modo, os organismos eucariotas expresan distintos xenes que dan lugar a: a actina α, que se encontra en estruturas contráctiles; a actina β, no bordo en expansión das células que empregan a proxección de estruturas celulares como método de mobilidade; e a actina γ, nos filamentos das fibras de estrés.[6] Ademais das similitudes existentes entre as isoformas dun organismo, tamén existe unha conservación evolutiva en canto á estrutura e función entre organismos do dominio eucariota, e mesmo en bacterias, na que se coñece o homólogo MreB, unha proteína que pode polimerizarse en microfilamentos,[7] e en arqueas, nas que existe un representante (Ta0583) aínda máis semellante ás actinas de eucariotas.[8]
A actina preséntase na célula en dúas formas: como monómeros globulares denominados actina G e como polímeros filamentosos denominados actina F (que son filamentos compostos de moitos de monómeros de actina G). A actina F pode denominarse tamén microfilamento. A cada febra de actina únese unha molécula de adenosín trifosfato (ATP) ou de adenosín difosfato (ADP), que á súa vez está asociada a un catión Mg2+. Das distintas combinacións posibles entre as formas de actina e o nucleótido trifosfato, na célula predominan a actina G-ATP e a actina F-ADP.[9][10]
En canto á súa estrutura molecular, a actina G posúe unha aparencia globular vista co microscopio electrónico de varrido; non obstante, por cristalografía de raios X pode apreciarse que está composta por dous lóbulos separados por unha fenda; a estrutura conforma o pregamento ATPase, un centro de catálise encimática ao que pode unirse o ATP e Mg2+ e pode hidrolizar o ATP a ADP e fosfato. Este pregamento é un motivo estrutural conservado que tamén está presente noutras proteínas que interaccionan con nucleósidos trifosfato como a hexoquinase (un encima do metabolismo enerxético) ou as proteínas Hsp70 (unha familia de proteínas que contribúen a que outras proteínas posúan estruturas funcionais).[11] A actina G só é funcional cando posúe ADP ou ATP na súa fenda; porén, na célula predomina o estado unido a ATP cando a actina está libre.[9]

A actina cristalizada por Kabsch, que é a máis utilizada como modelo en estudos estruturais, porque foi a primeira que se purificou, procede do músculo esquelético de coello. Ten unhas dimensións aproximadas de 67 x 40 x 37 Å, unha masa molecular de 41785 Da e un punto isoeléctrico estimado de 4,8. A súa carga neta a pH 7 é de -7.[13] [14]
A secuencia de aminoácidos completa deste tipo de actina determinárona Elzinga e colaboradores en 1973, e afinouse en traballos posteriores do mesmo autor. Contén 374 residuos de aminoácidos. O seu extremo N-terminal é moi ácido. Comeza cun aspartato acetilado no seu grupo amino, mentres que o seu C-terminal é básico, formado por unha fenilalanina precedida por unha cisteína de certa importancia funcional. Ambos os extremos sitúanse nunha posición moi próxima dentro do subdominio I. Presenta tamén algúns aminoácidos anómalos, como unha Nτ-metilhistidina en posición 73.[13]
Está formada por dous dominios coñecidos como grande e pequeno, separados por unha fenda que leva no seu centro ao lugar para a unión do ATP-ADP+Pi. Por debaixo deste existe unha greta de menor profundidade chamada "suco". Cando están na súa forma nativa, malia os seus nomes, ambos os dous dominios teñen un tamaño similar.[15]
Nos estudos topolóxicos, por convención, a proteína oriéntase de maneira que o dominio maior queda á esquerda, mentres que o menor se sitúa á dereita. Nesta posición, o dominio pequeno divídese á súa vez no subdominio I (posición inferior, residuos 1-32, 70-144 e 338-374) e subdominio II (posición superior, residuos 33-69). O dominio maior tamén se divide noutros dous, o subdominio III (inferior, residuos 145-180 e 270-337) e o subdominio IV (superior, residuos 181-269). A zona exposta dos subdominios I e III denomínase extremo "barbado", mentres que á dos subdominios II e IV se lle chama extremo "en punta de frecha". Esta denominación fai referencia ao feito de que debido á pequena masa do subdominio 2, a actina adquire polaridade, que se discutirá posteriormente ao falar da dinámica de ensamblaxe. Algúns autores nomean os subdominios como Ia, Ib, IIa e IIb, respectivamente.[16]
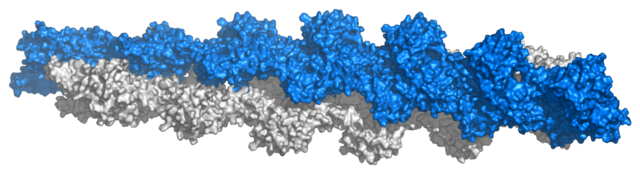
A descrición clásica da actina F indica que ten unha estrutura filamentosa interpretable como unha hélice levoxira monocatenaria cun xiro de 166º e incremento de 27,5 Å ou ben como unha hélice dextroxira bicatenaria con medio paso de rosca de 350-380 Å, e cada actina está rodeada doutras catro.[20] A simetría do polímero de actina, que é dunhas 2,17 subunidades por volta de hélice é incompatible coa formación de cristais, que só é posible cando estas son exactamente 2, 3, 4 ou 6 subunidades por volta. Por tanto, deben realizarse modelos interpretando datos procedentes de técnicas que salvan estes inconvenientes, como a microscopia electrónica, a criomicroscopia electrónica, cristais de dímeros en distintas posicións ou difracción de raios X.[7] En realidade, falar dunha "estrutura" non é correcto para algo tan dinámico como un filamento de actina, polo que sería mellor falar de distintos estados estruturais, entre os cales o dato máis constante é o incremento de 27,5 Å, mentres que a rotación das subunidades mostra unha considerable variabilidade, sendo normal observar desprazamentos de ata o 10% da súa posición ideal. Algunhas proteínas, como a cofilina, parecen incrementar o ángulo de xiro, pero, novamente, pódese interpretar que, en lugar diso, estabilizan algúns "estados estruturais" normais. Estes poderían ser importantes no proceso de polimerización.[21]
As medidas do raio de xiro ou grosor do filamento son máis controvertidas: mentres que os primeiros modelos lle asignaban unha lonxitude de 25 Å, datos actuais de difracción de raios X e de criomicroscopia electrónica coinciden nunha medida duns 23,7 Å. Estes mesmos estudos determinaron con bastante precisión os puntos de contacto entre monómeros. Uns establécense con unidades da mesma cadea, entre o extremo "barbado" dun monómero e o extremo "en punta de frecha" do seguinte, mentres que os monómeros de cadeas adxacentes fan contacto lateralmente por medio de proxeccións do subdominio 4, e as máis importantes son a formada polo C-terminal e un enlace hidrofóbico formado por tres corpos nos que interveñen os residuos 39-42, 201-203 e 286. Para formaren parte dun filamento, segundo este modelo, os monómeros estarían nunha configuración chamada "plana", na que os subdominios xiran entre si, e que tamén parece encontrarse no homólogo bacteriano da actina MreB.[7]
Dado que todas as subunidades dun microfilamento apuntan cara ao mesmo extremo, dise que o polímero presenta polaridade na súa estrutura. Este feito dá lugar a unha convención consistente en nomear o extremo que posúe unha subunidade de actina que expón o lugar polo que une ATP ao medio como «extremo (-)», mentres que o cabo oposto, no cal a fenda está dirixida a outro monómero adxacente, é o «extremo (+)».[6] A denominación «en punta de frecha» e «barbado» dos extremos dos microfilamentos débese ao seu aspecto vistos con microscopio electrónico de transmisión cando se procesan mediante unha técnica denominada «decoración». Este método consiste na adición de elementos S1 da miosina a tecidos fixados con ácido tánico; esta miosina únese de forma polar aos monómeros de actina, o que dá lugar a unha configuración semellante a frechas con plumas ao longo de todo o seu fuste, onde o fuste correspondería á actina e as plumas á miosina. Deste modo, o extremo do microfilamento que queda sen miosina sobresaíndo interprétase como a punta da frecha, e o extremo oposto denomínase barbado.[22]
No músculo, o filamento helicoidal da actina F contén tamén unha molécula de tropomiosina, unha proteína dunha lonxitude de 40 nanómetros que se enrola arredor da hélice de actina F. Durante o estado de repouso celular, a tropomiosina recobre os sitios activos da actina de modo que non pode producirse a interacción actina-miosina que orixina a contracción muscular. Unidas ao longo da febra de tropomiosina hai outras moléculas proteicas, as troponinas, complexos de tres polímeros: troponina I, troponina T e troponina C.[23]

A actina pode adquirir espontaneamente unha gran parte da súa estrutura terciaria.[25] Porén mostra un comportamento moi especial e case único na forma en que adquire a súa forma plenamente funcional a partir da súa forma nativa recentemente sintetizada. A razón da existencia dunha ruta tan especial podería ser a necesidade de evitar a presenza de monómeros de actina mal pregados, que serían tóxicos, porque poderían actuar de terminadores inadecuados da polimerización. En calquera caso, é clave para a estabilidade do citoesqueleto, e mesmo podería ser un proceso esencial para a coordinación do ciclo celular.[26][27]
Para asegurar o correcto pregamento emprega un tipo de chaperonina (proteína que axuda a outras a pregarse) citosólica do grupo II, chamada CCT, formada por un dobre anel de oito subunidades diferentes (heterooctamérica) que se distingue das demais chaperonas moleculares, e en especial da súa homóloga en arqueas GroEL, en que non precisa dunha co-chaperona que actúe de tapa sobre a cavidade central catalítica. Acepta substratos uníndose a eles por medio de dominios específicos, polo que en principio se pensou que era exclusiva da actina e tubulina, aínda que actualmente se comprobou por inmunoprecipitación que polo menos interacciona cun gran número de polipéptidos, que posiblemente funcionan como substratos. Actúa mediante cambios conformacionais dependentes de ATP, e en ocasións cómpren varias roldas de liberación e catálise para que complete o seu traballo.[28]
Para o seu correcto pregamento, a actina e a tubulina tamén necesitan especificamente da colaboración doutra proteína, a prefoldina, un complexo heterohexamérico (formado por seis subunidades distintas), que interaccionan tan especificamente que se cre que coevolucionaron. No caso da actina, esta proteína únese inmediatamente a ela mentres aínda se está a traducir, aproximadamente cando ten unha lonxitude de 145 aminoácidos, que son os correspondentes ao dominio N-terminal.[29]
Empréganse subunidades de recoñecemento diferentes para a actina e a tubulina, aínda que solapadas. Probablemente no caso da actina trátase das subunidades PFD3 e PFD4 que se unen á actina en dous lugares, o I, entre os residuos 60–79, e o II, entre os residuos 170–198. A actina recoñece, carga e entrega á CCT en conformación aberta pola parte interna do extremo dos "tentáculos" da prefoldina (ver imaxe e nota a rodapé).[30] O contacto cando se entrega a actina é tan breve que non se chega a formar un complexo ternario, liberándose a prefoldina inmediatamente.[24]

Posteriormente, a chaperonina citosólica (CCT) realiza o pregamento da actina de forma secuencial, e formando unións coas subunidades, no canto de simplemente encerrala na súa cavidade.[31] Para iso posúe zonas específicas de recoñecemento no seu dominio β apical. A primeira etapa do pregamento consistiría no recoñecemento dos residuos 245-249. Posteriormente, establecerían contacto outros determinantes.[32] Tanto a actina coma a tubulina únense á CCT en conformacións abertas en ausencia de ATP. No caso da actina, en cada cambio conformacional únese a dúas subunidades, a diferenza da tubulina, que o fai a catro. A actina ten secuencias de unión específicas, interaccionando coas subunidades CCTδ e β ou ben con CCTδ e CCTε. Trala unión de AMP-PNP á CCT, os substratos van movéndose pola cavidade da chaperonina. Parece ser tamén que no caso da actina cómpre a actuación da proteína CAP como un posible cofactor nos estadios finais do pregamento da actina.[27]
Aínda non se coñece con exactitude a regulación deste proceso, pero sábese que a proteína PhLP3 (proteína semellante á fosducina) regula a súa actividade inhibíndoa, por medio da formación dun complexo ternario.[28]
A actina é unha ATPase, é dicir, un encima que hidroliza ATP. Este conxunto de encimas caracterízase por actuar con extrema lentitude. Esta ATPase "actívase", ou o que é o mesmo, a súa velocidade aumenta unhas 40.000 veces cando a actina forma parte dun filamento.[21] Un valor de referencia para esta taxa de hidrólise baixo certas condicións ideais sería 0,3 s-1. Posteriormente, o Pi permanecería moito tempo unido á actina xunto ao ADP, liberándose preto do extremo do filamento.[33]
Polo momento non se coñecen os detalles moleculares do mecanismo catalítico. Pero, aínda que existe moita polémica ao respecto, parece claro que para a hidrólise do ATP cómpre que a proteína teña unha conformación "pechada", e crese que achega á distancia axeitada os residuos implicados.[21] Un dos residuos clave sería o Glu137, situado no subdominio 1. A súa función sería ancorar a molécula de auga que realiza un ataque nucleofílico ao enlace do fosfato γ do ATP, mentres o nucleótido se une fortemente aos subdominios 3 e 4. A lentitude do proceso catalítico deberíase á gran distancia e posición nesgada desta molécula de auga con respecto ao seu reactante. Con moita probabilidade, o cambio conformacional que se produce por rotación de dominios entre as formas G e F da actina aproxima o Glu137, permitindo a súa hidrólise. Segundo este modelo, a polimerización e a función ATPase estarían desacopladas nun primeiro momento.[7]
A actina é unha das proteínas máis conservadas ao longo da evolución porque interacciona cun gran número de proteínas. Hai un 80,2% de conservación de secuencia a nivel de xene entre a de Homo sapiens e a do lévedo Saccharomyces cerevisiae, e un 95% de conservación da estrutura primaria do produto proteico.
Aínda que a maioría dos lévedos teñen só un xene para a actina, os eucariotas superiores, en xeral, expresan varias isoformas de actina codificadas por unha familia de xenes relacionados. Os mamíferos teñen polo menos seis xenes de isoformas de actina codificadas en xenes separados,[34] que se dividen en tres clases (alfa, beta e gamma) segundo os seus puntos isoeléctricos. En xeral, as actinas alfa atópanse no músculo (α-esquelética, α-liso aórtico, α-cardíaca, e γ2-liso entérico), mentres que as isoformas beta e gamma son abundantes en células non musculares (β- e γ1-citoplásmicas). Aínda que as secuencias de aminoácidos e as propiedades in vitro das isoformas son moi similares, estas isoformas non poden substituírse completamente unhas por outras in vivo.[35]
O xene típico de actina ten aproximadamente un 5'-UTR duns 100 nucleótidos, unha rexión traducida de 1200 nucleótidos, e un 3'-UTR de 200 nucleótidos. A maioría dos xenes de actina están interrompidos por intróns, e teñen ata seis intróns en 19 posibles localizacións ben caracterizadas. A grande conservación da familia fai que a actina sexa o modelo favorito para realizar estudos que comparan modelos de intróns temperáns e tardíos da evolución dos intróns.
Todos os procariotas non esféricos parecen posuír xenes como o MreB, que codifican homólogos da actina; estes xenes son necesarios para o mantemento da forma da célula. O xene ParM derivado dun plásmido codifica unha proteína similar á actina cuxa forma polimerizada é inestable dinamicamente, e parece intervir para repartir o ADN do plásmido entre as células fillas durante a división celular por un mecanismo análogo ao empregado polos microtúbulos durante a mitose eucariótica.[36]

A actina F combina as cualidades de ser resistente e dinámica. A diferenza doutros polímeros, como o ADN, que manteñen unidos os seus elementos constitutivos mediante enlaces covalentes, nos filamentos de actina os monómeros ensámblanse por medio de enlaces máis febles de tipo non covalente. Isto, que en principio debilita a estrutura, porque se podería romper por axitación térmica, soluciónase grazas ao establecemento de enlaces laterais cos monómeros veciños. Ao mesmo tempo, os enlaces febles teñen a vantaxe de que os extremos do filamento poden liberar ou incorporar doadamente monómeros, de maneira que se poden remodelar rapidamente e cambiar a estrutura celular da que son responsables en resposta a estímulos ambientais. Isto último xunto co mecanismo bioquímico polo que se efectúa é o que se coñece como "dinámica de ensamblaxe".[4]
A polimerización e despolimerización da actina é necesaria para a quimiotaxe e a citocinese. Cómpren factores nucleantes para estimular a polimerización da actina. Un deses factores nucleantes é o complexo Arp2/3, que imita ao dímero de actina G para estimular a nucleación (ou formación do primeiro trímero) de actina G monomérica. O complexo Arp2/3 únese aos filamentos de actina cun ángulo de 70º para formar novas ramas de actina nos filamentos de actina existentes. Ademais, aos filamentos de actina únese ATP, e a hidrólise deste ATP estimula a desestabilización do polímero.
O crecemento dos filamentos de actina pode ser regulado polas proteínas timosina e profilina. A timosina únese á actina G para amortecer o proceso de polimerización, mentres que a profilina únese á actina G para intercambiar ADP por ATP, promovendo a adición monomérica ao extremo barbado (+) dos filamentos de actina F.
Os estudos da dinámica de adición e perda de subunidades dos microfilamentos realizáronse in vitro (é dicir, no laboratorio, fóra de sistemas celulares) debido a que o polímero de actina resultante dá lugar á mesma actina F producida in vivo, onde este proceso está controlado por moitas proteínas para responder ás necesidades celulares, de modo que sería moi difícil observar as súas condicións básicas.[37] In vitro, este feito prodúcese de forma secuencial: primeiro, dáse unha «fase de activación», na que a unión e intercambio de catións divalentes en lugares específicos da actina G, unidos a ATP, producen un cambio conformacional, coñecido ás veces como Actina G* ou monómero de actina F, porque é máis parecida ás unidades que se sitúan no filamento.[16] Isto prepáraa para a seguinte «fase de nucleación», na cal a actina G dá lugar a pequenos fragmentos inestables de actina F con capacidade de polimerizar. Inicialmente, fórmanse dímeros e trímeros de maneira inestable. Cando o número destes é grande dabondo, ten lugar a «fase de elongación», na que o filamento se forma e medra rapidamente por adición reversible de novos monómeros a ambos os extremos.[38] Finalmente, no «equilibrio estacionario», os monómeros de actina G intercámbianse nos extremos do microfilamento sen que varíe a lonxitude total do polímero.[3] Nesta última fase defínese a «concentración crítica Cc» como a relación entre as constantes de ensamblaxe e desensamblaxe (trátase, pois, dunha constante de disociación), e representa a concentración de actina G na cal a dinámica de adición e eliminación de monómeros non produce unha modificación na lonxitude do microfilamento. Nas condicións usuais in vitro, Cc é 0,1 μM,[39] o que significa que a valores maiores dáse unha polimerización e a valores menores, unha despolimerización.[40]
Un asunto importante que se introduciu no apartado anterior é o feito de que, aínda que a actina hidroliza ATP, todo parece indicar que isto non intervén na ensamblaxe, porque, por unha parte, a hidrólise prodúcese en grande medida no interior do filamento, e por outra, o ADP tamén pode polimerizar. Isto formula a cuestión de comprender cal é o proceso termodinamicamente desfavorable que require un gasto de enerxía tan enorme. O chamado "ciclo da actina", que liga a hidrólise á polimerización, consiste na adición de monómeros de Actina G-ATP preferentemente no extremo barbado, creando un fluxo de monómeros cara ao extremo en punta de frecha no que se coñece como "cinta de transporte" (treadmilling, en inglés), onde os monómeros estarían en forma de Actina F-ADP e serían liberados, intercambiando posteriormente este ADP por ATP e pechando dese modo o ciclo.
Pouco despois da adición, prodúcese a hidrólise do ATP de forma relativamente rápida. Existen dúas hipóteses sobre como se produce, a estocástica, na que a hidrólise se produciría ao chou influída en certo modo polas moléculas veciñas, e a vectorial, na que só se produciría no límite con outras moléculas que xa hidrolizaron o seu ATP. En calquera caso, non se libera o Pi resultante, senón que permanece un tempo unido non covalentemente á actina-ADP, de maneira que nun filamento existirían tres especies de actina: ATP-Actina, ADP+Pi-Actina e ADP-Actina.[33] O contido dun filamento en cada unha destas especies depende da súa lonxitude e estado: ao comezo da elongación, o filamento ten unha composición aproximadamente equivalente de monómeros con ATP e ADP+Pi e só unha pequena cantidade xunto ao extremo (-) de actina-ADP. A medida que se acada o estado estacionario, a situación invértese, e a maior parte do filamento está con ADP e só a zona preto do extremo (+) contén ADP+Pi, mentres que o ATP está reducido ao extremo.[41]
Se comparamos os filamentos de actina-ADP puros con aqueles que incorporan ATP, nos primeiros as constantes críticas son similares en ambos os extremos, mentres que nos outros dous nucleótidos a Cc é diferente: No extremo (+) Cc+=0,1 μM, mentres que no extremo (-) Cc-=0,8 μM, co cal se dan as seguintes situacións:[6]
Por tanto, pódese deducir que a enerxía da hidrólise utilízase para crear un verdadeiro "estado estacionario", é dicir, crear un fluxo en lugar dun simple equilibrio, o cal dota ao filamento de dinamismo, polaridade e forza de tracción, o que xustifica o gasto pola ganancia de funcións biolóxicas esenciais.[33] Ademais, as proteínas que se unen á actina que controlan este dinamismo detectan a configuración dos distintos tipos de monómeros, como se verá na próxima sección.
Nos estereocilios parece existir unha excepción na forma de acoplamento típica dos microfilamentos mediante cinta de transporte (treadmilling). Neste caso, o control do tamaño da estrutura sería totalmente apical e dalgunha maneira controlada pola expresión xénica, é dicir, pola cantidade total de monómero de proteína sintetizada nun momento dado.[42]

In vivo, o citoesqueleto de actina non está composto exclusivamente de actina, senón que para a súa xeración, permanencia e función require outras proteínas; estas denomínanse proteínas de unión a la actina ou proteínas que se unen á actina (ABP, actin binding proteins) e interveñen na súa polimerización e despolimerización, estabilidade, organización en feixes ou redes, e na súa fragmentación e destrución.[3] A diversidade destas proteínas é tan grande, que se considera que a actina é a proteína que participa no maior número de interaccións proteína-proteína de todas as coñecidas.[44] Por exemplo, existen elementos que secuestran a actina G, impedindo a súa incorporación aos microfilamentos. De igual maneira, existen proteínas que estimulan a súa polimerización ou que dotan de complexidade ás redes en síntese.[6] Entre elas están:

Outras proteínas que se unen á actina regulan a lonxitude dos microfilamentos realizando cortes neles, o que dá lugar a novos extremos activos para a polimerización. Por tanto, se un microfilamento, que posúe dous extremos aos que poden unirse ou disociarse monómeros, é cortado dúas veces, orixínanse tres novos microfilamentos con seis extremos; a nova situación favorece a dinámica de ensamblaxe e desensamblaxe. Entre estas proteínas salientan a xelsolina e a cofilina. O corte realízano primeiramente mediante cambios na conformación do monómero de actina ao que se unen no polímero, e despois quedan recubrindo o novo extremo (+) xerado, o que impide o agregado ou o intercambio de novas subunidades de actina G e, como os extremos (-) quedan sen recubrir, favorecen a despolimerización dos filamentos.[49]
Outro tipo de proteínas que se unen á actina recobren os extremos da actina F para estabilizalos, mais sen capacidade de rompelos. Exemplos destas proteínas son CapZ (que une os extremos (+) segundo os niveis de Ca2+/calmodulina da célula, niveis que dependen de sinais externos e internos da célula e que interveñen na regulación das súas funcións biolóxicas)[50] ou a tropomodulina (que se une aos extremos (-)). A tropomodulina é esencial como estabilizador da actina F presente nas miofibrilas dos sarcómeros do músculo, estruturas caracterizadas pola súa grande estabilidade.[51]

O complexo Arp2/3 está amplamente difundido en todos os organismos eucariotas.[53] Está composto por sete subunidades, algunhas das cales posúen unha topoloxía claramente relacionada coa súa función biolóxica: dúas das súas subunidades, denominadas «ARP2» e «ARP3», posúen unha estrutura moi semellante á dos propios monómeros de actina. Dita homoloxía permite a ambas as unidades comportarse como axentes nucleantes da polimerización dos monómeros de actina G a actina F. Ademais, este complexo é necesario para establecer estruturas dendríticas e en anastomose (bifurcadas ou en rede), e, por tanto, máis complexas, de actina F.[54]

Existen varias toxinas que interfiren coa dinámica das actinas, tanto despolimerizándoas (latrunculina e citocalasina D) coma estabilizándoas (faloidina):
A proteína actina encóntrase tanto no citoplasma coma no núcleo celular.[59] A súa localización está regulada polas vías de transdución de sinais que integran os estímulos que a célula recibe e que permite a reestruturación das redes de actina en resposta a eles. En Dictyostelium, intervén a ruta dos fosfoinosítidos mediada pola fosfolipase D.[60] Os filamentos de actina son especialmente abondosos e estables nas fibras musculares. Dentro do sarcómero (a unidade morfolóxica e fisiolóxica das fibras musculares) a actina disponse formando as bandas I e A; nestas últimas, preséntase conxuntamente coa miosina.[61]

Os microfilamentos interveñen no movemento de todas as células móbiles, mesmo nas non musculares, porque se describiu que os fármacos que desorganizan a actina F (como as citocalasinas) afectan á actividade de ditas células. A proteína actina supón o 2% do total de proteínas en hepatocitos, o 10% en fibroblastos, o 15% en amebas e ata o 50-80% en plaquetas activadas.[62] Existen distintos grupos de actina, con estrutura e funcións lixeiramente distintas. A actina α é exclusiva das fibras musculares, e a actina presente noutras células adoita ser dos tipos β e γ. Ademais, a actina de tipos distintos ao α adoita ter unha alta taxa de recambio que provoca que a maior parte dela non forme parte de estruturas permanentes. Así, os microfilamentos nas células non musculares aparecen de dúas formas:[63]
En lévedos, o citoesqueleto de actina é clave durante os procesos de endocitose, citocinese, determinación da polaridade celular e durante a morfoxénese. Estes procesos, ademais de depender da actina, implican a 20 ou 30 proteínas asociadas, moi conservadas evolutivamente, xuntro con multitude de moléculas de sinalización; a combinación de todos estes elementos permite unha ensamblaxe modulada espacial e temporalmente que define a bioloxía celular en resposta a estímulos internos e externos.[64]
Os lévedos posúen tres grandes tipos de elementos produto da asociación da actina: parches, cables e aneis que, malia detectarse durante longos períodos de tempo, vense sometidos a un equilibrio dinámico debido á continua polimerización e despolimerización. Como proteínas accesorias, posúen unha cofilina/ADF de 16 kDa (codificiada por un único xene, denominado COF1); o Aip1, un cofactor da cofilina que favorece a desensamblaxe dos microfilamentos; o Srv2/CAP, un regulador da dinámica relacionado con proteínas adenilil ciclases; unha profilina de aproximadamente 14 kDa que se asocia aos monómeros de actina; e a twinfilina, unha proteína de 40 kDa implicada na organización das estruturas tipo parche.[64]
Os estudos de xenómica de plantas revelaron a existencia de isovariantes proteicas dentro da familia de xenes da actina. En Arabidopsis thaliana, unha dicotiledónea empregada como organismo modelo, existen polo menos dez tipos de actinas, nove de α tubulinas, seis de β tubulinas, seis de profilinas e ducias de miosinas. Tal diversidade explícase pola necesidade evolutiva de posuír variantes lixeiramente diferentes na súa pauta de expresión temporal e espacial; porén, a maioría delas exprésanse conxuntamente nos tecidos analizados. O entramado de redes de actina distribúese por todo o citoplasma das células cultivadas in vitro, cun reforzo arredor do núcleo que se conecta, mediante raios, ao córtex celular; dito entramado é moi dinámico, experimentando unha continua polimerización e despolimerización.[65]

Aínda que as células vexetais posúen xeralmente unha parede celular que define a súa morfoloxía e impide o seu movemento, os seus microfilamentos xeran as forzas necesarias para varias actividades celulares, por exemplo, as correntes citoplasmáticas xeradas polos microfilamentos e as miosinas. Ademais, a actina intervén no movemento de orgánulos e morfoxénese celular, procesos que inclúen a división celular, a elongación e a diferenciación.[67]
En canto ás proteínas asociadas ao citoesqueleto de actina presentes en plantas pódense mencionar as seguintes:[67] a vilina, unha proteína pertencente á familia da xelsolina/severina, que pode cortar microfilamentos e unir monómeros de actina en presenza do catión calcio; a fimbrina, un elemento que pode recoñecer e unir monómeros de actina e que intervén na formación de entramados (mediante unha regulación diferente á que hai en células animais e de lévedos);[68] as forminas, proteínas que poden actuar como axentes nucleantes da polimerización a actina F; a miosina, típico motor molecular propio de eucariotas que, en Arabidopsis thaliana, está codificado por 17 xenes clasificados en dúas clases distintas; a CHUP1, con capacidade de unir actina e implicado na distribución espacial dos cloroplastos na célula; a KAM1/MUR3, unha proteína que define a morfoloxía do complexo de Golgi e a composición en xiloglicanos da parede celular; a NtWLIM1, proteína que facilita a aparición de estruturas con forma de nobelo de actina; e a ERD10, que participa na asociación entre orgánulos delimitados por membranas e os microfilamentos e que parece desempeñar un papel especialmente importante en condicións de estrés.
A actina é esencial para a transcrición feita polas ARN polimerases Pol I, Pol II e Pol III. Na transcrición feita por Pol I, a actina e a miosina (MYO1C, que se une ao ADN) actúan como motores moleculares. Para a transcrición feita por Pol II, cómpre β-actina para a formación do complexo de preiniciación. A Pol III contén β-actina como unha subunidade. A actina pode tamén ser un compoñente dos complexos de remodelación da cromatina e de partículas de pre-mRNP (formadas polo pre-ARNm envolto en proteínas), e está implicada na exportación nuclear de ARNs e proteínas.[69]

No músculo, o filamento helicoidal da actina F contén tamén unha molécula de tropomiosina, que é unha proteína dunha lonxitude de 40 nanómetros que se enrola arredor da hélice de actina F. Durante o estado de repouso celular, a tropomiosina recobre os sitios activos da actina de modo que non se pode producir a interacción actina-miosina (esta interacción dá lugar a un esvaramento entre ambos os filamentos que, por coordinación de moitas copias destes elementos dispostos nos músculos, produce a súa contracción). Unidas ao longo da febra de tropomiosina hai outras moléculas proteicas, as troponinas, complexos de tres polímeros: troponina I, troponina T e troponina C.[23] A función moduladora da tropomiosina depende da interacción coa troponina en presenza de ións de Ca2+.[70]
A actina, xunto coa miosina, intervén na contracción e relaxación dos músculos, e entre as dúas supoñen o 90% das proteínas musculares.[71] O proceso global dispárase mediante un sinal externo, tipicamente mediante un potencial de acción excitador do músculo que contén as células especializadas ricas en filamentos de actina e miosina. O ciclo de contracción-relaxación comprende os seguintes pasos:[72]
O estudo clásico da función da actina circunscribíaa ao mantemento do citoesqueleto e, por tanto, á organización e movemento dos orgánulos e determinación da forma celular.[63] Porén, o papel da actina é bastante máis amplo na fisioloxía celular eucariota; e mesmo existen elementos semellantes en procariotas.

Na maioría dos mamíferos existen seis xenes diferentes para a actina. Dous deles están relacionados co citoesqueleto (ACTB e ACTG1) mentres que as catro restantes o están co músculo esquelético (ACTA1), músculo liso (ACTA2), músculo liso entérico (ACTG2) e co músculo cardíaco (ACTC1). As mutacións que afectan a estes xenes eran descoñecidas ata 1998, e viuse que producen miopatías, variacións no tamaño e a función cardíaca e xordeira. Ademais, a actina do citoesqueleto está implicada no mecanismo de patoxenicidade de moitos axentes infecciosos, entre eles o VIH. A inmensa maioría das mutacións que afectan á actina son de tipo puntual e teñen un efecto dominante, agás polo menos seis mutacións de miopatía nemalínica. Isto débese a que en moitos casos a variedade mutante do monómero de actina actúa como unha "tapa" que impide a elongación da actina F.[16]
ACTA1 é o xene que codifica a isoforma α da actina humana, presente principalmente no músculo esquelético, e que tamén se expresa no músculo cardíaco e na glándula tiroide.[87] A súa secuencia consta de sete exóns, que producen cinco transcritos coñecidos.[88] En 2006, o ENMC (European Neuromuscular Centre) publicara 116 mutacións relacionadas con patoloxías coñecidas como actinopatías. A maior parte delas consisten en substitucións puntuais de aminoácidos, que en moitos casos poden ser asociadas co fenotipo que determina a gravidade e o curso da doenza.[16][88]

Maniféstanse alterando a estrutura e a función do músculo esquelético producindo tres formas de miopatía: miopatía nemalínica tipo 3, miopatía conxénita con exceso de microfilamentos (CM) e miopatía conxénita con desproporción de tipos de fibra (CFTDM). Tamén se detectaron mutacións que producen miopatías core (con zonas desprovistas de actividade oxidativa).[90] Aínda que os seus fenotipos son similares, ademais da miopatía nemalínica típica e a de bastóns intranucleares, algúns especialistas distinguen un tipo de miopatía, chamada actínica da miopatía nemalínica. Na primeira acumúlanse agregados de actina en troques dos típicos bastóns. Un paciente pode mostrar máis dun destes fenotipos na biopsia.[91] Os síntomas máis habituais consisten nunha morfoloxía facial típica (facies miopática), debilidade muscular e atraso no desenvolvemento motor e dificultades respiratorias. O curso, a gravidade e a idade de aparición son moi variables, e encóntranse formas de miopatía solapadas. Na miopatía nemalínica aparecen unhas estruturas non patognomónicas en diversas localizacións das fibras musculares tipo 1 coñecidas como "bastóns nemalínicos", cunha composición similar á dos discos Z do sarcómero.[92]
A patoxénese é moi variada. Moitas mutacións danse na zona da fenda da actina, próximas ao lugar de unión para os nucleótidos, mentres que outras se dan no dominio 2, ou nas zonas de interacción coas proteínas asociadas, o que explica a gran variedade de agregados que se forman nestes casos, como corpos nemalínicos, intranucleares ou corpos cebra.[16] Na miopatía nemalínica prodúcense cambios no pregamento e nas propiedades de agregación da actina, e tamén na expresión doutras proteínas asociadas. Nalgunhas variantes nas que se encontran corpos intranucleares, o cambio no pregamento agocha o sinal de exportación nuclear, de tal xeito que a agregación da forma mutante de actina se produce no núcleo celular.[93] Ao contrario, parece que nas mutacións de ACTA1 que dan lugar a CFTDM está máis afectada a función sarcomérica que a propia estrutura.[94] En traballos recentes tratouse de aclarar o aparente paradoxo de que non exista unha correlación clara entre a abundancia de bastóns e a debilidade muscular. Parece ser que algunhas mutacións particulares poden inducir unha maior taxa de apoptose nas fibras musculares de tipo II.[26]

Existen dúas isoformas que codifican actinas do músculo liso:
ACTG2 codifica a isoforma máis longa de actina, que ten nove exóns, un deles, o situado no extremo 5', que non se traduce.[95] Trátase dunha γ actina que se expresa no músculo liso entérico. Non se atoparon mutacións que se correspondan a patoloxías neste xene, aínda que se viu mediante microarrays que esta é a proteína que, con diferenza, máis aumenta a súa expresión nos casos de resistencia á quimioterapia con cisplatino.[96]
ACTA2 codifica unha α actina localizada no músculo liso, e tamén no músculo liso vascular. A mutación MYH11 podería ser responsable de polo menos un 14% dos casos de aneurismas de aorta torácica hereditarios, concretamente o tipo 6, porque a variante mutada produce unha ensamblaxe incorrecta dos filamentos e unha redución da capacidade de contracción do músculo liso vascular. Nestes individuos obsérvase unha dexeneración aórtica medial, con áreas de desorganización e hiperplasia, e estenose dos vasa vasorum da aorta.[97] O número de doenzas nas que se cre que podería estar implicado este xene está en aumento. Foi relacionado coa enfermidade de Moyamoya, e parece ser que algunhas mutacións en heterocigose poderían predispoñer a moitas patoloxías vasculares, como o aneurisma de aorta torácica e a cardiopatía isquémica.[98] A α-actina do músculo liso tamén é un interesante marcador para avaliar a progresión da cirrose hepática.[99]
ACTC1 é o xene que codifica a isoforma da α actina presente no músculo cardíaco. Secuenciárono por primeira vez Hamada e colaboradores en 1982, que comprobaron que estaba interrompido por cinco intróns.[100] Foi o primeiro xene dos seis onde se encontraron alelos implicados en procesos patolóxicos.[101]

Describíronse varios trastornos estruturais que orixinan unha disfunción cardíaca asociados a mutacións puntuais neste xene, como a miocardiopatía dilatada tipo 1R e a miocardiopatía hipertrófica tipo 11. Recentemente viuse que algúns defectos do septo atrial tamén poderían estar relacionados con estas mutacións.[103][104]
No caso da cardiomiopatía dilatada estudáronse dous casos nos que en ambos os dous se produce unha substitución en aminoácidos moi conservados pertencentes aos dominios que se unen aos discos Z e discos intercalados, todo o cal leva á hipótese de que a dilatación se produce por un defecto de trasmisión da forza contráctil nos miocitos.[20][101]
As alteracións de ACTC1 son responsables de menos do 5% das cardiomiopatías hipertróficas.[105] Demostrouse tamén a existencia de varias mutacións puntuais, como son:[106]
A patoxénese parece obedecer a un mecanismo compensatorio: as proteínas mutantes actuarían como "tóxico" cun efecto dominante, diminuíndo a capacidade de contracción cun rendemento mecánico anormal, de modo que a hipertrofia, que adoita ser tardía, sería consecuencia dunha resposta normal do músculo cardíaco ao estrés.[107]
Recentemente atopáronse mutacións de ACTC1 implicadas noutros dous procesos patolóxicos: a miocardiopatía restritiva idiopática infantil,[108] e o miocardio ventricular esquerdo non compacto.[109]
O locus ACTB é moi complexo. Existen moitos pseudoxenes repartidos por todo o xenoma, e a súa secuencia contén seis exóns que poden dar lugar ata 21 transcritos diferentes por splicing alternativo, coñecidos como actinas β. En correspondencia con esta complexidade, tamén os seus produtos teñen localizacións e forman parte de procesos moi distintos (citoesqueleto, complexo NuA4 histona-aciltransferase, núcleo celular) e asociáronse a este mecanismo gran cantidade de procesos patolóxicos (carcinomas, distonía xuvenil, mecanismos de infeccións, malformacións no sistema nervioso e invasividade de neoplasmas, entre outras).[110] Atopouse unha nova forma de actina kappa, que parece substituír a actina β en procesos tumorais.[111]

Ata o momento puidéronse detectar tres procesos patolóxicos que se deben a unha alteración directa da secuencia dun xene:
ACTG1 é o locus que codifica a proteína da γ actina citosólica responsable da formación de microfilamentos do citoesqueleto. Contén 6 exóns, dando lugar a 22 ARN mensaxeiros distintos, o cal produce 4 isoformas completas, posiblemente expresadas dunha forma dependente de tecido. Tamén ten dous promotores alternativos.[116] Atopouse que as secuencias traducidas deste locus e o da β actina son máis semellantes do agardado, o que suxire que puido existir unha secuencia ancestral común que sufriu duplicación e conversión xénica.[117]
Desde o punto de vista patolóxico, asociouse a procesos como a amiloidose, a retinite pigmentosa, mecanismos de infección, enfermidades renais e diversas perdas auditivas conxénitas.[116]
Relacionadas con seis mutacións puntuais autosómicas dominantes na secuencia, encontramos diversas formas de perdas de audición, en especial a sensorineural tipo 20/26. Parece que afectan de forma específica aos estereocilios das células ciliadas do órgano de Corti. A β actina é a proteína máis abundante nos tecidos humanos, pero non así nas células ciliadas, o que explicaría a localización da patoloxía. Por outra parte, parece que a maior parte destas mutacións afectan a zonas de unión con outras proteínas, en especial a actomiosina.[16] Algúns experimentos suxiren que o mecanismo patoxénico deste tipo de xordeira se debe a que a actina F dos mutantes sería máis sensible do habitual á cofilina.[118]
Por outra parte, aínda que non se ten constancia de ningún caso patolóxico, sábese que a γ actina tamén se expresa no músculo esquelético, e aínda que en cantidades moi pequenas, os modelos animais mostraron que a súa ausencia podería dar lugar a miopatías.[119]
Algúns axentes infecciosos utilizan a actina, especialmente a citoplasmática, no seu ciclo de vida. En bacterias existen basicamente dúas formas desta utilización:
Ademais do exemplo citado anteriormente, nas etapas iniciais da internalización dalgúns virus, notablemente o VIH, estimúlase a polimerización da actina, por exemplo inactivando a cofilina.[124]
Nos procesos de invasión das células cancerosas, as protrusións baseadas en actina desempeñan un papel aínda non determinado.[125]
O citoesqueleto eucariota ten algúns compoñentes que presentan unha grande semellanza ao longo da escala filoxenética, especialmente a actina e a tubulina. Por exemplo, a proteína codificada polo xene ACTG2 de humanos posúe unha equivalencia absoluta cos ortólogos presentes en rata e rato, aínda que a nivel de nucleótidos a identidade diminúe ao 92 %.[126] Porén, existen maiores diferenzas cos equivalentes en procariotas (FtsZ e MreB), que, á súa vez, presentan unha identidade de secuencia de entre un 40−50% entre as distintas especies de bacterias e arqueas. Algúns autores suxiren que a proteína ancestral que deu lugar ao modelo básico de actina eucariota aseméllase ás do citoesqueleto bacteriano presentes na actualidade.[127]

Alguúns autores salientan que a actina, a tubulina e as histonas, un tipo de proteínas implicadas na estabilización e regulación do ADN, presentan similitudes na súa capacidade de unir nucleótidos e no seu funcionamento baseado no aproveitamento do movemento browniano, e suxiren que todas elas poderían derivar dun devanceiro común.[128] Por tanto, os mecanismos evolutivos diversificaron a proteína ancestral nas variantes hoxe presentes, conservando, entre outras, as actinas como moléculas eficaces para abordar procesos biolóxicos antigos e esenciais, como a endocitose.[129]
As bacterias non teñen un citoesqueleto comparable en complexidade ao dos eucariotas, mais describíronse proteínas que teñen unha grande semellanza cos monómeros e polímeros de actina. A proteína MreB de bacterias polimeriza formando filamentos delgados, non helicoidais e, máis raramente, formando estruturas helicoidais semellantes á actina F.[7] Ademais, a súa estrutura cristalina é moi similar á da actina G (en conformación tridimensional), e mesmo existen equivalencias entre os protofilamentos de MreB e a actina F. O citoesqueleto bacteriano tamén posúe entre os seus compoñentes as proteínas FtsZ, semellantes á tubulina.[130]
Por tanto, as bacterias posúen un citoesqueleto con elementos homólogos á actina (por exemplo, MreB, ParM, e MamK), pero a secuencia aminoacídica destas proteínas diverxe do das presentes en células animais. Non obstante, MreB e ParM posúen unha alta similitude estrutural coa actina eucariota. Os microfilamentos, moi dinámicos, xerados por agregación de MreB e ParM son esenciais para a viabilidade celular e participan na morfoxénese da célula, segregación do xenóforo e polaridade celular. ParM, un homólogo da actina codificado nun plásmido, intervén na regulación do ADN de plásmidos.[131]
O aproveitamento da actina nos laboratorios de ciencia e tecnoloxía deriva da súa participación como pista sobre a que se moven motores moleculares como a miosina (tanto no músculo coma fóra del), e da súa presenza necesaria para o funcionamento celular. Tamén se usa como ferramenta de diagnóstico, xa que algunhas variantes anómalas da actina están relacionadas coa aparición de patoloxías.

A actina observouna experimentalmente por primeira vez en 1887 W.D. Halliburton, que extraeu do músculo unha proteína que coagulaba preparacións de miosina, á que denominou "fermento da miosina".[140] Pero Halliburton non foi quen de efectuar a súa caracterización, polo que o descubrimento da actina se atribúe a Brúnó F. Straub, que daquela era un bioquímico mozo que traballaba no laboratorio de Albert Szent-Györgyi no Instituto de Química Médica da Universidade de Szeged, en Hungría.
En 1942, Straub desenvolveu unha nova técnica para a extracción de proteínas musculares que lle permitía illar cantidades substanciais de actina relativamente pura. Este método é o mesmo que esencialmente se utiliza nos laboratorios actualmente. Szent-Györgyi describira previamente unha forma máis viscosa de miosina, producida por extraccións lentas en músculo, como "miosina activada", e, como a proteína de Straub producía o efecto activador, denominouna actina. A viscosidade diminuía se se engadía ATP á mestura de ambas as proteínas, coñecida como actomiosina. O traballo de ambos os investigadores non puido publicarse nos países occidentais debido ao ambiente bélico da segunda guerra mundial, pero saíu á luz en 1945 ao publicarse como suplemento na Acta Physiologica Scandinavica.[141] Straub continuou traballando na actina ata 1950, publicando que podía unirse ao ATP e que, durante a súa polimerización para formar microfilamentos, hidrolizábase a ADP + Pi, que permanecía unido ao microfilamento. Straub suxeriu que esta reacción desempeñaba un papel na contracción muscular, pero isto só é certo no caso do músculo liso e non se verificou experimentalmente ata 2001.[142][143]
A secuencia de aminoácidos completárona Elzinga e colaboradores en 1973,[15] e a estrutura cristalográfica da actina G determinárona en 1990 Kabsch e colaboradores, aínda que se trataba dun cocristal no que formaba un complexo coa desoxirribonuclease I,[17] e nese mesmo ano Holmes e colaboradores propuxeron un modelo para a actina F.[144] Este procedemento de cocristalización con diferentes proteínas foi empregado repetidamente durante os seguintes anos, ata que en 2001 se conseguiu cristalizar a proteína illada xunto con ADP. Foi posible grazas ao emprego dun conxugado de rodamina que impedía a polimerización bloqueando o aminoácido cys-374.[12] Ese mesmo ano produciuse o falecemento de Christine Oriol-Audit, a investigadora que en 1977 conseguiu cristalizar por primeira vez a actina en ausencia de proteínas unidas á actina (ABP). Os cristais eran demasiado pequenos para a tecnoloxía da época.[145]
Aínda que actualmente non existe un modelo de alta resolución da forma filamentosa, o equipo de Sawaya realizou en 2008 unha aproximación máis exacta baseándose en múltiples cristais de dímeros de actina que contactan en diferentes lugares.[146] Este modelo foi refinado polo propio autor e por Lorenz. Outros enfoques, como o uso de criomicroscopia electrónica ou radiación sincrotrón permitiron recentemente aumentar o nivel de resolución e comprender con maior profundidade a natureza das interaccións e os cambios conformacionais implicados na formación do filamento de actina.[7][147]
Seamless Wikipedia browsing. On steroids.
Every time you click a link to Wikipedia, Wiktionary or Wikiquote in your browser's search results, it will show the modern Wikiwand interface.
Wikiwand extension is a five stars, simple, with minimum permission required to keep your browsing private, safe and transparent.