kémiai elem, rendszáma 8, vegyjele O From Wikipedia, the free encyclopedia
Az oxigén a periódusos rendszer kémiai elemeinek egyike. Vegyjele O, rendszáma 8. Neve görög eredetű, a ὀξύς (oxys; ’sav’, szó szerint ’heveny’, utalva a savak savanyú ízére) és a -γενής (-genes; ’nemző’) szavak összetételéből származik; mert elnevezése idején még tévesen úgy gondolták, hogy az oxigén az összes savhoz szükséges összetevő. Régies magyar elnevezése éleny vagy savító.[3] Standard hőmérsékleten és nyomáson az oxigénatomok párosával egymáshoz kötődnek, az így létrejött kétatomos dioxigén (O2) színtelen, szagtalan, íztelen gáz. Ez a molekula a légkör fontos részét képezi, nélkülözhetetlen a szárazföldi élet fenntartásához.
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Általános | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Név, vegyjel, rendszám | oxigén, O, 8 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Latin megnevezés | oxygenium | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Elemi sorozat | nemfémek | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Csoport, periódus, mező | 16, 2, p | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Megjelenés | színtelen  | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Atomtömeg | 15,99903–15,99977 g/mol[1][2] | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Elektronszerkezet | [He] 2s2 2p4 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Elektronok héjanként | 2, 6 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Fizikai tulajdonságok | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Halmazállapot | gáz | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Sűrűség | (0 °C, 101,325 kPa) 1,429 g/l | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Hármaspont | 54,36 K, 152 Pa | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Olvadáspont | 54,36 K (-218,79 °C, -361,82 °F) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Forráspont | 90,20 K (-182,95 °C, -297,31 °F) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Kritikus pont | 154,59 K, 5,043 MPa | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Olvadáshő | (O2) 0,444 kJ/mol | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Párolgáshő | (O2) 6,82 kJ/mol | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Moláris hőkapacitás | (25 °C) (O2) 29,378 J/(mol·K) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Atomi tulajdonságok | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Kristályszerkezet | köbös | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Oxidációs szám | −2, −1; 0; +1; +2 (semleges oxid) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Elektronegativitás | 3,44 (Pauling-skála) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Ionizációs energia | 1.: 1313,9 kJ/mol | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 2.: 3388,3 kJ/mol | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 3.: 5300,5 kJ/mol | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Atomsugár | 60 pm | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Atomsugár (számított) | 48 pm | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Kovalens sugár | 66±2 pm | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Van der Waals-sugár | 152 pm | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Egyebek | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Mágnesség | paramágneses | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Hővezetési tényező | (300 K) 26,58 mW/(m·K) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Hangsebesség | (gáz, 27 °C) 330 m/s | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| CAS-szám | 7782-44-7 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Fontosabb izotópok | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Hivatkozások | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Az oxigén az oxigéncsoport elemei közé tartozik; erősen reaktív nemfémes elem, amely más elemekkel könnyen képez vegyületeket (úgynevezett oxidokat), a három legkönnyebb nemesgáz, a hélium, a neon és az argon kivételével.[4] Az oxigén nagyon erős oxidálószer, az elemek közül csak a fluor elektronegativitása nagyobb.[5] Az oxigén – tömegre vetítve – a világegyetem harmadik leggyakoribb eleme a hidrogén és a hélium után;[6] egyben a Föld leggyakoribb eleme is, hiszen a földkéreg tömegének majdnem felét oxigén teszi ki (természetesen kötött állapotban).[7] Az oxigén kémiailag túl reaktív ahhoz, hogy hosszabb ideig elemi formában megmaradjon a légkörben. Az élő szervezetek fotoszintézise – melynek során a napfény energiájának felhasználásával vízből elemi oxigént állítanak elő – biztosítja folyamatos utánpótlását. A szabad, elemi oxigén mintegy 2,5 milliárd évvel ezelőtt kezdett felhalmozódni a légkörben (nagy oxigenizációs esemény) körülbelül egymilliárd évvel ezen organizmusok első megjelenése után.[8] A kétatomos oxigéngáz a levegő térfogatának 20,8%-át alkotja.[9]
Az élőlények tömegének legnagyobb részét az oxigén képezi, mert azok fő alkotóeleme a víz (például az emberi testtömeg körülbelül kétharmada).[10] Az oxigén megtalálható az élő szervezetekben előforduló számos fontos szerves kémiai vegyületcsoportban – mint például a fehérjék, nukleinsavak, szénhidrátok, és zsírok –, akárcsak a jelentős szervetlen vegyületekben, amelyek az állati fogakat, csontokat, héjakat, páncélokat alkotják. A cianobaktériumok, algák és növények által termelt elemi oxigént minden bonyolult élet a sejtlégzéskor használja fel. Az oxigén mérgező a szigorúan anaerob szervezetek számára, melyek a korai élet domináns formái voltak a Földön, amíg az O2 el nem kezdett felhalmozódni a légkörben. Az oxigén allotrop módosulata, az ózon (O3), jelentős mértékben elnyeli az UV-B sugárzást, így a nagy magasságban kialakult ózonréteg megvédi a bioszférát az ultraibolya sugárzás káros hatásaitól. Az ózon ugyanakkor a felszín közelében a szmog melléktermékeként kialakuló szennyezőanyag. Ennél nagyobb magasságban, alacsony Föld körüli pályán az atomos oxigén jelentős mennyiségben van jelen, ez okozza az űrjárművek erózióját.[11]
Az oxigént egymástól függetlenül fedezte fel Carl Wilhelm Scheele 1773-ban (vagy korábban) Uppsalában; illetve Joseph Priestley 1774-ben Wiltshire-ben; mivel azonban Priestley munkája előbb jelent meg, gyakran neki tulajdonítják az elsőséget. Az oxigén nevet Antoine Laurent de Lavoisier francia kémikus alkotta meg 1777-ben,[12] akinek az elemmel elvégzett kísérletei hozzájárultak az égés és korrózió akkoriban népszerű flogisztonelméletének megcáfolásában. Az oxigént az iparban cseppfolyósított levegő szakaszos lepárlásával; víz elektrolízisével; illetve zeolitok és nyomás adszorpció (pressure swing adsorption) alkalmazásával állítják elő. Az oxigént számos területen alkalmazzák, beleértve a műanyag-, textil- és acélgyártást; az acél és más fémek forrasztását, hegesztését és vágását; a rakéta-hajtóanyagot; az oxigénterápiát; illetve a repülőgépek, tengeralattjárók, az űrrepülés és a búvárkodás létfenntartó rendszereit.
Standard hőmérsékleten és nyomáson az oxigén színtelen, szagtalan gáz. Molekulaképlete O2, melyben a két oxigénatom triplett spinű elektronkonfigurációban kapcsolódik egymáshoz. Ennek a kötésnek a kötésrendje 2, de gyakran egyszerűen csak kettős kötésként[13] vagy egy kételektronos és két háromelektronos kötés kombinációjaként hivatkoznak rá.[14]

A triplett oxigén (nem tévesztendő össze az O3 vegyképletű ózonnal) az alapállapotú dioxigén molekula.[15] A molekula elektronszerkezete két párosítatlan elektront tartalmaz, amelyek két degenerált molekulapályán találhatóak.[m 1] Ezek a molekulapályák lazítónak minősülnek (a kötésrendet háromról kettőre csökkentik); így a kétatomos oxigén kötése gyengébb, mint a kétatomos nitrogén hármas kötése.[15]
Normál triplett állapotban a dioxigénmolekula paramágneses, azaz a párosítatlan elektronok spinjének mágneses momentuma és a szomszédos molekulák közötti negatív kicserélődési energia miatt az oxigén mágneses mező jelenlétében mágnest alkot.[16] A folyékony oxigén olyan mértékben vonzódik a mágneshez, hogy laboratóriumi bemutatók során egy erős mágnes pólusai között kialakult folyékony oxigénhíd akár még saját súlyát is képes lehet megtartani.[17][m 2]
A szingulett oxigén több, nagyobb energiájú (gerjesztett állapotú) molekuláris oxigén fajtát takar, amelyekben az összes elektronspin párosított. Sokkal reakcióképesebb a szerves molekulákkal szemben, mint önmagában a közönséges dioxigén. A természetben a szingulett oxigén általában vízből, fotoszintézis során keletkezik, a napfény energiájának felhasználásával.[19] A troposzférában az ózon fotolízise által keletkezik, rövid hullámhosszú fény hatására;[20] valamint az immunrendszer is előállítja mint aktív oxigénforrás.[21] A fotoszintetizáló organizmusokban (és esetleg még az állatokban) található karotinoidok fontos szerepet játszanak a szingulett oxigén energiájának elnyelésében, és gerjesztetlen alapállapotúvá alakításában, még mielőtt az kárt okozhatna a szövetekben.[22]
Az elemi oxigén leggyakoribb allotrop módosulata a Földön az O2 vegyképletű dioxigén. Ebben a molekulában a kötés hossza 121 pm, a kötés energiája pedig 498 kJ·mol−1.[23] Ez az oxigén azon formája, melyet a komplex élet a sejtlégzés során hasznosítani tud, illetve amely a Föld légkörének jelentős részét teszi ki.

A trioxigén (O3) vagy ismertebb nevén ózon, az oxigén egy nagyon reaktív allotrópja, amely károsítja a tüdőszöveteket.[24] Az ózon a felső légkörben keletkezik, amikor az O2 atomos oxigénnel egyesül; ez utóbbi a kétatomos oxigénmolekula ultraibolya (UV) sugárzás általi felhasítása révén jön létre.[12] Mivel az ózon jól elnyeli az elektromágneses sugárzás UV tartományba eső részét, ezért a földi felső légkör ózonrétege mintegy védőpajzsként szolgál e sugárzással szemben.[12] Közel a Föld felszínéhez azonban az ózon szennyezőanyag, amely a gépjárművek kipufogógázainak melléktermékeként alakul ki.[24] A metastabil tetraoxigén (O4) molekulát 2001-ben fedezték fel,[25][26] és azt feltételezték, hogy a szilárd oxigén hat fázisának egyikében létezik. 2006-ban igazolták, hogy ez a 20 GPa nyomáson létrejövő fázis valójában romboéderes O8 klaszter.[27] Ez a klaszter potenciálisan sokkal erősebb oxidálószer, mint akár az O2, akár az O3, ezért felhasználható lehet rakéta-hajtóanyagban.[25][26] Fémes fázisát 1990-ben fedezték fel, amikor szilárd oxigént 96 GPa feletti nyomásnak tettek ki,[28] 1998-ban pedig kimutatták, hogy ez a fázis nagyon alacsony hőmérsékleten szupravezetővé válik.[29]
Az oxigén apoláris tulajdonsága miatt a vízben rosszul, bár a nitrogénnél jobban oldódik. A levegővel egyensúlyi állapotban levő vízben két oldott N2-molekulára körülbelül egy O2-molekula jut, szemben a légköri mintegy 4:1-es aránnyal. Az oxigén vízoldhatósága hőmérsékletfüggő, 0 °C-on körülbelül kétszer annyi (14,6 mg/l), mint 20 °C-on (7,6 mg/l).[30][31] 25 °C-on, normál légköri nyomáson (101,3 kPa) az édesvíz literenként körülbelül 6,04 milliliter; míg a tengervíz literenként körülbelül 4,95 milliliter oxigént tartalmaz.[32] 5 °C-on az oldhatóság édesvíz esetében 9,0 milliliterre; tengervíz esetében 7,2 milliliterre emelkedik literenként.

Az oxigén −182,95 °C-on (90,20 K) lecsapódik, és −218,79 °C-on (54,36 K) megfagy.[33] Folyékony és szilárd halmazállapotban is tiszta, halvány égkék színű anyag; színét a vörös tartományba eső fény abszorpciója okozza (ellentétben az ég kékjével, melynek oka a kék fény Rayleigh-szórása). Nagy tisztaságú folyékony oxigént általában cseppfolyósított levegő szakaszos lepárlásával (frakcionált desztilláció) állítanak elő.[34] Folyékony oxigént a levegőből történő kondenzálásával is elő lehet állítani, ehhez folyékony nitrogén hűtőközeget használnak. A cseppfolyós oxigén rendkívül reakcióképes anyag, gyúlékony anyagoktól el kell különíteni.[35]
Az oxigén szobahőmérsékleten kevéssé reakcióképes, magasabb hőmérsékleten azonban csaknem minden elemmel egyesül. Szobahőmérsékleten is képes oxidálni elemeket, magas hőmérsékleten exoterm reakcióban egyesül velük (égés). Erős oxidálószer, az oxidáció a vele kapcsolatos megfigyelések folyományaként kapta a nevét. Apoláris oldószerekben jól oldódik. Az egyatomos oxigén (mint minden naszcensz atom) annyira reagens, hogy a természetben csak nagyon rövid ideig létezik (jelölése 'O').
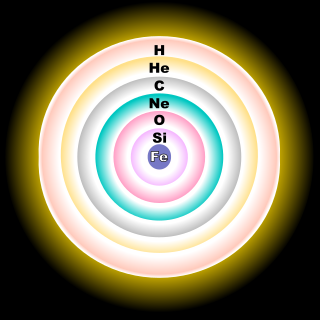
A természetben előforduló oxigén három stabil izotópból áll: 16O, 17O és 18O; melyek közül a leggyakoribb az oxigén-16 (természetes előfordulása 99,762%).[36] A legtöbb oxigén-16 a nagyobb tömegű csillagokban, a hélium fúzió (háromalfa-ciklus) végén szintetizálódik, de valamennyi a neon-égési folyamat során is keletkezik.[37] Az oxigén-17 izotóp elsősorban a CNO-ciklus során keletkezik, amelyben a hidrogén héliummá ég el; így gyakori izotóp a csillagok hidrogén-zónájában.[37] Az oxigén-18 legnagyobb részben akkor keletkezik, amikor a CNO-ciklusban létrejött 14N befogja a 4He atommagot. Emiatt az oxigén-18 a fejlett, nagy tömegű csillagok héliumban gazdag zónáiban gyakori izotóp.[37]
Az oxigén tizennégy radioizotópja ismert. 122,24 másodperc felezési idővel a legstabilabb az oxigén-15, őt követi az oxigén-14, melynek felezési ideje 70,606 s.[36] Az összes többi radioaktív izotóp felezési ideje kevesebb, mint 27 s; de a többségre elmondható, hogy 83 ms-nél is rövidebb.[36] Az 16O-nál könnyebb radioizotópok leggyakoribb bomlási módja a β+ bomlás,[38][39][40] amely nitrogént eredményez; a 18O-nál nehezebb izotópok béta-bomlása fluor keletkezéséhez vezet.[36]
Az oxigén a földi bioszféra; a légkör, a tengerek és a szárazföldek tömegének leggyakoribb kémiai eleme. A hidrogén és a hélium után az oxigén a harmadik leggyakoribb elem az univerzumban.[6] A Nap tömegének körülbelül 0,9%-át oxigén alkotja.[9] A földkéreg tömegének 49,2%-a oxigén,[7] és a fő alkotóeleme a világ óceánjainak (88,8 tömegszázalék); mind kötött, mind szabad állapotban előfordul.[9] Az oxigéngáz a Föld légkörének második leggyakoribb eleme (20,8 térfogatszázalék), tömege mintegy 1015 tonna (23,1 tömegszázalék).[9][42][m 3] A Föld szokatlan a Naprendszer bolygói között abban a tekintetben, hogy a légkörben ilyen nagy mennyiségben található meg az oxigéngáz: a marsi (0,1 térfogatszázalék) és vénuszi légkör jóval alacsonyabb koncentrációban tartalmazza. A környező bolygókon azonban az O2 kizárólag az oxigéntartalmú molekulák (például szén-dioxid) ultraibolya sugárzás hatására történő felhasadása révén jön létre.

A szokatlanul magas oxigénkoncentráció a Földön az oxigénciklus eredménye. Ez a biogeokémiai ciklus írja le az oxigén mozgását annak három fő tározója közt a Földön: a légkör, a bioszféra és a litoszféra. Az oxigén ciklus legfőbb tényezője a fotoszintézis, amely a Föld mai légköréért is felelős. A fotoszintézis ugyanis oxigént szabadít fel, amely a légkörbe kerül; ezzel szemben a biológiai oxidáció (légzés) és az élőlények pusztulása (bomlás) révén kikerül onnan. A jelenlegi egyensúlyi állapotban az oxigéntermelés és -fogyasztás azonos mértékű, évente körülbelül a teljes légköri oxigén mennyiségének kétezred részét teszi ki.
A világ víztesteiben oldott állapotú szabad oxigén is előfordul. Az O2 alacsonyabb hőmérsékleten megnövekvő oldhatósága fontos következményekkel jár a tengeri életre nézve, a magasabb oxigéntartalom miatt a poláris óceánokban az élet sokkal gazdagabb és sokszínűbb.[43] Ezért (is) okoz komoly problémát, ha kőolaj kerül a víz felszínére, az ugyanis filmréteget képezve elzárja az oxigént a víztől, így az képtelen abban oldódni. A már oldott oxigén ugyanakkor „átvándorol” az olajba, ezzel tovább csökkentve a vízben oldott oxigén mennyiségét. A növényi tápanyagokkal – mint például nitrátokkal és foszfátokkal – szennyezett vizekben az eutrofizációnak nevezett folyamat fokozza az algák növekedését; ezen szervezetek, illetve más bioanyagok lebomlása pedig csökkenthetik az eutróf vizekben oldott oxigén mennyiségét. Ezen okból kifolyólag a tudósok a vízminőség mérésére a víz biokémiai oxigénigényét, vagy a normál koncentráció visszaállításához szükséges oxigén mennyiséget használják.[44]
A természetben, a szabad oxigén a fotoszintézis – a víz fényenergia hatására való elbontása – során keletkezik. Egyes becslések szerint, a tengerekben élő zöldmoszatok és cianobaktériumok állítják elő a Földön található szabad oxigén mintegy 70%-át, és csupán a többit termelik meg a szárazföldi növények.[45] A különböző becslések az atmoszférikus oxigénhez való óceáni hozzájárulás mértékét magasabbra, mások alacsonyabbra teszik; összességében azt sejtetve, hogy az óceánok a légköri oxigén 45%-át termelik meg évente.[46] A fotoszintézis folyamatának egyszerűsített képlete:[47]
vagy egyszerűbben:
A fotolitikus oxigén-fejlődés a fotoszintetizáló szervezetek tilakoid membránjában következik be, és négy fotonnyi energiát igényel.[m 4] A folyamat sok lépésből áll, végeredményben proton átmenet keletkezik az egész tilakoid membránon, amely a fotofoszforiláció során adenozin-trifoszfátot (ATP) szintetizál.[48] A vízmolekula oxidációja után hátramaradt dioxigén ezután a légkörbe távozik.[m 5] A molekuláris dioxigén (O2) az összes aerob szervezet sejtlégzéséhez elengedhetetlen. Az oxigén a mitokondriumban hasznosítódik: az oxidatív foszforiláció során segíti az ATP keletkezését. Az aerob légzés folyamata lényegében fordított fotoszintézis, egyszerűsített felírással:
A gerincesekben az oxigén átdiffundál a membránon keresztül a tüdőbe, majd a vörösvérsejtekbe. Itt a hemoglobin megköti a dioxigént, ezzel a színét kékesvörösről világosvörössé változtatva.[24] (A hemoglobin más részén a Bohr-effektus révén szén-dioxid szabadul fel). Más állatok hemocianint (puhatestűek és néhány ízeltlábú), vagy hemeritrint (pókok és homárok) használnak.[42] Egy liter vér 200 cm³ O2-t képes feloldani.[42] A reaktív oxigénszármazékok, mint például a szuperoxid-anion (O2•-) és a hidrogén-peroxid (H2O2), az organizmusok oxigén-felhasználásának veszélyes melléktermékei.[42] A magasabb rendű szervezetek immunrendszereinek bizonyos részei azonban létrehozhatnak peroxidot, szuperoxidot és szingulett oxigént, hogy elpusztítsák a támadó mikrobákat. Ezek a gyökök szintén fontos szerepet játszanak a növények kórokozó-támadásra adott hiperszenzitív válaszában.[48]
Az oxigén parciális nyomása egy élő gerinces szervezetében a légzőrendszerben a legmagasabb, majd az artériák, a perifériás szövetek és a vénák mentén haladva egyre csökken. Az oxigén parciális nyomása, az a nyomás, amely akkor lenne, ha egyedül töltené ki a rendelkezésre álló teret.[52]
Egy nyugalmi állapotban lévő felnőtt ember 1,8-2,4 gramm oxigént lélegez be percenként.[53] Ez a teljes emberiségre vetítve évente több mint 6 milliárd tonna belélegzett oxigént jelent.[m 6]

A szabad oxigéngáz szinte nem is létezett a Föld légkörében a fotoszintetikus archeák és baktériumok 3,5 milliárd évvel ezelőtti kifejlődését megelőzően. Az oxigén jelentősebb mennyiségben először a paleoproterozoikum eon (2,5 és 1,6 milliárd évvel ezelőtt) idején jelent meg. Az első egymilliárd évben, minden oxigén, amelyet ezen organizmusok termeltek egyesült az óceánokban oldott vassal; sávos vas formációkat (üledékes kőzet) hozva létre. Amikor 2,7 milliárd évvel ezelőtt az ilyen oxigén-elnyelők telítetté váltak, az oxigén kilépett az óceánokból, és mintegy 1,7 milliárd évvel ezelőtt elérte a jelenlegi szint 10%-át.[54]
A nagy mennyiségű oldott és szabad oxigén jelenléte az óceánokban és a légkörben, a legtöbb anaerob organizmust kipusztította a mintegy 2,4 milliárd évvel ezelőtti nagy oxigenizációs esemény (oxigénkatasztrófa) folyamán. Ugyanakkor, lehetővé tette a O2-t sejtlégzésre használó aerob organizmusok számára, hogy sokkal több ATP-t állítsanak elő; ezzel elősegítette, hogy azok uralják a földi bioszférát.[55]
A kambrium időszak 540 millió évvel ezelőtti kezdete óta, az O2-szint 15 és 30 térfogatszázalék között ingadozott.[56] A légköri oxigén szintje a karbon korszak vége felé (mintegy 300 millió évvel ezelőtt) érte el maximumát 35 térfogatszázalékkal;[56] amely jelentősen hozzájárulhatott a nagy számú rovarhoz és kétéltűhöz ebben az időben.[57] Az emberi tevékenység, beleértve az évi 7 milliárd tonna fosszilis tüzelőanyag elégetését, nagyon kevés hatással van a légköri oxigén mennyiségére.[16] A jelenlegi ütem mellett a fotoszintézis körülbelül 2000 év alatt újítja meg a teljes légköri O2-mennyiséget.[58]
Az egyik legkorábbi, az égés és a levegő kapcsolatát vizsgáló kísérletet Bizánci Philón görög mérnök végezte el az i. e. 2. században. A Pneumatica című munkájában leírt kísérletében Philón egy égő gyertyát egy másik edénnyel takart le, és a nyakát vízzel vette körbe. Megfigyelte, hogy a víz kismértékben felemelkedett az edény nyakában.[59] Philón tévesen azt gondolta, hogy az edényben lévő levegő egy része átalakult a klasszikus tűz elemmé, és így képes volt kijutni az üveg pórusain. Sok évszázaddal később Leonardo da Vinci vitte tovább Philón munkáját megfigyelve, hogy a levegő egy része felhasználódik az égés és a légzés során.[60]
A 17. század végén Robert Boyle arra a következtetésre jutott, hogy a levegő az égés egyik feltétele. John Mayow (1641–1679) angol kémikus tovább finomította Boyle munkáját azzal, hogy megmutatta, a tűz csak a levegő egy részét használja fel, melyet ő spiritus nitroaereusnak vagy csak nitroaereusnak nevezett.[61] Kísérletében azt találta, hogy egy egeret vagy egy égő gyertyát a zárt edény alá helyezve a víz megemelkedett, és a levegő eredeti térfogatának 14 százalékát töltötte ki, mielőtt a vizsgált tárgyak elenyésztek.[62] Ebből arra a feltételezésre jutott, hogy mind a légzés, mind az égés nitroaereust fogyaszt.
Mayow megfigyelte, hogy az antimon súlya hevítés hatására megnő; ebből arra következtetett, hogy a nitroaereus egyesül azzal.[61] Arra is rájött, hogy a tüdő elválasztja a nitroaereust a levegőtől, és átadja azt a vérnek; illetve, hogy az állati hő- és izommozgás a nitroaereus és a szervezetben lévő más anyagok reakciójából ered.[61] Ezeket, illetve más elvégzett kísérleteit és gondolatait 1668-ban, Tractatus duo című munkájának De respiratione fejezetében publikálta.[62]

Robert Hooke, Ole Borch, Mihail Lomonoszov és Pierre Bayen valamennyien előállították az oxigént a 17. és a 18. századi kísérleteikben, de egyikük sem ismerte fel, hogy az egy új kémiai elem.[30] Ez részben az égés és a korrózió úgynevezett flogisztonelméletének is köszönhető, amely igen népszerű volt abban az időben.
A Johann Joachim Becher német alkimista által 1667-ben felállított, és a Georg Ernst Stahl kémikus által 1731-ben módosított flogisztonelmélet azt állította, hogy minden éghető anyag két részből áll.[63] Az egyik rész, az úgynevezett flogiszton, az égés során távozott az anyagból; míg a másik, flogisztontartalmától megfosztott részről azt gondolták, hogy az az anyag igazi formája, vagy más néven calx.[60]
A jól égő, és kevés maradékot (hamut) hagyó anyagokról, mint például a fáról vagy a szénről, azt gondolták, hogy nagyrészt flogisztonból épülnek fel; míg a nem éghető, korrodálódó anyagok, mint a vas, csak kis részben tartalmazzák. A levegő nem játszott szerepet a flogisztonelméletben, és nem történtek kezdetleges, mennyiségi kísérletek sem az elmélet igazolására. Ehelyett, az elméletet arra alapozták, hogy mi történik ha valami elég; és megállapították, hogy a hétköznapi tárgyak az elégetés hatására könnyebbnek tűnnek, mintha elveszítenének valamit a folyamatban.[60] Azt a tényt, hogy az elégett anyag, például a fa tömege megnő az égés során, a gáznemű égéstermékek felhajtóereje elrejtette. A fémek voltak az első nyomai a flogisztonelmélet hibás mivoltának, ugyanis tömegük a rozsdásodás hatására megnőtt, habár az elmélet szerint azok is flogisztont veszítettek.


Az oxigént a svéd gyógyszerész, Carl Wilhelm Scheele fedezte fel. Higany-oxid és a különböző nitrátok hevítésével 1772-ben sikerült oxigéngázt előállítania.[9][60] Scheele tüzes levegőnek nevezte el a gázt, mert ez volt az égés egyetlen ismert támogatója. Felfedezéséről Értekezés a levegőről és a tűzről címmel beszámolót is írt, és 1775-ben elküldte kéziratát a kiadónak. Ugyanakkor, a dokumentumot 1777-ig nem publikálták.[64]
Időközben, 1774. augusztus 1-jén, a brit lelkész Joseph Priestley is elvégzett egy kísérletet: a Nap fényét üvegcsőben elhelyezett higany-oxidra (HgO) fókuszálta, amely gázt szabadított fel; ezt a gázt Priestley deflogisztonizált levegőnek nevezte el.[9] Felfedezte, hogy a gyertyák fényesebb lánggal égnek benne, illetve az egér aktívabb volt és tovább élt, ha belélegezte a gázt. Miután ő maga is belélegezte, ezt írta: „A tüdőm nem érzett különbséget a közönséges levegőtől, de úgy emlékszem, hogy utána egy ideig különösen könnyednek éreztem a mellkasom.”[30][65] Priestley 1775-ben publikálta felfedezéseit Beszámoló további felfedezésekről a levegővel (An Account of Further Discoveries in Air) című tanulmányában; amely a Kísérletek és megfigyelések különböző levegőkkel című könyvének második kötetében volt olvasható.[60][66] Mivel előbb publikálta eredményeit, általában Priestley-nek tulajdonítják a felfedezés elsőségét.
A neves francia kémikus, Antoine Laurent Lavoisier később azt állította, hogy az új anyagot önállóan fedezte fel. Priestley azonban 1774 októberében meglátogatta, és elmondta neki a kísérletét, és miképp szabadította fel az új gázt. Scheele is írt egy levelet Lavoisier-nek 1774. szeptember 30-án, melyben leírta a korábban ismeretlen anyag felfedezését, de Lavoisier sosem ismerte el, hogy megkapta azt (a levél másolatát Scheele ingóságai között találták meg halála után).[64]

Amit Lavoisier kétségkívül megtett (bár azt abban az időben még vitatták), az az oxidáció első, megfelelő mennyiségi kísérletének elvégzése volt; illetve elsőként magyarázta meg helyesen az égés folyamatát.[9] 1774-től kezdődően elvégezte ezeket, illetve más hasonló kísérleteket; hogy megcáfolja a flogisztonelméletet és bebizonyítsa, hogy a Priestley és Scheele által felfedezett anyag egy új kémiai elem.
Az egyik kísérletben Lavoisier megfigyelte, hogy amikor ónt és levegőt hevített egy zárt tartályban, összességében nem volt súlygyarapodás.[9] A tartály felnyitásakor azt tapasztalta, hogy kívülről levegő áramlott be; ami azt jelezte, hogy a tartályban lévő levegő egy része elhasználódott. Azt is megfigyelte továbbá, hogy az ón tömege megnőtt; méghozzá pontosan a beáramolt levegő tömegével azonos mértékben. Ezt, és az égéssel kapcsolatos más kísérleteit a Sur la combustion en général című könyvében dokumentálta, melyet 1777-ben publikáltak.[9] Ebben a művében azt bizonyította, hogy a levegő két gáz keverékéből áll: a létfontosságú (vital) levegőből, amely elengedhetetlen az égéshez és a légzéshez; illetve az azótból (görög: ἄζωτον "élettelen"), amelyik egyiket sem táplálta. Az azót ma magyarul a nitrogén néven ismert elem, de franciául és néhány európai nyelven még mindig így hívják.[9]
Lavoisier 1777-ben átnevezte a létfontosságú (vital) levegőt a görög eredetű – az ὀξύς (oxys) ’sav’ és -γενής (-genēs) ’nemző, képző’ szavak összetételéből származó – oxygène-re, mert tévesen azt hitte, hogy az oxigén minden sav alkotóeleme.[12] A kémikusok (nevezetesen Sir Humphry Davy 1812-ben) végül bebizonyították, hogy Lavoisier tévedett ebben a tekintetben (a sav-bázis kémia sarokköve ugyanis a hidrogén-ion), de ekkor már túl késő volt.

John Dalton eredeti atomhipotézise azt feltételezte, hogy minden elem monoatomikus, és hogy a vegyületekben lévő atomok a legegyszerűbben aránylanak egymáshoz. Például Dalton azt gondolta, hogy a víz képlete HO, így az oxigén atomtömege nyolcszorosa a hidrogénének, szemben a mai 16-szoros értékkel.[67] 1805-ben Joseph Louis Gay-Lussac és Alexander von Humboldt megmutatta, hogy a víz két térfogatrész hidrogénből és egy térfogatrész oxigénből áll; 1811-ben pedig Amedeo Avogadro megadta a víz összetételének helyes értelmezését, a később róla elnevezett Avogadro-törvény és a kétatomos molekulák létezésének feltételezése alapján.[68][m 7]
A 19. század végére a tudósok felismerték, hogy a levegő cseppfolyósítható és az összetevői szétválaszthatók, ha a levegőt komprimálják (összenyomják), és lehűtik. A svájci kémikus és fizikus, Raoul Pictet Pierre kaszkád módszer alkalmazásával folyékony kén-dioxidot párologtatott el annak érdekében, hogy így folyékony szén-dioxidot állítson elő, amit aztán szintén elpárologtatott, hogy kellően le tudja hűteni az oxigéngázt a cseppfolyósodáshoz. 1877. december 22-én táviratot küldött a párizsi Francia Tudományos Akadémiának, hogy bejelentse a folyékony oxigén felfedezését.[69] Mindössze két napra rá, Louis Paul Cailletet francia fizikus is bejelentette saját módszerét a folyékony molekuláris oxigén előállítására.[69] Mindkét esetben csupán néhány cseppnyi folyadékot sikerült előállítani, így értelmes elemzést nem lehetett elvégezni. Stabil állapotú folyékony oxigént először a lengyel Jagelló Egyetem tudósainak (Zygmunt Wróblewski és Karol Olszewski) sikerült előállítania 1883. március 29-én.[70]
1891-ben James Dewar skót vegyész képes volt a tanulmányozáshoz elegendő mennyiségű folyékony oxigént előállítani.[16] Az első kereskedelmileg is életképes folyékonyoxigén-előállító eljárást 1895-ben egymástól függetlenül fejlesztette ki Carl von Linde német és William Hampson brit mérnök. Mindketten addig csökkentették a levegő hőmérsékletét, amíg az folyékonnyá nem kondenzálódott; majd az összetevő gázokat egyesével felforralva desztillációval különválasztották.[71] Később, 1901-ben bemutatták az oxiacetilén hegesztést, amelyben sűrített O2-t és acetilént kevertek és égettek el. Ez a hegesztési, illetve lemezvágási eljárás később széles körben elterjedt.[71]
1923-ban Robert H. Goddard amerikai tudós lett az első ember akinek sikerült rakétahajtóművet építenie. A hajtóműve benzint használt tüzelőanyagként, és folyékony oxigént oxidálószerként. Goddard sikeresen lőtt fel egy kis folyékony üzemanyagú rakétát 1926. március 16-án a massachusettsi Auburnban 56 m magasra, 97 km/h sebességgel.[71][72]

Az iparban évente 100 millió tonna oxigént állítanak elő a levegőből, melynek két fő eljárása ismert.[64] A leggyakoribb eljárás a levegő szakaszos lepárlása (frakcionált desztilláció) alkotóelemeire, amely során az oxigén folyékony, a nitrogén gőzállapotú.[64]
A másik eljárás, tiszta, száraz levegő zeolit molekuláris szűrőágy-pár egyikén való átáramoltatása, amely elnyeli a nitrogént, és a kiáramló gáz 90-93% oxigéntartalmú.[64] Ezzel párhuzamosan a másik, nitrogénnel telített zeolit ágyban lecsökkentik a kamra üzemi nyomását, illetve fordított irányban átáramoltatják rajta az oxigéngáz áram egy elterelt részét; így a kamrában nitrogéngáz szabadul fel. Adott idő elteltével a kamrák szerepe felcserélődik, így a vezetékekben folyamatos oxigéngáz áramlás tartható fenn. Ez az úgynevezett adszorpciós nyomásfordítás (pressure swing adsorption, PSA). Az oxigéngázt egyre inkább ezekkel a nem-kriogén technológiákkal állítják elő.[73]
Az oxigéngáz víz elektrolízisével is előállítható, mely során a víz molekuláris oxigénre és hidrogénre bomlik. Az elektrolízis során az elektródákra egyenáramot kapcsolnak. Váltóáram esetén mindkét oldali kémcsőben a hidrogén és oxigén robbanásveszélyes 2:1 arányú elegye keletkezik, mivel az anód és a katód a váltóáram frekvenciájának megfelelően folyamatosan felcserélődik. A közhiedelemmel ellentétben, az egyenáramú elektrolízis során tapasztalható 2:1-es arány nem bizonyítja a víz H2O vegyképletét, kivéve, ha élünk bizonyos feltételezésekkel a hidrogén és az oxigén formulájáról magáról. Hasonló módszer az oxidok és oxosavak elektrokatalitikus O2-evolúciója. Természetesen kémiai katalizátorok is használhatóak, mint például a kémiai oxigén generátor vagy az oxigéngyertya, amelyeket a tengeralattjárók létfenntartó rendszerébe építenek be, illetve alapfelszereltségként alkalmazzák a kereskedelmi repülőgépjáratokon dekompressziós vészhelyzet esetén. További levegő-szeparációs technológia a levegő nagy nyomás hatására, vagy elektromos áram révén kényszerített feloldása cirkónium-dioxidból készült kerámia membránokban, amely során csaknem tiszta oxigéngáz termelődik.[44]
A folyékony oxigén ára nagy mennyiségben, 2001-ben körülbelül 0,21 dollár/kg (47,8 Ft/kg) volt.[74][m 8] Mivel az elsődleges termelési költség a levegő cseppfolyósításának energiaköltsége, a termelési költségek az adott terület energiaárai alapján változnak.
Gazdasági okokból az oxigént gyakran cseppfolyós állapotban, speciálisan szigetelt tankerekben szállítják, mivel egy liter cseppfolyós oxigén légköri nyomáson és 20 °C-on 840 liter oxigéngázzal egyenértékű.[64] Az ilyen tankerekkel töltik fel a kórházak és egyéb nagy mennyiségű tiszta oxigéngázt felhasználó intézmények oxigéntároló tartályait, amelyekből a folyékony oxigén hőcserélőkön keresztül áramolva, csak gázhalmazállapotban jut be az épületbe. A sűrített oxigéngázt ugyanakkor nagynyomású, kék színű acélpalackokba is kitöltik és szállítják, ez bizonyos hordozható orvosi eszközökhöz, hegesztéshez és lemezvágáshoz előnyös kiszerelési forma.[64] A palack kezelése rendkívüli elővigyázatosságot igényel a nagy fokú robbanásveszély miatt.

A légzés alapvető célja az oxigén felvétele a levegőből, így az oxigénpótlást a gyógyászatban is használják. A kezelés nemcsak megnöveli a beteg vérében lévő oxigén szintjét, de megvan az a másodlagos hatása, hogy számos tüdőbetegség esetén csökkenti a vér áramlási ellenállását, így könnyít a szív terhelésén. Az oxigénterápiát használják a tüdőtágulat (emphysema), a tüdőgyulladás, bizonyos szívbetegségek (pangásos szívelégtelenség) kezelésére; illetve minden olyan betegségnél és rendellenességnél, amely a tüdőartéria fokozott vérnyomásával jár együtt, vagy rontja a szervezet oxigénfelvevő képességét.[75]
A kezelés elég rugalmas ahhoz, hogy ne csak a kórházakban alkalmazzák, de akár a beteg otthonában, vagy egyre inkább hordozható eszközök segítségével. Régebben elterjedt volt az oxigénsátor alkalmazása, de mára szinte teljesen felváltotta az oxigénmaszk és a nazális kanül.[76]
A hiperbár (nagynyomású) gyógyászat speciális oxigénkamrát használ, hogy megnövelje az oxigén parciális nyomását a páciens – és ha szükséges – az orvosi személyzet körül.[77] A szén-monoxid-mérgezés, a gázgangréna (sercegő üszök) és a dekompressziós betegség kezelhető a segítségével.[78] A megnövelt O2-koncentráció a tüdőben segít kiszorítani a szén-monoxidot a hemoglobin hem csoportjából.[79][80] Az oxigéngáz mérgező a gázgangrénát okozó anaerob baktériumok számára, így a parciális nyomás megemelése segít megölni őket.[81][82] A dekompressziós betegség túl gyorsan emelkedő búvárok esetében fordul elő, akik vérében inert gázbuborékok – főleg nitrogén és hélium – keletkezik. A kezelés része az oxigén nyomásának minél hamarabbi megnövelése.[75][83][84]
Oxigént használnak azoknál a betegeknél is, akiknél gépi lélegeztetés szükséges; gyakran a környezeti levegő 21%-os koncentrációját meghaladó mértékben.

Az oxigéngáz figyelemre méltó alkalmazási területe a modern űrruha, amely körülöleli a viselő testét a kis nyomású gázzal. Egyes űrruhákban csaknem tiszta oxigént alkalmaznak, melynek nyomása körülbelül egyharmada a normál légköri nyomásnak, így tartva fenn az oxigén normális parciális nyomását a vérben.[85][86] A nagy nyomásról kis nyomásra való átváltás azért volt szükséges, hogy továbbra is megfelelően rugalmas és hajlékony ruhákat lehessen készíteni.
A búvárok és a tengeralattjárón szolgáló tengerészek is mesterségesen szállított oxigénre támaszkodnak, de a leggyakrabban normál nyomást vagy levegő és oxigén keverékét használják. A tiszta vagy majdnem tiszta oxigén használata a búvárkodásban az újralégző készülékre; illetve a dekompresszió, vagy sekély mélységű (~6 méter mély, vagy kevesebb) sürgősségi kezelésre korlátozódik.[87][88] Ennél mélyebbre merüléskor az oxigént más gázokkal – nitrogénnel vagy héliummal – jelentősen hígítani kell, hogy elkerüljék az oxigénmérgezést.[87]
A hegymászók és a nem túlnyomásos merevszárnyú repülőgéppel repülők gyakran visznek magukkal kiegészítő oxigént.[m 9] A kereskedelmi (túlnyomásos) repülőgépekkel utazók vészhelyzeti oxigén tartalékkal rendelkeznek, amelyet az utastér nyomáscsökkenése esetén automatikusan megkapnak. A hirtelen nyomáscsökkenés aktiválja az egyes ülések fölötti kémiai oxigén generátorokat, és az oxigénmaszkok leesnek. A maszkok felvétele – a biztonsági előírásoknak megfelelően – a tartály belsejében lévő vasreszeléket a nátrium-klorátba kényszeríti, ezzel az exoterm reakció révén folyamatos oxigéngáz áramlás indul meg.[44]
Az oxigénnek, mint feltételezhetően enyhe euforikus hatású gáznak, nagy múltja van a rekreációs felhasználását illetően az oxigénbárokban és a sportban. Az ilyen oxigénbárok az 1990-es évektől kezdődően megtalálhatóak Japánban, Kaliforniában, és a nevadai Las Vegas völgyben, amelyek térítés ellenében a szokásosnál nagyobb oxigénmennyiséget kínálnak belélegzésre.[89] A profi sportolók, különösen az amerikaifutballban a play-ek között időnként elhagyják a pályát, hogy oxigén maszkot viseljenek, és növeljék teljesítményüket. Ezen technikák farmakológiai hatása kétséges, a placebo hatás sokkal valószínűbb magyarázat.[89] A rendelkezésre álló tanulmányok alátámasztják a dúsított O2-keverék teljesítménynövelő hatását, de csak akkor, ha azt a testmozgás alatt lélegezték be.[90]
Az oxigén további felhasználási területe lehet a pirotechnika, többek között George H. Goble öt másodperces barbecue grillsütése (folyékony oxigén felhasználásával).[91]

A vasérc acéllá alakítása használja fel a kereskedelmileg előállított oxigén 55%-át.[44] Ez az eljárás az úgynevezett LD-konverteres eljárás, amely során a konverterben felhevített, olvadt nyersvasra egy felülről beengedett oxigénlándzsán keresztül nagy sebességgel oxigéngázt fújnak be. Az oxigén kiégeti a nyersvasban lévő kén szennyeződéseket, illetve a vas széntartalmát, melyből rendre SO2 és CO2 keletkezik. A reakció exoterm, a konverter hőmérséklete így akár 1700 °C-ig is emelkedhet.[44]
További 25% előállított oxigént a vegyipar használ fel.[44] Az etilént oxigénnel reagáltatva etilén-oxidot állítanak elő,[92] majd abból pedig etilénglikolt. Az etilénglikol számos termék gyártásának elsődleges kiindulóanyaga, beleértve a fagyállót, illetve a poliészter polimereket (amelyek még több műanyag és szövet prekurzorai).[44] Oxigént vagy levegőt használnak az oxidatív krakkolásnál,[93] szerves vegyületek (akrilsav,[94][95] 2,5-diformil-furán,[96] benzoesav[97]) illetve szervetlen vegyületek (kénsav, salétromsav, hidrogén-peroxid[98]) szintézisénél. A vegyiparban illetve belső égésű motorokban keletkezett káros gázok utókezelésére oxidatív konvertereket használnak.[99][100]
A fennmaradó 20%-ot orvosi célokra, hegesztésre, lemezvágásra, rakéta-hajtóanyaghoz, illetve víztisztításhoz használják fel.[44] Az oxiacetilén hegesztéskor a hegesztőpisztolyban acetilén és oxigéngáz keverékét égetik el, amely rendkívül forró lánggal ég. A lemezvágási eljárásnál a legfeljebb 60 cm vastag lemezt egy kisebb oxiacetilén lánggal előhevítik, majd egy nagyobb oxigénsugárral hirtelen elvágják.[101]

A paleoklimatológusok mérik a tengeri élőlények héjában és vázában található oxigén-16 és oxigén-18 izotópok mennyiségét, hogy meghatározzák milyen volt az éghajlat évmilliókkal ezelőtt. A tengervíz molekulái, amelyek a könnyebb oxigén-16 izotópot tartalmazzák, valamivel gyorsabb ütemben párolognak el, mint a 12%-kal nehezebb oxigén-18 izotópot tartalmazó vízmolekulák; ez a különbség alacsonyabb hőmérsékleten növekszik.[102] Az alacsonyabb globális hőmérsékletű időszakok során az elpárolgott vízből keletkező hó és eső általában oxigén-16-ban, a hátrahagyott tengervíz pedig általában oxigén-18-ban gazdagabb. A tengeri élőlények így több oxigén-18 izotópot építenek be a vázszerkezetükbe, mint tennék azt melegebb éghajlat esetén.[102] A paleoklimatológusok közvetlenül is mérik ezt az arányt a jégmag mintákból származó vízmolekulákban, amelyek akár több százezer évesek is lehetnek.
A planetáris geológusok az oxigénizotópok előfordulási gyakoriságára különböző értékeket mértek a Földről, a Holdról, a Marsról és meteoritokról származó mintákban, de a Napra jellemző izotópgyakorisági értéket még nem sikerült meghatározni – utóbbiról feltételezik, hogy azonos az ősi szoláris ködével (primordial solar nebula). Ugyanakkor a földbe csapódott Genesis űrszonda által visszahozott, az űrben napszélnek kitett szilícium szeletek elemzése azt mutatta, hogy a Nap nagyobb arányban tartalmaz oxigén-16 izotópot, mint a Föld. Az eredmény azt jelenti, hogy egy még ismeretlen folyamat kimerítette a Nap protoplanetáris korongjának oxigén-16 tartalmát, még mielőtt a porszemcséi összeolvadhattak volna, és létrehozták volna a Földet.[103]
Az oxigén két spektrofotometriás abszorpciós sávval rendelkezik, melyek csúcsai 687 és 760 nm hullámhossznál találhatóak. Néhány távérzékeléssel foglalkozó tudós felvetette, hogy a növényzet egészségi állapota vizsgálható lenne műholdas platformról, a vegetáció lombozatának ezen sávokba eső sugárzásának mérése révén.[104] Ez a megközelítés azt használja ki, hogy ezekben a sávokban a növényzet reflexiója elkülöníthető annak fluoreszcenciájától, amely sokkal gyengébb. A mérés technikailag nehezen kivitelezhető az alacsony jel-zaj viszony és a növényzet fizikai struktúrája miatt; de javasolt lehetséges eljárás a szén-körciklus globális nyomonkövetésére.
Az oxigén oxidációs száma szinte minden ismert vegyületében −2.[105] Néhány vegyületében, például a peroxidokban előfordul a −1 oxidációs szám is. Az oxigént más oxidációs állapotban tartalmazó vegyületek nagyon ritkák: −1/2 (szuperoxidok), −1/3 (ozonidok), 0 (elemi állapot, hipofluorossav), +1/2 (dioxigenil), +1 (dioxigén-difluorid) és +2 (oxigén-difluorid).


A víz (H2O) a hidrogén oxidja, egyben a legismertebb oxigénvegyület. A vízmolekulában a hidrogénatomok kovalens kötéssel kapcsolódnak az oxigénatomhoz, de ezen kívül további vonzást mutatnak (hidrogénatomonként körülbelül 23,3 kJ/mol) más vízmolekulák oxigénatomjai felé is.[106] Ez a hidrogénkötés 15%-kal közelebb tartja egymáshoz a vízmolekulákat annál, mint ahogy az egy közönséges folyadékban a Van der Waals-erők alapján várható lenne.[107][m 10]
Nagy elektronegativitása miatt az oxigén magas hőmérsékleten majdnem az összes elemmel kémiai kötéseket képez, a megfelelő oxidokat hozva létre. Mindazonáltal több elem szabványos nyomáson és hőmérsékleten is könnyen alkot oxidokat, ennek egyik példája a rozsdásodó vas. Az alumíniumhoz és titánhoz hasonló fémek felülete levegő jelenlétében oxidálódik; vékony, tömör oxidréteg jön létre, amely passziválja a fémet, és lelassítja a további korróziót. Néhány természetben megtalálható nem-sztöchiometrikus átmenetifém-oxidban valamivel kevesebb fém található, mint amennyi a vegyképletéből következne. Például a természetben előforduló FeO (wüstit) valójában Fe1 − xO formában írható fel, ahol x általában 0,05 körüli érték.[108]
Az oxigén egyik vegyülete – a szén-dioxid (CO2) – nyomokban megtalálható a légkörben. A földkéreg kőzeteinek jelentős részét alkotják a különböző elemek oxidjai, mint például a szilícium- (a szilícium-dioxid (SiO2) alkotóeleme a gránitnak és a homoknak), az alumínium- (alumínium-oxid (Al2O3), a bauxitban és korundban), a vas-oxidok (vas(III)-oxid (Fe2O3), a hematit és a rozsda) és a kalcium-karbonát (mészkő). A földkéreg többi részében szintén megtalálhatóak oxigénvegyületek, főleg a különböző komplex szilikátok (a szilikátásványokban). A földkéregnél jóval nagyobb tömegű földköpenyt főként magnézium- és vas-szilikátok alkotják.
A vízoldható szilikátokat (például Na4SiO4, Na2SiO3 és Na2Si2O5) mosószerekként és ragasztókként használják.[109]
Az átmenetifémek esetében az oxigén ligandumként is viselkedik, és fém-O2 kötéseket képez az irídiumatommal a Vaska-komplexben,[110] a platinával a PtF6-ban,[111] valamint a hemoglobin hem csoportjában a központi vassal.


A legfontosabb oxigéntartalmú szerves vegyületek (az „R” valamilyen szerves csoportot jelöl): alkoholok (R−OH), éterek (ROR), ketonok (R−CO−R), aldehidek (R−CO−H), karbonsavak (R−COOH); észterek (R−COO−R); savanhidridek (R−CO−O−CO−R) és az amidok (RC(O)−NR2). Számos fontos, oxigéntartalmú szerves oldószer ismert, beleértve a következőket: aceton, metanol, etanol, IPA, furán, tetrahidrofurán, dietil-éter, dioxán, etil-acetát, DMF, DMSO, ecetsav és hangyasav. Az aceton ((CH3)2CO) és a fenol (C6H5OH) számos különböző anyag szintéziséhez elengedhetetlen alapanyag. Egyéb fontos, oxigéntartalmú szerves vegyület még a glicerin, a formaldehid, a glutáraldehid, a citromsav, az ecetsav-anhidrid és az acetamid. Az epoxidok olyan éterek, amelyekben az oxigénatom egy háromatomos gyűrű része.
Az oxigén számos szerves vegyülettel szobahőmérsékleten vagy annál alacsonyabb hőmérsékleten spontán reakcióba lép, ezt a folyamatot autooxidációnak nevezzük.[112] A legtöbb szerves vegyület amely oxigént tartalmaz, nem az oxigéngáz közvetlen reakciója során képződik. Az iparban és a kereskedelemben is fontos szerves vegyületek etilén-oxid és perecetsav tartalmú prekurzorok közvetlen oxidálásával gyárthatók.[109]
Az elem szinte mindegyik biomolekulában megtalálható, amely fontos az élet számára (vagy éppen az állította elő). Csak néhány komplex biomolekula, mint például a szkvalén és a karotinok nem tartalmaznak oxigént. A biológiailag releváns szerves vegyületek közül a szénhidrátok tartalmaznak oxigént a legnagyobb tömegarányban. Minden zsír, zsírsav, aminosav és fehérje tartalmaz oxigént (a karbonilcsoportok jelenléte miatt a savakban, illetve azok észter származékaiban). Az oxigén előfordul a biológiailag fontos energiahordozó ADP és ATP molekulák foszfátcsoportjaiban (PO3−4), az RNS és DNS molekula vázában, a purin- és a pirimidinbázisokban (az adenin kivételével), valamint a csontokban kalcium-foszfát és hidroxiapatit formájában.
A naszcensz latin szó, jelentése ’a születés pillanatában lévő’. A kémiában a keletkezés, kiválás pillanatában lévő, még atomos állapotú elemekre (gázokra) használják. Az ilyen naszcensz elemek atomos állapotuk miatt rendkívül reakcióképesek. Az ózonból és a hidrogén-peroxidból naszcensz oxigén szabadul fel, ezért ezek az anyagok nagyon erős oxidálószerek.


Az NFPA 704 szabvány a sűrített oxigéngázt egészségre nem veszélyes, nem gyúlékony és nem reaktív, ugyanakkor égést segítő oxidálószerként sorolja be. A hűtött, folyékony oxigén (LOX) egészségügyi szempontból 3-as besorolású a kondenzált gőzök okozta hyperoxia fokozott kockázata, illetve a fagyási sérülések miatt; de minden más szempontból azonos a sűrített oxigéngázzal.


A nagy parciális nyomású oxigéngáz (O2) mérgező lehet, amely görcsökhöz és más egészségi problémákhoz vezet.[87][114][m 11] Az oxigénmérgezés általában 50 kilopascal (kPa) parciális nyomáson kezd kialakulni, amely egyenlő a normál tengerszinti O2 parciális nyomás (~21 kPa) két és félszeresével vagy más megközelítésben légköri nyomáson (100 kPa) 50%-os oxigén összetételt jelent. Ez elég szélsőséges ahhoz, hogy a hétköznapokban ne okozzon problémát, kivéve a lélegeztetőgépre kötött betegeket, esetükben az oxigénmaszkon keresztül érkező levegőben az oxigén részaránya 30-50 térfogatszázalék (körülbelül 30 kPa normál nyomáson),[30] habár ez az érték a maszk típusától függően széles tartományban változhat.
Egy időben a koraszülötteket oxigéndús levegővel teli inkubátorba helyezték, de ezt a gyakorlatot megszüntették, miután egyes babák megvakultak a túl magas oxigéntartalomtól.[30]
Az űripari alkalmazásokban – mint például a modern űrruhákban és a korai Apollo űrhajókban – a tiszta oxigén belélegzése azért nem okozott gondot, mert az oxigén össznyomása kicsi volt.[85][115] Az űrruha esetében a belélegzett gázkeverékben lévő O2 parciális nyomása 30 kPa (a normál érték 1,4-szerese), míg az űrhajós vérében oldott O2 parciális nyomása alig haladja meg a tengerszinten mérhető értéket.
A tüdő és a központi idegrendszer oxigénmérgezése önálló készülékes (SCUBA) és ipari búvárkodás (felszíni levegőtáplálásos) során is előfordulhat.[30][87] 60 kPa parciális nyomású oxigént tartalmazó gázkeverék huzamosabb ideig történő belélegzése tartós tüdőfibrózist okoz.[116] 160 kPa (1,6 atm) vagy annál nagyobb parciális nyomású oxigéngáznak való kitettség görcsökhöz vezethet, amely a búvárok számára általában végzetes. A rohamokat okozó, és emiatt a búvárok számára legfélelmetesebb akut oxigénmérgezés 21%-os oxigéntartalom mellett 66 m (tiszta, 100% oxigéntartalom esetében már 6 m) mélységben bekövetkezik.[116][117][118][119]

A rendkívül koncentrált oxigén elősegíti a gyors égést. Tűz- és robbanásveszély áll fenn, ha a koncentrált oxigén és az éghető anyag közvetlen közelségbe kerül; az égés megindításához ugyanakkor valamilyen gyújtóhatásra – például hőre vagy szikrára – is szükség van.[120] Az oxigén maga nem éghető, de az égést táplálja (oxidálószer). A tűzveszélyesség az oxigén azon vegyületeire is fennáll, amelyek magas oxidációs potenciállal rendelkeznek, mivel ezek oxigénnel táplálhatják a tüzet. Ilyen vegyületek például a peroxidok, klorátok, nitrátok, perklorátok és dikromátok.
A tömény oxigén lehetővé teszi, hogy az égés gyorsan és energetikusan terjedjen.[120] A légnemű és folyékony oxigén szállítására használatos acélcsövek maguk is éghető anyagokként viselkednek, ezért az ilyen O2-rendszerek tervezése és gyártása speciális képzettséget igényel annak érdekében, hogy a gyújtóforrások száma minimalizálható legyen.[120]
Az Apollo–1 legénységének halálát egy tűzeset okozta, amely egy indítóállási teszt során keletkezett. A teszt alatt a kapszulát tiszta oxigénnel töltötték fel, azonban a légkörinél valamivel nagyobb nyomással; így a rövidzárlat következtében felcsapó lángok olyan hevesen és gyorsan égtek, hogy az űrhajósok percek alatt megfulladtak.[m 12][121][122]
Ha az elszivárgó folyékony oxigén szerves anyagokba – például fába, aszfaltba vagy petrolkémiai termékekbe – szívódik be, akkor ezen anyagok mechanikai behatásra később kiszámíthatatlanul berobbanhatnak.[120] Más kriogén anyagokhoz hasonlóan az emberi testtel érintkezve a bőr és a szem fagyási sérülését okozhatja.
Seamless Wikipedia browsing. On steroids.