Un ARN non codificante ou ARNnc (en inglés ncRNA) é unha molécula de ARN funcional que non se traduce a proteínas. Outros sinónimos menos frecuentes son ARN non codificador de proteínas, ARN non mensaxeiro e ARN funcional. O termo ARN pequeno úsase con frecuencia para referirse aos ARNnc curtos bacterianos. A secuencia de ADN a partir da que se transcribe un ARN non codificante denomínase a miúdo xene de ARN.
Entre os xenes dos ARN non codificantes inclúense os de ARNs moi abundantes e importantes funcionalmente como os ARN transferentes (ARNt) e ARN ribosómicos (ARNr), xunto cos ARN nucleolares pequenos, microARNs, ARN interferentes pequenos, os ARN que interacionan con piwi e os ARNnc longos como Xist e HOTAIR. O número de ARNnc codificados no xenoma humano descoñécese, pero recentes estudos de transcritómica e bioinformática suxiren a existencia de miles de ARNnc.[1][2][3][4], pero ver [5] Como a moitos dos ARNnc recentemente identificados non lles se confirmou a súa función, é posible que moitos sexan non funcionais.[6]
Hai ARNs non codificantes de varias clases distintas e están implicados en moitos procesos celulares. Hai ARNnc de importancia central para os seres vivos que foron conservados en todos ou na gran maioría das especies, e outros máis específicos presentes nunha ou nunhas poucas especies relacionadas. Os ARNnc máis conservados pénsase que son fósiles moleculares ou reliquias do último antepasado común universal (LUCA) e do mundo de ARN.[7][8][9]
Os ARNs non codificantes na tradución de proteínas

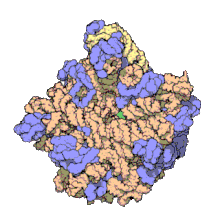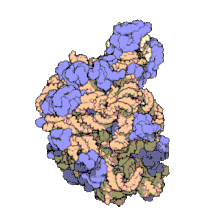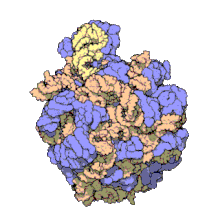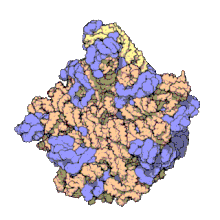
Moitos dos ARNnc conservados, esenciais e abundantes están implicados na tradución. As partículas ribonucleoproteicas chamadas ribosomas son os lugares onde ten lugar a tradución na célula. O ribosoma consta de máis dun 60% de ARN ribosómico, constituído por tres ARNnc distintos nos procariotas e catro nos eucariotas. Os ARNs ribosómicos catalizan a tradución de secuencias de nucleótidos a proteínas. Outro conxunto de ARNnc son os ARN transferentes, que son "moléculas adaptadoras" entre o ARNm e as proteínas. Os snoRNA de caixa H/ACA e de caixa C/D son ARNnc que se encontran nas arqueas e eucariotas, a RNase MRP está restrinxida aos eucariotas, e ambos os grupos de ARNnc están implicados na maduración do ARNr. Os snoRNAs dirixen a realización de modificacións covalentes do ARNr, ARNt e ARN nuclear pequeno; a RNase MRP cliva (corta) o espazador transcrito interno 1 entre os ARNr 18S e 5,8S. A RNase P é un ubicuo ARNnc, que ten un parentesco evolutivo coa RNase MRP.[11] A RNase P madura as secuencias de ARNt xerando extremos 5' maduros de ARNt por medio da clivaxe dos elementos líder 5' dos ARNts precursores. Outra ribonucleoproteína ubicua chamada partícula de recoñecemento do sinal (SRP) recoñece e transporta proteínas nacentes específicas ao retículo endoplasmático dos eucariotas e á membrana plasmática nos procariotas. Nas bacterias o ARN transferente-mensaxeiro (ARNtm) é unha ribonucleoproteína implicada no rescate de ribosomas estancados (que non poden completar a tradución dun polipéptido), marcando os polipéptidos incompletos e promovendo a degradación do ARNm aberrante.
Os ARNs non codificantes no splicing do ARN

Nos eucariotas o espliceosoma realiza as reaccións do splicing do ARN esenciais para eliminar as secuencias dos intróns, proceso que se require para a formación de ARNm maduro. O espliceosoma é outra ribonucleoproteína tamén chamada snRNP ou tri-snRNP. Hai dúas formas diferentes de espliceosoma, chamadas espliceosoma maior e menor. Os compoñentes de ARNnc do espliceosoma maior son U1, U2, U4, U5, e U6. Os compoñentes de ARNnc do espliceosoma menor son U11, U12, U5, U4atac e U6atac.
Outro grupo de intróns poden catalizar a súa propia eliminación do transcrito no que se hospedan, e denomínanse ARNs de auto-splicing. Hai dous grupos principais de ARNs de autosplicing, que son o intrón catalítico grupo I e intrón catalítico grupo II. Estes ARNnc catalizan a súa propia excisión dos precursores do ARNm, ARNt e ARNr nunha ampla gama de organismos.
Nos mamíferos atopouse que os snoRNAs poden tamén regular o splicing alternativo do ARNm; por exemplo o snoRNA HBII-52 regula o splicing do receptor 2C da serotonina.[12]
Nos nematodos, o ARNnc SmY parece estar implicado no trans-splicing do ARNm.
Os ARNs non codificantes na regulación xénica
A expresión xénica de miles de xenes está regulada por ARNncs. Esta regulación xénica pode ocorrer actuando a través doutra molécula, o que se chama en trans (trans-acting) ou ben de forma directa ou en cis (cis-acting).
ARNs non codificantes que actúan en trans
Nos eucariotas superiores os microARNs regulan a expresión xénica. Un só microARN pode reducir os niveis de expresión de centos de xenes. O mecanismo de actuación das moléculas de micro ARN maduras está baseado na complementariedade de bases parcial cunha ou máis moléculas de ARN mensaxeiro, xeralmente na zona 3' UTR. A principal función dos microARN é regular á baixa a expresión xénica.
O ARNnc RNase P tamén inflúe na expresión xénica. No núcleo das células humanas requírese a RNase P para a transcrición normal e eficiente de varios ARNnc transcritos pola ARN polimerase III. Entre eles están os ARNt, o ARNr 5S, o ARN da SRP, e o snRNA U6. A RNase P exerce a súa función na transcrición asociándose coa ARN polimerase III e a cromatina de xenes de ARNt e ARNr 5S activos.[13]
Pola súa parte, o ARN 7SK, que é un ARNnc de metazoos, actúa como un regulador negativo do factor de elongación P-TEFb da ARN polimerase II, e a súa actividade está influída polas vías de resposta ao estrés.
O ARN de 6S é un ARNnc bacteriano que se asocia especificamente co holoencima da ARN polimerase, que contén o factor de especificidade sigma70. Esta interacción reprime a expresión desde un promotor durante a fase estacionaria do crecemento bacteriano.
Outro ARNc bacteriano é o ARN OxyS, que reprime a tradución ao unirse ás secuencias Shine-Dalgarno e impide así a unión do ribosoma. O ARN OxyS é inducido en resposta ao estrés oxidativo en Escherichia coli.
O ARN B2 é un pequeno transcrito de ARNnc producido pola ARN polimerase III que reprime a transcrición do ARNm en resposta ao choque térmico nas células de rato. O ARN B2 inhibe a transcrición ao unirse ao núcleo da ARN polimerase II. Por medio desta interacción, o ARN B2 únese aos complexos de preiniciación no promotor e bloquea a síntese de ARN.[14]
Un estudo recente mostrou que a transcrición dunha secuencia de ARNnc pode ter unha influencia na expresión xénica. Requírese a transcrición por parte da ARN polimerase II de ARNnc para que se produza a remodelación da cromatina no lévedo Schizosaccharomyces pombe. A cromatina pasa progresivamente a unha configuración aberta a medida que se transcriben varias especies de ARNnc.[15]
ARNs non codificantes que actúan en cis
Nas rexións 5' UTR dos xenes que codifican proteínas (xenes de ARNm) están incluídos varios ARNnc, que inflúen na súa expresión de varios xeitos. Por exemplo, un riboswitch (ribointerruptor) pode unirse directamente a unha pequena molécula diana, e esta unión afecta á actividade do xene.
As secuencias líder do ARN encóntranse augas arriba do primeiro xene dos operóns para a biosíntese de aminoácidos. Estes elementos de ARN cis-regulatorios forman unha das dúas posibles estruturas en rexións que codifican secuencias de péptidos moi curtas que son ricas no aminoácido que é o produto final do operón. Fórmase unha estrutura terminadora cando hai un exceso de aminoácidos regulatorios e non está impedido o movemento do ribosoma sobre o transcrito líder. Cando hai unha deficiencia do ARNt que leva o o aminoácido regulatorio, o ribosoma que está traducindo o péptido líder detense e fórmase a estrutura antiterminadora. Isto permite que a ARN polimerase transcriba o operón. Entre os ARN líderes coñecidos están o líder do operón da histidina, o líder do operón da leucina, o líder do operón da treonina e o líder do operón do triptófano.
Os elementos de resposta ao ferro (IRE, Iron Response Elements) únense a proteínas de resposta ao ferro (IRP). O IRE atópase nas rexións UTR (Rexións Non Traducidas) de varios ARNm, cuxos produtos están implicados no metabolismo do ferro. Cando a concentración de ferro é baixa, as IRPs únense ao IRE do ARNm da ferritina, o que leva a reprimir a tradución.
O sitio de entrada ao ribosoma interno (IRES) é unha estrutura de ARN que permite a iniciación da tradución no medio dunha secuencia de ARNm como parte do proceso de síntese de proteínas.
Os ARNs non codificantes e a defensa do xenoma
Os ARN que interaccionan con piwi (piRNAs) exprésanse nos testículos dos mamíferos e en células somáticas, e forman complexos ARN-proteínas coas proteínas piwi. Estes complexos con piRNA (piRCs) foron asociados ao silenciamento de xenes transcricional de retrotransposóns e outros elementos xenéticos en células da liña xerminal, especialmente na espermatoxénese.
As CRISPR (Regularly Interspaced Short Palindromic Repeats) son repeticións que se encontran no ADN de moitas bacterias e arqueas. As repeticións están separadas por espazadores de lonxitude similar. Foi demostrado que estes espazadores poden derivar dun fago e axudan a protexer a célula da infección.
Os ARNs non codificantes e a estrutura dos cromosomas
A telomerase é un encima ribonucleoproteico que engade secuencias repetidas de ADN específicas ("TTAGGG" en vertebrados) ás rexións teloméricas, que forman os extremos dos cromosomas eucarióticos. Os telómeros conteñen ADN condensado, que lle dá estabilidade aos cromosomas. O encima é unha reversotranscriptase que leva ARN, que se utiliza como molde cando se elongan os telómeros, os cales se acortan despois de cada ciclo de replicación celular.
O Xist é un xene de ARNnc longo situado no cromosoma X de mamíferos placentarios que actúa como un efector principal no proceso de inactivación do cromosoma X orixinando os corpos de Barr. Un ARN antisentido chamado Tsix funciona como regulador negativo de Xist. Os cromosomas X que carecen de expresión de Tsix (e dese modo teñen altos niveis de transcrición de Xist) son inactivados máis frecuentemente do que os cromosomas normais. En drosofílidos, que tamén utilizan un sistema de determinación do sexo XY, os ARNs roX (ARN no cromosoma X) están implicados na compensación de dose.[16] Tanto Xist coma roX operan por medio de regulacións epixenéticas da transcrición ao recrutaren encimas que modifican as histonas.
ARN bifuncional
Os ARNs bifuncionais, ou os ARNs de función dual, son ARNs que teñen dúas funcións distintas.[17][18] A maioría dos ARN bifuncionais coñecidos son á vez ARNm codificadores de proteínas e ARNnc. Porén, hai tamén un número crecente de ARNnc que se clasifican á vez en dúas categorías de ARNnc, como o snoRNA de caixa H/ACA e o microARN.[19][20]
Dous exemplos ben coñecidos de ARNs bifuncionais son o ARN SgrS e o ARNIII. Porén, coñécense algúns outros como o activador do receptor de esteroides/SRA,[21] ARN VegT,[22][23] o ARN Oskar [24] e o ENOD40.[25] Os ARNs bifuncionais están sendo obxecto de publicacións especiais da revista Biochimie.
Igual que ocorre coas proteínas, as mutacións ou desequilibrios no repertorio de ARNnc no corpo poden causar diversas enfermidades.
Cancro
Moitos ARNnc presentan patróns de expresión anormais en tecidos cancerosos. Entre eles os microARNs,[26] os ARNnc longos,[27][28] GAS5,[29] SNORD50,[30] o ARN da telomerase e os ARN Ys.[31] Os microARNs están implicados na regulación a grande escala de moitos xenes que codifican proteínas,[32][33] os ARN Y son importantes para a iniciación da replicación do ADN,[34] o ARN da telomerase serve como cebador para a telomerase, a cal estende os telómeros dos cromosomas. A función directa dos ARNnc longos está menos clara.
As mutacións na liña xerminal nos precursores primarios de miR-16-1 e miR-15 son moito máis frecuentes en pacientes de leucemia linfocítica crónica en comparación coa poboación de control.[35][36]
Propúxose que o raro polimorfismo dun só nucleótido rs11614913 que solapa o has-mir-196a2 está asociado co carcinoma pulmonar de células non pequenas.[37] Igualmente, un exame de 17 microARNs que se predicira que regulaban varios xenes asociados ao cancro de mama encontrou variacións nos microARN miR-17 e miR-30c-1 en pacientes que non eran portadores das mutacións BRCA1 ou BRCA2, o que abre a posibilidade de que o cancro de mama familiar poida ser causado por variacións nestes microARNs.[38]
O supresor de tumores p53 pode dicirse que é o factor máis importante para previr a formación e progresión de tumores. A proteína p53 funciona como un factor de transcrición que ten un papel crucial en organizar a resposta ao estrés celular. Ademais do seu importante papel no cancro, a p53 foi implicada noutras enfermidades como a diabetes, morte celular despois da isquemia, e varias enfermidades neurodexenerativas como as de Huntington, Parkinson, e Alzheimer. Algúns estudos suxiren que a expresión da p53 está suxeita a regulación por ARN non codificante.[4]
Síndrome de Prader–Willi
A deleción de 48 copias do snoRNA de caixa C/D SNORD116 é a causa primaria da síndrome de Prader Willi.[39][40][41] Esta síndrome é un trastorno do desenvolvemento asociado con sobrealimentación e dificultades de aprendizaxe. O SNORD116 ten sitios diana potenciais en varios xenes que codifican proteínas, e podería ter un papel na regulación do splicing alternativo.[42]
Autismo
O locus cromosómico que contén o clúster de xenes do ARN nucleolar pequeno SNORD115 está duplicado en aproximadamente o 5% das persoas con trazos de autismo.[43][44] Un experimento que usou como modelo ratos modificados xeneticamente para teren unha duplicación no clúster SNORD115 mostrou que tiñan comportamentos de tipo autista.[45]
Hipoplasia cartilaxe-pelo
As mutacións na RNase MRP causan hipoplasia cartilaxe-pelo, unha doenza asociada cun conxunto de síntomas como curta estatura, pelo escaso, anormalidades esqueléticas e sistema inmunitario suprimido, que é frecuente entre os Amish e os fineses.[46][47][48] A variante mellor caracterizada é unha transición de A a G no nucleótido 70 que está nunha rexión bucle dúas bases en dirección 5' dun pseudonó conservado. Porén, moitas outras mutacións na RNase MRP tamén causan esta hipoplasia.
Enfermidade de Alzheimer
O ARN antisentido BACE1-AS transcríbese da cadea oposta ao BACE1 e está sobreexpresado en pacientes de Alzheimer.[49] O BACE1-AS regula a expresión de BACE1 ao incrementar a estabilidade do ARNm do BACE1 e xerar máis BACE1 por medio dun mecanismo postranscricional de proalimentación (feed-forward). Polo mesmo mecanismo eleva as concentracións de beta amiloide, o principal constituínte das placas senís. As concentracións de BACE1-AS están elevadas en suxeitos con enfermidade de Alzheimer e nos ratos transxénicos con proteína precursora amiloide.
O miR-96 e a perda de audición
As variacións na rexión semente do miR-96 maduro foron asociadas coa perda de audición autosómica dominante, progresiva en humanos e ratos. Os ratos mutantes homocigotos teñen xordeira profunda, e non mostran respostas cocleares. Os ratos e humanos heterocigotos perden progresivamente a audición.[50][51][52]
Varias publicacións [53][54][55] están empezando a utilizar o termo ARN funcional (ARNf ou fRNA), como oposto a ARNnc, para describir rexións funcionais de ARN que poden ou non orixinar transcritos autónomos de ARN. Por tanto, todo ARNnc é un ARNf, pero existen ARNf (como os riboswitches, elementos SECIS, e outras rexións cis-regulatorias) que non son ARNnc. E mesmo o termo ARNf podería tamén incluír aos ARNm, xa que codifican unha proteína e son funcionais. Adicionalmente os ARNs feitos evolucionar artificialmente tamén entrarían dentro deste termo paraugas de ARNf. Algunhas publicacións [56] afirman que os termos ARNnc e ARNf son case sinónimos.

Os ácidos nucleicos foron descubertos en 1868 por Friedrich Miescher[57] e no ano 1939 sabíase que o ARN estaba implicado na síntese de proteínas.[58] Dúas décadas despois, Francis Crick predixo a existencia dun compoñente de ARN funcional que mediaba a tradución; e considerou que un ARN era máis axeitado para unirse por apareamento de bases ao transcrito de ARNm ca un polipéptido puro.[59]
O primeiro ARN non codificante que foi caracterizado foi o ARNt da alanina do lévedo de panadaría, cuxa estrutura foi publicada en 1965.[60] Para obter unha mostra de ARNt da alanina purificado, Robert W. Holley et al. tiveron que utilizar 140 kg de lévedo de panadaría comercial dos que extraeron só 1 g de ARNtAla purificado para a súa análise.[61] O ARNt de 80 nucleótidos foi secuenciado despois de dixerilo primeiro con ribonuclease pancreática (producindo fragmentos que acababan en citosina ou uridina) e despois con tacadiastase ribonuclease Tl (producindo fragmentos acabados en guanosina). A cromatografía e a identificación dos extremos 5' e 3 axudou despois a ordenar os fragmentos e establecer a secuencia do ARN.[61] Das tres estruturas propostas orixinalmente para este ARNt,[60] a estrutura en "folla de trevo" propúxose independentemente en varias publicacións.[62][63][64][65] A estrutura secundaria en folla de trevo finalizouse utilizando análises de cristalografía de raios X realizadas por dous grupos de investigadores independentemente en 1974.[66][67]
Seguidamente descubriuse o ARN ribosómico. Desde entón continuaron descubríndose novos ARN non codificantes como o snoRNAs, Xist, CRISPR e moitos máis.[56] Descubrimentos recentes salientables son os riboswitches (ribointerrruptores) e o microARN, e o descubrimento da interferencia de ARN e o seu mecanismo asociado, que lles valeu a Craig C. Mello e Andrew Fire a concesión do Premio Nobel de Medicina de 2006.[68]
Wikiwand in your browser!
Seamless Wikipedia browsing. On steroids.
Every time you click a link to Wikipedia, Wiktionary or Wikiquote in your browser's search results, it will show the modern Wikiwand interface.
Wikiwand extension is a five stars, simple, with minimum permission required to keep your browsing private, safe and transparent.