埃博拉出血热
传染病 来自维基百科,自由的百科全书
埃博拉出血热(又名:埃博拉病毒病;通称:埃博拉;英语:Ebola Hemorrhagic Fever)是一种由埃博拉病毒引起,多出现于灵长动物身上的人畜共患传染病,因在埃博拉河附近发现,因此得名。[1]罹患此病的人会在2天至3周内陆续出现发烧、头痛、肌肉疼痛、呕吐、腹泻以及出疹等症状。病情之后会进一步恶化为肝衰竭、肾衰竭[1],步入此阶段,病人或会出现体内、体外出血现象,并可能在首个症状出现后的6至16天内因血容量过低或多重器官衰竭而死亡。[2][3]
| 埃博拉出血热 | |
|---|---|
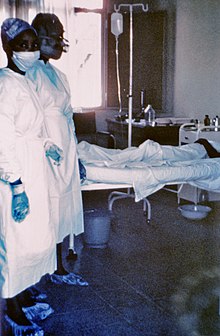 | |
| 1976年萨伊爆发期间的一帧照片:两名护士站在一名埃博拉患者(金沙萨第三宗病例)的病床前。该名患者于几天后死于严重内出血 | |
| 症状 | 恶心、呕吐、头痛、腹泻、发热、疹、呼吸困难、关节疼痛、结膜炎、出血、流鼻血、内出血、肌肉疼痛、肚痛、中毒[*] |
| 类型 | 病毒性出血热、Filoviridae infectious disease[*]、病毒感染、医疗照顾相关感染、疾病、易流行疾病[*] |
| 病因 | 埃博拉病毒属、扎伊尔埃博拉病毒 |
| 诊断方法 | 体格检查、全血细胞计数、酶联免疫吸附试验、病毒培养、聚合酶链式反应、电子显微镜、免疫萤光[*] |
| 治疗 | 镇痛药、输血、hydration[*]、血浆、解热剂、输液[*]、对症治疗 |
| 分类和外部资源 | |
| 医学专科 | 传染病科 |
| ICD-11 | 1D60.0、1D60.01 |
| ICD-10 | A98.4 |
| DiseasesDB | 18043 |
| MedlinePlus | 001339 |
| eMedicine | 216288 |
| Orphanet | 319218 |
| “Ebola”的各地常用译名 | |
|---|---|
| 中国大陆 | 埃博拉 |
| 港澳 | 埃博拉、伊波拉 |
| 台湾 | 伊波拉 |
| 世卫组织 | 埃博拉 |
埃博拉患者多因接触了带有病毒的体液(包括血液)、器官,或间接触摸到最近受污染之器具而染病。[1]目前尚未有足够的证据显示病毒能经空气微粒在灵长动物间传播。[4]患者的精液或母乳在其康复后的数周至数月内,仍可能载有病毒。[1][5]果蝠被认为是埃博拉病原体的天然宿主,能在自身不受影响的状况下将之散播。[1]疫症的控制在于医疗界以及一定程度的社区配合。前线医学措施包括:快速的病例侦测、实验室诊断、接触者追踪、正确看护、谨慎处理医疗废物,以及妥善安葬或火化尸体。[1][6]减少接触受感染的个体为社区防疫的一大重点。在近距离接触患者时,应穿着完整的连身型防护衣物,并勤加洗手。[1]丛林肉易沾染病毒,故在彻底煮熟后方能进食;在处理这类产物时,也需佩戴医用手套。[1]
尽可能撇除诸如疟疾、霍乱、脑膜炎、其他病毒性出血热等可造成近似症状的疾病为诊断埃博拉出血热的首要工作。血液样本中之抗病毒体、病毒的核糖核酸或病毒本身均为鉴定的指标。[1]目前尚未有针对性的治疗方案,疫苗及药物尚待研发。[1]病人大多接受口服补液治疗或静脉注射等,但这只是提高存活率的舒缓性疗法,以降低疾病所带来的伤害及并发症的风险。[1]深切治疗则能进一步应对器官衰竭问题。[7]根据过往疫情,该出血热可造成高达25-90%(平均约五成)的综合临床致死率。[1][8]
该病在1976年首次出现于当时的苏丹及萨伊[注 1][1],并常于非洲撒哈拉以南的地区造成间歇性爆发。直至2013年,世界卫生组织共公布了2,387宗确诊个案,合计24次爆发,总死亡人数为1,590名。[1][9]最严重的一次流行,为肆虐西非的2013-16年疫症;这次爆发最终感染了28,637人,夺取了11,315人的性命。[10][11][12]
病症与症状

埃博拉出血热的潜伏期(感染与发病的时间差)为2-21天不等[1][13],但多数为4-10天[2]。一项近期发表的数学模型评估推算,约有5%的病人为多于3周。[14]
罹患此病的早期症状与普通感冒大同小异,且为突发性。初期症状为:疲倦、乏力、食欲不振、发烧,以及肌肉、关节、咽喉和头部疼痛。[13][2][15][16]患者体温往往超越38.3℃(101℉)。[17]腹泻、呕吐、腹痛、呼吸困难、胸痛、水肿、意识下降、肝与肾衰竭亦会随之而来。[16]除此,约有五成的病患者会在发病后的5-7天内起斑丘疹。[2][17]
到了后期,一些病人开始出现体内、外出血的现象[1](多始于第一个病症出现后的5-7天内[18]);所有患者均有凝血障碍[17]。出血位置通常为黏膜处(主要为消化道、鼻腔和牙龈)及针管的穿刺点。[19]这还会导致红眼、吐血、咳血及便血。[20]流血处若伸延至皮肤的话,则会引起瘀点、瘀斑、紫斑和血肿(尤其是针刺处附近)。[7]但大量出血的情况属于罕见,亦只发生在消化道。[17][21]
若病人能成功抵抗病毒,就会在病发后的7-14天内逐步康复[16];否则会在6-16天内逝世,死因多为血容量过低或多重器官衰竭[3][2]。宏观而言,出血表示了患者的病情较差,因失血过多而死的机会颇高。[15]死者在临终前均会陷入昏迷状态。[16]生还者则会产生至少10年有效的天然抗体,但暂不清楚此是否足以抵挡后继感染。[22]
病源

埃博拉出血热的病原体为五种埃博拉病毒属的成员——本迪布焦病毒(Bundibugyo virus)、雷斯顿病毒(Reston virus)、苏丹病毒(Sudan virus)、塔伊森林病毒(Taï Forest virus)及旧称“扎伊尔埃博拉病毒”的埃博拉病毒(Ebola virus)。[23]后者是此属的模式种且最具危险性,因其造成了最大规模的爆发及最高的死亡率。[24]雷斯顿病毒可以无症状感染人类,尚未被发现有导致人类患病的能力,但已在其他灵长动物身上诱发疾病。[25][26]它们的特征与马尔堡病毒相似。[23]


埃博拉病毒属的成员为已有数百万年历史的丝状病毒之一。[27]病毒学家利用分子时钟法追溯当中的源流,发现埃博拉与马尔堡病毒虽极为相似,但其实早已于数千年前分化。[28]
与其他丝状病毒一样,埃博拉病毒体型修长。它们呈“6”或“U”字状,有时亦会卷曲成环状,并带分支。这类病毒的平均宽度为80纳米,长度参差甚大——从974到14,000纳米不等。[29]
埃博拉病毒具有线性、非结段型、不具感染性的单股核糖核酸基因组。此基因组为反义,并具有互补性的3'及5'端。其不含5'端帽、不具多腺苷酸化性,亦并非以共价键与蛋白质相连。[30]它们的基因组约有一万九千个碱基对,内含7个以“3'-UTR-NP-VP35-VP40-GP-VP30-VP24-L-5'-UTR”次序排列的基因。[31]这五种埃博拉病毒的基因组以基因重叠的位置及数量区分。
埃博拉病毒会与宿主体内特定的细胞受体(如:“DC-SIGN”、C-型凝集素及整合素)结合进行胞饮作用,开始它们的生命周期。[32]成功入侵后,病毒会移动至细胞的核内体和溶酶体处,使自身含有独特糖蛋白(“GP1”及“GP2”)的包膜分解,以便和细胞膜内壁的蛋白物融合并释放病毒核衣壳。[32][33]由 L 基因编码的病毒核糖核酸聚合酶解封核衣壳,并将有关基因转录为正荷单链信使核糖核酸。此核糖核酸后进一步被翻译为数种结构与非结构性蛋白物,其中以核蛋白的数量最多,它的浓度亦决定着何时从基因转录推进至基因组复制。基因组复制会产生完整的反义基因组物质,并被再转录为新病毒的基因组。[34]此乃埃博拉病毒自我复制的方式。新产生的病毒组合物,会聚集到细胞膜的内壁将之穿破,沿途亦会夺取适用的合成物以制造自身的包膜。新生病毒继续袭击其他细胞,并重复以上周期。埃博拉病毒的特质使研究工作困难重重。[35]
目前还未能铁定埃博拉病毒的天然宿主,但是根据过往的调查,蝙蝠(尤其是锤头果蝠、反曲肩果蝠及小领果蝠)的机会最高。[36][37]1996年发表的一份报告指出,在24种植物及19种脊椎动物中,只有蝙蝠受到埃博拉病毒(模式种)的感染,可它们事后并没有发病,此乃天然宿主的一大特点。[38]1976-98年期间,共有30,000只哺乳类、鸟类、爬行类、两栖类及节肢类动物接受检验,惟研究者只在六只中非共和国的啮齿动物(彼得鼠与非洲柔毛鼠)及一只鼩鼱动物(大森林鼩鼱)的体内找到过病毒的遗传痕迹,其他均一无所获。[39][40]2001及2003年疾病爆发期间,人们在一些大猩猩及黑猩猩的尸体中,发现埃博拉病毒(模式种)的构成物。可见此病对灵长动物的杀伤力高,故他们作为天然宿主的机会微乎其微。[39][41]一项于2002-03年、涉及1,030只动物的实验显示,679只加蓬及刚果蝙蝠中的13只,带有模式种的核糖核酸片段。[42]专家另也于孟加拉国的果蝠身上,找到针对模式种及雷斯顿种的抗体,故埃博拉病原体亦可能存在于亚洲。[43]

虽只是一知半解,但专家相信与带病动物或尸体的直接接触为指示病例出现之因。除了蝙蝠本身,黑猩猩、大猩猩、羚羊等野生动物,亦可因摄取了曾被蝙蝠啃咬的果实而沾染埃博拉病毒。[44][45]猪只、犬只等家畜也有机会携带病原体。前者被证实有能力将病毒传染给非人类的灵长动物,但后者却并无此说且甚少出现病症。[46]
病毒绝少直接在天然宿主与人类群体间散播,而是通过首批患者的体液传染给其他人。[47][48]病毒最常从患者的血液、粪便与呕吐物,通过鼻腔、口腔或伤口进入被感染者的体内。只有重症病人的唾液及大体积的呼吸道分泌物(如飞沫)具传染性,不慎触摸则有机会染病。[49]接触到受病毒污染的医疗器具(特别是针管)亦可致病[36],故照顾埃博拉病人的医护人员为高危人士[22],特别是他们未有正确穿着保护衣物或没有妥善处理医疗废物。埃博拉病毒能在干燥物件表面生存数小时,若伴随体液的话则可达数天。[22]院内感染的情况于一些医疗体系较不完善的非洲地区见怪不怪[50],特别是他们重用已进行了皮下注射的针管[51][16]。此烈性病潜伏期短,病发时,患者往往无法自由行动,使之易被警觉,故其在有能力进行完善隔离的医学发达地区展开大规模流行的机会不大。[52]男性患者的精液在其康复后的7周内仍可携带病毒,并有机会透过性交将之传播;女性病人的乳汁亦然,惟暂不清楚何时方能进行安全喂哺。[1][5]除以上两种情况外,痊愈者不再具传染性。[22]
埃博拉病人的尸体同样可传播病毒。一些传统的土葬或遗体保存技术,因涉及触摸尸体故具一定风险。[53]
目前没有足够的证据,显示埃博拉病毒能通过空气微粒于人类间传播。[4][47][36]此传染模式仅曾在设定了多项条件的猴子实验里出现。[54][55]另一项研究证实了猪只能在不接触的情况下将病毒传染给猴子,但未能证明同样的情况出现于猴子之间。[56]不像猪只,病毒多滋生于灵长动物的血液里而非呼吸道表面,故后者无法通过咳嗽、打喷嚏的方式隔空传播大量的病毒给其他个体。[57]
致病机理

埃博拉出血热的病理生理学为医学界的热门讨论议题之一。埃博拉病毒主要透过粘膜处及表皮伤口入侵宿主身体。[47]它们能在多种细胞内进行高效繁殖,包括:单核细胞、巨噬细胞、内皮细胞、肝细胞、成纤维细胞、肾上腺细胞。[58]这一过程会触发细胞素风暴,导致败血症。[59]巨噬细胞首当其冲受到影响,淋巴细胞后会一并进入细胞凋亡阶段。[60]因此,病人往往会出现淋巴细胞缺乏症及免疫力衰退。[47]病毒在数天后开始侵袭血管内皮细胞,破坏血管的凝聚。[60]负责处理细胞粘附及细胞间结构的整合素,会随着病毒糖蛋白数量的上升而下降。[2]带病者的肝脏亦受到破坏。[2]持续的出血会导致水肿及低血容量休克。[61]弥散性血管内凝血常见于埃博拉病人身上。这是因病毒促使了单核及巨噬细胞分泌过剩的组织因子,导致了血液凝固作用级联。[2][62]
其中,先天性免疫力破坏为埃博拉致病机理的一大重点。[32][34]病毒使患者身体无法对一型干扰素(α 与 β)及二型干扰素伽玛作出自然反应。[33][63]一般而言,数种位于宿主细胞基质内、外的受体(主要为钟形受体)会辨认出病原相关分子,并进入活化阶段。期间,干扰素控制因子(3及7)触发通信级联,令一型干扰素表露并被释放,使之与邻近细胞表面的相关受体结合。[33]结合完成后,信使蛋白“STAT1”及“STAT2”被活化并转移至细胞核刺激干扰素激活性基因,以制造出抗病毒蛋白。[33]埃博拉病毒(模式种)的“V24”及“VP35”蛋白,分别封锁了“STAT1”的去路及直接阻挡了β干扰素的释放。[33][63]通过抑制这些免疫反应,病毒能迅速蔓延至全身。[60]
预防措施

医护与研究人员需严格遵守个人保护指引。美国疾病控制与预防中心建议,在照顾病人或处理其排泄物时,应先穿着全套保护衣物(包括:连身型防护衣、口罩、手套、保护镜),不应暴露身体任何的部分。[65][64][注 2]当局亦提出加强对非洲医护人员在这一方面的训练。[66]曾接触患者分泌物的医疗仪器均需一并消毒。[65]西非疫症中,当地儿童获分配保护装备及消毒用品,以留在家中照顾患病的家人,解决医院床位不足的问题。[67]故传授基本看护知识及保证医疗用品的供应成为了无国界医生的首要任务。[68]于存有生物危害品实验室工作的人员,需接受严格的个人防疫训练,并需在适当的设施中操作埃博拉样本。[69]
高温或化学消毒法能有效清除埃博拉病毒。持续至少30分钟的60℃或5分钟的100℃高温可将病毒分解。 一些诸如酒精制品、洗洁精、漂白水(次氯酸钠)及漂白粉(次氯酸钙)等的表面清洁剂,在适当的浓度下同样为有效的消毒用品。[70][71]勤加以清水及肥皂洗手也是有效的防疫措施。[15] 丛林肉易沾染病毒且为人类感染埃博拉出血热的源头之一,故有关产物需在彻底烹饪后方能进食,亦不宜赤手触摸。[1]传统土葬殡仪涉及尸体触碰,故应被劝阻或由社会人类学家协助改良。[72][64][65][73]
适当的公共卫生政策也是重要的一环。截至2014年8月,世卫认为旅游禁令非为有效之防疫政策[74],但飞机机组人员应按照指引,第一时间隔离并上报任何疑似案例[4]。2014年10月,美国疾病预防中心制定了一套四级制的风险评估,衡量相关赴美人士罹患埃博拉出血热的机会,以决定是否限制其活动。[75][注 3]隔离检疫(即强制隔离)将具传染性的个体与正常人群分隔,能有效阻止埃博拉出血热的扩散。[76][77][78]接触者追踪旨在寻找与感染者曾有密切接触的人士,并将之隔离以进行医学测试及相应治疗。[79][80]
诊断方式
患者的病史对诊断埃博拉出血热极为重要。
血小板减少症、肝细胞谷丙转氨酶与天冬氨酸氨基转移酶的上升、血凝力失常(多伴随着弥散性血管内凝血)、白细胞减少症与白细胞增生症的先后出现,均为诊断埃博拉出血热的非针对性指标。[81]
针对性测试方面,若病人血液样本被验出含有病毒、病毒的核糖核酸或蛋白质、相关抗体的话,即被确诊感染埃博拉病毒。细胞培养病毒测试法、聚合酶链式反应病毒核糖核酸测试法、酶联免疫吸附试验病毒蛋白测试法于早期病患者及尸体身上较为有效,而抗体测试法则适用于后期病人或痊愈者。[82]丝状病毒(包括埃博拉病毒)因具有独特虫状构造而容易透过电子显微镜辨认,惟此无法进一步鉴定具体种类。[29]疾病爆发期间,提取病毒的测试方式不太适用。故聚合酶链式反应及酶联免疫吸附试验为实地检查或流动医院中,最常用之诊断方法。[83]2014年于利比里亚推行的新型流动测试设备,能在样本呈交后的3-5小时之内给予结果。[84]
埃博拉出血热病症与马尔堡出血热的如出一辙。[85]其亦容易与其他一些常见于非洲赤道地区的疾病混为一谈(如:其他的病毒性出血热、疟疾、伤寒、志贺杆菌病、立克次体病(尤其是斑疹伤寒、霍乱、革兰氏阴性菌败血症)及诸如回归热及出血性肠道炎等的莱姆病)。除此,钩端螺旋体病、恙虫病、鼠疫、Q型流感、念珠菌病、组织胞浆菌病、锥虫病、器官利甚曼病、出血性天花、麻疹和急性重症型病毒性肝炎亦位列鉴别诊断的名单上。[86]有机会与埃博拉出血热混淆的非传染性疾病有:急性早幼粒细胞白血病、溶血性尿毒综合症、蛇咬中毒、凝血因子缺乏症/血小板疾病、血栓性血小板减少紫斑症、遗传性出血性血管扩张症、川崎氏病,以及华法林中毒。[87][88][89][90]
病情监控
目前尚未有针对性的埃博拉治疗方案,所有的措施均旨在舒缓疾病所带来的伤害及降低并发症的风险。[91]美国食品药品监督管理局亦呼吁大众要提防假冒产品。[92][93]
及早接受口服补液治疗或静脉注射等舒缓性疗法,有助提升存活率。[1]这包括了痛楚控制、体温控制、止吐、抗忧郁。于发病早期注射抗凝剂(如肝素)可减少弥散性血管内凝血的危害;而在后期注射凝固剂则可降低出血的程度。另外,抗生素有助杜绝由细菌或真菌(于已受埃博拉病毒破坏之器官)所引起的继发性感染。[94][95][96]世卫呼吁避免使用阿斯匹林及布洛芬这两种容易导致出血的药物止痛。[97]浓缩红血球血包、血小板及冰冻血浆一类的血液制品,在必要时也可一并使用。[98]
已发展国家一般可为病人提供深切治疗。[7]首要工作为保持患者体液及电解质的平衡,以降低脱水对身体带来的影响。血液透析与体外膜氧合则可分别解决肾衰竭及肺功能下降的问题。[7]
预后
罹患埃博拉出血热的综合死亡率位于25-90%之间,平均值为五成(模式种病毒的威胁则更高)。[1][8]临床实例证明,持续感染会造成长期的后遗症,如:睾丸炎、关节疼痛、肌肉疼痛、脱屑、脱发及多种眼部症状(畏光、溢泪、葡萄膜炎、脉络膜视网膜炎,甚至失明)。[1]除此,康复者大多都会出现慢性肌肉与关节疼痛、肝炎、听力下降以及诸如长期疲劳、胃口下降、无法恢复体重等的全身症状。[16][59]
流行概况
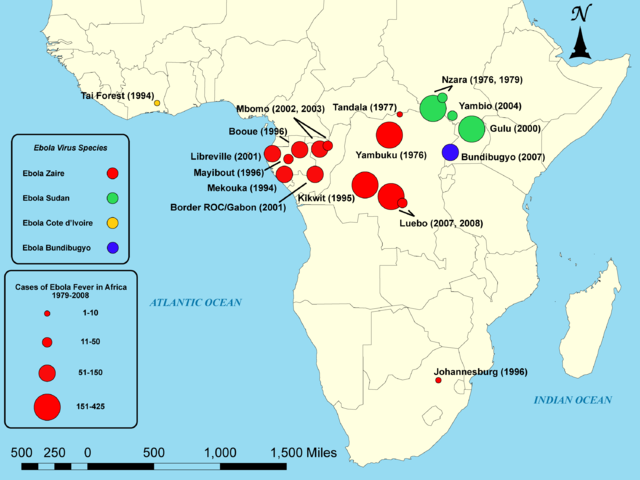
埃博拉出血热常间歇性地出现于非洲撒哈拉以南的地区,走向风里杨花。从1976年(人类首次发现此病)至2013年为止,世卫一共公布了2,387宗确诊个案,共24次爆发,总死亡人数为1,590名。[1][9]最具规模的一次流行,为2014—16年的西非疫症。

人类史上第一宗埃博拉出血热确诊个案,出现于现在的南苏丹(当时的苏丹)一个名为“恩扎拉”的村落。[23][100][101]该病人为当地一家棉织厂的主人。他于6月27日发病,三天后入院,并在7月6日死亡。[7][102]引发此次爆发的元凶,为最终夺取了151人性命(总患病人数为284名)的苏丹病毒。虽然世卫人员知道他们面对的是一种新型疾病,但在相隔数月后的扎伊尔爆发中,病原体才被深入了解及命名。[102]
同年8月26日,现在的刚果民主共和国(当时的扎伊尔)北部蒙加拉省的亚布库村庄,爆发了埃博拉出血热。[103][104]首名患者是当地一所学校的校长。他早前于8月12至22日期间,到埃博拉河接近中非共和国的边沿地带旅行,回家后在8月26日出现症状。[105]起初,有关卫生所对此病例不以为然,列作疟疾处理,分配了奎宁作治疗药物。可是,他的病情持续恶化,最终于9月5日被送入当地的教会医院,至发病后的第14天(即9月8日)病逝。[106][107]多名与这位校长有近距离接触的人士先后出现症状,并陆续死亡,全村陷入恐慌。[105][108][109][110]当地卫生局及时任扎伊尔总统的蒙博托·塞塞·塞科宣布,将包括国都金沙萨在内的有关地区划为检疫区,禁止外人进入,另对水、陆、空运输实施戒严。美国疾病控制与预防中心的研究员彼得·皮奥特在视察该地时指出,当地的比利时修女使用了未经彻底消毒的针管为孕妇注射多余的维他命,无意地促成了这次流行。疾病爆发期间,恩戈伊·莫索拉(Ngoy Mushola)医生首度为此病作出了临床描述:“罹患这病的典型特征为:39℃或以上的高烧、吐血、便血、胸骨下腹痛、关节“重感”、虚脱及以平均三天的速度死亡。”[111]起先,元凶被误认为是形态相似的马尔堡病毒,后发现其乃前所未见的新型种,并与早前的苏丹爆发有所关联(时下各种埃博拉病毒尚未被划分)。专家以位于亚布库(此病最早的爆发确认点)附近的埃博拉河为依据,将此病原体定名为“埃博拉病毒”。[7][注 4]疾病爆发最终在26天后,因隔离检疫生效及防疫意识上升而结束,检疫期为时2周。[113]此次的流行由模式种病毒引起,最终在318位感染者中夺取了280人的性命。[114][115]

埃博拉出血热在相隔多年后死灰复燃。[116]继1979年再次侵袭苏丹后,又在1994年首次出现于加蓬[117],2000年蔓延至乌干达[118]。2003年的刚果共和国爆发录得了至今最高的埃博拉病死率——143名病患者中的128人死亡(致死率为90%)。[119]模式种及苏丹种病毒其后间歇性地出现于以上各地。[116]另外,一种名为“本迪布焦病毒”的新型埃博拉病毒,在2007年的西乌干达本迪布焦区爆发中首度亮相。[120][121]

西非疫症乃埃博拉出血热有史以来最严重的一次爆发,亦是该病首次登陆西非。[116][122]一名于2013年12月6日死亡的婴儿或为是此流行的源头。[123]疫症一发不可收拾。几内亚于2014年的3月,由世卫确认出现首宗病例;8月底,疾病已蔓延至尼日利亚及塞内加尔。[124]同年8月8日,世卫宣布此次爆发为“国际突发性公共卫生事件”,并呼吁各国积极及迅速协助受影响地区。[125][126]相关陆军封锁了疫区,防止病毒进一步扩散。[127]8月中旬,无国界医生表示,利比里亚首都蒙罗维亚的情况为“灾难性”及“每况愈下”。当地医疗系统运作瘫痪,工作人员处于恐慌之中,很多罹患其他疾病的人士未能得到及时的看护[128];逾百位医护人员殉职[129]。世卫于9月26日的报告中总结:“西非埃博拉疫症是人类当代最严重且紧急的一次公共卫生危机。即便是其他第四类生物危险品亦没有如此迅速、持续地感染多个地区的人们。”[130]截至2016年1月14日[update],是次爆发已有28,637宗疑似个案被上报,共11,315宗死亡案例被证实[10][11][12],惟此或低于实际情况[131]。
除了人命伤亡,疫症亦造成了经济损失及社会动荡。《金融时报》一篇报告指出,由疾病引发之资源短缺问题造成了比病毒本身更大的负面影响。[132]数以千计的利比里亚、几内亚和塞拉利昂居民受到检疫隔离,长时间缺乏足够的食物,联合国世界粮食计划署采取了相应行动。[128]8月16日,蒙罗维亚西点的检疫隔离中心发生了骚乱。一群示威者大肆破坏以示对政府及医护人员的不满,他们称此次爆发乃当局的凿空之论。不少正受医疗监护的病人(连带沾有鲜血的床上用品)逃脱,为疫情雪上加霜。[133]
2014年8至11月期间,刚果民主共和国第七度爆发埃博拉出血热,地点为赤道省博恩区。疫情最终在世卫及联合国儿童基金会等各方的致力帮助下得到控制。[134]此次爆发与西非疫症无直接关系。[135]
自2018年8月疫情暴发以来,已报告超过3000例埃博拉病例,其中超过2000人死亡。到目前为止,疫情主要集中在东部的 North Kivu 和 Ituri 省,但最近它传播到了靠近卢旺达边境的Goma市,该市有近200万人口,属于地区交通枢纽,每天有1.5万人穿过边界从 Goma 进入卢旺达。该市还有国际航班。WHO总干事 Tedros Adhanom Ghebreyesus 博士2019年7月18日宣布,刚果民主共和国的埃博拉疫情为国际突发公共卫生事件。[136]
受到西非疫症的影响,其他地区亦相继出现零星个案。英国有一名护士染病,后在伦敦皇家自由医院的高危隔离病房接受诊治,并成功康复。[137]美国与西班牙分别出现四宗(其中一人死亡)及一宗的境外移入案例,患者均为医护人员。在严格的医疗监控下,病毒没有进一步扩散。[138]
2018年5月,刚果民主共和国西北部赤道省比科罗镇及周边地区暴发新一轮埃博拉疫情,累计疑似病例45例,其中14例确诊,25人死亡。世卫组织将疫情在刚果民主共和国全国传播的风险评估等级从“高”级别提升至“非常高”,地区传播风险等级由“中等”提升至“高”[139]。
2018年爆发,截至2019年7月17日累计病例2896例、累计死亡人数1698人,目前持续发生。2019年7月17日世卫组织列为“国际关注的突发公共卫生事件”(Public Health Emergency of International Concern, PHEIC)
2020年6月1日,刚果民主共和国爆发新一轮埃博拉疫情,但总体严重程度低于同时期爆发的2019冠状病毒病疫情。[140]
2022年9月20日,乌干达中部穆本德区的一名死者被检出埃博拉-苏丹病毒株,这是十多年来首次在乌干达发现埃博拉-苏丹病毒株,此轮埃博拉疫情约从9月初左右开始蔓延,截至2022年9月25日[update],本轮疫情已导致16人确诊感染,另有18人疑似感染[141]。
社会文化议题
埃博拉病毒属的所有成员均被归入第四类生物危险品及美国疾病预防控制中心的甲级生物恐怖主义范畴[58][142];此类病毒具备成为生物武器的潜能[143][144],但因无法长久逗留于空气中而难以成为大规模杀伤性武器[145]。不过,前苏联生化武器研究部副主任肯·阿里贝克相信,埃博拉能与天花结合,成为一种具有大杀伤力及高传染性的基因重组病毒。[146]
过去数十年来,多部畅销小说及电影著作均以埃博拉出血热为题,以戏剧化或写实的方式叙述不同年份的爆发。[147][148][149]西非疫症期间,多部以电子或印刷书籍形式对外发表的私人著作,含有误导成分。世卫及联合国批评有关资讯助长了疾病的流行。[150]
其他动物
科学家自本世纪初起,密切监察着其他动物的疫情,希望能尽量预防人类感染个案。[152]
埃博拉病毒对其他灵长动物同样致命。[153]2002至2003年间,在一个名为“Lossi”的保育区,埃博拉疫症使每420平方公里的黑猩猩跟踪率下降了88%。[154]这些动物染病的主因是进食了受污染的肉类,而非为相互触摸或触碰到尸体。[155]雷斯顿病毒于初次亮相时,夺取了不少实验室猴子的性命。1989年末,隶属黑泽尔顿科研产品公司(Hazelton Research Products)的雷斯顿检疫区中,一群由菲律宾运来的食蟹猕猴罹患神秘致命疾病,并被误诊为感染猴出血热病毒。动物病理学家后将活组织样本,寄给了位于马里兰德特里克堡的美国陆军传染病医学研究院。酶联免疫吸附试验的结果证实了此样本含有针对埃博拉病毒的抗体[156],结果与电子显微镜映像相乎[157]。尚未因病致死的猴子被人道毁灭,尸体交由德特里克堡的病理及病毒学家研究,最终被安全弃置。[156]178名曾接触这些猴子的工作人员中,有6位出现血清转换的现象(即其血清被检测到抗体,却并无出现任何症状)。[158][61]最后,研究人员独立出一种出现于亚洲、名为“雷斯顿病毒”的新型埃博拉病毒种。[156]美国疾病预防控制中心总结,雷斯顿种虽与其他埃博拉病毒共被归入第四类生物危险品,但它对人类的致病性不高。[159]
埃博拉病毒也出现于其他种类的动物身上。雷斯顿病毒曾感染了宾夕法尼亚州、德克萨斯州及意大利的猪只。[46]虽然一项于2012年进行的实验证实了这类病毒能在没有接触的情况下,从猪扩散至其他灵长动物身上,但该测试无法证明病毒能以同样的方式,于灵长动物间传播。[160] 在非洲,犬只经常进食或含有埃博拉病毒的腐肉,但甚少出现病症。一项2005年的测试显示,出现在埃博拉爆发地的狗对模式种病毒的血清阳性率为30%,但处于较远地区的则为9%。[161]另外,羚羊也是主要的带病动物。[100]
世卫建议使用次氯酸钠(即漂白水)或其他适当的清洁剂定期消毒农场,并隔离任何疑似感染个案,以防病毒传染至其他动物群体。[1]
科研概论

目前尚未有安全、可供广泛使用的埃博拉出血热治疗药物或预防疫苗,各个方向的科研项目仍在进行之中。
多种药物均具备治疗埃博拉出血热的潜质,当中以抗病毒及抗体药物为主流的研究对象。获日本官方批准存货的法匹拉韦在老鼠身上取得理想成效。[15][162]美国 BioCryst 药厂研发的广谱分子“BCX4430”及“Brincidofovir”亦为候选者之一:前者获美国陆军传染病医学研究所承认其动物测试结果[163];而后者则获美国食物安全中心批准进入临床试验程序[164]。一名利比里亚医生在2014年9月,以原本用于抑制艾滋病病毒的药物拉米夫定辅以抗生素(针对机会性细菌感染)及静脉注射,治愈了15名埃博拉病人中的13人。[165]由于不肯定因素过多及样本量太少,病毒学家对此疗法表示怀疑;美国国立卫生研究院亦未能于初步体外试验中证实其功效,但表示会继续研究。[166]由中国四环医药公司及军事医学院研制了“JK-05”,宣称通过动物测试且进入临床试验阶段。[167]除此,研究者一叩洪钟,向其他种类的抗病毒物质着手。[168][169]一些天然化合物(如:“Scytovirin”及“Griffithsin”)[170][171]、合成药(“DZNep”、“FGI-103”、“FGI-104”、“FGI-106”、“dUY11”与“LJ-001”)[172]、不同组合性生化物质均包括在内[173]。名为“ZMapp”的实验性、含三种单克隆抗体的药物于猕猴身上取得成效。[174][175]。美国卫生及公共服务部促请多个研究中心加快生产,以备不时之需。[176]有泰国研究团队宣布成功以病毒合成片段制成了一种抗体药物。世卫及美国国立卫生研究院已经安排测试,惟此药物仍有待改进。[177]原用以治疗不育及乳癌的克罗米芬及托瑞米芬亦见有效[178],它们分别治愈了90%及50%的实验白鼠[178]。2014年的一项体外测试发现,用以治疗心律失常的粒子通道阻滞药胺碘酮能阻止埃博拉病毒进入细胞。[179]
反译治疗的技术同样获得关注。针对埃博拉病毒(模式种)的核糖核酸聚合酶L蛋白,短干扰核糖核酸及吗啉基两种化学物质于其他灵长动物身上起到治疗的功效。[180][181]现处于第一临床试验阶段的实验性药物“TKM-Ebola”便含有短干扰核糖核酸的成分。[174][182]由美国研发的萨雷普塔治疗则已经通过第一期临床试验的阶段。[183]
1999年六月的刚果民主共和国爆发,8个被感染的病人被输入了康复者的血液,当中有7人痊愈。[184],但此治疗方法具有争议性[185]。静脉注射免疫球蛋白获证实能在非人类灵长动物身上能抵御埃博拉病毒。[186]
2019年底前未有人类预防疫苗被批准上市。[1][187][91]去氧核糖核酸疫苗[188]及以提取腺病毒[189]、水疱性口膜炎病毒[190][191][192]或丝状病毒粒子[193]而制成的疫苗于其他灵长动物身上见效。[194][195][196]埃博拉刺状蛋白-腺病毒媒介疫苗在食蟹猕猴身上取得过更快的免疫功效。[189]两年后,一种埃博拉(或马尔堡)混合水疱性口膜炎病毒的减毒重组疫苗同样保护了非人类灵长动物。[197][198][199]2011年12月6日,一种成功在老鼠身上建立抗埃博拉免疫能力的疫苗面世。与众不同的是,这种新制成品能以冷冻干燥法长时间储存,以待疫症的爆发。[200]虽说已有部分疫苗进入了人类测试阶段[194],但因受到风险监控而不能与实际的感染情况同日而语[201],故仍未能确定它们的实际功效。
位于温尼伯的加拿大国家微生物学实验室特殊病原体部研究的埃博拉疫苗rVSV-ZEBOV;研制工作获得过加拿大一个打击生物恐怖主义的国防项目200万美元的经费赞助。2014年至2016年西非三国埃博拉疫情的末期即2015年3月7月在几内亚开始III期临床试验,结果免疫效果显著,只接种一剂疫苗的五千多人随后均无感染病例。2015年7月31日,相关试验结果发表在《柳叶刀》杂志上。2016年12月,多个机构的科学家联合在《柳叶刀》(Thelancet)发表文章,公布对这款疫苗进行试验的结果:疫苗对出现症状未超过10天的患者100%有效。2019年11月11日,欧盟宣布这款埃博拉疫苗(现称为默沙东减毒活疫苗Ervebo)获得上市许可,成为全球首款正式获批上市的埃博拉疫苗。2019年12月21日,美国FDA便批准了这款名为Ervebo的减毒活疫苗在美国上市。[202]
附注
参考文献
外部链接
Wikiwand - on
Seamless Wikipedia browsing. On steroids.


