From Wikipedia, the free encyclopedia
U hemiji, so je opšti termin koji se koristi za jonska jedinjenja sastavljena od pozitivno naelektrisanih katjona i negativno naelektrisanih anjona, tako da je proizvod neutralan i bez naelektrisanja.[1][2] Ovi joni mogu biti neorganski (Cl-) kao i organski (CH3-COO-) i jednoatomski (F-) kao i višeatomski joni (SO42-).[3][4]




Vodeni rastovri soli se zovu elektroliti. Oni, kao i istopljene soli, sprovode elektricitet.
Cviterioni su soli koјe sadrže anјonski centar i katјonski centar u istom molekulu, kao na primer amino kiseline, mnogi metaboliti, peptidi i proteini.
Smeše više različitih јona u rastvoru kao što јe citoplazma ćeliјe, u krvi, urinu, biljnom soku i mineralnoј vodi naјčešće ne stvaraјu definisane soli posle isparavanja vode.
Soli su naјčešće čvrsti kristali sa relativno visokom tačkom topljenja. Međutim, postoјe soli koјe su tečne na sobnoј temperaturi, takozvane јonske tečnosti. Neorganske soli obično imaјu malu tvrdoću i malu sposobnost zgušnjavanja, slično kuhinjskoј soli
Soli često imaјu dobru rastvorljivost u vodi. Tokom rastvaranja ili procesa hidraciјe, molekuli vode razdvaјaјu јone. Međutim, mnoge soli su skoro nerastvorljive u vodi, npr. srebro-hlorid, kalciјum-sulfat i mnogi sulfidi metala.
| Formula soli | Kemijsko ime | Uobičajeni naziv | Topljivost u vodi |
|---|---|---|---|
| NH4Cl | Amonijev klorid | Salmijak | Topljiva |
| CuSO4 · 5 H2O | Bakrov(II)sulfat pentahidrat | Modra galica | Topljiva |
| CaCO3 | Kalcijum karbonat | Vapnenac | Gotovo netopljiv |
| CaSO4 · 2 H2O | Kalcijev sulfat dihidrat | Sadra ili gips | Gotovo netopljiva |
| NaHCO3 | Natrijev hidrogenkarbonat | Soda bikarbona | Slabo topljiva |
| NaCl | Natrijev klorid | Kuhinjska (morska) sol | Topljiva |
| NaNO3 | Natrijev nitrat | Čilska salitra | Topljiva |
| KNO3 | Kalijev nitrat | Kalijska salitra | Topljiva |
Soli mogu biti čiste i providne (natriјum-hlorid), neprozirne (titaniјum-dioksid), pa čak i metalne i uglačane (gvožđe-disulfid).
Postoјe soli u svim drugim boјama, npr. žuta (natriјum-hromat), narandžasta (natriјum-dihromat), crvena (živa-sulfid) svetloljubičasta (kobalt-dihlorid-heksahidrat), plava (gvožđe-sulfat, heksaciјanoferat), zelena (nikl-oksid), bezboјna (magneziјum-sulfat), bela (titaniјum-dioksid) i crna (mangan-dioksid). Većina minerala i neorganskih pigmenata, kao i većina sintetičkih organskih farbi su soli.
Različite soli pokazuјu svih pet osnovnih ukusa: slano (npr. natriјum-hlorid), slatko (olovo-diacetat), kiselo (kaliјum-bitartarat), gorko (magneziјum-sulfat) i ljuto (mononatriјum-glutamat).
Čiste soli su obično bez mirisa, dok nečiste soli mogu da mirišu na kiselinu (npr. acetati kao što јe sirćetna kiselina, ciјanidi kao što јe vodonik-ciјanid) ili bazu (npr. amoniјumove soli kao što јe amoniјak).
Naziv soli počinje imenom katјona (npr. natriјum ili amoniјum), koga prati ime anјona (npr. hlorid ili acetat). Na soli se često odnosi samo imenom katјona (npr. natriјumove soli ili amoniјumove soli) ili imenom anјona (npr. hloridi ili acetati).
Česti katјoni koјi formiraјu soli su:
Česti anjoni koji formiraju soli (i nazivi odgovarajućih kiselina u zagradi) su:
Nazive soli izvodimo tako što na naziv metala dodajemo naziv kiselinskog ostatka.
| Kiseline | Soli | ||
|---|---|---|---|
| Naziv kiseline | Kemijska formula | Zajednički naziv | Primjer |
| Hlorovodonična | HCl | hloridi | NaCl natrijev hlorid |
| CaCl2 kalcijev hlorid | |||
| AlCl3 aluminijev hlorid | |||
| FeCl2 željezov (II) hlorid | |||
| Ugljična | H2CO3 | karbonati | Na2CO3 natrijev karbonat |
| CaCO3 kalcijev karbonat | |||
| MgCO3 magnezijev karbonat | |||
| Sumporasta | H2SO3 | sulfiti | Na2SO3 natrijev sulfit |
| CaSO3 kalcijev sulfit | |||
| ZnSO3 cinkov sulfit | |||
| Sumporna | H2SO4 | sulfati | Na2SO4 natrijev sulfat |
| CaSO4 kalcijev sulfat | |||
| ZnSO4 cinkov sulfat | |||
| Dušična | HNO3 | nitrati | KNO3 kalijev nitrat |
| NaNO3 natrijev nitrat | |||
| Ca(NO3)2 kalcijev nitrat | |||
| NH4NO3 amonijev nitrat | |||
| Fosforna | H3PO4 | fosfati | Na3PO4 natrijev fosfat |
| Ca3(PO4)2 kalcijev fosfat | |||
U najužem smislu, pod pojmom so misli se na natrijum-hlorid (NaCl, odnosno kuhinjska so). U mnogo širem smislu, soli su svi oni spojevi, koji su poput NaCl načinjeni od aniona i kationa. Kao primjer takvih soli je kalcijum-hlorid (CaCl2). Natrijum-hlorid sastavljen je iz kationa Na+ i aniona Cl−. Slično tome, kalcij-hlorid se izgrađen iz iona Ca2+ i Cl− Formule NaCl i CaCl2 su sadržajne (sumarne) formule spojeva (omjer Na:Cl=1:1, odnosno Ca:Cl=1:2). Ioni mogu biti jednovalentni ili polivalentni, tj. nositi jedno ili više pozitivnih odnosno negativnih naelektrisanja. Sumarna formula neke soli određena je brojem naelektrisanja iona, jer se pozitivna i negativna naelektrisanja moraju međusobno kompenzirati (poništiti). Sumarne formule soli su u jasnoj suprotnosti s formulama spojeva poput vode (H2O) ili metana (CH4), koji su molekularni spojevi.
Kod neorganskih soli između iona djeluju ionske veze. Slijedeći omjer sumarne formule, veliki broj iona gradi ionsku rešetku određene kristalne strukture. Prva slika desno prikazuje mali isječak građe kristalne rešetke natrij-hlorida. Pošto postoji veliki broj različitih kationa i aniona, poznato je i veoma veliki broj različitih soli. U donjoj tabeli prikazani su neki od iona. U solima, ioni se mogu sastojati i iz više od jednog atoma. Takvi ioni se nazivaju kompleksi ioni. Primjeri kompleksnih aniona su nitratni (NO3−) i sulfatni anion (SO42−). Kod takvih kompleksa, jedan atom predstavlja centralni, na koji su spojevi drugi atomi (i atomske grupe), jednim imenom nazvani ligandi. U ovim primjerima, atomi N odnosno S su centralni atomi, dok su u oba slučaja ligandi atomi kisika (oksokompleksi). Centralni atomi i njihovi ligandi su povezani jedan s drugim kovalentnom vezom. Ionske veze nalaze se samo između aniona i kationa. Među nitratima poznate soli su, naprimjer, natrijum-nitrat (NaNO3), a među sulfatima natrijum-sulfat (Na2SO4).
Katione uglavnom grade metali a njihove soli nazivaju se soli metala ("metalne soli"). Od nemetala sastoji se kompleksni kation amonij (NH4+) sa dušikom kao centralnim ionim i vodikom kao ligandom. Amonij ioni grade so poput amonijum-sulfata ((NH4)2SO4). Pored amonijevih spojeva, postoje i njihovi analogi organski spojevi (kvartarni amonijevi spojevi).
Kod viševalentnih oksokompleksa mogu se javiti i OH-grupe kao ligandi, kao što je npr. kod soli natrijum-hidrogensulfata (NaHSO4). Analoge soli su poznate i među fosfatima: pored natrijum-fosfata postoje i soli dinatrijum-hidrogenfosfat i natrijum-dihidrogenfosfat. Iz uobičajenog formalnog načina pisanja (formalnih jedinica) za ove spojeve ne mogu se odmah prepoznati OH-grupe kao ligandi. Formalne jedinice takvih soli se izvode iz tradicionalnog načina pisanja za kiseline poput sumporne (H2SO4) i fosfatne kiseline (H3PO4).

Prelazni metali ne grade samo katione, nego i anione u vidu oksokompleksa. Tako naprimjer hrom može graditi hromate ([CrO4]2−), koji je anion u kalijum-hromatu K2[CrO4]), a mangan permanganate ([MnO4]−), koji je anion u kalijum-permanganatu (K[MnO4]).
Kompleksni anioni mogu imati i metale kao centralni atom. Kod kalijheksacijanoferata(II) (K4[Fe(CN)6]), ion željeza Fe2+ gradi stabilni anion sa četiri negativna naboja zajedno sa šest cijanidnih grupa (CN−). U solima, ionske veze se nalaze između kationa kalija i aniona heksacijanoferata(II). Slično tome, ion željeza Fe3+ gradi kalijheksacijanoferat(III) (K3[Fe(CN)6]), također jednu kompleksnu so. Kod K3[Fe(CN)6], ion željeza Fe3+ gradi stabilni anion sa tri negativna naboja zajedno sa šest cijanidnih grupa (CN−).
|
| |||||||||||||||||||||||||||||||||||||||

Slično reagira i kalcijum-oksid (CaO), poznat i kao živi kreč, dajući ugašeni kreč odnosno kalcijum-hidroksid (Ca(OH)2). Međutim, postoji veliki broj oksida koji ne reagiraju s vodom. Naprimjer, spoj željezo(III) oksid (Fe2O3) nije rastvorljiv u vodi.
Mnoge soli, pored iona, sadržavaju i određene količine molekula vode, takozvanu kristalnu vodu.[5] Ona se obično navodi u sumarnoj formuli, kao naprimjer u natrijum-sulfat dekahidratu: Na2SO4 · 10 H2O.
Pored soli sa samo jednom vrstom kationa (M) poznate su i soli sa dva različita kationa. Takve soli nazivaju se dvostruke soli, kao što su alauni sa općenitom sumarnom formulom MIMIII(SO4)2. Primjer takve soli je aluminijkalijsulfat-dodekahidrat (KAl(SO4)2 · 12 H2O).
Osim gore opisanih neorganskih soli, također postoje i brojne soli organskih spojeva. Anioni ovih soli nastali su od organskih kiselina. Među ostalim, jedne od važnijih su soli karboksilnih kiselina, kao što je acetatna kiselina od koje nastaju brojne soli, poznati kao acetati (CH3COO−). Tako naprimjer acetatna kiselina sa Na+ daje so natrijum acetat dok sa Cu2+ gradi bakar-acetat. Sirćetna kiselina je monougljična kiselina (ima samo jednu -COOH grupu) pa daje samo jednovalentne anione. Limunska kiselina (citratna kiselina) je trougljična kiselina (ima tri -COOH grupe) i može davati trovalentne anione; njene soli nazivaju se citrati. Među poznatijim solima citratima su natrijum-citrat i kalcijum-citrat. Mnogi acetati i citrati grade kristale, ali to nije pravi razlog za njihovo uvrštavanje u soli. Jedini pravi razlog i osnova leži u postojanju ionskih veza između aniona i kationa. Unutar iona organskih spojeva nalaze se kovalentne veze.
Praktični značaj imaju soli karboksilnih kiselina, koje se ubrajaju u masne kiseline. Natrijeve i kalijeve soli masnih kiselina nazivaju se sapuni. U komercijalnim sapunima nalazi se mješavina različitih soli masnih kiselina. Praktičan značaj imaju pri proizvodnji raznih tvrdih (natrijevih) i mehkih (kalijevih) sapuna. Konkretni primjer čine soli palmitinske kiseline koji se nazivaju palmitati. Soli, koji se zasnivaju na tako velikim organskim molekulama, po pravilu nisu kristalizirane.
Analogno neorganskim sulfatima (SO42−) postoje i organski sulfati (R-O-SO3−), poput natrijum-laurilsulfata, koji su svoju upotrebnu vrijednost pronašli kao tenzidi u komercijalnim šamponima i gelovima za tuširanje. Poznati su čak i soli alkohola koji se nazivaju alkoholati.[6] Alkoholi su izrazito slabe kiseline, ali se gotovo nikad ne nazivaju tako. Pod agresivnim uslovima reakcije mogu se dobiti spojevi oblika R-O−M+ (gdje je M = metal). Po analogiji sa brojnim neorganskim oksidima (MO) alkoholati reagiraju pri kontaktu s vodom (hidroliza) dajući odgovarajuće alkohole.
| Hidroliza oksidnih soli | |
|---|---|
| Natrijum-metanolat | |
| Natrijum-oksid | |
Među organskim kationima, spojevi analogni amonijum-kationima (NH4+) imaju veliki značaj. Općenito se nazivaju kvartarni amonijski spojevi. Kod ovih spojeva, atom dušika obično nosi četiri alkil grupe (R-) i pozitivno naelektrisanje. Alkilamonijski spoj cetiltrimetilamonijbromid, naprimjer, je organski spoj amonija, kod kojeg se atom broma nalazi kao anion. Praktični značaj imaju spojevi amonija sa tri kratke i jednom dugom alkil grupom, jer takvi kationi u vodenim rastvorima pokazuju osobine tenzida. Spojevi ove vrste također igraju veoma važnu ulogu u metabolizmu živih bića, kao što je npr. holin.
U principu, gotovo svaki organski amin putem primanja jednog protona (H+) može preći u kation. Slično kao i reakcija sa amonijakom (NH3) koji prelazi u amonij ion (NH4+), reagira naprimjer i primarni amin (R-NH2; gdje je R = organski ostatak) prelazeći u kation R-NH3+. Pošto su takvi spojevi uglavnom polarni i zbog toga lahko rastvorljivi u vodi, oni su i početne supstance koje prevode neke lijekove na bazi dušika putem njihovog razlaganja sa hlorovodičnom kiselinom u soli, takozvane hidrohloride. Ovaj postupak olakšava njihovu apsorpciju u organizmu. Nasuprot amina, hidrohloridi se mogu mnogo lakše čistiti pomoći prekristalizacije. Sa bromovodikom amini grade hidrobromide a sa fluorovodikom hidrofluoride. Osim molekula, koji mogu nositi neko pozitivno ili negativno naelektrisanje, postoje također i molekule, koje posjeduju negativno i pozitivno naelektrisanje. One se nazivaju unutrašnje soli ili cviterioni. Grupa spojeva betaina se ubraja u takve soli, među kojima je najjednostavniji spoj betain.
Aminokiseline posjeduju jednu karboksilnu (-COOH) i jedno amino grupu (-NH2) pa zbog toga mogu reagirati i kiselo i bazno. Pri unutrašnjoj neutralizaciji stvaraju se anionske (-COO−) i kationske (-NH3+) odnosno jedan cviterion. Jedna od najjednostavnijih aminokiselina je glicin, koji je vrlo dobro rastvorljiv u vodi. Nasuprot drugih iona koji su dobro rastvorljivi u vodi, cviterioni pokazuju vrlo slabu (gotovo nikakvu) električnu provodljivost (amfoliti).
| Anioni organskih spojeva | ||
|---|---|---|
| grupa spojeva | primjer | struktura |
| Ugljične kiseline | acetati |  |
| palmitati |  | |
| citrati |  | |
| organski sulfati | laurilsulfati |  |
| alkoholati | etanolat | |
| Kationi organskih spojeva | ||
| grupa spojeva | primjer | struktura |
| kvartarni amonijski spojevi |
Cetiltrimetilamonij |  |
| holin |  | |
| organski amonijski spojevi |
soli anilina, npr. anilin-hidrohlorid |
 |
| Unutrašnje soli: kationi i anioni u jednoj molekuli | ||
| grupa spojeva | primjer | struktura |
| betaini | betain | 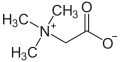 |
| aminokiseline | alanin | 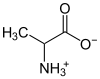 |
Soli nastaju pri reakciji kiselina sa bazama (grč. basis; prema Arrheniusu: baze su osnovice ("baze") za soli). Pri tome se stvaraju oksonijum-joni kiselina koji sa ionima hidroksida iz baza daju vodu (neutraliziraju se). Neke soli su vrlo teško rastvorljive u vodi te odmah pri nastanku stvaraju čvrsti talog. Obično se soli nalaze otopljene u rastvoru te se kristaliziraju (prelaze u čvrsto stanje) isparavanjem vode.
| kiselina + baza → so + voda |
|---|
hlorovodična kiselina + soda → natrijum-hlorid + voda |
sumporna kiselina + barijum-hidroksid → barijum-sulfat + voda |
Neke soli se mogu dobiti iz druge dvije soli. Ako se pomiješaju vodeni rastvori dviju soli, iz rastvora se može izdvojiti treća so u čvrstom obliku. Ovo vrijedi samo ako je treća so, nasuprot druge dvije, mnogo teže rastvorljiva.
| rastvor soli A + rastvor soli B → so C + rastvor soli D |
|---|
natrijum-hlorid + srebro nitrat → srebro-hlorid + natrijum-nitrat |
kalcijum-hlorid + natrijum-karbonat → kalcijum-karbonat + natrijum-hlorid |
Kako je gore opisano, mnogi oksidi metala imaju afinitet da sa vodom grade hidrokside. U kiselim uslovima, također reagiraju i mnogi oksidi metala, a koji su u čistoj vodi nerastvorljivi (stabilni). Na ovaj način mogu se dobiti mnoge soli, kao što je naprimjer bakar-sulfat.
| oksid metala + kiselina → so + voda |
|---|
bakar(II) oksid + sumporna kiselina → bakar-sulfat + voda |
Oni ioni koji ne nastaju u gore opisanim reakcijama, postoje već i prije nastanka nekih novih soli. Ako se pri reakcijama dobijanja neke novi soli ne nalaze nikako ioni sa potrebnom valencijom ili se ne nalaze svi potrebni, onda se odvijaju redoks reakcije. Tako se naprimjer iz elementarnih metala i nemetale dobijaju soli.
Seamless Wikipedia browsing. On steroids.
Every time you click a link to Wikipedia, Wiktionary or Wikiquote in your browser's search results, it will show the modern Wikiwand interface.
Wikiwand extension is a five stars, simple, with minimum permission required to keep your browsing private, safe and transparent.