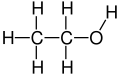
Etanol
sebatian kimia alkohol From Wikipedia, the free encyclopedia
Etanol (juga dipanggil etil alkohol, alkohol bijian, alkohol minum (beer, wine, whisky, spirit), atau hanya alkohol) merupakan kandungan alkohol utama yang terkandung dalam minuman alkohol, yang dihasilkan melalui proses penapaian gula dengan menggunakan yis. Etanol mampu menyebabkan kemabukan. Selain itu, etanol juga digunakan sebagai pelarut, antiseptik, bahan api fosil dan cecair aktif dalam termometer raksa.
| |||
| |||
| Nama | |||
|---|---|---|---|
| Nama IUPAC sistematik
Ethanol[1] | |||
| Pengecam | |||
Imej model 3D Jmol |
|||
| ECHA InfoCard | 100.000.526 | ||
CompTox Dashboard (EPA) |
|||
| |||
| |||
| Sifat | |||
| C2H6O | |||
| Jisim molar | 46.07 g·mol−1 | ||
| Ketumpatan | 0.789 g/cm3 (dalam 25°C) | ||
| Takat lebur | −114 °C (−173 °F; 159 K) | ||
| Takat didih | 78.37 °C (173.07 °F; 351.52 K) | ||
| Keasidan (pKa) | 15.9 (H2O), 29.8 (DMSO)[2][3] | ||
| Bahaya | |||
| Takat kilat | 16 °C (61 °F; 289 K) | ||
Suhu autopenyalaan |
365 °C (689 °F; 638 K) | ||
| Dos maut (LD) atau kepekatan dos maut (LC) | |||
LD50 (median dos) |
7060 mg/kg (oral, tikus)[4] | ||
| Sebatian berkaitan | |||
Kecuali jika dinyatakan sebaliknya, data diberikan untuk bahan-bahan dalam keadaan piawainya (pada 25 °C [77 °F], 100 kPa). | |||
| pengesahan (apa yang perlu: /?) | |||
| Rujukan kotak info | |||
Etanol merupakan cecair tidak berwarna yang meruap dan mudah terbakar dengan struktur formula CH3CH2OH, yang sering disingkatkan sebagai C2H5OH atau C2H6O. Etanol juga boleh ditulis sebagai EtOH, Et merujuk kepada kumpulan etil, C2H5−.
Penamaan
Etanol ialah nama sistenamik yang ditakrifkan mengikut piawaian IUPAC; Et- menandakan kumpulan alkil dengan dua atom karbon; -an- menandakan ikatan tunggal di antara dua atom karbon tersebut, dan -ol menandakan kumpulan berfungsi hidroksil, -OH.[5]
Nama etanol adalah berdasarkan keputusan yang dibuat dalam Persidangan Tatanama Kimia Antarabagnsa pada April 1892 di Geneva, Switzerland.[6]
Sejarah
Manusia pada zaman purba telah mengenali etanol sebagai suatu bahan yang beracun. Sisa-sisa pada tembikar berusia 9,000 tahun dari China membuktikan bahawa manusia Zaman Neolitik minum minuman beralkohol.[7] Bukti-bukti berkenaan cara penghasilan minuman beralkohol juga ditemui pada artifak Dinasti Ketiga Mesir serta tablet tamadun Mesopotamia.[8]
Proses penyulingan etanol berjaya dilakukan oleh tamadun Islam pada abad kesembilan oleh ahli-ahli kimia seperti Al-Kindi dan Al-Razi melalui penyulingan wain.[9][10] Proses penyulingan yang dilakukan di Timur Tengah kemudian dibawa ke kawasan Itali dan India pada masa itu seperti Kesultanan Delhi pada abad ke-14.[11][12] Bukti arkeologi menunjukkan proses penyulingan mula dijalankan di China pada abad ke-12 sama ada oleh dinasti Jin atau Song Selatan.[13]
Pada 1796, ahli kimia, Johann Tobias Lowitz memperoleh etanol tulen dengan mencampurkan etanol separa tulen dengan alkali kontang berlebihan lalu disulingkan dengan haba yang sedikit.[14] Pada 1825, etanol berjaya dihasilkan secara sintetik oleh Michael Faraday menerusi penghidratan etilena bermangkinkan asid.
Etanol mula digunakan sebagai minyak pelita di Amerika seawal 1840, tetapi menjadi tidak menguntungkan akibat cukai yang dilaksanakan terhadap alkohol industri ketika Perang Saudara Amerika hingga cukai itu dimansuhkan pada 1906.[15] Etanol mula digunakan sebagai bahan api kenderaan sejak 1908 apabila Ford Model T membenarkan penggunaan bahan api etanol di samping petrol.[16]
Sifat-sifat etanol
Etanol asli ialah cecair jernih yang mudah terbakar dengan takat didih pada 78.5 °C dan takat beku pada -114.5 °C. Takat tigaan etanol ialah 150 K pada tekanan 4.3 × 10−4 Pa. Etanol digunakan sebagai bahan antibeku dan mempunyai bau vodka.
Ketumpatan etanol ialah 789 g/l, iaitu kurang 20% daripada ketumpatan air. Etanol mudah larut dalam air, dan merupakan pelarut yang baik untuk pewangi, cat, dan tinktur. Ini membolehkan perisa ditambah ke dalam etanol semasa proses pembruan (brewing).
Etanol sedikit lebih banyak membiaskan cahaya berbanding air dengan indeks biasan bernilai 1.36242 (jarak gelombang cahaya 589.3 nm dan 18.35 °C).[17]
Etanol ialah pelarut yang larut campur dengan air dan pelbagai pelarut organik seperti asid asetik, aseton, benzena, karbon tetraklorida, kloroform, dietil eter, etilena glikol, gliserol, nitrometana, piridina dan toluena.[17] Sifat berkutub kumpulan OH- membenarkan etanol melarutkan pelbagai jenis sebatian ion.[17] Selain itu, sifat hujung molekul etanol yang tak berkutub membolehkan etanol melarutkan sebatian-sebatian tidak berkutub.
Etanol merupakan asid lemah, lebih lemah daripada air dan membentuk ion etanoat, C2H5O-.
Kewujudan alami
Etanol ialah hasil sampingan proses metabolisme yis, dan oleh itu, boleh ditemui dalam semua habitat yis. Etanol boleh ditemui dalam buah-buahan yang terlebih masak.[18] Etanol juga ditemui di angkasa lepas sebagai bahan yang membentuk suatu lapisan ais pada debu-debu awan antara najam, tetapi cara etanol terhasil di situ masih tidak diketahui.[19]
Penghasilan
Etanol dihasilkan sebagai bahan petrokimia melalui penghidratan etilena atau proses biologi, yakni penapaian gula dengan yis. Pada 2005, Amerika Syarikat dan Brazil bertanggungjawab ke atas lebih 90% penghasilan etanol sedunia dengan jumlah penghasilan sebanyak 29 juta tan.[20]
Penghidratan
Etanol dengan penggunaan industri atau larutan dihasilkan daripada tindak balas penghidratan (penambahan satu molekul air) etilena seperti dalam persamaan di bawah:
- C2H4 + H2O → CH3CH2OH.
Tindak balas ini lazimnya dijalankan dengan mangkin asid, paling lazim ialah asid fosforik.[21]
Sebuah proses yang lama dan sudah lapuk ialah penghidratan etilena secara tidak terus, yakni melakukan tindak balas etilena dengan asid sulfurik pekat untuk menghasilkan etil sulfat lalu mengalami hidrolisis untuk mendapatkan etanol dan asid sulfurik semula. Proses ini pertama kali digunakan dalam industri oleh Union Carbide pada 1930.[22]
Penapaian
Etanol dalam minuman beralkohol dihasilkan melalui proses penapaian. Sesetengah yis seperti Saccharomyces cerevisiae dapat menjalankan tindak balas metabolisme terhadap gula menjadi etanol dan karbon dioksida seperti dalam persamaan kimia di bawah:
Pemprosesan karbon dioksida
Karbon dioksida boleh diturunkan menjadi etanol dengan bantuan mikroorganisma seperti Clostridium ljungdahlii.[23] Selain itu, etanol boleh dihasilkan melalui cara ini secara elektrokimia dalam suhu dan tekanan piawai.[24][25]
Tindak balas
Etanol ialah sejenis alkohol primer, iaitu sebatian alkohol dengan atom karbon yang terikat dengan kumpulan hidroksil juga terikat dengan dua atom hidrogen.
Pengesteran
Dengan mangkin asid, etanol bertindak balas dengan asid-asid karboksilik untuk menghasilkan etil ester dan air:
- RCOOH + HOCH2CH3 → RCOOCH2CH3 + H2O.
Tindak balas ini banyak digunakan dalam industri dan memerlukan pembuangan air daripada hasil tindak balas memandangkan ester boleh bertindak tindak balas dengan asid atau bes untuk mendapatkan semula etanol dan garam, yakni proses penyabunan, tindak balas yang lazim digunakan dalam penghasilan sabun. Etanol juga boleh membentuk ester dengan asid tak organik.
Pendehidratan
Etanol boleh ditindak balas secara pendehidratan (buang satu molekul air) untuk menghasilkan etilena seperti di bawah:[26]
- CH3CH2OH → H2C=CH2 + H2O.
Selain itu, proses ini juga boleh menghasilkan dietil eter:
- 2 CH3CH2OH → CH3CH2OCH2CH3 + H2O.
Tindak balas ini biasanya menggunakan mangkin asid seperti silikon dioksida dan asid sulfurik pekat. Dalam tindak balas ini, dietil sulfat beracun boleh terhasil dalam keadaan tertentu.[27]
Pembakaran
Pembakaran lengkap etanol menghasilkan air dan karbon dioksida seperti di bawah:
- C2H5OH (c) + 3 O2 (g) → 2 CO2 (g) + 3 H2O (c); −ΔHc = 1371 kJ/mol[28] = 29.8 kJ/g = 327 kcal/mol = 7.1 kcal/g,
- C2H5OH (c) + 3 O2 (g) → 2 CO2 (g) + 3 H2O (g); −ΔHc = 1236 kJ/mol = 26.8 kJ/g = 295.4 kcal/mol = 6.41 kcal/g.[29]
Muatan haba etanol ialah 2.44 kJ/(kg·K).
Pengoksidaan
Proses pengoksidaan etanol lazimnya berlaku dalam hati oleh enzim alkohol dehidrogenase. Dalam tindak balas ini, etanol kehilangan atom hidrogen dan menjadi asetaldehid, dan seterusnya menjadi asid asetik, bergantung kepada reagen dan keadaan.[30] Tindak balas ini tidak memiliki kepentingan dalam industri.
Kegunaan
Etanol lazimnya digunakan dalam tiga kegunaan, yakni dalam minuman keras, perubatan dan sebagai bahan api.
Perubatan
Antiseptik
Etanol digunakan dalam ubat sapu perubatan dan pensanitasi tangan antibakteria sebagai antiseptik.[31] Etanol membunuh mikroorganisma dengan menyahaslikan protein dan melarutkan lipid, dan berkesan terhadap kebanyakan bakteria, fungi dan pelbagai jenis virus. Namun begitu, etanol tidak berkesan terhadap spora bakteria.[32]
Larutan etanol yang paling berkesan ialah larutan etanol 70%; etanol tulen boleh menyahaktifkan mikrob tanpa membunuh mikrob tersebut kerana etanol tidak dapat terserap ke dalam membran mikrob secara keseluruhan.[33][34]
Penawar
Etanol mungkin digunakan sebagai penawar bagi keracunan metanol atau etilena glikol.[35][36] Dalam keracunan metanol, etanol membantu menghambat penukaran molekul metanol oleh alkohol dehidrogenase kepada formaldehid yang beracun kerana molekul etanol lebih mudah dan kuat terikat dengan enzim tersebut berbandingkan molekul metanol.[37]

Bahan api
Kegunaan paling utama etanol ialah sebagai bahan api atau bahan tambahan dalam bahan api. Selain bahan api etanol tulen, etanol juga dicampurkan dengan bahan api lain seperti gasohol atau E10 (90% petrol dengan 10% etanol) dan E85 (85% etanol dengan 15% petrol). Etanol juga pernah digunakan sebagai bahan api roket, tetapi kini tidak digunakan berikutan penemuan bahan-bahan api roket yang lebih cekap.[38]
Menurut kumpulan penyokong bahan api etanol, etanol dikatakan mengurangkan pengeluaran karbon monoksida, oksida nitrogen dan zarah-zarah pencemar dari kenderaan.[39] Sebuah kajian menunjukkan bahawa penggunaan campuran biodiesel-petrodiesel menunjukkan pengurangan zarah pencemar udara sebanyak 8%, etanol E85 menunjukkan pengurangan 17% dan etanol selulosa memberikan pengurangan sehingga 64% berbanding dengan petrol tulen.[40] Meskipun begitu, pembakaran etanol dalam enjin pembakaran dalam boleh menghasilkan formaldehid serta terbitan asetaldehid lain.[41]
Bioetanol ialah sejenis bahan api dengan etanol yang diperoleh daripada sumber semula jadi seperti hasil pertanian, dan lazimnya memiliki bahan-bahan sampingan seperti metanol dan alkohol fusel.[42] Penggunaan bioetanol untuk menggantikan bahan api konvensional memiliki perdebatan seperti isu kenaikan harga hasil pertanian dan isu pencemaran dalam proses penghasilan bioetanol.[43][44]
Minuman keras
Etanol ialah molekul lazim dalam minuman keras, dan merupakan dadah psikoaktif paling lazim diambil; etanol bertindak sebagai depresan sistem saraf pusat.[45] Etanol kadangkala ditambah ke dalam sesetengah jenis minuman keras untuk menghentikan penapaian secara serta-merta yang membawa kepada rasa manis.[46][47] Bir "tanpa alkohol" mungkin memiliki sebanyak-banyaknya 0.5% etanol.[48]
Pelarut
Etanol disifatkan sebagai pelarut semesta memandangkan etanol boleh melarutkan sebatian berkutub serta tak berkutub. Takat didih etanol yang rendah juga memudahkan proses pengeluaran etanol daripada suatu campuran. Etanol digunakan dalam cat, pen penanda dan barangan penjagaan diri seperti minyak pewangi.
Kegunaan lain
Etanol juga digunakan sebagai sebatian perantara bagi penghasilan sebatian-sebatian kimia lain seperti dietil eter dan asid asetik. Etanol juga boleh ditukar kepada etilena dengan tujuan seperti penghasilan polietilena.
Pendiang-pendiang di rumah dengan tujuan pemanasan atau perhiasan juga boleh menggunakan etanol.[49] Cecair etanol boleh digunakan sebagai bahan penyejuk ketika menyimpan bahan-bahan yang memerlukan penyimpanan bersuhu rendah. Selain itu, etanol digunakan untuk mengawet makanan.[50]
Keselamatan
Etanol tulen akan merengsa mata dan kulit. Simptom-simptom yang boleh terbit akibat menelan etanol termasuk loya, muntah dan mabuk, manakala pengambilan etanol pada jangka masa lama boleh menyebabkan kerosakan hati. Etanol terbukti membawa kesan terhadap metabolisme lipoprotein, penghasilan kolesterol, dan penghasilan serta perembesan asid hempedu.[51]
Suatu larutan etanol-air boleh bernyala apabila dipanaskan dalam suhu melebihi takat kilat.[52] Bagi larutan etanol 20% jisim, takat kilat ialah kira-kira 25 °C. Takat kilat etanol tulen ialah 13 °C,[53] tetapi boleh sedikit terpengaruh dengan keadaan-keadaan atmosfera seperti tekanan dan kelembapan. Campuran etanol boleh bernyala di bawah suhu bilik.
Rujukan
Pautan luar
Wikiwand - on
Seamless Wikipedia browsing. On steroids.