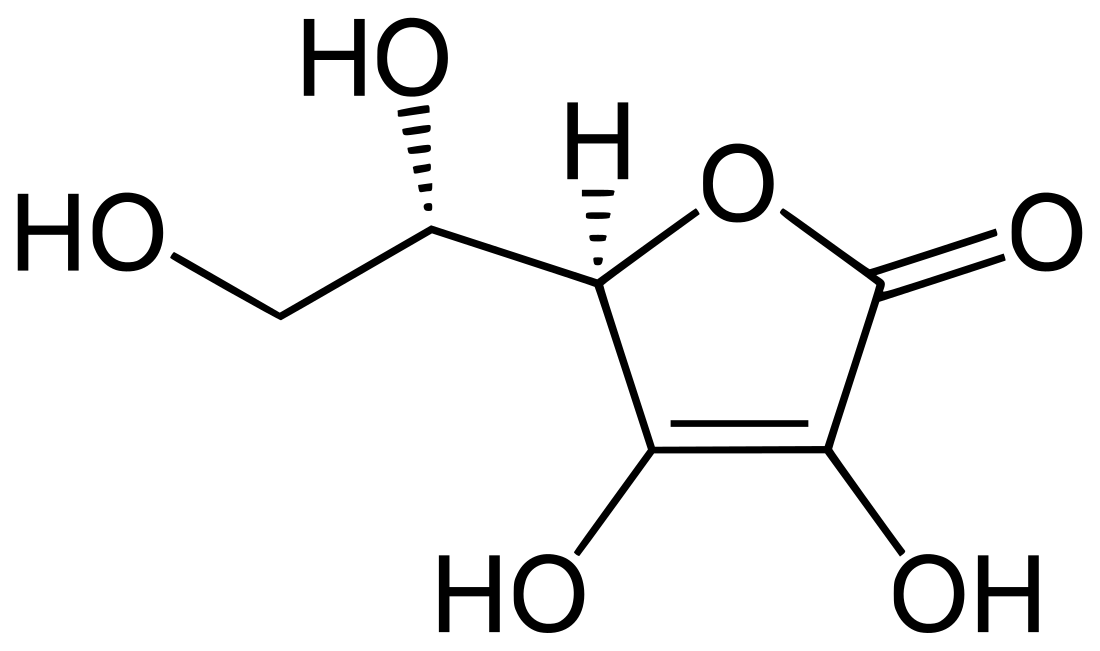
Acido ascorbico
vitamina Da Wikipedia, l'enciclopedia libera
L'acido L-ascorbico, acido ascorbico, principio antiscorbutico o semplicemente vitamina C, è un composto chimico di formula C6H8O6 che in condizioni normali si presenta come una polvere cristallina di colore tra il bianco e il giallo pallido dal gradevole gusto acido e quasi completamente inodore.[3]
| Acido ascorbico | |
|---|---|
 | |
 | |
| Nome IUPAC | |
| 5R-(1S,2-diidrossietil)-3,4-diidrossifuran-2(5H)-one | |
| Nomi alternativi | |
| Vitamina C | |
| Caratteristiche generali | |
| Formula bruta o molecolare | C6H8O6 |
| Massa molecolare (u) | 176,12 |
| Aspetto | solido giallo o bianco |
| Numero CAS | |
| Numero EINECS | 200-066-2 |
| PubChem | 54670067 |
| DrugBank | DBDB00126 |
| SMILES | OC[CH](O)[CH]1OC(=O)C(=C1O)O |
| Proprietà chimico-fisiche | |
| Densità (g/l, in c.s.) | 1,650 |
| Costante di dissociazione acida (pKa) a 298,15 K | 4,17 (prima dissociazione) 11,6 (seconda dissociazione) |
| Solubilità in acqua | 330 g/L |
| Coefficiente di ripartizione 1-ottanolo/acqua | -1,6 |
| Temperatura di fusione | 190–192 °C (463–465 K) con decomposizione |
| Indicazioni di sicurezza | |
| Temperatura di autoignizione | 380 °C[1] |
| Frasi H | --[2] |


Storia
Riepilogo
Prospettiva
La sua storia si riallaccia a quella dello scorbuto, una patologia legata a una carenza di questo composto nella dieta. Questa malattia era già descritta nella medicina greca attorno al V secolo a.C. Nel XVI secolo, soprattutto tra le popolazioni marinare, era noto come lo scorbuto potesse essere curato e prevenuto dall'assunzione di verdure e frutta fresca, o dall'estratto di aghi di pino.
Tuttavia la prima prova di ciò venne nel maggio del 1747 da parte di James Lind, un chirurgo della marina reale inglese. Lind sottopose a un esperimento 12 membri dell'equipaggio affetti da scorbuto, dividendoli in sei gruppi da due persone ciascuno. A ogni gruppo fece assumere, oltre alle normali razioni alimentari, un composto particolare: sidro, acido solforico, aceto, spezie ed erbe, acqua di mare, arance e limoni. I risultati ottenuti permisero di dimostrare che effettivamente quest'ultima aggiunta permetteva di prevenire l'insorgere dello scorbuto. Lind pubblicò i risultati di questo studio nel 1753. Nel 1795 la marina inglese stabilì di aggiungere succo di limone o di lime alla dieta dei marinai.
Nel XVIII e XIX secolo venne usato il termine di antiscorbutico per tutti quei cibi che erano in grado di prevenire la comparsa dello scorbuto. Tra essi, oltre ai limoni, alle arance e ai lime, vi sono: i crauti, il cavolo salato, il malto e il brodo portatile. Pare che James Cook per il suo primo famoso viaggio d'esplorazione nel Pacifico abbia utilizzato i crauti.[4][5]
Nel 1912 Casimir Funk, da studi su malattie carenziali, ipotizzò la presenza di composti che denominò vitamine. Sebbene avesse studiato soprattutto il beri-beri, ipotizzò che anche altre malattie, tra cui lo scorbuto, dipendessero da mancanza di specifiche vitamine.
Nel 1921 il composto antiscorbutico venne denominato vitamina C e tra il 1928 e 1933 fu isolato e cristallizzato da Joseph Svirbely e dall'ungherese Albert Szent-Gyorgyi Von Nagyrapolt e, in modo indipendente, da Charles Glen King. Nel 1934 Sir Walter Norman Haworth e Tadeusz Reichstein, in maniera indipendente, riuscirono a sintetizzare la vitamina C. Nel 1937 Szent-Gyorgyi ricevette il Premio Nobel per la medicina per le sue scoperte sui processi biologici di combustione, con particolare riguardo alla vitamina C, e alla catalisi dell'acido fumarico. Lo stesso anno Haworth venne insignito del Premio Nobel per la chimica.
Nel 1955 J.J. Burns scoprì che il motivo per cui alcuni mammiferi, compresa la specie umana, non riescono a produrre autonomamente la vitamina C risiede nella mancanza dell'ultimo enzima della catena metabolica responsabile della sintesi di tale molecola: la L-gulonolattone ossidasi.
Caratteristiche strutturali e fisiche
Dal punto di vista strutturale l'acido l-ascorbico ricade nella classe dei lattoni,[3] si tratta dell'enantiomero L dell'acido ascorbico e l'acido coniugato dell'L-ascorbato.[6] In particolare si tratta di un composto a sei atomi di carbonio correlato al glucosio.[7] Il composto risulta solubile in acqua,[3] insolubile in etere, cloroformio, benzene, etere di petrolio, oli, grassi, solventi grassi,[8] etanolo, glicerolo e propanolo.[9]
| N. donatori di legami a idrogeno | 4 | |
| N. accettori di legami a idrogeno | 6 | |
| N. atomi pesanti | 12 | |
| N. elementi stereogenici | 2 | |
| N. legami ruotabili | 2 | |
| Superficie polare | 107 Ų | |
| Sezione d'urto[11][12] | [M+Na]+ | 141,6 Ų |
| [M-H]- | 127,7 Ų | |
| [M+H]+ | 138,6 Ų | |
| Massa monoisotopica | 176,03208797 u | |
| Densità[10] | 1,65 g/cm3 a 25 °C |
| Gravità specifica[3] | 1,65 |
| Tensione superficiale[13] | 4,039 x 10-2 N/m |
| Potere rotatorio[14] | [α]D/20 tra + 20,5° e + 21,5° (10 % w/v soluzione acquosa) |
| Punto di fusione[10] | 191°C |
| Entalpia di vaporizzazione[13] | 1,487x10+8 J/kmol a 465,.15 K |
| pH[15] | 2,4 - 2,8 |
Abbondanza e disponibilità
L'acido ascorbico viene sintetizzato dagli eucarioti, con l'eccezione nota dei primati e di alcuni altri gruppi animali che hanno perso la funzionalità dell'enzima gulonolattone ossidasi. I procarioti non sintetizzano ascorbato e non necessitano di un apporto di questo composto che viene sostituito da altri.[16]
Presente negli agrumi, in altri frutti e nelle verdure.[17] La cottura può comportare perdita di vitamina (in taluni casi fino al 75%); questa perdita può essere ridotta adottando una cottura che sia il più possibile rapida.[18]
La vitamina C è presente in alcuni alimenti, insieme con bioflavonoidi, soprattutto nei vegetali a foglia verde, peperoni, pomodori, kiwi e negli agrumi, particolarmente concentrata nel frutto di ciliegia amazzonica, l'acerola, e nella rosa canina. La vitamina può perdersi nel caso in cui questi alimenti vengano tenuti all'aria per molto tempo o dentro contenitori di metallo, per esempio di rame.
Sintesi del composto
Riepilogo
Prospettiva
La sintesi dell'acido ascobico inizia dalla sintesi classica di Reichstein - Grüssner inizia con la riduzione del D-glucosio a D-sorbitolo mediante idrogenazione su un catalizzatore di nichel. Segue l'ossidazione microbiologica del D-sorbitolo a L-sorbosio effettuata con A. xylinum. Il trattamento del L-sorbosio con acetone a bassa temperatura in presenza di acido solforico porta alla formazione di 2,3:4,6-di-O-isopropilidene-alfa-L-sorbofuranosio.[19]
La protezione del di-O-isopropilidenile dei gruppi ossidrilici in C-2, C-3 e C-4, C-6 consente un'ossidazione ad alta resa in acido di-O-isopropilidene-2-cheto-gulonico, evitando sovra-ossidazioni o altre reazioni indesiderate. L'ossidazione viene eseguita con permanganato di potassio in soluzione alcalina.
Segue il trattamento dell'acido di-O-isopropilidene-2-cheto-gulonico con acqua calda che produce acido 2-cheto-L-gulonico, il quale viene convertito in acido L-ascorbico mediante riscaldamento in acqua a 100 °C (resa del 20%) oppure per esterificazione e successivo trattamento con metossido di sodio in metanolo seguito da acidificazione con acido cloridrico, ottenendo circa il 70% di acido L-ascorbico. La resa complessiva di acido ascorbico a partire da D-glucosio è pari al 15-18%.[19]
Reattività e caratteristiche chimiche
Riepilogo
Prospettiva
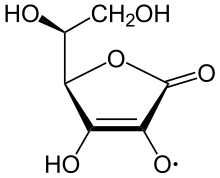
Questa vitamina in condizioni fisiologiche e a pH 7 si trova in forma dissociata, cioè di riducente monoelettrico (ascorbato), questo perché il gruppo - OH enolico legato al C2 dell'anello lattonico, possiede una pKa di 4,2 che lo rende debolmente acido.[20] La capacità dell'ascorbato di donare elettroni gli permette di agire come un agente di eliminazione dei radicali liberi e di ridurre stati di ossidazione più elevati del ferro a Fe²⁺. Queste reazioni costituiscono la base della sua attività biologica, insieme alla relativa stabilità del radicale monodeidroascorbato stabilizzato per risonanza.[16]
Reagisce come un agente riducente relativamente forte e decolora molti coloranti. Forma sali metallici stabili. Incompatibile con ossidanti, coloranti, alcali, ferro e rame. Incompatibile anche con sali ferrici e sali di metalli pesanti, in particolare rame, zinco e manganese.[3]
Grazie alla forte azione riducente la vitamina C è utilizzata in molte reazioni di ossidoriduzione. In particolare la vitamina è in grado di donare un elettrone, formando così l'acido semideidroascorbico che può donare un secondo elettrone, generando così l'acido deidroascorbico. I potenziali redox di queste reazioni sono:
- acido semiidroascorbico/acido ascorbico 0,28 V,
- acido deidroascorbico/acido semiidroascorbico −0,17 V.
Ciò fa della vitamina C un valido donatore di elettroni. L'acido deidroascorbico, il prodotto finale delle reazioni descritte, può venir ridotto da parte della deidroascorbato reduttasi, un enzima dipendente dal glutatione, rigenerando così l'acido ascorbico. Solamente l'enantiomero L è biologicamente attivo. Per la spiccata azione antiossidante della vitamina C e la sua capacità di mantenere stabili le vitamine A, E, l'acido folico e la tiamina, la vitamina C viene utilizzata dall'industria alimentare come additivo nei cibi, come tale o sotto forma di sale sodico, potassico e calcico.
Spettri analitici
Ne sono disponibili i seguenti spettri analitici:
Determinazione analitica
È possibile determinare la quantità di vitamina C in diverse sostanze attraverso l'utilizzo del reattivo di Lugol; la reazione che avviene tra l'acido ascorbico e il reattivo di Lugol è:
Lo iodio ossida con facilità l'acido ascorbico convertendolo in acido deidroascorbico. Nelle analisi quantitative il campione di acido ascorbico viene trattato con una quantità nota di iodio superiore a quella necessaria a ossidare l'intero campione; l'eccesso di iodio non reagito viene quindi retrotitolato con una soluzione a concentrazione nota di tiosolfato di sodio.
Biochimica
Riepilogo
Prospettiva
È un potente agente riducente e antiossidante che agisce nella lotta contro le infezioni batteriche, nelle reazioni disintossicanti e nella formazione di collagene nel tessuto fibroso, nei denti, nelle ossa, nel tessuto connettivo, nella pelle e nei capillari.[17] Funziona come coenzima in diverse vie metaboliche.[7]
Tra i processi più noti in cui la vitamina dovrebbe intervenire ci sono:
- idrossilazione della lisina e della prolina da parte della prolina idrossilasi e della lisina idrossilasi, reazioni importanti per la maturazione del collagene
- idrossilazione della dopamina per formare la noradrenalina
- sintesi della carnitina
- catabolismo della tirosina
- amidazione di alcuni peptidi con azione ormonale
- sintesi degli acidi biliari
- sintesi degli ormoni steroidei per intervento durante le reazioni di idrossilazione
- riduzione dell'acido folico per costruire la forma coenzimatica
- aumento dell'assorbimento di ferro per riduzione del Fe (III) a Fe (II)
- azione di rigenerazione della vitamina E per cessione di un elettrone al radicale α-tocoferossilico.
Inoltre sembra che la vitamina C possa diminuire la formazione di nitrosammine intestinali e ridurre vari composti ossidanti tra cui il radicale superossido, l'acido ipocloroso e i radicali idrossilici. Recenti studi sull'acido ascorbico indicano che può ridurre il tempo di ventilazione nei pazienti in condizioni critiche.[29]
La carenza di vitamina C determina la comparsa dello scorbuto, patologia che riguarda particolarmente l'insufficiente produzione di collagene e di sostanza cementante intercellulare. Ciò determina alterazioni a livello dei vasi sanguigni con comparsa di emorragie, rallentamento della cicatrizzazione delle ferite, gengiviti con alterazioni della dentina, gengivorragie e osteoporosi. Nei bambini si ha anche un arresto della crescita. Le varie emorragie sviluppantesi possono portare anche a un quadro di anemia sideropenica.
Bassi livelli di acido ascorbico sufficienti alla sopravvivenza, ma al di sotto di quelli necessari, sembrano favorire l'aterosclerosi, sia per l'ipotesi ossidativa sia per l'ipotesi risposta alla lesione. Per la scarsità di vitamina C nell'organismo si instaurano situazioni come la progressiva crescita dell'azione devastante dello stress ossidativo e dei radicali liberi sulle pareti cellulari vascolari e/o il progressivo impoverimento e cedimento di collagene nelle pareti cellulari vascolari che venendo tamponato da derivati di alfa lipoproteine produce, col progressivo accumulo, l'aterosclerosi e, di conseguenza, tutte le altre pericolosissime sue patologie derivate a cascata.
Farmacologia e tossicologia
Riepilogo
Prospettiva
Si calcola che la quantità minima di vitamina C necessaria per prevenire lo scorbuto sia di circa 10 mg/die, tuttavia le quantità raccomandate dai sistemi sanitari sono di poco superiori. Anzi, nella comunità scientifica vi è ancora acceso dibattito sul dosaggio efficace effettivo, su limite soglia e sovradosaggio. Le indicazioni sono:
- 30 mg/die per il Codex Alimentarius
- 40 mg/die in Regno Unito (Food Standards Agency)[30]
- 45 mg/die per l'OMS-WHO[31]
- 60 mg/die in Canada[32]
- 75–120 mg/die per gli adulti, 2 g/die come limite di tolleranza: Food and Nutrition Board, Institute of Medicine, National Academy of Sciences, Ministero della Salute, USA.[33]
Farmacocinetica
Sebbene la maggior parte della vitamina C sia completamente assorbita nell'intestino tenue, la percentuale di vitamina C assorbita diminuisce all'aumentare delle concentrazioni intraluminali.[34] Nel plasma la vitamina circola per il 90-95% come acido ascorbico e nel 5-10% come acido deidroascorbico. La vitamina C viene immagazzinata nei tessuti dell'organismo, in particolare nel surrene e nel fegato. La quota plasmatica che non viene immagazzinata viene eliminata con le urine.
Farmacodinamica
Effetti del composto e usi clinici
Viene usato per trattare la carenza di vitamina C, lo scorbuto, la guarigione ritardata delle ferite e delle ossa, l'acidificazione delle urine, nella prevenzione e nel trattamento dell'anemia sideropenica e in generale come antiossidante. È stato anche suggerito che sia un efficace agente antivirale.[7]
Sebbene alcune medicine alternative, come per esempio la medicina ortomolecolare, propongano megadosi di vitamina C come pratica terapeutica, non esistono prove scientifiche in merito e in taluni casi sono anzi controindicate.[35][36][37][38] Poiché la vitamina C diminuisce i livelli di acido urico, il consumo di elevate quantità di questa vitamina potrebbe avere un effetto preventivo verso l'iperuricemia (concentrazione sierica di acido urico > 6 mg/dL) e la gotta.[39]
Tossicologia
I sintomi dell'esposizione a questo composto possono includere irritazione della pelle, degli occhi e delle vie respiratorie. L'ingestione di grandi quantità può causare disturbi gastrointestinali e diarrea. L'esposizione può anche causare la formazione di calcoli renali di ossalato di calcio. Ci sono stati casi di reazione allergica con eczema, orticaria e asma. L'effetto mucolitico di questo composto potrebbe rendere il muco cervicale meno permeabile agli spermatozoi.[3]
Pericoli
Può essere sensibile all'esposizione prolungata alla luce e all'aria. Sensibile all'umidità. È soggetto a degradazione in condizioni anaerobiche. Quando riscaldato fino alla decomposizione emette fumo acre e fumi irritanti.[3]
Controindicazioni ed effetti collaterali
La vitamina C può provocare emolisi nei pazienti con carenza eritrocitaria di G6PD o favismo.[40]
La somministrazione di vitamina C per via orale come forma farmaceutica solida (compresse) è stata associata a danni esofagei dovuti all'acidificazione del pH o della soluzione acquosa in cui è disciolta la compressa o della saliva. Il danno esofageo in genere è risultato transitorio e autolimitante ed è consistito nella formazione di ulcere localizzate che regrediscono dopo la sospensione del farmaco e non causano stenosi.[41][42]
Non esiste una dose letale accertata per l'uomo, esiste invece una LD50 per i ratti che corrisponde a 11,9 grammi per chilogrammo di peso corporeo in una sola dose per via orale. Un uomo medio di 70 kg dovrebbe dunque ingerirne circa 850 g in un'unica soluzione.[43]
Dosi superiori ai 1 g/die di vitamina C, assunte sotto forma di acido ascorbico, possono portare alla presenza di alcuni disturbi come nausea e mal di testa.[44][45] Inoltre secondo alcuni studi sembra che venga aumentata l'eliminazione tramite le urine di ossalati, che potrebbero facilitare la formazione di calcoli renali in un numero limitato di soggetti.[46][47]
Interazioni
Applicazioni
L'acido ascorbico viene utilizzato oltre che in medicina anche come:
- additivo alimentare (E300, E301, E302, E303, E304)[48]
- agente di trattamento delle farine[49]
- pesticida[50]
- nei cosmetici[51]
- in analisi di laboratorio (es. determinazione colorimetrica dell'uranio)[52]
- rivelatore per la fotografia analogica in bianco e nero[53]
- agente per il trattamento delle superfici[54]
Note
Bibliografia
Altri progetti
Collegamenti esterni
Wikiwand - on
Seamless Wikipedia browsing. On steroids.