Tirosina
composto chimico Da Wikipedia, l'enciclopedia libera
La tirosina è un amminoacido polare, la sua molecola è chirale.
| Tirosina | |
|---|---|
 | |
| Nome IUPAC | |
| acido 2(S)-ammino-3-(4-idrossifenil)propanoico | |
| Abbreviazioni | |
| Y TYR | |
| Nomi alternativi | |
| L-tirosina
3-(4-idrossifenil)-L-alanina | |
| Caratteristiche generali | |
| Formula bruta o molecolare | C9H11NO3 |
| Massa molecolare (u) | 181,19 |
| Aspetto | solido cristallino incolore |
| Numero CAS | |
| Numero EINECS | 200-460-4 |
| PubChem | 6057 e 6942100 |
| DrugBank | DBDB00135 |
| SMILES | C1=CC(=CC=C1CC(C(=O)O)N)O |
| Proprietà chimico-fisiche | |
| Costante di dissociazione acida a 293 K | pK1: 2,20 pK2: 9,21 |
| Punto isoelettrico | 5,64 |
| Solubilità in acqua | 0,38 g/l a 293 K |
| Temperatura di fusione | 342 °C (615 K) con decomposizione |
| Proprietà termochimiche | |
| ΔfH0 (kJ·mol−1) | −685,1 |
| S0m(J·K−1mol−1) | 214,0 |
| C0p,m(J·K−1mol−1) | 216,4 |
| Indicazioni di sicurezza | |
| Simboli di rischio chimico | |

| |
| attenzione | |
| Frasi H | 315 - 319 - 335 |
| Consigli P | 261 - 305+351+338 [1] |
L'enantiomero L è uno dei 20 amminoacidi ordinari e il suo gruppo laterale è un p-idrossibenzile. Negli esseri umani non è essenziale, poiché l'organismo umano è in grado di sintetizzarla.
La tirosina è biologicamente importante in quanto precursore di vari ormoni, quali la tiroxina (un ormone tiroideo) e le catecolammine (dopamina, noradrenalina e adrenalina), e della melanina.
Essendo stata scoperta dal chimico tedesco Justus von Liebig all'interno della caseina, la tirosina deve il suo nome al vocabolo greco tyros, formaggio[2].
Biosintesi
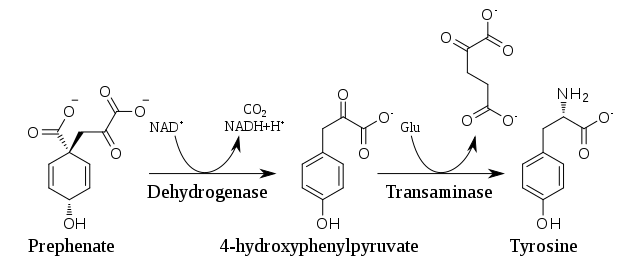
Nelle piante e nella maggior parte dei microrganismi, la tirosina è prodotta tramite il prefenato, intermedio della via dell'acido scichimico. Il prefenato è sottoposto a decarbossilazione ossidativa NAD-dipendente con ritensione dell'idrossile, dando luogo al p-idrossifenilpiruvato, successivamente sottoposto ad una reazione di transaminazione dove il glutammato è il donatore del gruppo amminico.
I mammiferi sintetizzano la tirosina dall'aminoacido essenziale fenilalanina (phe), introdotto tramite l'alimentazione. La conversione della fenilalanina in tirosina è catalizzata dall'enzima fenilalanina idrossilasi, un'ossigenasi a funzione mista che utilizza un cofattore pterinico, la tetraidrobiopterina. Questo enzima catalizza la reazione di conversione aggiungendo un gruppo ossidrile sull'atomo di carbonio in posizione 6 dell'anello aromatico della fenilalanina.
Metabolismo
Riepilogo
Prospettiva

Fosforilazione e solfatazione
Alcuni residui di tirosina possono essere marcati con un gruppo fosforico (fosforilato) da proteine chinasi. La fosforilazione della tirosina può essere considerata come un passaggio chiave nella trasduzione del segnale e nella regolazione dell'attività enzimatica. La fosfotirosina può essere rilevata tramite specifici anticorpi. I residui di tirosina possono essere inoltre modificati tramite l'aggiunta di un gruppo solfato in una reazione nota come solfatazione della tirosina.[3] Come nel caso della fosfotirosina, anche la solfotirosina può essere individuata tramite specifici anticorpi.
Tirosina come precursore di ormoni
Nella ghiandola surrenale, la tirosina è convertita in levodopa dall'enzima tirosina idrossilasi (TH). La TH è implicata anche nella sintesi della dopamina, della norepinefrina (noradrenalina) e dell'epinefrina.
Gli ormoni tiroidei triiodotironina (T3) e tiroxina (T4) nella tiroide derivano dai residui di tirosina della tireoglobulina. Due residui di tirosina iodinata della stessa catena polipeptidica possono reagire tra loro formando i precursori di T3 o T4, che vengono rilasciati sotto forma di ormone maturo mediante proteolisi. La iodurazione dell'anello della tirosina può essere ostacolata da una carenza di iodio causando un patologico ingrossamento della ghiandola tiroide detto gozzo.
Tirosina come precursori di alcaloidi
Nel Papaver somniferum, il papavero officinale, la tirosina è usata per produrre l'alcaloide morfina.
Tirosina come precursore di pigmenti
La sintesi delle melanine dalla tirosina ha luogo nelle cellule che producono pigmenti, i melanociti. Nel primo passaggio della reazione, che converte l'aminoacido nel 2,3-diidrossifenilalanina o dopa, è coinvolta una perossidasi. L'enzima tirosinasi è coinvolto nel passaggio successivo della via biosintetica che produce dopachinone. In una prima ramificazione della via, il dopachinone viene convertito in melanine nere polimeriche, mentre la reazione con la cisteina forma una serie di polimeri simili tra loro detti melanine rosse polimeriche.
La mancanza dell'enzima tirosinasi non permette la sintesi di melanina, dando così l'albinismo. Gli albini sono caratterizzati una deficienza di pigmentazione della pelle, della coroide, dei peli e dei capelli e da una maggior sensibilità alla luce solare.
Catabolismo

La via degradativa della tirosina comporta in prima istanza la sua transaminazione ad opera di una tirosina aminotransferasi. Sul prodotto, il p-idrossifenilpiruvato, agisce la p-idrossifenilpiruvato diossigenasi, un enzima che catalizza la decarbossilazione e il seguente spostamento della catena laterale utilizzando come cofattore l'ascorbato. Il prodotto di questa prima serie di reazioni è un composto detto omogentisato o acido omogentisico. Quest'ultimo viene ossidato da un enzima contenente ferro, l'acido omogentisico diossigenasi. Il maleilacetato isomerizza a fumarilacetoacetato che a sua volta si scinde in fumarato e acetoacetato.
Orto- e meta-tirosina

Sono noti tre isomeri della tirosina. Oltre al comune aminoacido L-tirosina che corrisponde all'isomero para (para-tyr, p-tyr o 4-idrossifenilalanina) vi sono altri due isomeri definiti meta-tirosina (m-tyr o 3-idrossifenilalanina o L-m-tirosina) e orto-tirosina (o-tyr o 2-idrossifenilalanina). Gli isomeri rari m-tyr e o-tyr hanno origine da una idrossilazione non enzimatica della fenilalanina ad opera del radicale ossidrilico in condizioni di stress ossidativo.[4][5]
m-Tirosina e i suoi analoghi (rari in natura) presentano una possibile applicazione nel Parkinson, Alzheimer e artrite.[6]
Uso medico
Riepilogo
Prospettiva
La tirosina rappresenta un fondamentale substrato per la sintesi di neurotrasmettitori (Dopamina, Noradrenalina e Adrenalina) e aumenta i livelli ematici degli stessi (in particolar modo Dopamina e Noradrenalina[7]) con piccoli effetti sull'umore.[8][9][10] L'effetto sull'umore è maggiormente osservabile in pazienti con condizioni di stress.
Una grande quantità di studi indicano l'utilità dell'assunzione di tirosina in condizioni di stress, freddo, affaticamento,[11] lavoro prolungato e insonnia,[12][13] con riduzione dei livelli ormonali in condizione di stress,[14] di stress indotto in seguito a perdita di peso,[15] aumento delle performance intellettuali e fisiche.[9][16][17]
La tirosina non mostra effetti significativi in condizioni normali.[18][19][20] Il dosaggio giornaliero di tirosina si aggira attorno ai 500–12000 mg al giorno. Non è consigliabile eccedere i 12000 mg (12 g) al giorno. Alte dosi possono abbassare i livelli di dopamina[18] e l'assorbimento di altri aminoacidi e di L-dopa.
Un recente studio[21] condotto dal Trinity College di Dublino in collaborazione al Max Plank di Berlino ha osservato in 398 soggetti sani che maggiore introito di tirosina dalla dieta (prevalentemente da carne rossa), è associato a maggiore massa cerebrale, migliore attenzione visiva e una riduzione dell'invecchiamento cerebrale.
Uso sportivo
La tirosina è un amminoacido precursore delle catecolammine (adrenalina, noradrenalina e dopamina) nel cervello, ed è stato rilevato che la sua supplementazione possa accelerare la sintesi di queste molecole nel sistema simpatoadrenale[22]. Gli studi sugli effetti della supplementazione di tirosina in ambito sportivo non hanno registrato effetti rilevanti sulla prestazione anche ad alti dosaggi[23]. La tirosina non ha dimostrato alcun miglioramento della performance anche se combinato con i carboidrati[24]. Alcune evidenze empiriche suggeriscono che la tirosina possa avere un impatto come stimolante se assunta come supplemento nel pre-allenamento in concomitanza con altre sostanze, esercitando un effetto sinergico. Studi su animali hanno dimostrato che la tirosina possa potenziare gli effetti dell'associazione caffeina/efedrina[25].
Alcuni autori suggeriscono la combinazione di 1-3 g di l-tirosina con 200 mg di caffeina e carboidrati ad alto indice glicemico (l'insulina aiuta a guidare gli impulsi del sistema nervoso) per ottenere effetti stimolanti simili a quelli riscontrati con il connubio caffeina/efedrina e un miglioramento della performance[26].
Note
Voci correlate
Altri progetti
Collegamenti esterni
Wikiwand - on
Seamless Wikipedia browsing. On steroids.
