From Wikipedia, the free encyclopedia
Մարդու միկրոբիոմ, մարդու[1] օրգանիզմում բնակեցված բոլոր մանրէների ամբողջականությունը, ներառյալ այնպիսի հատվածներ, ինչպիսիքն են մաշկը, կաթնագեղձերը, սեռական օրգանները, թոքերը, լորձաթաղանթները, կենսաբանական հեղուկները, լեղուղիները և ստամոքսաղիքային ուղին։

Մարդու միկրոբիոմը ներկայացված է բակտերիաներից, սնկերից, նախակենդանիներից, վիրուսներից և արքեաներից[2]։ Չնայած միկրոօրգանիզմները նույնպես կարող են ապրել մարդու մարմնի վրա, բայց դրանք սովորաբար բացառվում են այս սահմանումից։ Գենոմիկայի համատեքստում «մարդու միկրոբիոմ» հասկացությունը երբեմն օգտագործվում է ռեզիստենտ միկրօրգանիզմների կոլեկտիվ գենոմների նշանակությամբ՝ միաժամանակ «մարդու մետագենոմ» հասկացությունը ունի նմանատիպ նշանակություն և իմաստ։ Սկզբնական գնահատականը, որը տալիս էր պատկերացում մարդու օրգանիզմում բնակվող միկրոօրգանիզմների քանակի մասին՝ ենթադրում է, որ միկրոբային բջիջների քանակը տասն անգամ ավելի է, քան մարդու օրգանիզմի բջիջների քանակը, բայց ավելի ուշ գնահատականներով այդ հարաբերակցությունը իջեցվել է 3:1-ի կամ նույնիսկ մատավորապես նույն թվին համարժեք[2][3][4][5][6][7]։ Միկրոօրգանիզմների մի մասը հանդիսանում է մարդու օրգանիզմի կոմենսալներ, այսինքն՝ նրանք գոյատևում են վնաս չհասցնելով մարդկանց, մեկ այլ խումբ ցուցաբերում են մուտալիստական (փոխշահավետ) փոխհարաբերություն սեփական տիրոջ օրգանիզմի հետ։ Եվ հակառակը որոշ ախտածին (պաթոգեն) միկրոօրգանիզմներ կարող են վնաս հասցնել մարդու օրգանիզմին իրենց նյութափոխանակության արգասիքների միջոցով, այնպիսի նյութերով, ինչպիսիքն են տրիմեթիլամինը, որը մարդու օրգանիզմում վերածվում է N-օքսիդ տրիմեթիլամինի FMO3 օքսիդացնող համալիրի միջոցով[8][9]։
Որոշ միկրոօրգանիզմներ կատարում են մի շարք կարևոր գործողություններ, որոնք ինչպես հայտնի է շատ օգտակար են հյուրընկալող տիրոջ օրգանիզմի համար, բայց դրանց մեծ մասի դերը ամբողջականությամբ պարզ չէ։ Նորմալ միկրոբիոտիա երբեմն համարվում է այն, որ պետք է ներկա լինի նորմալ պայմաններում, առանց հիվանդություն պատճառելու[2]։
Մարդու միկրոբիոտիայի հետազոտության համար անց է կացվել «Մարդու միկրոբիոմ» նախագիծը, որոշելու համար այնպիսի հարցեր, որոնցից են մարդկային միկրոբիոտիայի գենոմի համադրումը և վերլուծությունը, առանձնահատուկ ուշադրություն դարձնելով մաշկի, բերանի, քթի, մարսողական ուղիների և հեշտոցի բնակեցված միկրոբիոտիային։ Այն հասավ իր բեկումնային մակարդակին 2012 թվականին, երբ հրապարակեց իր նախնական արդյունքները[10] ։
Չնայած նրան, որ այնպիսի տերմիններ ինչպիսիք են՝ ֆլորան և միկրոֆլորան հաճախ օգտագործվում են գրականության մեջ, տեխնիկական տերմիններով դա հանդիսանում է սխալ հասկացություն, քանի որ «ֆլորա» բառի արմատը վերաբերում է բույսերին, իսկ «բիոտա» տերմինը վերաբերում է որոշակի էկոհամակարգում օրգանիզմների ընդհանրությանը։ Ներկայումս օգտագործվում է ավելի հարմար «միկրոբիոտա» տերմինը, չնայած նրա օգտագործումը ստվեր չի գցում «միկրոֆլորա» հասկացության վրա։ Երկու տերմիններն էլ օգտագործվում են տարբեր գրականություններում[7]
2014 թվականի դրությամբ տարբեր աղբյուրներ հաճախ հայտնել են, որ մարդու մարմնում մանրէային բջիջների քանակը մոտ 10 անգամ ավելին է, քան մարդու բջիջների քանակը։ Այս ցուցանիշը հիմնված է այն գնահատականների վրա, որ մարդու միկրոբիոտան ունի մոտ 100 տրիլիոն մանրէային բջիջ, իսկ հասուն մարդու օրգանիզմում կա 10 տրիլիոն բջիջներ[3]։ 2014 թվականին Ամերիկական Մանրէաբանական Ակադեմիան հրապարակեց հաճախ տրվող հարցերը, որոնք շեշտում էին, որ մանրէային բջիջների քանակը և մարդու բջիջների քանակը հանդիսանում են մոտավոր։ Նրանք նաև նշել են, որ վերջին ուսումնասիրությունները տվել են մարդու բջիջների քանակի նոր գնահատական՝ մոտավորապես 37,2 տրիլիոն, որը նշանակում է, որ մանրէային բջիջների նախնական գնահատմամբ 100 տրիլիոն բջիջների հաշվով մանրէային և մարդկային բջիջների հարաբերակցությունը մոտ 3:1-ի է[3][4]։ 2016 թվականին մեկ այլ գիտական խումբ տվեց նոր գնահատական, ցույց տալով, որ փոխհարաբերությունը կազմում է ուղիղ 1:1-ի[5][6]։
Միկրոբիոմի որոշման խնդիրը կապված է մանրէաբանական ամբողջության ներկայացուցիչների նույնականացնելու մեջ, որոնք ներառում են մանրէներ, նախակենդանիներ և վիրուսներ[11]։ Մասնավորապես ներկայացուցիչներին տարբերակելու համար օգտագործում են ԴՆԹ-ն, չնայած կան հայտնի դեպքեր երբ օգտագործվել է ՌՆԹ-ն, սպիտակուցները և նյութափոխանակության արգասիքները[11][12]։ Միկրոբիոմի հետազոտությունը հիմնված ԴՆԹ-ի վրա հնարավոր է վերագրել մետագենոմիկական վերջին ուսումնասիրություններին սեկվենավորման եղանակով։ Այս եղանակը իրենից ներկայացնում է մի ամբողջ մետագենետիկական մոտեցում, որը նաև հնարավոր է օգտագործել տարբեր մանրէային համայնքների ֆունկցիոնալ ներուժը ուսումնասիրելու համար[11]։ Մարդու միկրոբիոմի ուսումնասիրություններում առկա խնդիրներից մեկն այն է, որ հետազոտության մեջ մարդկային ԴՆԹ-ն ներգրավված չէ[13]։
Հիմնական հարցերից մեկը, բացի մարդու միկրոբիոմի պարզ վերլուծությունից, այն է կա արդյոք ընդհանուր « կմախք» կամ գոյություն ունի միկրոօրգանիզմների ընդհանուր խումբ, որը հետագայում կունենա մարդկանց օրգանիզմում տեսակային բազմազանություն[14][15]։ Եթե այդպիսի կմախք գոյություն ունի, ապա հնարավոր կլինի նույնականացնել զարգացող հիվանդությունները՝ կախված տեսակների կազմի փոփոխությունից, ինչը «Մարդու միկրոբիոմ» նախագծի նպատակներից մեկն է։
Հայտնի է, որ մարդու միկրոբիոմը (աղիների միկրոբիոմը) խիստ տատանողական է և հանդիսանում է յուրահատուկ բոլոր մարդկանց մոտ, ինչը նաև նկատվեց մկների խմբի թեստավորման արդյունքում[7]։
2012 թվականի հունիսի 13-ին NIH-ի տնօրեն Ֆրենսիս Կոլլինսլը հայտարարություն տարածեց « Մարդու միկրոբիոմ» (HMP) պրոյեկտի կարևորության մասին[10]։ Հայտարարությունը ուղեկցվեց մի շարք գիտական հոդվածներով հրատարակված Nature[16][17] ամսագրում և հասարակական գիտական գրադարանում (PLOS) հենց նույն օրը։ Վերլուծելով առողջ մարդկանց միկրոբիոմի քարտեզը ստացված սեկվենավորման (համահարթեցման) մեթոդով, գիտնականները ստեղծեցին տվյալների բազա միկրոբային համայնքի նորմալ տատանումների վերաբերյալ։ 242 առողջ կամավորներից ստեղծել էին 5000 կենսաբանական նմուշներ, որոնք վերցվել էին մարմնի տարբեր մասերից։ Արդյունքում վերլուծվել է մարդու ամբողջական ԴՆԹ-ն և նրանում բնակվող միկրոբիոտիան։ Նրանք կարողացել են մեկնաբանել այդպիսի տվյալներ ինդենտիֆիկացնելով բակտերիալ ռիբոսոմային ՌՆԹ, 16Sr ՌՆԹ գեները։ Հետազոտողները պարզել են, որ ավելի քան 10 000 տեսակի միկրոօրգանիզմներ կազմում են բարդ էկո համակարգ մարդու օրգանիզմում, որոշելով էկոհամակարգի 81-99 %-ի տեսակները։
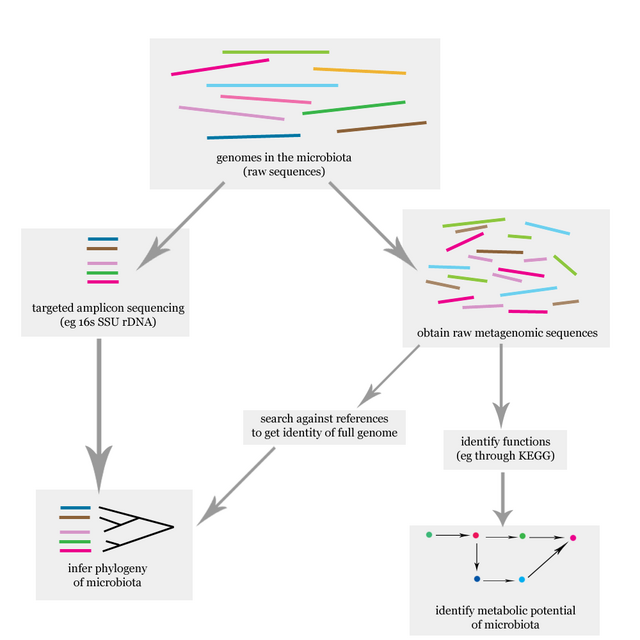
Հաճախ անհնար է լաբորատորիաներում աճեցնել բակտերիաների, արքեաների կամ վիրուսների հսկայական բազմազանությունը։ Այս խնդրի լուծումը սեկվենավորման տեխնոլոգիան օգտագործելն է մետագենոմիկայի տեխնոլոգիայի մեջ։ Մանրէային տեսակների գործառույթների և բնութագրերի պատկերի ամբողջական վերլուծությունը ունեն հսկայական ներուժ թերապիայի բացահայտման և առողջական վիճակի ախտորոշման համար[18]։
Հիմնական խնդիրը վերլուծության համար բավականաչափ մանրէաբանական ԴՆԹ հավաքելն է, միաժամանակ պահելով նմուշի մաքրությունը՝ այդ պատճառով օգտագործում են տարբեր եղանակներ։ Մասնավորապես, ԴՆԹ-ի անջատման մեթոդը ունիվերսալ գործիք է մանրէային ցանկացած շտամի հետ աշխատելիս, ինչում կարևոր է մեկուսացնել գենոմի դիմացկուն հատվածները, որոնք արագ լիզիսի չեն ենթարկվում։
Մեխանիկական անջատումը ընդհանուր առմամբ ավելի գերադասելի է, քան քիմիականը[18] ։
Սեկվենավորման ռեակցիաների համար ավելի հաճախ օգտագործում են այնպիսի հարթակներ, ինչպիսիքն են Illumina ,Yan Torrent, Oxford Nanopore Min ION և Pacific Biosciens Sequel։ Որևէ ցուցակում չկա օգտագործման նմուշի ճիշտ քանակությունը[18]։
Չնայած այն հանգամանքներին, որ մոտեցումները, ակտիվորեն կիրառվում են, կան որոշակի դժվարություններ, որոնք պետք է հաղթահարել։ Տեղեկությունը կախված է միկրոբային համայնքի յուրաքանչյուր գենոմի առկայությունից․ գենոմները, որոնք ունեն ցածր արժեքներ կարող են ենթարկվել մասնատման, եթե սեկվենավորման խորությունը անբավարար է (օգտագործվում է բացերից խուսափելու համար)։ Բարեբախտաբար գոյություն ունեն հավաքիչներ, որոնք պարզեցնում են մետագենոմի համար հարաբերակցության որոնումը, քանի որ եթե հարյուրավոր շտամներ առկա են, ապա հաջորդականացման խորությունը պետք է առավելագույնի հասցվի[18]։
Նախապես հայտնի չէ թե որ գենոմից է տեղի ունենում յուրաքանչյուր conting (ԴՆԹ-ի համընկնում ), ոչ էլ նմուշում առկա գենոմների քանակն է հայտնի։ Այս քայլի հիմնական նպատակն է conting-ները բաժանել տարբեր տեսակների։ Այս վերլուծության իրականացման հիմքում ընկած մեթոդներըկարող են լինել վերահսկվող (օրինակ՝ հայտնի հաջորդականությամբ տվյալների բազան) կամ չվերահսկվող (conting խմբի հավաքած տվյալների ուղիղ հսկում)։ Այնուամենայնիվ, երկու մեթոդներն էլ պահանջում են մետրիկաներ գնահատականների տարբերակման համար՝ հավաստի conting-ի և այն խմբի, որը պետք է լինի օգնող և ալգորիթմային խմբային բախշման մեջ նմանությունները վերափոխելու համար[18]։
Պարտադիր է անցկացնել ստատիստիկական վերլուծությունների շարք, ինչպիսինն է ANOVA-ն, պարզելու համար արդյունքների հավաստիությունը։ Այդպիսի տեստերը կարող են գնահատել և տարբերակել տարբեր խմբերում տարբերությունների աստիճանը։ Եթե տեստերը կապված են գրաֆիկական գործիքների հետ, ապա հնարավոր է հեշտ անցկացնել արդյունքների մեկնաբանություն՝ ավելի հեշտ ներկայացնելու և հասկանալու համար[18]։
Այն դեպքում երբ հնարավոր կլինի մետագենոմը հավաքել ճիշտ հաջորդականությամբ, ապա կստացվի միկրոբիոմի ֆունկցիոնալ պոտենցիալի ճիշտ պատկեր։ Այդպիսի հաշվարկված համակարգերի դեպքում գործում են խնդիրների մի շարք, որոնցից է մետագենոմի համակարգի հավաքումը, որը կարող է ունենալ ավելի ցածր որակ, այնպիսի դժվարության պատճառով, որ գեները կարող են լինել ոչ լրիվ և ֆրագմենտավորված։ Գեների ինդենտիֆիկացիայի քայլից հետո տվյալները կարող են օգտագործվել ֆունկցիոնալ անոտացիա անցկացնելու համար՝ թիրախային գեների բազմակի հավասարեցմամբ՝ օրթոլոգների տվյալների բազաներով[19]։
Այս տեխնիկայի դեպքում օգտագործում են պրայմերներ հատուկ գենետիկական հատվածներ թիրախավորվելու համար, այն նպատակով որպեսզի հիմնեն ֆիլոգենետիկական շարք։ Գենետիկական հատվածը բնութագրվում է խիստ փոփոխական տարածաշրջանով, որը կարող է մանրամասն նույնականացում ապահովել։ Այս շարքում առկա են այնպիսի պահպանողական հատվածներ, որոնք գործում են որպես վայր պրայմերների կապման, պոլիմերազային շղթայական ռեակցիայում օգտագործվող։ Բակտերիաների և արքեաներին նկարագրող հիմնական գենը հանդիսանում է 16S r ՌՆԹ-ն, մինչ դեռ սնկերի նույնականացումը հիմնված է ITS-ի վրա։ Այս մեթոդը հանդիսանում է արագ և բավարար միկրոօրգանիզմների համայնքային դասակարգումը ստանալու համար։ Մեթոդը հարմար է նաև ԴՆԹ-ի ախտոտվածությունը որոշելու համար (ախտոտված տիրոջից)[20]։
Հետևողականորեն ճիշտ պրայմերի ընտրությունը կարող է օգնել նվազեցնել այդպիսի սխալներ հաշվի առնելով միկրոօրգանիզմների մասին գիտելիքները և նրանց հարաբերական թվաքանակը[20]։
Գենի մարկերների վերլուծությունը կարող է կախված լինել պրայմերի ընտրությունից՝ այս ձևով վերլուծությունը գերադասելիորեն իրականացվում է լավ փորձարկված ձեռնարկների միջոցով (օրինակ այնպիսինները,որոնք օգտագործվել են «Երկրի Միկրոբիոմ» նախագծում)։ Այս հետազոտության առաջին քայլը սեկվենավորման սխալները ջնջելն է։ Սեկվենավորման շատ հարթակներ շատ հուսալի են, բայց հաջորդականության ակնհայտ բազմազանության մեծ մասը դեռևս պայմանավորված է սեկվենավորման գործընթացում թույլատրված սխալներով։ Այս սխալների քանակը նվազեցնելու համար կարող ենք օգտագործել OTU-ն, որը արդեն օգտագործվում է հաջորդ քայլերում, բայց այս մեթոդը անտեսում է ONP-ն, քանի որ դրանք համատեղվում են մեկ այլ OTU-ի մեջ։ Մեկ այլ մեթոդ հիմնված է օլիգոտիպավորման վրա, որն իր մեջ ներառում է հատուկ տեղեկություններ 16s r ՌՆԹ-ի հաջորդականության վերաբերյալ՝ փոքր նուկլեոտիդային տատանումները հայտնաբերելու համար։ Այս մեթոդները տալիս են ԴՆԹ-ի հաջորդականությունների և յուրաքանչյուր նմուշում բաղադրության իրական պատկեր։ Դա արվում է մեքենայական ուսուցման միջոցով, որոնք ճշգրտության են հասնում յուրաքանչյուր տեսակի համար մոտավորապես 80% -ով։ Այլ հայտնի վերլուծական փաթեթներ աջակցություն են ցուցաբերում տեսակային դասակարգմանը օգտագործելով ճշգրիտ համընկնումներ տվյալների տեղեկատու շտեմարաններից և պետք է ապահովեն ավելի մեծ յուրահատկություն, բայց ունեն ավելի վատ զգայունություն[20]։
Շատ եղանակներ հիմնված ֆիլոգենետիկական ենթադրությունների վրա, օգտագործում են 16 sp ՌՆԹ գեները արքեաների և բակտերիաների, 18 SRNA գենը նախակենդանիների բջիջների ուսումնասիրման համար[21]։
Ֆիլոգենետիկական համեմատական մեթոդները հիմնված են միկրոօրգանիզմների բազմաթիվ առանձնահատկությունների համեմատության վրա, սկզբունքը հետևյալն է․ ինչքան մոտ են միմյանց կապերը, այնքան ավելի շատ են ընդհանրություններ ունեն։ Սովորաբար այս մեթոդը օգտագործվում է ֆիլոգենետիկական ընդհանրացված նվազագույն խորանարդային կամ այլ վիճակագրական վերլուծություններով՝ ավելի իմաստալից արդյունքներ ստանալու համար։ Դա սովորաբար հիմնված է PICRUST ծրագրի վրա, օգտագործելով տեղեկությունների բազայի տվյալները։
Բակտերիաները և սնկերը տեղակայվում են մարդու մաշկի և լորձաթաղանթների տարբեր մասերում։ Նրանց դերը հանդիսանում է նորմալ, առողջ մարդու ֆիզիոլոգիան կառուցելու մի մասը դառնալը, սակայն եթե մանրէների քանակը նրանց բնորոշ սահմաններից դուրս է (հիմնականում իմունային համակարգի խանգարման դեպքում), կամ եթե մանրէները բնակեցվել են մարմնի այնպիսի հատվածներում (օրինակ՝ վատ հիգիենայի կամ տրավմայի արդյունքում), որոնք գաղութացման ենթակա չեն կամ ստերիլ են (օրինակ՝ արյուն, ստորին շնչառական ուղիներ կամ որովայնի խոռոչ) դա կարող է հանգեցնել լուրջ հիվանդությունների առաջացման (համապատասխանաբար՝ առաջացնելով բակտերեմիա սեպսիս, թոքաբորբ և պերիտոնիտ (որովայնաբորբ))[22]։
«Մարդու միկրոբիոմ» նախագծի վրա կատարած աշխատանքների արդյունքները ցույց են տվել, որ մարդկանց մարմնի տարբեր մասերում պարունակում են հազարավոր բակտերիաներ՝ իրենց առանձնահատկություններով։ Այնպիսի հատվածներ, ինչպիսիքն են մաշկը և հեշտոցը բակտերիաների ավելի քիչ տեսակային բազմազանություն ունեն, քան բերանը և աղիները, որտեղ բազմազանությունը չափազանց մեծ է։ Նաև բերանի խոռոչում հայտնաբերված նույն տեսակի մանրէներն ունեն մի քանի ենթատեսակներ, որոնք ապրում են բերանի խոռոչի տարբեր հատվածներում.[23][24]։
Ըստ գնահատման՝ մարդու աղիքներում ապրող 500-ից 1000 տեսակ մանրէները պատկանում են մի քանի խմբերի, հիմնականում գերակշռում են Firmicutes և Bacteroidetes, բայց հանդիպում են նաև Proteobacteria, Verrumicrobia, Actinobacteria, Fusobacteria, Cyanobacteria[25]:
Մի շարք բակտերիաներ, ինչպիսիք են Actinomyces Viscosus-ը և A.naes Lundii-ն, ապրում են բերանի խոռոչում և հանդիսանում են կպչում մի նյութի մասը, որը կոչվում է ատամնափառ։ Եթե դրանք չեն հեռացվում ատամների մաքրման ժամանակ, ամբողջ զանգվածը կարծրանում է և ձևավորվում է ատամնաքար։ Որոշ բակտերիաներ արտադրում են մի շարք թթուներ, որոնք քայքայում են ատամի էմալը առաջացնելով կարիես։
Հեշտոցի միկրոֆլորան բաղկացած է հիմնականում տարբեր տիպի լակտոբացիլներից։ Երկար ժամանակ ենթադրվում էր, որ տեսակներից ամենատարածվածը Lactobacillus acidophilus-ն է, բայց հետագայում պարզ դարձավ, որ ամենատարածվածը հանդիսանում է Lactobacillus iners-ը, որին հաջորդում է Lactobacillus crispatus-ը։ Այլ լակտոբացիլներից, որոնք հայտնաբերվել են հեշտոցում, հանդիսանում են L.jensenii, L.delbruekii և L.gasseri-ն։ Հեշտոցի միկրոֆլորայի խախտումը կարող է առաջացնել ինֆեկցիաներ, այնպիսիք, ինչպիսիք են բակտերիալ վագինոզը կամ կանդիդոզը։
Արքեաները ներկայացված են մարդու աղիներում, բայց շատ անգամ ավելի քիչ քան բակտերիաների քանակությունն է[26]։ Գերիշխող խումբ են հանդիսանում մեթանոգենները[27], առանձնապես Methanobrevibacter smithii և Methanospaera stadtmanae։ Այնուամենայնիվ միայն մարդկանց 50% մոտ է հայտնաբերվում արքեաների տվյալ բազմազանությունը[28]։
2007 թվականի դրությամբ չեն հայտնաբերվել հստակ ախտածին տեսակներ[29][30], չնայած առաջարկվել է մեթանոգենների և պարադոնտիտի որոշակի փոխհարաբերական կապի առկայություն[31]։
Սնկերը, մասնավորապես խմորասնկերը առկա են մարդու աղիներում[32][33][34][35]։ Առավել ուսումնասիրված են կանդիդիա սնկի շտամները[33][34][35], որոնք ունակ են վերածվելու ախտածին իմունադիֆիցիտային վիճակների ժամանակ և նույնիսկ հարուցում են հիվանդություն առողջ տիրոջ մոտ։ Սնկերի որոշ տեսակներ գաղութացնում են մաշկը[32], այնպիսիները, որոնցից է Malasseria սնկի շտամները օգտագործում են ճարպագեղձերի կողմից արտադրված ճարպը[36][37]։
Վիրուսները, մասնավորապես բակտերային վիրուսները (բակտերոֆագերը), բնակվում են մարմնի տարբեր մասերում՝ ներառյալ մաշկը[38], աղիները[39], թոքերը[40] և բերանի խոռոչը[41]։ Վիրուսների և որոշակի հիվանդությունների միջև կապ է հաստատվել։ Վիրուսները բակտերիաների հետ գտնվում են բարդ փոխհարաբերությունների մեջ[42][43][44]։
Տասն առողջ մարդկանց յուրաքանչյուրի մաշկի 20 տարբեր հատվածների ուսումնասիրության արդյունքում հայտնաբերվել են 205 բակտերիաներ՝ նույնականացված 19 բակտերիալ տեսակներ, որոնցից շատերը պատկանում են հիմնականում չորս տեսակի ՝ Actinobacteria (51,8%), Firmicutes (24,4%), Proteobacteria (16,5%) և Bacteroidetes (6,3%)[45]։ Առողջ մարդկանց մաշկի վրա կան մեծ թվով սնկերի տեսակներ՝ մարմնի հատվածների որոշակի փոփոխություններով, այնուամենայնիվ ախտաբանական պայմաններում որոշակի տեսակներ ունեն գերակայող ազդեցություն ախտահարված հատվածում (օրինակ ատրոպիկ դերմատիտի ժամանակ գերակշռում է Malassezia-ն)[32]։
Մաշկը հանդիսանում է պատնեշ, որը խոչընդոտում է ախտածին մանրէների օրգանիզմ ներթափանցմանը, որը հանդիսանում է ժամանակավոր կամ մշտական բնակավայր նրանց համար։ Ռեզիդենտ միկրոօրգանիզմների տեսակները տարբերվում են՝ կախված մարդու մարմնի մաշկի տեսակից։ Մանրէների մեծ մասը տեղակայված են մաշկի մակերեսային բջիջների վրա կամ նախընտրում են բնակվել գեղձերի ծորաններում (ճարպագեղձեր և քրտնագեղձեր), քանի որ դրանք մանրէների ապահովում են ջրով, ամինաթթուներով և այլ սննդանյութերով[2]։
Շաղկապենում սովորաբար առկա են սնկերի և բակտերիաների փոքր քանակություններ[32][46], ներառյալ Գրամ դրական կոկեր (staphylococcus և steeptococcus), Գրամ բացասական ցուպիկներ և կոկեր (Haemoohilus and Naisseria)[46] և սնկեր (Candidia, Aspergillus և Penicillium)[32]։ Արցունքը պարունակում է մանրէասպան նյութեր, որոնցից է լիզոցիմը, արդյունքում միկրոօրգանիզմները դժվար կարող են ապրել և կոլոնիզացիայի ենթարկել էպիթելային մակերեսները։
Մարդու միկրոբիոմը առաջանում է ծննդյան օրից և կախված է թե երեխան ինչ ճանապարհով է ծնվել[47]։ Օրինակ կեսարյան հատմամբ ծնված երեխաները կրում են ավելի ախտածին միկրոֆլորա, ինչպիսինն են Escherichia coli և Staphylococcus և զգալիորեն մեծանում է ոչ ախտածին միկրոօրգանիզմների զարգացման ժամանակաշրջանը և օգտակար միկրոբիոտիան ուշ է ձևավորվում[48]։ Այն երեխաները, ովքեր ծնվել են նորմալ, բնական ճանապարհով ոչ ախտածին, օգտակար միկրոբիոտիան նման է մայրական օրգանիզմի միկրոբիոտիայի բաղադրությանը[49]։

Աղիքային միկրոբիոտիայի և մարդու օրգանիզմի փոխհարաբերությունները ոչ միայն կոմմենսալային են (ոչ վնասակար), այլ նաև մուտուալիստական (փոխշահավետ)[2]։ Որոշ միկրոօրգանիզմներ տիրոջ օրգանիզմում օգնում են տարբեր սննդային մանրաթելեի ներծծել կարճ շղթայի ճարպաթթուների մեջ, ինչպիսիք են քացախաթթուն և կարագաթթուն, որոնք հետագայում ներծծվում են մարդու օրգանիզմում[7][50]։ Աղիների բակտերիաները ունեն մեծ դերակատարում վիտամին B-ի և վիտամին K-ի սինթեզի պրոցեսում, ինչպես նաև լեղաթթուների, ստերինների և կսենոբիոտիկների նյութափոխանակության մեջ[2][50]։ Նյութափոխանակային պրոցեսների արդյունքում բակտերիաները առաջացնում են հորմոնների պես նյութեր և ըստ երևույթին մարդու միկրոբիոմը աշխատում է ինչպես էնդոկրին գեղձ։ Աղիքային միկրոբիոտիայի խանգարումը կապված է բազմաթիվ բորբոքային և աուտոիմուն պրոցեսների հետ[7][50][51]։
Մարդու աղիքային ֆլորայի կազմը փոխվում է ժամանակի հետ, երբ փոխվում է ընդհանուր առողջական վիճակը[7][51]։ 2016 թվականի հունիսից սկսած կարգավորված ձևով 15 ռանդմիզիացված հետազոտությունները մարդկանց մասնակցությամբ, ցույց տվեց որոշ պրոբիոտիկական մանրէների շտամներ՝ Bifidobacterium և Lactobacillus (B. longum, B. breve, B. infantis, L. Helveticus, L. Rhamnosus, L. Plantarum L. Casei.) տեսակների ընդունումը ներքին ընդունման ձևով օրական 10 9 −10 10 KOE 1-2 ամսվա համար, ցուցաբերում է բուժական ազդեցություն (այսինքն բարելավում են արդյունքները) կենտրոնական նյարդային համակարգի որոշակի խանգարումների դեպքում՝ ներառյալ անհանգստությունը, դեպրեսիան, աուտիզմի սպեկտրի և օբսենսիվ-կոմուլսիվ խանգարումները, բարելավում է հիշողության որոշակի ասպեկտներ[52]։
Այնուամենայնիվ միկրոբիոմի փոփոխությունների կարող են օրգանիզմում առաջացնել վնասակար տեղաշարժեր, որոնք առողջության խաթարման են բերում։ Musso et al. աշխատությունում ներկայացված էր, որ աղիքային միկրոբիոմը ճարպակալած անհատների մոտ պարունակում է ավելի շատ Firmicutes տեսակի բակտերիաներ և ավելի քիչ Bacteroidetes տեսակի ի տարբերություն առողջ մարդկանց միկրոբիոմի։ Gordon et al. կողմից անցկացված մեկ այլ հետազոտություն[53], հաստատեց, որ հենց միկրոբիոմի ներկայացուցիչներն են հարուցում ճարպակալում, այլ ոչ թե հակառակը։ Դա ապացուցվել է ճարպոտ և հատուկ սննդակարգով սնվող մկների աղիքային միկրոֆլորան փոխպատվաստելով վերահսկվող խմբի միկրոբիոմից զերծ մկներին։ Նրանք պարզեցին, որ այն մկների մոտ, որոնք փոխպատվաստվել են հավելյալ ճարպակալում ունեցող մկների միկրոբիոմից, նրանց մոտտ ճարպի քանակությունը ավելի մեծ է քան այն մկների որոնք փոխպատվաստվել էին հատուկ սննդակարգով սնվող մկների միկրոբիոմով[54]։
Պարզվում է, որ միզասեռական համակարգում կա միկրոբիոտիա[55][56], ինչը անսպասելի փաստ է, քանի որ դասական միկրոբիոլոգիական լաբորատոր եղանակով, որոնք պարզում են միզուղիների վարակները չի հայտնաբերվում այդ միկրոբիոտիան[57]։ Դասական կուլտիվացիոն մեթոդով չեն հայտնաբերվում միզասեռական համակարգի մի շարք բակտերիաներ և այլ միկրոօրգանիզմներ[57]։ Սակայն սեկվենավորման մեթոդով հնարավոր եղավ միկրոօրգանիզմների հայտնաբերումը, այն նպատակով՝ պարզել արդյոք կա տարբերություն առողջ մարդու միզասեռական համակարգի միկրոբիոմի և այն մարդկանց միջև ովքեր ունեն միզասեռական ուղիների վարակ[55][56]։
Հեշտոցի միկրոբիոմը իր մեջ պարունակում է օրգանիզմներ, որոնք կատարում են կարևոր դեր՝ հեշտոցը պաշտպանելով վարակներից և այն պահելով առողջ[58] : Ամենատարածված միկրոօրգանիզմները, որոնք հայտնաբերվել են կնոջ մոտ նախադաշտանադադարի ժամանակ պատկանում են Lactobacillus տեսակին, որոնք խանգարում են ախտածին օրգանիզմների աճը արտադրելով ջրածնի պերօքսիդ և կաթնաթթու[59][58][60] : Միկրոբիոմի կառուցվածքը խիստ կախվածության մեջ է դաշտանային ցիկլից[2][61] : Հայտնաբերվել է կապ սեռական հարաբերությունների, հակաբիոտիկների և կանանց օրգանիզմում[60] լակտոբացիլների նվազման միջև։ Ամենից զատ, հետազոտությունները ցույց տվեցին, որ սեռական հարաբերությունները պահպանակով հանգեցնում են հեշտոցում[60] լակտոբակտերիաների նվազման և աղիքային ցուպիկների շատացման։ Բոլոր այս փոփոխությունները, որոնք տեղի են ունենում հեշտոցային միկրոբիոմում կարող են հանգեցնել տարբեր ինֆեկցիաների զարգացման, ներառյալ կանդիդիոզի և բակտերիալ վագինոզի[32][35][59]։
Երկար ժամանակ պլացենտան համարվում էր ստերիլ, այնուամենայնիվ, հայտնաբերվել են մի շարք ոչ ախտածին բակտերիաներ պլացենտայի հյուսվածքում[62][63][64]։
Մինչև վեջերս կնոջ վերարտադրողական համակարգը համարվում էր ստերիլ միջավայր։ Մի շարք միկրօրգանիզմներ բնակվում են առողջ, անախտանիշ վերարտադրողական տարիքի կանանց արգանդում։ Արգանդի միկրոբիոմը էականորեն տարբերվում է հեշտոցի և աղեստամոքսային համակարգի միկրոբիոմից[65]։
Բերանի խոռոչում առկա են նպաստավոր պայմաններ, ներառյալ ջուր, սննդանյութեր և նորմալ ջերմաստիճան միկրոօրգանիզմների աճի և բազմացման համար[2]։ Անօդակյաց բակտերիաներից, որոնք ներկայացված են բերանի խոռոչում առավել տարածված են՝ Actinomyces, Arachnia, Bacteroides, Bifidobacterium, Eubacterium, Fusobacterium, Lactobacills, Leptotrichia, Peptococcus, Peptostreptococcus, Propionibacterium, Selenomonas, Veillella, Trepone[66]: Ներկայացված սնկերի տեսակներն են՝ Candida, Cladosporium, Aspergillus, Fusarium, Glomus, Alternaria, Penicillium և Cryptococcus[32]:
Բակտերիաները ինչպես կոշտ, այնպես էլ բերանի խոռոչի փափուկ հյուսվածքներում կոնգլոմերատի ձևով, որը նրանց հնարավորություն է տալիս դրանց դառնալ կպչուն։ Արդյունքում նրանք ստանում են պաշտպանություն շրջակա միջավայրի գործոններից և հակամանրէային հակամարմիններից[67]։ Թուքը առանցքային դեր է խաղում կոնգլոմերատի աճի և բակտերիաների գաղութացման համար պարունակելով բավարար քանակի սննդանյութեր և պահպանելով նրանց կենսագործունեության համար անհրաժեշտ ջերմաստիճանը։ Ինչպես նաև վերահսկում է միկրոօրգանիզմների աճը կոնգլոմերատի հեռացման միջոցով։ Բերանի խոռոչի բակտերիաները մշակել են մեխանիզմներ, որպեսզի զգան իրենց շրջապատող միջավայրը և խուսափեն տիրոջ օրգանիզմում փոփոխություններ կատարելուց[68][69]։
Այնուամենայնիվ, բարձր արդյունավետությամբ օժտված մարդու բնածին պաշտպանական համակարգը մշտապես վերահսկում է մանրէների գաղութացումը և կանխում է բակտերիաների ներթափանցումը տեղային հյուսվածք։ Ատամնային փառի բակտերիաների և օրգանիզմի բնածին պաշտպանական համակարգի միջև կա դինամիկ հավասարակշռություն[70]։
Առողջ հավասարակշռությունը սիմբիոզի մի տեսակ է, երբ բերանի խոռոչի միկրոբիոմը սահմանափակում է ախտածինների աճը և բազմացումը, իսկ մարդու օրգանիզմն ապահովում է դրանց աճի և զարգացման պայմանները[67][71]։ Մարդու կյանքի փոփոխությունները, ներառյալ նրա իմունային համակարգը, սնունդը, բերում են տեսակային կազմի փոփոխության խաթարելով հավասարակշռությունը՝ փոխշահավետից վերածելով մակաբուծականի[67]։ Պարզվել է, որ շաքարային դիաբետը և սիրտանոթային հիվանդությունները կապ ունեն բերանի առողջության հետ[71]։
Բերանի մշտական հիգիենան, տարբեր հիվանդությունների զարգացումը կանխող հիմնական մեթոդն է[71]։
Բերանի խոռոչի մաքրումը նվազեցնում է պոտենցիալ ախտածին միկրոօրգանիզմների քանակը[69]։ Այնուամենայնիվ, բերանի խոռոչի պատշաճ հիգիենան կարող է բավարար չլինել, քանի որ այն բարդ համակարգ է, որի դեպքում պետք է հաշվի առնել իմունային պատասխանը, գենետիկական և տեսակային կազմը։ Հակաբիոտիկները կարող են օգտագործվել ինֆեկցիաների դեմ պայքարում, սակայն կարող է լինել ոչ արդյունավետ միկրոբային կոնգլոմերատի դեպքում[69]։
Ինչպես բերանի խոռոչը, վերին և ստորին շնչառական ուղիները ունեն մեխանիկական հատկություններ, որոնք կարող են ոչնչացնել մանրէները։ Գավաթաձև բջիջները արտադրում են սեկրետ, որոնք կլանում են մանրէները և դրանք դուրս են մղում շնչառական ուղիներից էպիթելային հյուսվածքի հակառակ ուղղություն ունեցող թարթիչների միջոցով[2]։ Սրա հետ մեկտեղ, մանրէազերծող հատկությամբ օժտված է լորձի մեջ պարունակվող նյութը, որը կոչվում է լիզոցիմ։ Թոքային միկրոբիոմը ներկայացված է ինը տեսակով՝ Prevotella, Sphingomonas, Pseudomonas, Acinetobacter, Fusobacterium, Megasphaera, Veillonella, Staphylococcus և Streptococcus: Համարվում է, որ այս միկրոօրգանիզմներից որոշները կարող են շատ լուրջ հիվանդություններ հարուցել այն մարդկանց մոտ, որոնք ունեն թուլացած իմունային համակարգ։ Այդ բակտերիաներից են՝ Streptococcus pyogenes, Haemophilus influenzae, Streptococcus pneumoniae, Neisseria meningitidis և Staphylococcus aureus: Սնկային տեսակները որոնք կազմում են թոքային միկրոբիոմը, հետևյալն են՝ Candida, Malassezia, Neosartorya, Saccharomyces, Aspergillus և ուրիշներ[32]։
Բակտորիալ և սնկային տեսակների անսովոր հարաբրություն շնչառական ուղիներում նկատվում է մուկովիսցիդոզի (ցիստիկ ֆիբրոզ) ժամանակ[32][72]։ Մուկովիսցիդոզով հիվանդների մանրէային միջավայրը հաճախ պարունակում է հակաբիոտիկակայուն և դանդաղ աճող բակտերիաները, և այդ ախտածինների հաճախականությունը տատանվում է տարիքին զուգընթաց[72]։
Ավանդաբար համարվում է, որ լեղային ծորանները սովորաբար ստերիլ են, իսկ միկրոօրգանիզմնեի առկայությունը լեղուղիներում ախտաբանական գործընթացի ցուցիչ է։ Այս ենթադրությունները առաջարկվեցին այն բանից հետո, երբ լեղուղիներից հնարավոր չեղավ առանձնացնել մանրէային շտամներ։ 2013 թվականին հայտնի դարձավ, որ լեղային ուղիների նորմալ միկրոբիոտիան իրենից ներկայացնում է առանձին ֆունկցիոնալ շերտ, որոնք պաշտպանում են լեղուղիները արտաքինից ներթափանցող ախտածին միկրոօրգանիզմների գաղութացումից։
Մետագենոմային և համաճարակաբանական հետազոտությունները ցույց տվեցին մարդկային միկրոբիոմի կարևորությունը հիվանդությունների լայն տեսականին կանխելու գործում՝ սկսած շաքարային դիաբետի երկրորդ տեսակից, ճարպակալումից, աղիքային բորբոքային հիվանդություններից մինչև Պարկինսոնի հիվանդություն և նույնիսկ հոգեբուժական հիվանդություններ, այնպիսին ինչպիսինն է դեպրեսիան[73]։ Աղիքային միկրոբիոմի և տարբեր մանրէների սիմբիոտիկ կապը կարող է ազդել մարդու իմունային համակարգի վրա[74]։ Առավել առաջադեմ ուսումնասիրությունները ցույց են տալիս, որ միկրոբիոմի կորեկցիոն բուժումը կարող է լինել էֆֆեկտիվ շաքարային դիաբետի բուժման ժամանակ[75]։
Չնայած նրան, որ քաղցկեղը համարվում է ընտանեկան գենետիկական հիվանդության և արտաքին գործոնների փոխազդեցության արդյունք, միկրոբները ներգրավված են դրա զարգացման դեպքերի 20%-ում[76]։
Հաստ աղու քաղցկեղի որոշ գործոններ ցույց են տալիս, որ հաստ աղում մանրէների թիվը միլիոն անգամ ավելի են, քան բարակ աղիներում և ուղիղ 12 անգամ շատ դեպքերում քաղցկեղը հաստ աղում համեմատած բարակ աղու ավելի շատ է հանդիպում։ Կա ենթադրություն, որ ախտածին միկրոբիոմը ունի մեծ դերակատրում ուղիղ աղու քաղցկեղի զարգացման ժամանակ[77]։
Մանրէաբանական հետազոտությունը կարող է օգտագործվել որպես կոլոռեկտալ քաղցկեղի կանխատեսող գործիք՝ գնահատման համար[77]։ Միկրոբիոտիան կարող է քաղցկեղածնության պատճառ դառնալ 3 հիմնական ուղիներով՝ (i) փոխելով պրոլիֆերացիայի և ուռուցքային բջիջների մահվան դիսբալանսը, (ii) առաջացնելով իմունային համակարգի գործառույթի խանգարում և (iii) ազդեցություն ունենալով նյութափոխանակության վրա, փոխելով սննդի և դեղորայքի ազդեցությունները[77]։
Տարբեր հատվածներում առաջացած ուռուցքները սովորաբար պարունակում են միկրոբիոտիա։ Այս հատվածներում միկրոբները ավելի լավ են հարմարված՝ նվազած թթվածնի և սննդի լրացուցիչ աղբյուրների պայմաններում։ Յուրահատուկ միկրոբների պոպուլյացիայի քչացումը կամ հարուցված օքսիդատիվ սթրեսը կարող է մեծացնել քաղցկեղի զարգացման ռիսկը[76]։ 1030 հայտնի մանրեներից առանձնացված են որպես քաղցկեղածին քաղցկեղի դեմ պայքարի միջազգային գործակալության կողմից[76][77]։ Բակտերիաները կարող են արտադրել սպիտակուցներ և այլ գործոններ, որոնք ուղղակիորեն վերահսկում են մարդկանց բջիջների պրոլիֆերացիան, որը կարող է արագացնել և թուլացնել տիրոջ օրգանիզմի իմունային համակարգը, այդ թվում հարուցում են սուր և քրոնիկական բորբոքումներ։ Տիրոջ օրգանիզմի և միկրոբիոտիայի միջև հավասարակշռության խանգարումը նվազեցնում է չարորակ նորագոյացություններին օրգանիզմի դիմադրողականությունը՝ առաջացնելով բորբոքման և քաղցկեղի հնարավորություն։ Պաշտպանական խոչընդոտները հաղթահարելուց հետո մանրէները տարբեր եղանակներով առաջացնում են իմունային հիշողությունը ճնշող և հակաբորբոքային օրգանիզմներ։ Օրինակ՝ քաղցկեղի առաջացման հետ կապված մանրէները, հավանաբար ակտիվացնում են NF-kB ազդանշանների հաղորդումը ուռուցքների միկրոմիջավայրում[76]։ Այլ ռեցեպտորներ ինչպիսիքն են Nod-նման ընկալիչները կարող են դեր ունենալ կոլոռեկտալ քաղցկեղի առաջացման հարցում։ Նմանապես Helicobacter pylori-ն ըստ երևույթին, մեծացնում է ստամոքսի քաղցկեղի ռիսկը, իր քրոնիկական բորբոքում առաջացնելու հատկության շնորհիվ[77]։
Աղիների բորբոքային հիվանդություններ են հանդիսանում խոցային կոլիտը և կրոնի հիվանդությունը։ Այս հիվանդությունները ուղեկցվում են աղիների միկրոբիոմի բաղադրության փոփոխությամբ (հայտնի է որպես դիսբիոզ) և դրսևորվում է աղիներում մանրէային բազմազանության նվազեցմամբ[78][79]։ Հայտնաբերվել է, որ դիսբիոզը փոխկապակցված է տիրոջ օրգանիզմի գենային խանգարումների հետ, որոնք փոխում են մարդու բնածին իմունային պատասխանը[78]։
Մարդու իմունային անբավարարության վիրուսովհարուցված հիվանդությունը հանգեցնում է աղիքային միկրոբիոմի փոփոխությանը։ Վիրուսը խաթարում է էպիթելային պատնեշի ամբողջականությունը՝ ազդելով ամուր կոնտակտների վրա։ Այս խանգարումները հանգեցնում են ՄԻԱՎ-ով տառապող մարդկանց մոտ բորբոքման զարգացմանը[80]։
Հեշտոցային միկրոբիոտիան խաղում է կարևոր դեր ՄԻԱՎ-ի փոխանցման հարցում։ Հիվանդանալու վտանգը բավականին մեծ է, եթե կինը ունի բակտերիալ վագինոզ։ Վարակվելու հավանականությունը նվազում է, եթե հեշտոցում Lactobacillus-ի քանակը ավելանում է, ինչը հանգեցնում է հակաբորբոքային վիճակի զարգացմանը[80]։
Նախնական ուսումնասիրությունները ցույց են տալիս, որ մարդու օրգանիզմում միկրոբիոմի փոփոխություններ կարող են առաջանալ մեկ այլ երկիր տեղափոխվելիս[81][82] : Պարզվել է, որ տեսակային բազմազանության զգալի նվազում ավելի բնորոշ է ճարպոտ մարդկանց և ներգաղթյալների երեխաներին[81][82]։
Seamless Wikipedia browsing. On steroids.
Every time you click a link to Wikipedia, Wiktionary or Wikiquote in your browser's search results, it will show the modern Wikiwand interface.
Wikiwand extension is a five stars, simple, with minimum permission required to keep your browsing private, safe and transparent.