element químic amb nombre atòmic 74 From Wikipedia, the free encyclopedia
El tungstè o wolframi és un element químic amb el símbol químic W i el nombre atòmic 74. El tungstè només es troba a la Terra combinat en compostos químics. Les menes més importants són la wolframita i la scheelita. L'element pur té unes característiques físiques fortes, especialment el fet que té el punt de fusió més alt de tots els metalls sense aliar i el segon més alt de tots els elements després del carboni. També és remarcable la seva alta densitat, 19,3 vegades la de l'aigua. Aquesta densitat és lleugerament superior a la de l'urani i un 71 % més que la del plom.[3] El tungstè policristal·lí és dur i fràgil; tanmateix, el tungstè monocristal·lí pur és més dúctil, i es pot tallar amb una serra d'arquet.[4]
| Tungstè | ||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
74W | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Aspecte | ||||||||||||||||||||||||||||||||||||||||||||||||||||
Blanc grisós, brillant Cristalls evaporats de tungstè i un cub d'1 cm³  Línies espectrals de tungstè | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Propietats generals | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Nom, símbol, nombre | Tungstè, W, 74 | |||||||||||||||||||||||||||||||||||||||||||||||||||
| Categoria d'elements | Metalls de transició | |||||||||||||||||||||||||||||||||||||||||||||||||||
| Grup, període, bloc | 6, 6, d | |||||||||||||||||||||||||||||||||||||||||||||||||||
| Pes atòmic estàndard | 183,84 | |||||||||||||||||||||||||||||||||||||||||||||||||||
| Configuració electrònica | [Xe] 4f14 5d4 6s2[1] 2, 8, 18, 32, 12, 2 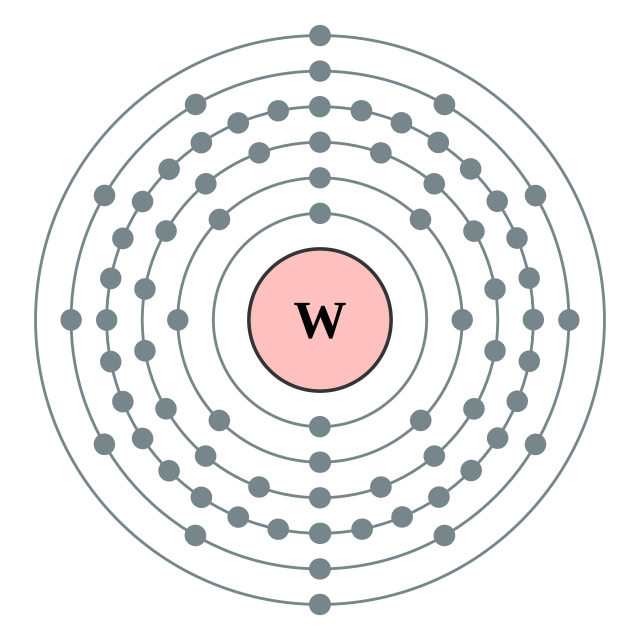 | |||||||||||||||||||||||||||||||||||||||||||||||||||
| Propietats físiques | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Fase | Sòlid | |||||||||||||||||||||||||||||||||||||||||||||||||||
| Densitat (prop de la t. a.) |
19,25 g·cm−3 | |||||||||||||||||||||||||||||||||||||||||||||||||||
| Densitat del líquid en el p. f. |
17,6 g·cm−3 | |||||||||||||||||||||||||||||||||||||||||||||||||||
| Punt de fusió | 3.695 K, 3.422 °C | |||||||||||||||||||||||||||||||||||||||||||||||||||
| Punt d'ebullició | 5.828 K, 5.555 °C | |||||||||||||||||||||||||||||||||||||||||||||||||||
| Punt crític | 13.892 K, MPa | |||||||||||||||||||||||||||||||||||||||||||||||||||
| Entalpia de fusió | 35,3 kJ·mol−1 | |||||||||||||||||||||||||||||||||||||||||||||||||||
| Entalpia de vaporització | 806,7 kJ·mol−1 | |||||||||||||||||||||||||||||||||||||||||||||||||||
| Capacitat calorífica molar | 24,27 J·mol−1·K−1 | |||||||||||||||||||||||||||||||||||||||||||||||||||
| Pressió de vapor | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Propietats atòmiques | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Estats d'oxidació | 6, 5, 4, 3, 2, 1, 0, −1, −2 (òxid àcid feble) | |||||||||||||||||||||||||||||||||||||||||||||||||||
| Electronegativitat | 2,36 (escala de Pauling) | |||||||||||||||||||||||||||||||||||||||||||||||||||
| Energies d'ionització | 1a: 770 kJ·mol−1 | |||||||||||||||||||||||||||||||||||||||||||||||||||
| 2a: 1.700 kJ·mol−1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Radi atòmic | 139 pm | |||||||||||||||||||||||||||||||||||||||||||||||||||
| Radi covalent | 162±7 pm | |||||||||||||||||||||||||||||||||||||||||||||||||||
| Miscel·lània | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Estructura cristal·lina | Cúbica centrada en la cara  | |||||||||||||||||||||||||||||||||||||||||||||||||||
| Ordenació magnètica | Paramagnètic[2] | |||||||||||||||||||||||||||||||||||||||||||||||||||
| Resistivitat elèctrica | (20 °C) 52,8 nΩ·m | |||||||||||||||||||||||||||||||||||||||||||||||||||
| Conductivitat tèrmica | 173 W·m−1·K−1 | |||||||||||||||||||||||||||||||||||||||||||||||||||
| Dilatació tèrmica | (25 °C) 4,5 µm·m−1·K−1 | |||||||||||||||||||||||||||||||||||||||||||||||||||
| Mòdul d'elasticitat | 411 GPa | |||||||||||||||||||||||||||||||||||||||||||||||||||
| Mòdul de cisallament | 161 GPa | |||||||||||||||||||||||||||||||||||||||||||||||||||
| Mòdul de compressibilitat | 310 GPa | |||||||||||||||||||||||||||||||||||||||||||||||||||
| Coeficient de Poisson | 0,28 | |||||||||||||||||||||||||||||||||||||||||||||||||||
| Duresa de Mohs | 7,5 | |||||||||||||||||||||||||||||||||||||||||||||||||||
| Duresa de Vickers | 3.430 MPa | |||||||||||||||||||||||||||||||||||||||||||||||||||
| Duresa de Brinell | 2.570 MPa | |||||||||||||||||||||||||||||||||||||||||||||||||||
| Nombre CAS | 7440-33-7 | |||||||||||||||||||||||||||||||||||||||||||||||||||
| Isòtops més estables | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Article principal: Isòtops del tungstè | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||||||||||||
El tungstè és l'únic metall de la tercera sèrie de transició que es troba en biomolècules, i l'element utilitzat per éssers vius més pesant conegut.[5][6]

Fa més de 350 anys, els fabricants de porcellana a la Xina van incorporar un color préssec únic als seus dissenys mitjançant un pigment de tungstè que no es coneixia a Occident. El 1779, el químic i mineralogista irlandès Peter Woulfe (1727-1803), estudiant una mostra del mineral wolframita suggerí que podria contenir un nou element químic. Pocs anys després, el 1781, els químics suecs Carl Wilhelm Scheele (1742-1786) i Torbern Olof Bergman (1735-1784) proposaren que es podria obtenir un nou element reduint l'àcid túngstic obtingut del mineral scheelita, aleshores anomenat tungsten .[7]

El 1783, a Espanya, els germans Juan José de Elhúyar i Fausto de Elhúyar i Zubice, naturals de Logronyo i de família basco-francesa, trobaren un àcid a partir de la wolframita idèntic a l'àcid túngstic. Cal dir que Juan José havia ampliat estudis a la Universitat d'Uppsala amb Torben Bergmann i havia visitat a Scheele el 1782. Aconseguiren aïllar el nou element per mitjà d'una reducció amb carbó vegetal en el laboratori de la Reial Societat Bascongada d'Amics del País, al Seminari de Bergara, Guipúscoa.[8]

Mesclaren la wolframita amb carbonat de potassi i escalfaren la mescla obtenint una sal blanca, la qual tractaren amb àcid nítric i es formà una pols groga que, en escalfar-la intensificava el color groc. La sal blanca és el tungstat de potassi:[8]
En tractar el tungstat de potassi amb àcid nítric donà l'àcid túngstic:[8]

Escalfant l'àcid túngstic s'obté l'òxid de tungstè(VI):[8]
Finalment, van poder obtenir el metall pur, reduint l'òxid amb pols de carbó, en un gresol refractari ben tapat; és a dir, aconseguint generar a l'interior del gresol una atmosfera reductora de monòxid de carboni:[8]
El 28 de setembre de 1783 presentaren el treball a les Juntes Generals sota el nom: Análisis químico del volfram, y examen de un nuevo metal, que entra en su composición.[8]

La paraula «tungstè» procedix del suec tungsten, mot compost de tung ‘pesant’ i sten, ‘pedra’, és a dir, ‘pedra pesant’.[9] La paraula «wolframi» procedix de l'alemany Wolfram, ‘mineral de tungstat de ferro i manganès, d’on s’extreu el tungstè’, mot compost del mot alemany Wolf ‘llop’ i del mot de l'antic alemany mitjà râm ‘sutge’, ‘brutícia’, usat despectivament pels miners que en trobaren cercant estany.[10]
Al llibre Méthode de Nomenclature Chimique (1787), de Guyton de Morveau (1743-1794) i col., els químics Jean Henri Hassenfratz (1755-1827) i Pierre Auguste Adet (1763-1832) proposaren com a símbol del tungstè una T dins d'un cercle a partir del nom en llatí ‘T’ungstenum, que fou el que elegiren els autors[11] i no el proposat pels descobridors, els germans Juan José i Fausto de Elhúyar.[12] Representaren tots els metalls amb la primera lletra en majúscula del nom en llatí i una segona en minúscula si coincidia la primera. El 1814 el químic suec Jöns J. Berzelius (1779-1848) proposà el mateix sistema de Hassenfratz i Adet, però sense el cercle per a tots els elements químics. Com en altres elements, Berzelius fe servir en diferents parts de l'article original símbols diferents, en aquest cas W de ‘W’olframium i Tn de ‘T’u‘n’gstenum.[13] El 1834 Berzelius considerà millor el nom wolframi perquè el mineral tungsten s'havia reanomenat scheelita i generava confusió, i anomenar al nou element scheelium presentava dificultats en suec.[14] Aquesta proposta fou acceptada pels químics suecs i alemanys, però no pels francesos i britànics que mantingueren el nom emprat pels autors del Méthode.[15]
Durant molts d'anys es feren servir els dos noms de l'element, però el símbol que fou adoptat pels químics fou la W. El 2005 en la nova edició del Red Book de la Unió Internacional de Química Pura i Aplicada (IUPAC) el nom oficial elegit fou tungsten. Els químics espanyols presentaren una queixa defensant que el nom elegit pels descobridors espanyols era wolframium. Però la queixa no fou acceptada, malgrat que es permeté usar wolframio en castellà i altres llengües.[16][17]


El tungstè és un element poc abundant a l'escorça terrestre. Amb una concentració mitjana d'1 ppm, ocupa la 58a posició quant a abundància dels elements químics. En els sols se'l pot trobar en concentracions entre 1 i 2,5 ppm i a l'aigua de la mar la concentració mitjana és de 90 ppt. No se'n troba a l'atmosfera.[18]
El wolframi s'extreu de diversos minerals wolfràmics, com la wolframita , la scheelita , la ferberita , la hübnerita i la stolzita . S'han descrit quaranta-nou minerals que presenten tungstè en la seva composició. Els que en presenten en major abundància, més del 70 %, són: qusongita 93,45 %, krasnogorita 79,30 %, elsmoreïta 76,68 %, tungstenita 74,14 % i tungstita 73,58 %.[19]
El principal productor mundial de tungstè el 2022 fou la Xina amb 71.000 t, seguida del Vietnam (4.800 t), Rússia (2.300 t), Bolívia (1.400 t) i Ruanda (1.100 t). La producció mundial fou de 84.000 t i les reserves s'han calculat en 3,8 × 106 t.[20]
Per la seva obtenció, es fonen els minerals amb carbonat de sodi per adquirir una sal soluble que comprèn el wolframi. Posteriorment, es tracta amb àcid clorhídric per obtenir òxid de wolframi. Finalment, es redueix l'òxid per mitjà d'un corrent d'hidrogen. Així s'obté pols de wolframi que, després, es reescalfa per sinteritzar-lo, compactar-lo, forjar-lo i laminar-lo. Però a causa del seu gran temperament, s'han de fer refredaments molt lents en els recuits, fer recuits isotèrmics i temprar-lo amb dos banys.
Per obtenir-lo, en estat pur, amb la metal·lúrgia és senzill, però l'elevat punt de fusió del metall dificulta el tractament del producte final. El wolframi es pot treballar amb forjat, trefilat, extrusió i sinterització.
El tungstè és un metall no fèrric i refractari de color gris acerós brillant, amb un punt de fusió de 3.422 °C (el més alt de tots els metalls i el segon de tots els elements), un d'ebullició de 5.555 °C; molt dur i dens (densitat 19,3 g/cm³ a 20 °C); fràgil, resistent a la corrosió i de bona conductivitat elèctrica. Com és un metall tan dur, resulta difícil de mecanitzar. Tot i això, és molt dúctil, per obtenir fils d'aquest metall es necessita emprar fileres de diamant. També té molta resistència a la tracció. Això permet treballar el ferro a temperatures extremadament altes sense perdre les seves propietats físiques.[21]

La configuració electrònica del tungstè és [Xe] 4f145d46s2 i els estats d'oxidació del tungstè són: +2, +3, +4,+5 i +6.[21] A temperatura ambient, el tungstè no reacciona amb l'aire ni amb l'oxigen. A temperatures elevades es forma l'òxid de tungstè(VI) . El metall de tungstè finament dividit és pirofòric.[22]

El tungstè reacciona directament amb el fluor a temperatura ambient per formar fluorur de tungstè(VI) . Amb el clor hi reacciona a 250 °C i també amb el brom per formar, respectivament, clorur de tungstè(VI) i bromur de tungstè(VI) . En condicions acuradament controlades es forma clorur de tungstè(V) en la reacció entre el metall de tungstè i el clor. Sembla que el tungstè escalfat reacciona fins a cert punt amb el iode. Les reaccions són:[22]
El tungstè o es veu afectat per la majoria dels àcids ni per les bases.[22]
Es coneixen quaranta-dos isòtops del tungstè que tenen nombres màssics del 157 al 197. A la natura hom en troba cinc, de nombres màssics 180, 182, 183, 184 i 186, que presenten les proporcions 0,12 %, 26,50 %, 14,31 %, 30,64 % i 28,43 %. Estables només ho són el tungstè 182 i el tungstè 184. Tanmateix, els altres tres tenen períodes de semidesintegració superiors a l'edat de l'univers (13,8 × 10⁹ anys), per la qual cosa hom pot considerar-los també estables. Els períodes de semidesintegració són t½(180W) = 6,6 × 1017 anys, t½(183W) = 6,7 × 1020 anys i t½(186W) = 2,3 × 1019 anys.[23]

El tungstè, com que resisteix temperatures altes (és el metall amb el punt de fusió més alt 3 422 °C) i té una pressió de vapor baixíssima, fins i tot a altes temperatures, és pràcticament l'únic material utilitzat en la fabricació de filaments de les bombetes de projecció, les làmpades halògenes, les fluorescents, les de descàrrega d'alta intensitat, etc., i com a càtode emissor d'electrons (en tubs de raigs X).[24]

El tungstè forma, junt amb el carboni i el cobalt, el carbur de tungstè (widia), un aliatge de gran duresa que s'utilitza en la fabricació d'eines de tall com ara freses, broques, serres, corones de perforació, etc. L'addició de tungstè (en un 10 %) augmenta la duresa total dels acers d'alta velocitat (HSS, High Speed Steels) i permet treballar a altes temperatures. La bola de la punta dels bolígrafs està feta de carbur de tungstè.[24]
Quan s'afegeix tungstè a l'acer es forma un superaliatge molt resistent que s'empra en la fabricació dels motors dels avions i de les turbines de generació d'energia. L'acer al tungstè s'usa en la fabricació dels discos de les serres de diamant, ja que n'augmenta la resistència.[24]

Els elèctrodes de tungstè amb tori s'usen en soldadures d'acers inoxidables i aliatges especials.[24]
El tungstè s'utilitza en la fabricació de pesos per a la pesca i en perdigons, en substitució del plom.[24] També s’utilitza en la fabricació de puntes de fletxa d'alta qualitat.
Es coneix un paper biològic del tungstè en els organismes procariotes, per bé que encara no en els eucariotes. Els organismes millor caracteritzats pel que fa al seu metabolisme del tungstè són determinades espècies d'arqueus hipertermòfils (Pyrococcus furiosus i Thermococcus litoralis), metanògens (Methanobacterium thermoautotrophicum i Mb. wolfei), bacteris grampositius (Clostridium thermoaceticum, C. formicoaceticum i Eubacterium acidaminophilum), bacteris gramnegatius anaerobis (Desulfovibrio gigas i Pelobacter acetylenicus) i aerobis (Methylobacterium sp. RXM). D'aquestes, només les arquees hipertermòfiles semblen dependre obligatòriament del tungstè. S'han purificat quatre tipus diferents de tungstoenzim que catalitzen l'oxidació reversible dels aldehids.[25]
Seamless Wikipedia browsing. On steroids.
Every time you click a link to Wikipedia, Wiktionary or Wikiquote in your browser's search results, it will show the modern Wikiwand interface.
Wikiwand extension is a five stars, simple, with minimum permission required to keep your browsing private, safe and transparent.