Seaborgi
element químic amb nombre atòmic 106 From Wikipedia, the free encyclopedia
Remove ads
El seaborgi és l'element químic sintètic de símbol Sg i nombre atòmic 106. A la taula periòdica ocupa una posició al 7è període i forma part dels elements de transició del grup 6 i El seaborgi està anomenat en honor del físic i químic nord-americà Glenn T. Seaborg, descobridor de deu elements transurànids i pioner en la física nuclear.
Remove ads
Història
Tant el reconeixement de la síntesi del seaborgi com l'assignació d'un nom foren objecte d'una llarga controvèrsia, a causa de la competència entre investigadors soviètics i estatunidencs en els anys finals de la Guerra Freda.[5] Al juny de 1974, un equip d'investigadors de l'Institut de Recerca Nuclear de Dubnà, aleshores Unió Soviètica, encapçalats per Iuri Oganessian (1933), anuncià que havien obtingut i identificat l'element 106 mitjançant el bombardeig dels isòtops plom 207 i plom 208 amb crom 54.[6] Les reaccions són:[5]
El setembre d'aquest mateix any, un grup d'investigadors estatunidencs de la Universitat de Califòrnia a Berkeley i de Laboratori Nacional Lawrence Livermore, dirigit per Albert Ghiorso (1915-2010), informaren de l'obtenció i identificació de l'isòtop 263 del mateix element,[7] amb una vida mitjana de 0,9 segons, bombardejant californi 249 amb oxigen 18, segons la reacció:[5]
El descobriment fou reclamat pels dos grups d'investigadors i no es va resoldre fins que, en 1992, la Unió Internacional de Química Pura i Aplicada (IUPAC) conclogué que ambdós treballs s'havien dut a terme independentment al mateix temps, però que l'únic que demostrava la síntesi del nou element era el de l'equip estatunidenc.[5]

Després de moltes controvèrsies respecte al nom definitiu que se li podia assignar, al març de 1994, en la 207 reunió internacional de la Societat Química Americana en San Diego, decidiren proposar seaborgi en honor del químic estatunidenc Glenn T. Seaborg (1912-1999), co-descobridor de plutoni, americi, curi, berkeli, californi, einsteini, fermi, mendelevi i nobeli, i premi Nobel de Química en 1951. Aquesta decisió fou rebutjada per la IUPAC perquè fins llavors no se li podia assignar a un element el nom d'una persona viva, com era el cas de Seaborg en aquest moment. La American Chemical Society es mantingué ferma amb el nom fins que, finalment, en 1995, la IUPAC l'acceptà, juntament amb el símbol Sg. Fins al dia d'avui, juntament amb l'oganessó, són els únics elements que han estat nomenats en honor d'una persona viva en el moment de la seva assignació.[5]
Remove ads
Propietats
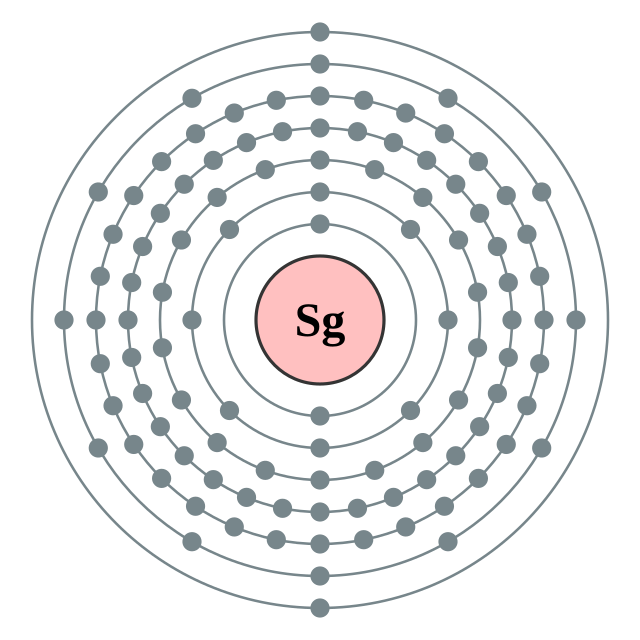
El seaborgi té una configuració electrònica calculada . És d'esperar que sigui sòlid en condicions normals, amb una estructura cristal·lina cúbica centrada en el cos similar al tungstè, l'element anterior del seu grup, el 6, en la taula periòdica, format per crom, molibdè i tungstè, i probablement la seva química és similar a la dels dos darrers. Tots tenen un estat d'oxidació +6 i els triòxids són solubles en àlcalis per a donar oxoanions. L'estabilitat de l'estat d'oxidació 6 augmenta en baixar en el grup, per la qual cosa aquest hauria de ser l'estat d'oxidació més estable de l'element. De fet, aquest és l'únic estat d'oxidació que es coneix experimentalment, a més del zero. Els estats +5 i +4 haurien de ser menys estables i l'estat +3, el més comú per al crom, hauria de ser el menys estable per al seaborgi. Els hexahalogenurs se suposa que seran inestables, i s'espera una major estabilitat de l'hexabromur, .[5]
Característiques físiques
S'espera que el seaborgi sigui sòlid en condicions normals i assumeixi una estructura cristal·lina cúbica centrat en el cos, similar al seu més lleuger congènere el tungstè (també anomenat wolframi).[8] Les primeres prediccions van estimar que hauria de ser un metall molt pesat amb una densitat al voltant de 35.0 g/cm3,[9] però càlculs el 2011 i el 2013 van predir un valor una mica més baix de 23–24 g/cm3.[10][11]
Remove ads
Isòtops
S'han obtingut fins a 18 isòtops radioactius del seaborgi, ja sigui mitjançant la fusió de dos àtoms o mitjançant la descomposició d'elements més pesants (hassi 269, darmstadti 271 i copernici 275).[12] Exemple d'aquest darrer cas hi ha la desintegració del hassi 269 en seaborgi 265 per emissió d'una partícula alfa:[13]
Els isòtops de seaborgi tenen nombres màssics des de 258 fins a 273 i amb períodes de semidesintegració des de 2,9 ms () fins a 3,1 min (). Els més pesants , i , són els més longeus, amb períodes de semidesintegració d'alguns minuts. Dels isòtops i , solament se'n coneixen estats metaestables.[14]
Els elements superpesants com el seaborgi es produeixen bombardejant elements més lleugers en acceleradors de partícules que indueixen reaccions de fusió. Mentre que la majoria dels isòtops de seaborgi es poden sintetitzar directament d'aquesta manera, alguns de més pesats només s'han observat com a productes de descomposició d'elements amb nombres atòmics més alts.[15]
Depenent de les energies involucrades, les reaccions de fusió que generen elements superpesants se separen en "calents" i "fredes". En les reaccions de fusió en calent, els projectils molt lleugers i d'alta energia s'acceleren cap a objectius molt pesats (actínids), cosa que dona lloc a nuclis compostos amb alta energia d'excitació (~40–50 MeV) que es poden fisionar o evaporar diversos (3 a 5) neutrons.[15] En les reaccions de fusió en fred, els nuclis fusionats produïts tenen una energia d'excitació relativament baixa (~10–20 MeV), fet que disminueix la probabilitat que aquests productes pateixin reaccions de fissió. l'estat fonamental requereixen l'emissió de només un o dos neutrons i, per tant, permeten la generació de més productes rics en neutrons.[16] Eaquest últim és un concepte diferent d'aquell en què la fusió nuclear pretenia aconseguir-se en condicions de temperatura ambient (vegeu fusió freda).[17]
El seaborgi no té isòtops estables o naturals. S'han sintetitzat diversos isòtops radioactius al laboratori, ja sigui mitjançant la fusió de dos àtoms o mitjançant l'observació de la descomposició d'elements més pesants. S'han detectat dotze isòtops diferents de seaborgi amb masses atòmiques 258–267, 269 i 271, tres dels quals, seaborgi-261, 263 i 265, tenen estats metaestables coneguts. Tots aquests decauen només a través de la desintegració alfa i la fissió espontània, amb l'única excepció del seaborgi-261 que també pot patir captura d'electrons a dubni-261.[18]
Hi ha una tendència cap a l'augment de la vida mitjana dels isòtops més pesants; per tant, els tres isòtops més pesats coneguts, 267Sg, 269Sg i 271Sg, també són els més longeus, amb vides mitjanes en minuts. Es prediu que alguns altres isòtops en aquesta regió tindran vides mitjanes comparables o fins i tot més llargues. A més, 263Sg, 265Sg i 265mSg tenen vides mitjanes mesurades en segons. Tots els isòtops restants tenen vides mitjanes mesurades en mil·lisegons, amb l'excepció de l'isòtop de vida més curta, 261 mSg, amb una vida mitjana de només 92 microsegons.[18]
Els isòtops rics en protons de 258Sg a 261Sg es van produir directament per fusió en fred; tots els isòtops més pesats es van produir a partir de la desintegració alfa repetida dels elements més pesats hassium, darmstadtium i flerovium, amb l'excepció dels isòtops 263mSg, 264Sg, 265Sg i 265mSg, que es van produir directament per fusió en calent mitjançant la irradiació d'objectius d'actínids. Els dotze isòtops de seaborgi tenen vides mitjanes que van des de 92 microsegons per a 261 mSg fins a 14 minuts per 269 Sg.[19][18]
Remove ads
Referències
Enllaços externs
Wikiwand - on
Seamless Wikipedia browsing. On steroids.
Remove ads


![{\displaystyle {{\vphantom {A}}_{\hphantom {82}}^{\hphantom {207}}{\mkern {-1.5mu}}{\vphantom {A}}_{{\vphantom {2}}{\llap {\smash[{t}]{82}}}}^{{\smash[{t}]{\vphantom {2}}}{\llap {207}}}\mathrm {Pb} {}+{}{\vphantom {A}}_{\hphantom {24}}^{\hphantom {54}}{\mkern {-1.5mu}}{\vphantom {A}}_{{\vphantom {2}}{\llap {\smash[{t}]{24}}}}^{{\smash[{t}]{\vphantom {2}}}{\llap {54}}}\mathrm {Cr} {}\mathrel {\longrightarrow } {}{\vphantom {A}}_{\hphantom {106}}^{\hphantom {260}}{\mkern {-1.5mu}}{\vphantom {A}}_{{\vphantom {2}}{\llap {\smash[{t}]{106}}}}^{{\smash[{t}]{\vphantom {2}}}{\llap {260}}}\mathrm {Sg} {}+{}{\vphantom {A}}_{\hphantom {0}}^{\hphantom {1}}{\mkern {-1.5mu}}{\vphantom {A}}_{{\vphantom {2}}{\llap {\smash[{t}]{0}}}}^{{\smash[{t}]{\vphantom {2}}}{\llap {1}}}\mathrm {n} }}](http://wikimedia.org/api/rest_v1/media/math/render/svg/9c7213da6164de552b343461fe1da55b790536cf)
![{\displaystyle {{\vphantom {A}}_{\hphantom {82}}^{\hphantom {208}}{\mkern {-1.5mu}}{\vphantom {A}}_{{\vphantom {2}}{\llap {\smash[{t}]{82}}}}^{{\smash[{t}]{\vphantom {2}}}{\llap {208}}}\mathrm {Pb} {}+{}{\vphantom {A}}_{\hphantom {24}}^{\hphantom {54}}{\mkern {-1.5mu}}{\vphantom {A}}_{{\vphantom {2}}{\llap {\smash[{t}]{24}}}}^{{\smash[{t}]{\vphantom {2}}}{\llap {54}}}\mathrm {Cr} {}\mathrel {\longrightarrow } {}{\vphantom {A}}_{\hphantom {106}}^{\hphantom {260}}{\mkern {-1.5mu}}{\vphantom {A}}_{{\vphantom {2}}{\llap {\smash[{t}]{106}}}}^{{\smash[{t}]{\vphantom {2}}}{\llap {260}}}\mathrm {Sg} {}+{}2\,{\vphantom {A}}_{\hphantom {0}}^{\hphantom {1}}{\mkern {-1.5mu}}{\vphantom {A}}_{{\vphantom {2}}{\llap {\smash[{t}]{0}}}}^{{\smash[{t}]{\vphantom {2}}}{\llap {1}}}\mathrm {n} }}](http://wikimedia.org/api/rest_v1/media/math/render/svg/dc6b637323c583ab35d8460585637a16124c9ad3)
![{\displaystyle {{\vphantom {A}}_{\hphantom {98}}^{\hphantom {249}}{\mkern {-1.5mu}}{\vphantom {A}}_{{\vphantom {2}}{\llap {\smash[{t}]{98}}}}^{{\smash[{t}]{\vphantom {2}}}{\llap {249}}}\mathrm {Cf} {}+{}{\vphantom {A}}_{\hphantom {8}}^{\hphantom {18}}{\mkern {-1.5mu}}{\vphantom {A}}_{{\vphantom {2}}{\llap {\smash[{t}]{8}}}}^{{\smash[{t}]{\vphantom {2}}}{\llap {18}}}\mathrm {O} {}\mathrel {\longrightarrow } {}{\vphantom {A}}_{\hphantom {106}}^{\hphantom {263}}{\mkern {-1.5mu}}{\vphantom {A}}_{{\vphantom {2}}{\llap {\smash[{t}]{106}}}}^{{\smash[{t}]{\vphantom {2}}}{\llap {263}}}\mathrm {Sg} {}+{}4\,{\vphantom {A}}_{\hphantom {0}}^{\hphantom {1}}{\mkern {-1.5mu}}{\vphantom {A}}_{{\vphantom {2}}{\llap {\smash[{t}]{0}}}}^{{\smash[{t}]{\vphantom {2}}}{\llap {1}}}\mathrm {n} }}](http://wikimedia.org/api/rest_v1/media/math/render/svg/c3d1da7a12a7caaab9458ac2542b1733b9d647e0)
![{\displaystyle {[\mathrm {Rn} ]~5\mathrm {f} {\vphantom {A}}^{14}~6\mathrm {d} {\vphantom {A}}^{4}~7\mathrm {s} {\vphantom {A}}^{2}}}](http://wikimedia.org/api/rest_v1/media/math/render/svg/2cf55c71637f853b91a450b82293b7484c718a5c)
![{\displaystyle {\mathrm {SgBr} {\vphantom {A}}_{\smash[{t}]{6}}}}](http://wikimedia.org/api/rest_v1/media/math/render/svg/e4fe7547ac00bd54734a78e71ed016a88d8c5165)
![{\displaystyle {{\vphantom {A}}_{\hphantom {108}}^{\hphantom {269}}{\mkern {-1.5mu}}{\vphantom {A}}_{{\vphantom {2}}{\llap {\smash[{t}]{108}}}}^{{\smash[{t}]{\vphantom {2}}}{\llap {269}}}\mathrm {Hs} {}\mathrel {\longrightarrow } {}{\vphantom {A}}_{\hphantom {106}}^{\hphantom {265}}{\mkern {-1.5mu}}{\vphantom {A}}_{{\vphantom {2}}{\llap {\smash[{t}]{106}}}}^{{\smash[{t}]{\vphantom {2}}}{\llap {265}}}\mathrm {Sb} {}+{}{\vphantom {A}}_{\hphantom {2}}^{\hphantom {4}}{\mkern {-1.5mu}}{\vphantom {A}}_{{\vphantom {2}}{\llap {\smash[{t}]{2}}}}^{{\smash[{t}]{\vphantom {2}}}{\llap {4}}}\mathrm {He} }}](http://wikimedia.org/api/rest_v1/media/math/render/svg/d3e5fde057c1e764128e666206a71c280d1b3f81)
![{\displaystyle {{\vphantom {A}}_{\hphantom {}}^{\hphantom {258}}{\mkern {-1.5mu}}{\vphantom {A}}_{{\vphantom {2}}{\llap {\smash[{t}]{}}}}^{{\smash[{t}]{\vphantom {2}}}{\llap {258}}}\mathrm {Sg} }}](http://wikimedia.org/api/rest_v1/media/math/render/svg/24ab6e5a16303ec58a61fb124233c9aaf2c5cd6d)
![{\displaystyle {{\vphantom {A}}_{\hphantom {}}^{\hphantom {269}}{\mkern {-1.5mu}}{\vphantom {A}}_{{\vphantom {2}}{\llap {\smash[{t}]{}}}}^{{\smash[{t}]{\vphantom {2}}}{\llap {269}}}\mathrm {Sg} }}](http://wikimedia.org/api/rest_v1/media/math/render/svg/1ca8416bafdcb45bf2b9a82e3e0301088c05517a)
![{\displaystyle {{\vphantom {A}}_{\hphantom {}}^{\hphantom {267}}{\mkern {-1.5mu}}{\vphantom {A}}_{{\vphantom {2}}{\llap {\smash[{t}]{}}}}^{{\smash[{t}]{\vphantom {2}}}{\llap {267}}}\mathrm {Sg} }}](http://wikimedia.org/api/rest_v1/media/math/render/svg/6cf299954cb4acc7be558130beb02bb766a4205c)
![{\displaystyle {{\vphantom {A}}_{\hphantom {}}^{\hphantom {271}}{\mkern {-1.5mu}}{\vphantom {A}}_{{\vphantom {2}}{\llap {\smash[{t}]{}}}}^{{\smash[{t}]{\vphantom {2}}}{\llap {271}}}\mathrm {Sg} }}](http://wikimedia.org/api/rest_v1/media/math/render/svg/c29521df19fa39de46be59c703186eb38ebc5b44)
![{\displaystyle {{\vphantom {A}}_{\hphantom {}}^{\hphantom {265}}{\mkern {-1.5mu}}{\vphantom {A}}_{{\vphantom {2}}{\llap {\smash[{t}]{}}}}^{{\smash[{t}]{\vphantom {2}}}{\llap {265}}}\mathrm {Sg} }}](http://wikimedia.org/api/rest_v1/media/math/render/svg/7424525a65ea5900eab5a6ff40c220ed8e4fa871)