
Метан
From Wikipedia, the free encyclopedia
Метан (), познат и као блатни гас је најпростији засићени угљоводоник (алкан). Уколико владају нормални услови он је безбојан гас. У природи метан настаје услед бескисеоничног распада органских материја (нпр. у мочварама). Метан је главни састојак земног гаса. Користи се као гас за грејање и као сировина за добијање органских једињења. Запаљен гори светлим модрикастим пламеном, а његовим сагоревањем у присуству кисеоника настаје угљен-диоксид и вода. Нерастворан је у води, а у смеши са ваздухом врло експлозиван. Релативно велика количина метана на Земљи даје му статус алтернативног, атрактивног извора енергије. Међутим, пошто је на нормалној температури и притиску у гасовитом стању, метан је веома тешко транспортовати из његових налазишта. Као гас, обично се превози путем гасовода или цистернама утечњен као течност на температури испод -162 °C (као ).
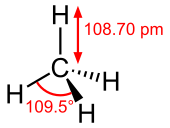 | |||
| |||
| Називи | |||
|---|---|---|---|
| Преферисани IUPAC назив
Метан[1] | |||
| Системски IUPAC назив
Карбан (није препоручен[1]) | |||
Други називи
| |||
| Идентификација | |||
| |||
3Д модел () |
|||
| B01453 | |||
| Бајлштајн | 1718732 | ||
| |||
| 100.000.739 | |||
| број | 200-812-7 | ||
| Гмелин Референца | 59 | ||
| KEGG[2] | |||
| MeSH | Methane | ||
| PA1490000 | |||
| UN број | 1971 | ||
| Својства | |||
| 4 | |||
| Моларна маса | 16,04 g·mol−1 | ||
| Агрегатно стање | Безбојни гас | ||
| Мирис | Без мириса | ||
| Густина | |||
| Тачка топљења | −182,5 °C; −296,4 °F; 90,7 K | ||
| Тачка кључања | −161,50 °C; −258,70 °F; 111,65 K[6] | ||
| 22,7 mg·L−1 | |||
| Растворљивост | Растворан у етанолу, диетил етру, бензену, толуену, метанолу, ацетону и није растворан у води | ||
| 1,09 | |||
| 14 | |||
| Конјугована киселина | Метанијум | ||
| Конјугована база | Метил анјон | ||
| Магнетна сусцептибилност | −12,2×10−6 | ||
| Структура | |||
| Облик молекула (орбитале и хибридизација) | Тетраедар | ||
| Диполни момент | 0 | ||
| Термохемија | |||
| Специфични топлотни капацитет, | 35,69 −1 | ||
Стандардна моларна ентропија (S |
186,25 −1 | ||
Стандардна енталпија стварања (ΔfH |
−74,87 −1 | ||
Стд енталпија сагоревања (298) |
−891,1 до −890,3 −1 | ||
| Опасности[7] | |||
| ГХС пиктограми |  | ||
| ГХС сигналне речи | Опасност | ||
ГХС извештаји опасности |
H220 | ||
ГХС изјаве предрострожност |
P210 | ||
| NFPA 704 | |||
| Тачка паљења | −188 °C (−306,4 °F; 85,1 K) | ||
| 537 °C (999 °F; 810 K) | |||
| Експлозивни лимити | 4,4–17% | ||
| Сродна једињења | |||
Сродна алкани |
|||
Уколико није другачије напоменуто, подаци се односе на стандардно стање материјала (на 25°C [77°F], 100 kPa). | |||
| Референце инфокутије | |||
Молекул метана има облик тетраедра. Атом угљеника с има хибридизацију. Остале орбитале граде хемијску везу са четири атома водоника. Све четири везе су подједнаке (углови између веза износе 109°28') и веома су мало поларизоване, што је заједно са недостатком слободних електронских парова велике постојаности овог једињења. Метан може да учествује само у реакцијама типичним за алкане (нпр: сагоревање).
Метан има потенцијално деловање као стакленички гас са високим потенцијалом за глобално затопљење са индексом од 72 (уз просек од 20 година) односно индексом 25 (уз просек од 100 година)[9]. Метан се у атмосфери оксидује, производећи угљен-диоксид и воду. Због тога, метан у атмосфери има полувреме постојања од око седам година.
Распрострањеност метана у Земљиној атмосфери у току 1998 године је процењена на 1745 (милијардити део, ), а процењује се да се у 1750. години у атмосфери налазило око 700 . Метан може задржавати и до 20 пута више топлоте од угљен-диоксида. У истом периоду (1750—1998) количина 2 у атмосфери је порасла са 278 на 365 . Топлотни ефект због овог повећања количине метана је око једне трећине од истог ефекта повећања 2[10]. Поред тога, постоје огромне али непознате количине метана у облику метан хидрата на дну океана. Земљина кора такође садржи огромне количине метана. Велике количине се произведу анаеробним путем метаногенезе. Остали извори метана су вулканске ерупције и ферментацијом унутар стоке (крава, оваца, коња и других животиња).


