Top Qs
Timeline
Obrolan
Perspektif
Biokimia
kimia mahkluk hidup Dari Wikipedia, ensiklopedia bebas
Remove ads
Biokimia atau kimia hayati, adalah ilmu yang mempelajari proses-proses kimia yang ada di dalam tubuh dan yang berhubungan dengan organisme hidup.[1] Sebagai subdisiplin dari biologi dan kimia, biokimia dapat dibagi menjadi tiga bidang: biologi struktural, enzim, dan metabolisme. Selama beberapa dekade terakhir pada abad ke-20, biokimia telah berhasil menjelaskan proses kehidupan melalui tiga subdisiplin ilmu ini. Hampir semua bidang ilmu hayat sedang ditemukan dan dikembangkan melalui metodologi dan penelitian biokimia.[2] Biokimia berfokus pada pemahaman dasar kimiawi yang memungkinkan molekul biologis memunculkan proses-proses yang terjadi di dalam sel hidup dan di antara sel,[3] yang pada gilirannya berkaitan erat dengan pemahaman jaringan dan organ, serta struktur dan fungsi organisme.[4] Biokimia berkaitan erat dengan biologi molekuler yang mempelajari mekanisme molekuler dari fenomena biologi.[5]
Sebagian besar biokimia berhubungan dengan struktur, fungsi, dan interaksi makromolekul biologis, seperti protein, asam nukleat, karbohidrat, dan lipid. Molekul-molekul ini membangun struktur sel dan melakukan banyak fungsi yang berhubungan dengan kehidupan.[6] Sifat kimiawi sel juga bergantung pada reaksi molekul dan ion kecil. Mereka dapat berupa senyawa anorganik (misalnya air dan ion logam) atau organik (misalnya asam amino yang digunakan untuk menyintesis protein).[7] Mekanisme yang digunakan oleh sel untuk memanfaatkan energi dari lingkungannya melalui reaksi kimia dikenal sebagai metabolisme. Temuan biokimia diterapkan terutama di bidang kedokteran, nutrisi, dan pertanian. Dalam pengobatan, ahli biokimia menyelidiki penyebab dan penyembuhan penyakit.[8] Ilmu gizi mempelajari bagaimana menjaga kesehatan dan kebugaran serta pengaruh dari kekurangan gizi.[9] Di bidang pertanian, ahli biokimia menyelidiki tanah dan pupuk. Meningkatkan budidaya tanaman, penyimpanan tanaman, serta pengendalian hama juga merupakan tujuan penerapan biokimia.
Remove ads
Sejarah
Ringkasan
Perspektif

Menurut definisi yang paling komprehensif, biokimia dapat dilihat sebagai studi tentang komponen dan komposisi makhluk hidup dan bagaimana mereka bersatu dan bekerja sama menjadi bentuk kehidupan. Dalam pengertian ini, sejarah biokimia dapat berasal dari zaman Yunani kuno.[10] Namun, biokimia sebagai disiplin ilmu yang spesifik dimulai sekitar abad ke-19, atau lebih awal, bergantung pada aspek biokimia mana yang difokuskan. Beberapa orang berpendapat bahwa biokimia mungkin dimulai sejak penemuan molekul enzim yang pertama, yaitu diastase (sekarang disebut amilase), pada tahun 1833 oleh Anselme Payen,[11] sementara yang lain menganggap demonstrasi Eduard Buchner mengenai proses biokimia kompleks pertama, yaitu fermentasi alkohol pada ekstrak yang bebas-sel pada tahun 1897 sebagai tanda kelahiran biokimia.[12][13] Beberapa orang juga mungkin menunjuk karya berpengaruh yang terbit pada tahun 1842 oleh Justus von Liebig, Kimia hewan, atau, Kimia organik dalam aplikasinya pada fisiologi dan patologi, yang mempresentasikan teori kimia tentang metabolisme, sebagai permulaan dari biokimia,[10] atau bahkan sejak studi abad ke-18 tentang fermentasi dan respirasi oleh Antoine Lavoisier.[14][15] Banyak pionir lain disebut sebagai pendiri biokimia modern karena membantu mengungkap kompleksitas biokimia. Emil Fischer, yang mempelajari kimia protein,[16] dan F. Gowland Hopkins, yang mempelajari enzim dan sifat dinamis biokimia, mewakili dua contoh ahli biokimia awal.[17]
Istilah "biokimia" sendiri berasal dari gabungan antara biologi dan kimia. Pada tahun 1877, Felix Hoppe-Seyler menggunakan istilah ini (biochemie dalam bahasa Jerman) sebagai sinonim untuk kimia fisiologis dalam kata pengantar untuk edisi pertama Zeitschrift für Physiologische Chemie (Jurnal Kimia Fisiologis) ketika ia menyarankan untuk mendirikan lembaga yang didedikasikan untuk bidang studi ini.[18][19] Ahli kimia Jerman Carl Neuberg sering dikutip bahwa telah menciptakan kata tersebut pada tahun 1903,[20][21][22] sementara beberapa orang lain mengkreditkannya ke Franz Hofmeister.[23]

Pada awalnya, orang-orang secara umum memercayai bahwa kehidupan dan materialnya memiliki beberapa sifat atau substansi esensial (yang sering disebut sebagai "prinsip vital") yang berbeda dari materi yang ditemukan pada benda tak hidup, dan menganggap bahwa hanya makhluk hidup yang dapat menghasilkan molekul kehidupan (senyawa organik).[25] Pada tahun 1828, Friedrich Wöhler menerbitkan tulisan tentang sintesis urea, yang membuktikan bahwa senyawa organik dapat dibuat secara artifisial.[26] Sejak itu, biokimia mulai maju, terutama sejak pertengahan abad ke-20 dengan perkembangan teknik baru seperti kromatografi, difraksi sinar-X, interferometri polarisasi ganda, spektroskopi NMR, pelabelan radioisotop, mikroskop elektron, dan simulasi dinamika molekuler. Teknik-teknik ini memungkinkan penemuan dan analisis yang lebih mendalam dari berbagai molekul dan jalur metabolisme sel, seperti glikolisis dan siklus Krebs (siklus asam sitrat), serta mengarah pada pemahaman tentang biokimia pada tingkat molekuler. Perkembangan ilmu baru seperti bioinformatika juga banyak membantu dalam peramalan dan pemodelan struktur molekul raksasa.
Peristiwa bersejarah penting lainnya dalam biokimia adalah penemuan gen dan perannya dalam mentransfer informasi di dalam sel. Pada tahun 1950-an, James D. Watson, Francis Crick, Rosalind Franklin, dan Maurice Wilkins berperan penting dalam penemuan struktur DNA dan menunjukkan hubungannya dengan transfer informasi genetik.[27] Pada tahun 1958, George Beadle dan Edward Tatum menerima Hadiah Nobel atas penelitian mereka mengenai fungi yang menunjukkan bahwa satu gen menghasilkan satu enzim.[28] Pada tahun 1988, Colin Pitchfork adalah orang pertama yang terbukti melakukan pembunuhan dengan digunakannya DNA sebagai alat bukti, yang mendorong perkembangan ilmu forensik.[29] Belum lama ini, Andrew Z. Fire dan Craig C. Mello menerima Hadiah Nobel 2006 untuk menemukan peran interferensi RNA (RNAi) dalam membungkam ekspresi gen.[30]
Remove ads
Bahan awal: unsur kimia kehidupan
Ringkasan
Perspektif

Sekitar dua lusin unsur kimia bersifat esensial untuk berbagai jenis kehidupan biologis. Mayoritas unsur paling langka di Bumi tidak dibutuhkan oleh organisme (kecuali selenium dan yodium),[31] sementara beberapa unsur yang umum ditemukan (aluminium dan titanium) tidak digunakan. Sebagian besar organisme membutuhkan unsur-unsur yang sama, tetapi ada perbedaan kebutuhan antara tumbuhan dan hewan. Misalnya, alga laut menggunakan brom, tetapi tumbuhan dan hewan darat tampaknya tidak membutuhkannya. Semua hewan membutuhkan natrium, tetapi beberapa tumbuhan tidak. Tumbuhan membutuhkan boron dan silikon, tetapi hewan mungkin tidak (atau mungkin membutuhkannya dalam jumlah yang sangat kecil).
Hanya enam unsur—karbon, hidrogen, nitrogen, oksigen, kalsium, dan fosfor—yang menyusun hampir 99% massa sel hidup, termasuk yang ada di tubuh manusia (lihat komposisi tubuh manusia untuk daftar lengkapnya). Selain enam unsur utama tersebut, manusia membutuhkan sekitar 18 unsur-unsur lain dalam jumlah yang lebih kecil.[32]
Remove ads
Biomolekul
Ringkasan
Perspektif
Ada empat kelas molekul utama dalam biokimia (sering disebut biomolekul), yaitu karbohidrat, lipid, protein, dan asam nukleat.[33] Banyak molekul biologis merupakan "polimer"; dalam terminologi ini, monomer merupakan makromolekul yang relatif kecil yang bergabung menjadi satu untuk membentuk makromolekul berukuran lebih besar, yang kemudian disebut sebagai polimer. Ketika banyak monomer bergabung untuk menyintesis sebuah polimer biologis, mereka melalui proses yang disebut dengan sintesis dehidrasi.
Karbohidrat
Glukosa, sebuah monosakarida
Amilosa, sebuah polisakarida yang disusun oleh beberapa ribu unit glukosa
Dua fungsi utama karbohidrat adalah sebagai penyimpan energi dan penyedia struktur. Gula (contoh umumnya adalah glukosa) merupakan karbohidrat, tetapi tidak semua karbohidrat adalah gula. Jumlah karbohidrat di Bumi lebih banyak daripada jumlah biomolekul mana pun; mereka digunakan untuk menyimpan energi dan informasi genetik, serta berperan penting dalam interaksi dan komunikasi dari sel ke sel.
Monosakarida
Tipe karbohidrat yang paling sederhana—sekaligus sebagai monomer—adalah monosakarida, yang antara lain mengandung atom karbon, hidrogen, dan oksigen, kebanyakan dengan perbandingan 1:2:1 (rumus umumnya CnH2nOn, dengan n paling kecil adalah 3). Contoh monosakarida adalah glukosa (C6H12O6), salah satu karbohidrat terpenting; contoh lainnya yaitu fruktosa (C6H12O6), gula yang diasosiasikan dengan rasa manis buah-buahan,[34][a] serta deoksiribosa (C5H10O4), yang menjadi komponen DNA. Monosakarida dapat beralih antara bentuk asiklik (rantai terbuka) dan bentuk siklik. Bentuk rantai terbuka dapat diubah menjadi cincin atom karbon yang dijembatani oleh atom oksigen yang dibuat dari gugus karbonil di satu ujung dan gugus hidroksil di ujung lainnya. Molekul siklik memiliki gugus hemiasetal atau hemiketal, bergantung pada apakah bentuk liniernya adalah aldosa (mempunyai grup aldehida di akhir rantainya, contohnya glukosa) dan ketosa (mempunyai grup keton di rantainya, contohnya fruktosa).[35]
Beberapa karbohidrat (terutama setelah terkondensasi menjadi oligosakarida dan polisakarida) memiliki jumlah C yang relatif lebih rendah dibandingkan H dan O. Ketika dua monosakarida melalui proses sintesis dehidrasi, maka air akan terbentuk, karena dua atom hidrogen dan satu atom oksigen telepas dari dua gugus hidroksil monosakarida.
Disakarida
Dua monosakarida dapat digabungkan oleh ikatan glikosidik atau eter menjadi disakarida melalui sintesis dehidrasi. Dalam reaksi ini, satu atom hidrogen dan satu grup hidroksil (OH-) akan dilepaskan dan bergabung membentuk molekul air (H-OH atau H2O) sehingga proses ini disebut "reaksi dehidrasi". Reaksi kebalikannya (reaksi pemecahan), ketika satu molekul air digunakan dalam pemecahan ikatan glikosidik pada satu molekul disakarida menghasilkan dua molekul monosakarida, disebut dengan hidrolisis. Jenis disakarida yang terkenal adalah sukrosa, yang juga dikenal sebagai gula tebu. Satu molekul sukrosa terdiri dari satu molekul glukosa dan satu molekul fruktosa. Contoh disakarida yang lain adalah laktosa dalam susu, yang terdiri dari satu molekul glukosa dan satu molekul galaktosa. Laktosa dapat dihidrolisis oleh enzim laktase. Defisiensi enzim ini mengakibatkan gangguan pencernaan yang disebut intoleransi laktosa.
Oligosakarida dan polisakarida
Ketika beberapa (sekitar tiga sampai enam) monosakarida bergabung, molekul penggabungannya disebut sebagai oligosakarida (oligo- artinya "sedikit"). Molekul-molekul ini cenderung digunakan sebagai penanda dan sinyal, serta memiliki beberapa kegunaan lain.[36] Jika banyak monosakarida bergabung menjadi satu, molekulnya akan disebut sebagai polisakarida. Monosakarida dapat bergabung membentuk satu rantai panjang yang linier atau mungkin bercabang-cabang. Dua jenis polisakarida yang paling dikenal adalah selulosa dan glikogen, keduanya terdiri dari monomer glukosa yang berulang. Selulosa merupakan komponen struktural penting yang membentuk dinding sel pada tumbuhan. Manusia tidak bisa membuat ataupun mencerna selulosa. Sementara itu, glikogen (nama lainnya adalah gula otot) digunakan oleh manusia dan hewan sebagai penyimpan energi.
Lipid

Lipid terdiri dari beragam molekul dan sampai batas tertentu merupakan sebutan untuk semua senyawa yang relatif tidak larut dalam air atau nonpolar yang berasal dari materi biologis, termasuk lilin, asam lemak, fosfolipid, serta turunan asam lemak seperti sfingolipid, glikolipid, dan terpenoid (misalnya retinoid dan steroid). Beberapa lipid merupakan molekul alifatik rantai terbuka yang linier, sementara lipid yang lain memiliki struktur cincin. Beberapa lipid bersifat aromatik (dengan struktur siklik [cincin] dan planar [datar]) sementara yang lainnya tidak. Beberapa di antara mereka fleksibel, sementara yang lain kaku.
Lipid biasanya terbentuk dari satu molekul gliserol yang bergabung dengan molekul lain. Pada trigliserida, kelompok utama sebagian besar lipid, ada satu molekul gliserol dan tiga molekul asam lemak. Dalam hal ini, asam lemak merupakan monomer dan bisa saja bersifat jenuh (tidak memiliki ikatan rangkap dalam rantai karbonnya) atau tak jenuh (memiliki satu ikatan rangkap atau lebih dalam rantai karbonnya).
Meskipun secara umum bersifat nonpolar, mayoritas lipid juga memiliki beberapa sifat polar. Sebagian besar strukturnya bersifat nonpolar atau hidrofobik ("takut air"), sedangkan bagian lain dari strukturnya bersifat polar atau hidrofilik ("suka air"). Hal ini menjadikan lipid sebagai molekul amfifilik (memiliki bagian hidrofobik dan hidrofilik). Pada kolesterol, gugus polarnya hanyalah –OH (hidroksil atau alkohol). Pada fosfolipid, gugus polarnya jauh lebih besar dan lebih polar.
Lipid merupakan bagian integral dari makanan sehari-hari. Sebagian besar minyak dan produk susu yang digunakan untuk memasak dan makan seperti mentega, keju, minyak samin, dan semacamnya terdiri dari lemak. Minyak nabati kaya akan berbagai asam lemak tak jenuh ganda (PUFA). Makanan yang mengandung lipid menjalani pencernaan di dalam tubuh dan dipecah menjadi asam lemak dan gliserol, yang merupakan produk degradasi akhir dari lemak dan lipid. Lipid, terutama fosfolipid, juga digunakan dalam berbagai produk farmasi, baik sebagai pelarut bersama (misalnya dalam infus parenteral) atau sebagai komponen pembawa obat (misalnya, dalam liposom atau transfersom).
Protein

Protein merupakan molekul yang sangat besar (biopolimer makro) yang tersusun dari monomer yang disebut asam amino. Ada 20 asam amino standar, yang masing-masing terdiri dari atom karbon alfa yang berikatan dengan empat gugus, yaitu gugus amino (-NH2), gugus asam karboksilat (-COOH; meskipun gugus ini juga ada sebagai -NH3+ dan -COO - dalam kondisi fisiologis), atom hidrogen sederhana, dan rantai samping (biasanya dilambangkan sebagai "-R"). Gugus "R" inilah yang menjadikan setiap asam amino berbeda, dan sifat rantai samping akan sangat memengaruhi bentuk tiga dimensi suatu protein. Beberapa asam amino memiliki fungsi sendiri-sendiri, misalnya glutamat berfungsi sebagai neurotransmiter. Sejumlah asam amino dapat digabungkan oleh ikatan peptida melalui sintesis dehidrasi. Dalam proses ini, molekul air akan dilepaskan dan ikatan peptida menghubungkan nitrogen dari satu gugus amino pada suatu asam amino ke karbon dari gugus asam karboksilat pada asam amino lainnya. Molekul yang dihasilkan disebut dipeptida. Rangkaian pendek asam amino (biasanya kurang dari tiga puluh) disebut peptida atau polipeptida. Rangkaian yang lebih panjang disebut protein. Sebagai contoh, protein albumin pada plasma darah terdiri dari 585 residu asam amino.[39]


Protein memiliki peran struktural dan/atau fungsional. Contohnya, pergerakan dari protein aktin dan miosin sangat berperan dalam kontraksi otot rangka. Satu sifat yang dimiliki banyak protein adalah bahwa mereka mengikat molekul atau kelompok molekul tertentu secara khusus dan mungkin sangat selektif. Antibodi adalah contoh protein yang hanya dapat mengikat satu tipe molekul saja. Salah satu jenis protein yang paling penting adalah enzim. Molekul enzim hanya dapat mengenali satu jenis molekul reaktan saja, yang disebut sebagai substrat. Enzim akan mengkatalis reaksi sehingga energi aktivasi akan menurun dan kecepatan reaksi dapat berlangsung hingga 1011 kali lebih cepat atau lebih. Sebuah reaksi mungkin akan memakan waktu 3.000 tahun untuk betul-betul selesai, tetapi dengan enzim reaksinya mungkin menjadi kurang dari satu detik. Enzim sendiri tidak digunakan dalam proses reaksinya sehingga akan langsung mengkatalis substrat lainnya.
Struktur protein bisa dijelaskan melalui empat tingkatan. Struktur primer protein terdiri dari rangkaian linier asam amino, misalnya, "alanin-glisin-triptofan-serin-glutamat-asparagin-glisin-lisin-…". Struktur sekunder lebih berkaitan dengan morfologi lokal (morfologi adalah studi tentang struktur). Beberapa kombinasi asam amino akan cenderung membentuk gulungan yang disebut dengan uliran alfa (α-helix) atau menjadi lembaran yang disebut dengan lembaran beta (β-sheet). Struktur tersier merupakan bentuk tiga dimensi protein secara keseluruhan. Bentuk ini ditentukan oleh urutan asam amino. Jika ada satu perubahan saja, keseluruhan struktur dapat berubah. Sebagai contoh, rantai alfa pada hemoglobin terdiri dari 146 residu asam amino; jika residu glutamat di posisi ke-6 digantikan dengan valin, sifat hemoglobin akan berubah dan mengakibatkan penyakit anemia sel sabit. Terakhir, struktur kuartener berkaitan dengan struktur protein dengan beberapa subunit peptida, misalnya hemoglobin dengan keempat subunitnya. Tidak semua protein memiliki lebih dari satu subunit.[40]

Protein yang masuk ke dalam tubuh akan dipecah menjadi asam amino atau dipeptida di dalam usus halus, baru kemudian bisa diserap oleh tubuh. Nantinya, asam amino ini dapat bergabung kembali untuk membentuk protein yang baru. Produk antara dari glikolisis, siklus asam sitrat, dan jalur fosfat pentosa dapat digunakan untuk membentuk kedua puluh macam asam amino. Sebagian besar bakteri dan tumbuhan memiliki semua enzim yang diperlukan untuk menyintesisnya. Manusia dan mamalia lainnya hanya dapat menyintesis sebagian dari ke-20 macam amino tersebut. Tubuh mereka tidak dapat menyintesis isoleusin, leusin, lisin, metionin, fenilalanin, treonin, triptofan, dan valin. Karena harus didapatkan dari luar tubuh, asam amino jenis ini merupakan asam amino esensial. Mamalia memiliki enzim untuk menyintesis asam amino nonesensial, yaitu alanin, asparagin, aspartat, sistein, glutamat, glutamin, glisin, prolin, serin, dan tirosin. Arginin dan histidin juga dapat disintesis oleh mamalia, tetapi hanya dapat diproduksi dalam jumlah terbatas sehingga terkadang juga disebut sebagai asam amino esensial.
Jika gugus amino dilepaskan dari sebuah asam amino, maka akan menyisakan kerangka karbon yang disebut asam keto-α. Enzim transaminase dapat dengan mudah memindahkan gugus amino dari satu asam amino (menjadikannya sebuah asam keto-α) ke asam keto-α lainnya (menjadikannya sebuah asam amino). Hal ini penting dalam biosintesis asam amino, seperti dalam banyak jalur, zat antara dari lintasan biokimia lainnya akan diubah menjadi kerangka asam keto-α, lalu sebuah gugus amino ditambahkan lewat transaminasi. Maka, asam amino dapat digabung-gabungkan untuk membentuk protein.
Proses yang mirip digunakan untuk memecah protein. Pertama-tama, protein akan dihidrolisis menjadi komponen-komponennya, yaitu asam amino. Amonia bebas (NH3) yang ada dalam bentuk ion amonium (NH4+) di dalam darah, akan berbahaya bagi tubuh sehingga harus dikeluarkan. Organisme uniseluler hanya tinggal melepaskan amonia ini keluar tubuh. Demikian pula ikan bertulang sejati yang dapat melepaskan amonia ke dalam air yang diencerkan dengan cepat. Secara umum, mamalia mengubah amonia menjadi urea, lewat siklus urea.
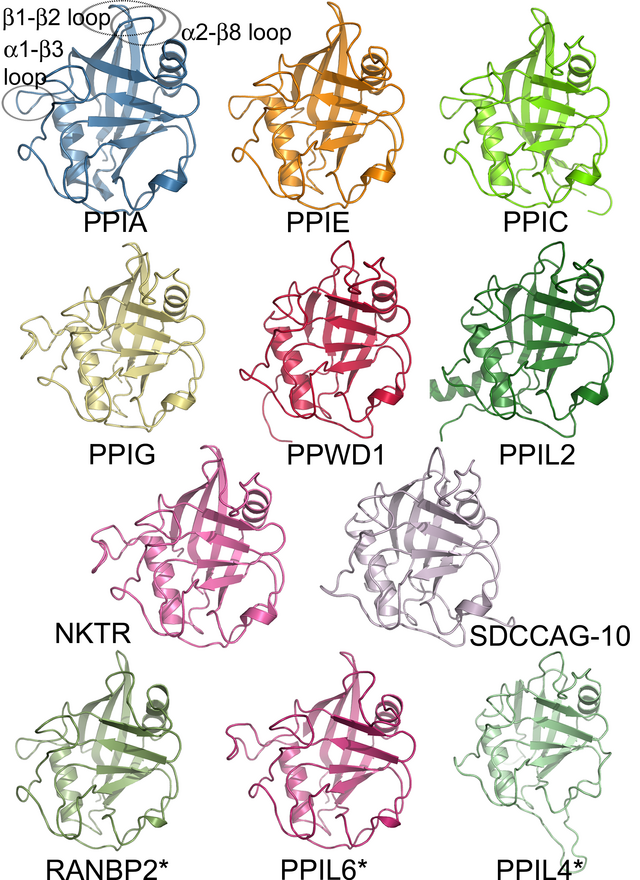
Untuk menentukan apakah dua protein saling terkait, atau dengan kata lain untuk memutuskan apakah mereka homolog atau tidak, para ilmuwan menggunakan metode perbandingan urutan. Metode seperti penjajaran urutan dan penjajaran struktural merupakan cara ampuh yang membantu ilmuwan mengidentifikasi homologi di antara molekul terkait. Selain untuk mengetahui pola evolusi keluarga protein, penemuan homologi protein juga untuk mengetahui kemiripan dua protein beserta struktur dan fungsinya.
Asam nukleat

Asam nukleat merupakan makromolekul biokimia yang kompleks dan memiliki berat molekul tinggi, yang dapat menyampaikan informasi genetik di semua sel hidup dan virus.[2] Penamaan asam nukleat diberikan karena awalnya ditemukan di nukleus (meskipun juga ditemukan di mitokondria dan kloroplas). Monomernya disebut nukleotida dan masing-masing terdiri dari tiga komponen: basa heterosiklik nitrogen (baik purin ataupun pirimidin), gula pentosa (gula dengan lima atom karbon), dan gugus fosfat.[41]

Asam nukleat yang paling umum adalah asam deoksiribonukleat (DNA) dan asam ribonukleat (RNA). Gugus fosfat dan gula dari masing-masing nukleotida saling terikat dan terhubung untuk membentuk "tulang punggung" asam nukleat yang sering disebut dengan "unting", sedangkan urutan basa nitrogen menentukan informasi genetik yang disimpannya. Basa nitrogen yang paling umum adalah adenin, sitosin, guanin, timin, dan urasil. Basa nitrogen dari setiap unting asam nukleat akan membentuk ikatan hidrogen dengan basa nitrogen pada unting lainnya secara berpasangan (mirip dengan ritsleting). Adenin berpasangan dengan timin dan urasil, timin hanya berpasangan dengan adenin, sementara sitosin dan guanin hanya dapat berpasangan satu sama lain.
Selain materi genetik sel, asam nukleat juga sering berperan sebagai pembawa pesan kedua, serta menjadi penyusun dasar adenosin trifosfat (ATP), sebuah molekul pembawa energi primer yang ditemukan di semua organisme hidup. Jenis basa nitrogen yang ada dalam DNA dan RNA berbeda: adenin, sitosin, dan guanin terdapat baik pada DNA maupun RNA, timin hanya ada pada DNA, dan urasil hanya ada pada RNA.
Remove ads
Metabolisme
Ringkasan
Perspektif
Karbohidat sebagai sumber energi
Glukosa merupakan sumber energi utama bagi sebagian besar makhluk hidup. Contohnya, polisakarida akan dipecah menjadi monomer-monomernya (fosforilase glikogen akan membuang residu glukosa dari glikogen). Disakarida seperti laktosa atau sukrosa akan dipecah menjadi dua komponen monosakaridanya.
Glikolisis (anaerob)
Glukosa terutama dimetabolisme oleh jalur metabolisme yang disebut glikolisis. Proses ini terdiri atas 10 langkah yang jika disederhanakan bertujuan memecah satu molekul glukosa menjadi dua molekul asam piruvat. Pada akhir glikolisis dihasilkan dua molekul ATP serta perubahan NAD+ (nikotinamida adenina dinukleotida: bentuk teroksidasi) menjadi NADH (nikotinamida adenina dinukleotida: bentuk tereduksi). Glikolisis tidak membutuhkan oksigen. Jika tidak ada suplai oksigen (atau sel tidak dapat menggunakan oksigen), NAD dipulihkan dengan mengubah piruvat menjadi asam laktat (misalnya pada manusia) atau menjadi etanol dan karbon dioksida (misalnya pada ragi). Monosakarida lain seperti galaktosa dan fruktosa dapat diubah menjadi zat antara dalam jalur glikolisis.[42]
Aerob
Dalam respirasi aerob ketika sel mendapat cukup oksigen, asam piruvat yang dihasilkan dari glikolisis akan dicerna kembali dan diubah menjadi Asetil Ko-A. Piruvat akan membuang satu atom karbonnya (menjadi karbon dioksida) dan akan memberikan elektronnya lagi pada NAD+ sehingga menjadi NADH. 2 molekul Asetil Ko-A akan memasuki tahap siklus Krebs, dan akan menghasilkan lagi 2 ATP, 6 molekul NADH, dan 2 ubiquinon (FADH2), serta karbon dioksida. Energi di NADH dan FADH2 nantinya akan digunakan di transpor elektron. Energi ini dipakai dengan cara dilepaskannya elektron dan H+ dari NADH dan FADH2 secara bertahap di sistem transpor elektron. Sistem transpor elektron akan memompa H+ keluar dari membran dalam mitokondria. Konsentrasi H+ di luar membran dalam mitokondria akan menyebabkan gradien proton, sehingga H+ akan masuk kembali ke membran dalam mitokondria melalui ATP sintase. Oksigen bertugas sebagai penerima elektron akhir, sehingga proses pembentukan ATP terus berlanjut. Oksigen yang bergabung dengan H+ akan membentuk air. NAD+ dan FAD akan digunakan kembali dalam sistem respirasi, seperti yang telah dijelaskan sebelumnya. Hal ini yang menyebabkan mengapa kita menghirup oksigen dan melepaskan karbon dioksida. Dalam 1 molekul glukosa akan dihasilkan total 36 ATP, dan satu ATP dapat melepaskan 7,3 kilokalori.
Glukoneogenesis
Dalam tubuh vertebrata, otot lurik yang dipaksa bekerja keras (misalnya saat mengangkat beban atau berlari) tidak akan mendapatkan oksigen yang cukup sehingga akan melakukan metabolisme anaerob, yang akan mengubah glukosa menjadi asam laktat. Organ hati akan menghasilkan kembali glukosa tersebut, melalui proses yang dinamakan glukoneogenesis. Proses glukoneogenesis sebenarnya membutuhkan energi tiga kali lebih banyak dibandingkan dengan yang dihasilkan dalam proses glikolisis (ada 6 ATP yang dibuat, sedangkan glikolisis hanya menghasilkan 2 ATP).
Remove ads
Hubungan dengan ilmu biologi "skala molekuler" lainnya
Ringkasan
Perspektif
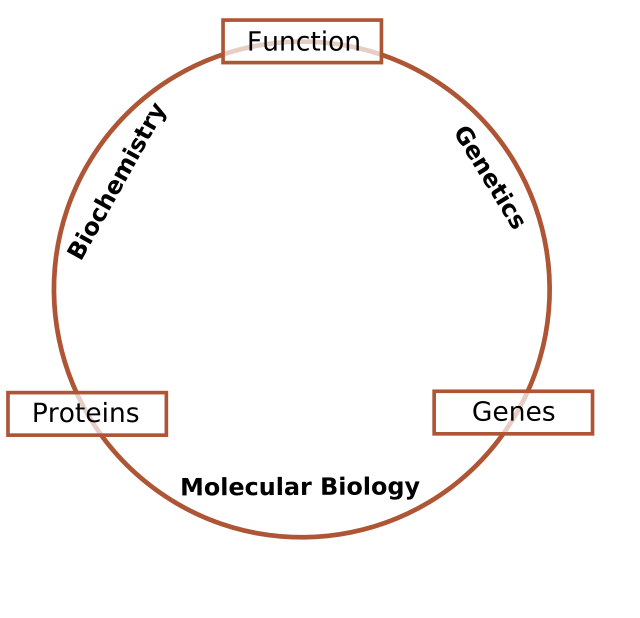
Para peneliti dalam biokimia menggunakan teknik-teknik khusus yang berasal dari biokimia, tetapi mereka semakin banyak menggabungkannya dengan teknik dan gagasan yang dikembangkan di bidang genetika, biologi molekuler, dan biofisika. Tidak ada garis jelas yang memisahkan antara berbagai disiplin ilmu ini. Biokimia mempelajari kimia yang diperlukan untuk aktivitas biologis molekul, biologi molekuler mempelajari aktivitas biologisnya, genetika mempelajari hereditasnya (pewarisan sifat), yang kebetulan dibawa oleh genomnya. Hal ini diperlihatkan dalam skema yang menggambarkan satu kemungkinan tampilan hubungan di antara ketiga bidang tersebut:
- Biokimia adalah studi tentang zat kimia dan proses penting yang terjadi pada organisme hidup. Ahli biokimia berfokus pada peran, fungsi, dan struktur biomolekul. Biokimia mempelajari kehidupan di tingkat atom dan molekul.
- Genetika adalah studi tentang perbedaan genetik pada organisme, serta pewarisannya. Genetika juga mempelajari tentang tentang mutasi genetik serta upaya manusia untuk mencegah, atau bahkan mendorongnya.
- Biologi molekuler adalah studi tentang dasar-dasar molekuler pada proses replikasi, transkripsi, translasi, dan fungsi sel. Dogma sentral biologi molekuler menguraikan proses ini. Biologi molekuler mempelajari kehidupan di tingkat molekul dan sel.
- ' Biologi kimiawi ' mengembangkan penerapan teknik-teknik kimia berbasis molekul kecil, melalui sintesis kimia, untuk mempelajari dan merekayasa sistem biologis.
Remove ads
Ekstremofil
Ekstremofil adalah mikroorganisme yang hidup dalam kondisi ekstrem. Misalnya, pada Juli 2019, sebuah studi ilmiah di tambang Kidd di Kanada menemukan organisme yang bernapas dengan belerang yang hidup 7.900 kaki di bawah permukaan dan menyerap belerang alih-alih oksigen untuk respirasi selnya. Organisme ini juga luar biasa karena memakan batuan seperti pirit sebagai sumber makanan reguler mereka.[43][44][45]
Enzim DNA polimerase dari bakteri termofil Thermus aquaticus, diekstraksi pada tahun 1968 dan dinamai Taq polimerase. Enzim ini adalah replikator DNA biokimia yang tahan terhadap suhu yang relatif tinggi (50–80 °C), yang memungkinkan ahli biologi molekuler menyederhanakan kerumitan dalam metode reaksi berantai polimerase (PCR).
Remove ads
Catatan
a. ^ Fruktosa bukan satu-satunya gula yang ditemukan dalam buah-buahan. Glukosa dan sukrosa juga ditemukan dalam jumlah yang bervariasi pada berbagai buah-buahan, dan terkadang melebihi fruktosa yang ada. Misalnya, 32% bagian kurma yang dapat dimakan adalah glukosa, dibandingkan dengan 24% fruktosa dan 8% sukrosa. Namun, persik mengandung lebih banyak sukrosa (6,66%) daripada fruktosa (0,93%) atau glukosa (1,47%).[46]
Remove ads
Lihat pula
- Daftar topik biokimia
- Biologi molekular
- Daftar biomolekul
- Ekologi kimia
- Biofisika
- Metabolom
- Metabolomika
- Obat-obatan molekular
- Biokimia tanaman
- Biologi struktural
- Stoikiometri
- Molekul kecil
Pranala luar
Wikimedia Commons memiliki media mengenai Biochemistry.
- The Virtual Library of Biochemistry and Cell Biology
- Biochemistry, 5th ed. Full text of Berg, Tymoczko, and Stryer, courtesy of NCBI.
- Biochemistry, 2nd ed. Diarsipkan 2008-07-05 di Wayback Machine. Full text of Garrett and Grisham.
- Biochemistry Animation Diarsipkan 2012-06-24 di Wayback Machine. (Narrated Flash animations.)
- SystemsX.ch - The Swiss Initiative in Systems Biology
- Biochemistry Online Resources – Lists of Biochemistry departments, websites, journals, books and reviews, employment opportunities and events.
- Perpustakaan Maya Biokimia dan Biologi Sel
Referensi
Wikiwand - on
Seamless Wikipedia browsing. On steroids.
Remove ads



