Loading AI tools
organische Verbindungen ohne Aromatenringe Aus Wikipedia, der freien Enzyklopädie
Aliphatische Kohlenwasserstoffe (altgriechisch ἄλειφαρ aleiphar ‚fettig‘) sind organische chemische Verbindungen, die aus Kohlenstoff und Wasserstoff zusammengesetzt und nicht aromatisch sind. Damit sind sie eine Untergruppe der Kohlenwasserstoffe. Nach der IUPAC-Nomenklatur sind aliphatische Verbindungen „acyclische oder cyclische, gesättigte oder ungesättigte Kohlenstoffverbindungen, außer aromatischen Verbindungen.“[1] Die einfachste Gruppe aliphatischer Kohlenwasserstoffe sind die gesättigten Alkane; weiterhin zählen die ebenfalls gesättigten Cycloalkane sowie die ungesättigten Kohlenwasserstoffe der Alkene und Alkine zur Gruppe der Aliphaten.

Wie alle reinen Kohlenwasserstoffe sind aliphatische Kohlenwasserstoffe unpolare, lipophile Verbindungen (also nicht wasserlöslich). Da laut IUPAC-Definition aliphatische Verbindungen den aromatischen Kohlenstoffverbindungen gegenübergestellt und damit durch eine Negation definiert werden, bedeutet dies im Umkehrschluss, dass alle nicht aromatischen organischen Verbindungen aliphatisch sind. Die Klassifizierung organischer Verbindungen in Aliphaten und Aromaten erfolgt durch die Aromatizitätskriterien. Die sogenannten alicyclischen Verbindungen bilden eine Untergruppe der Aliphaten und zeichnen sich – ähnlich den Aromaten – durch ringförmige Ketten aus, werden aber durch die Aromatizitätskriterien von den Aromaten unterschieden.
Die wichtigsten Stoffgruppen aliphatischer Verbindungen gemäß oben genannter Definition sind also:
Wichtige Beispiele aliphatischer Verbindungen finden sich in folgender Tabelle (angeordnet nach steigender Zahl der Kohlenstoff- bzw. der Wasserstoffatome):
| Formel | Name | CAS-Nummer | Strukturformel | Stoffgruppe | Synonyme |
|---|---|---|---|---|---|
| CH4 | Methan | 74-82-8 | 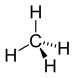 | Alkan | – |
| C2H2 | Ethin | 74-86-2 | Alkin | Äthin, Acetylen, Azetylen | |
| C2H4 | Ethen | 74-85-1 | 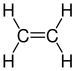 | Alken | Ethylen, Äthen, Äthylen, Elaylgas, Vinylwasserstoff, Etherin, Acetan, R-1150 |
| C2H6 | Ethan | 74-84-0 | 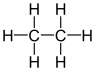 | Alkan | Äthan |
| C3H4 | Propin | 74-99-7 | 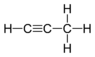 | Alkin | Methylacetylen, Allylen |
| C3H6 | Propen | 115-07-1 | 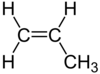 | Alken | Propylen |
| C3H8 | Propan | 74-98-6 |  | Alkan | |
| C4H6 | 1,2-Butadien | 590-19-2 |  | Dien | Buta-1,2-dien, Methylallen |
| C4H6 | 1-Butin | 107-00-6 |  | Alkin | Ethylacetylen |
| C4H8 | Buten | — | z. B. 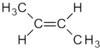 | Alken | Butylen |
| C4H10 | n-Butan | 106-97-8 | 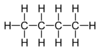 | Alkan | |
| C5H12 | n-Pentan | 109-66-0 | Alkan | Amylhydrid | |
| C6H10 | Cyclohexen | 110-83-8 | Cycloalken | 1,2,3,4-Tetrahydrobenzol | |
| C7H14 | Cycloheptan | 291-64-5 | Cycloalkan | Heptamethylen | |
| C7H14 | Methylcyclohexan | 108-87-2 | 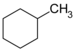 | Cycloalkan | Hexahydrotoluol, Cyclohexylmethan |
| C8H8 | Cuban | 277-10-1 |  | Pentacyclo[4.2.0.02,5.03,8.04,7]octan | |
| C9H20 | Nonan | 111-84-2 | Alkan | n-Nonan | |
| C10H12 | Dicyclopentadien | 77-73-6 |  | Dien, Cycloalken | 3a,4,7,7a-Tetrahydro-4,7-methanoinden, Tricyclo[5.2.1.02,6]deca-3,8-dien, TCD, DCPD, dimeres Cyclopentadien |
| C10H16 | Phellandren | 99-83-2 | 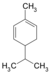  | Terpen, Dien, Cycloalken | α-Phellandren: 2-Methyl-5-(1-methylethyl)-1,3-cyclohexadien, β-Phellandren: 3-Methylen-6-(1-methylethyl)cyclohexen |
| C10H16 | α-Terpinen | 99-86-5 | 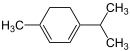 | Terpen, Cycloalken, Dien | Mentha-1,3-dien, 1-Isopropyl-4-methyl- 1,3-cyclohexadien |
| C10H16 | Limonen | 5989-27-5 |  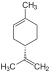 | Terpen, Dien, Cycloalken | 1-Methyl-4-prop-1-en-2-ylcyclohexen, Carven, p-Mentha-1,8-dien, 1-Methyl-4-isopropenyl-1-cyclohexen, 1-Methyl-4-(1-methylethenyl)cyclohexen, 4-Isopropenyl-1-methylcylohexen, Dipenten, Kautschin, Cinen, Cajeputen |
| C11H24 | Undecan | 1120-21-4 | Alkan | Undekan, n-Undecan, n-Undekan, Hendekan | |
| C30H50 | Squalen | 111-02-4 | Terpen, Polyen | 2,6,10,15,19,23-Hexamethyl- 2,6,10,14,18,22-tetracosahexaen, Spinacen, Supraen | |
| C2nH4n | Polyethylen | 9002-88-4 | Alkan | Polyethen, PE |
Aliphatische C-H-Valenzschwingungen von nicht konjugierten C-H-Bausteinen in einem Molekül haben im IR-Spektrum im Bereich von 3000 bis 2750 cm−1 charakteristische Peaks. Im Gegensatz dazu befinden sich die Peaks bei konjugierten C-H-Bausteinen jenseits der 3000 cm−1-Grenze.
Im 1H-NMR Spektrum befinden sich die meisten aliphatischen Peaks im Bereich von 1–2 ppm. Höhere Werte bis etwa 5 ppm werden bei benachbarten elektronenziehenden Gruppen erhalten.
Hauptquelle der Gewinnung von aliphatischen Verbindungen ist das Erdöl. Das wichtigste Verfahren der Erdölaufbereitung ist das Steamcracken, bei dem u. a. Ethan, LPG, Naphtha und Gasöl oder andere geeignete Kohlenwasserstoffe gecrackt werden.[2] Die Gasphase der Steamcrackerprodukte enthält die aliphatischen Grundchemikalien Ethylen, Propylen, den C4-Schnitt (hauptsächlich Buten, Isobuten und 1,3-Butadien) sowie Isopren.
Die bedeutendsten aliphatischen Folgeprodukte hieraus werden aus den Stoffen Eth(yl)en, Prop(yl)en und But(yl)en hergestellt. Es sind:
Seamless Wikipedia browsing. On steroids.
Every time you click a link to Wikipedia, Wiktionary or Wikiquote in your browser's search results, it will show the modern Wikiwand interface.
Wikiwand extension is a five stars, simple, with minimum permission required to keep your browsing private, safe and transparent.