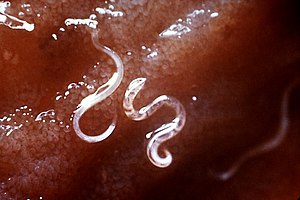
鉤蟲感染
来自维基百科,自由的百科全书
鉤蟲感染(英語:Hookworm infection)是由一種被稱為鉤蟲的腸道寄生蟲引起的感染。[1][5]最初,感染部位可能會出現瘙癢和皮疹。那些僅受少量鉤蟲感染的人可能不會表現出任何症狀;而那些被大量鉤蟲感染的人可能會出現腹痛、腹瀉、體重減輕、疲倦和貧血。兒童的心理和身體發育也可能會受到影響。[1]
人類中常見的兩種鉤蟲感染是鉤蟲病和板口線蟲病,分別由十二指腸鉤口線蟲和美洲板口線蟲引起。鉤蟲的卵沉積在感染者的糞便中。如果這些卵進入環境中,它們便可孵化成幼蟲,然後穿透人類的皮膚以實現感染。其中一種類型還可以通過受污染的食物進行傳播。風險因素包括在氣候溫暖、衛生條件較差的地方赤腳行走。診斷是通過用顯微鏡檢查糞便樣本來進行的。[1]
通過不在該疾病常見的地區赤腳行走,可以在個人層面上預防該疾病。從人群層面來看,減少戶外排便、不使用未經處理的糞便作為肥料以及進行大規模驅蟲是有效的。[1]根治鉤蟲感染通常須使用阿苯達唑或甲苯咪唑等藥物進行一至三天的治療。貧血患者可能還需要補充鐵劑。[3]
截至2015年,鉤蟲感染了約4.28億人。[4]兒童和成人均可能發生嚴重感染,但成人感染者較少。[2]鉤蟲感染很少致命。[6]鉤蟲感染是一種土源性蠕蟲病,被歸類為一種被忽視的熱帶疾病。[7]
症狀和體徵
鉤蟲感染沒有特定的症狀或體徵,但會引起腸道炎症、進行性缺鐵性貧血和蛋白質缺乏。嚴重感染有時會導致咳嗽、胸痛、喘息和發燒。早期或晚期感染可能出現上腹痛、消化不良、噁心、嘔吐、便秘和腹瀉等症狀,但胃腸道症狀通常會隨著時間的推移而減輕。晚期嚴重感染的症狀包括貧血、蛋白質缺乏症、消瘦、心力衰竭、全身性水腫和腹脹伴腹水。[來源請求]
鉤蟲幼蟲侵入皮膚(主要在美洲地區)會引發一種稱為皮膚幼蟲移行症(Cutaneous larva migrans,CLM,也稱為移動性幼蟲疹)的皮膚病。這些幼蟲的宿主不是人類,它們只能穿透皮膚的上五層,並引起強烈的局部瘙癢,通常發生在腳部或小腿上,因此被稱為地痒疹(Ground itch)。這種感染是由巴西鉤口線蟲(Ancylostoma braziliense)的幼蟲引起的。幼蟲在皮膚基底細胞層和角質層之間的曲折通道中遷移,引起匍行性水泡病變。隨著幼蟲的進一步移動,病變的後部逐漸變得乾燥並結痂。這些病變部位通常會劇烈瘙癢。[8]
成因

常見的人類鉤蟲感染包括鉤蟲病(Ancylostomiasis)和板口線蟲病(Necatoriasis)。鉤蟲病是由十二指腸鉤口線蟲(Ancylostoma duodenale)引起的,這種鉤蟲在中東、北非、印度和(以前)南歐地區較為常見。板口線蟲病是由美洲板口線蟲(Necator americanus)引起的,這種鉤蟲在美洲、撒哈拉以南非洲、東南亞、中國和印度尼西亞地區較為常見。[10]
其他動物如鳥類、狗和貓也可能受到感染。例如,管形鉤口線蟲(Ancylostoma tubaeforme)感染貓,犬鉤口線蟲(Ancylostoma caninum)感染狗,而巴西鉤口線蟲(Ancylostoma braziliense)和狹頭彎口線蟲(Uncinaria stenocephala)可以感染貓和狗。其中一些感染也可能傳染給人類。[11]
十二指腸鉤口線蟲呈灰白色或粉紅色,頭部相對於身體其他部分略微彎曲。這種彎曲在前端形成了明顯的鉤形,鉤蟲因此而得名。它們口器非常發達,並具有兩對牙齒。雄蟲長約1厘米,寬約0.5毫米;而雌蟲通常更長且更粗。此外,可以根據突出的後交配囊的存在來區分雄性和雌性。[12]
美洲板口線蟲在形態上與十二指腸鉤口線蟲非常相似。美洲板口線蟲通常比十二指腸鉤口線蟲小,雄蟲長約5至9毫米,而雌蟲長約1厘米。美洲板口線蟲在頰囊中擁有一對切割板。此外,板口線蟲的鉤形比鉤口線蟲的更加明顯。[12]


鉤蟲在溫度超過18°C的溫暖土壤中繁衍生息。鉤蟲主要存在於沙土或壤土中,而無法在黏土或淤泥中生存。鉤蟲只能生存在年均降雨量超過1000毫米的地區。[13]只有具備這些條件,鉤蟲的卵才能孵化。美洲板口線蟲的感染性幼蟲可以在較高的溫度下生存,而十二指腸鉤口線蟲的感染性幼蟲更能適應較冷的氣候。一般來說,鉤蟲在自然條件下最多只能存活幾周,在陽光直射或乾燥的條件下幾乎會立即死亡。[14]
感染宿主的是幼蟲而不是卵。雖然十二指腸鉤口線蟲可以通過口腔攝入,但較常見的感染方式是通過皮膚,這通常是由於赤腳在被糞便污染的地區行走引起的。幼蟲能夠穿透足部的皮膚,一旦進入體內,幼蟲就會通過血管系統遷移到肺部,並從那裡進入氣管,然後被吞咽。接著,幼蟲會沿著食道進入消化系統,最終幼蟲將逗留在腸道,並在腸道中成長為成蟲。[15][16]
一旦進入宿主的腸道,板口線蟲往往會引發長期感染,通常將持續1至5年(許多成蟲在感染後一兩年內就會死亡),但據記錄,一些成蟲最多可以存活18年。[10][17]鉤口線蟲成蟲的壽命很短,平均只能存活約6個月左右。[18]然而,感染可能會延長,因為幼蟲可以進入休眠狀態,在宿主的組織中存活數年。當成蟲死亡後,休眠的幼蟲可以被激活,發育成新的成蟲,繼續感染。這可能會導致感染患病率和強度的季節性波動(除了正常的傳播季節性變化)。
它們在宿主體內交配,雌蟲每天產下多達3萬個卵,一生中大約產下1800至5400萬個卵,這些卵會隨糞便排出體外。[19]由於成蟲需要5至7周的時間才能成熟、交配和產卵,因此在感染非常嚴重的早期階段,可能會出現急性症狀,但在患者的糞便中不會檢測到任何蟲卵。這會導致診斷變得非常困難。[來源請求]
美洲板口線蟲和十二指腸鉤口線蟲的卵可以在溫暖、潮濕的土壤中找到,最終孵化成第一階段幼蟲,即L1。L1是非感染性橫杆狀階段,以土壤微生物為食,最終蛻變成第二階段幼蟲,即L2,同樣也處於橫杆狀階段。它會攝食約7天,然後蛻變成第三階段幼蟲,即L3。這是寄生蟲的絲狀階段,即幼蟲的非攝食感染性形式。L3幼蟲活動能力極強,會尋找地勢較高的地方以增加穿透人類宿主皮膚的機會。L3幼蟲在沒有宿主的情況下可以存活長達2周。美洲美洲板口線蟲幼蟲僅通過皮膚穿透進行感染,而十二指腸鉤口線蟲幼蟲可以通過穿透和口腔感染。L3幼蟲成功進入宿主後,它們會穿過人類宿主的皮下微靜脈和淋巴管。最終,L3幼蟲通過肺毛細血管進入肺部,然後鑽出到肺泡中。接著它們沿著氣管向上移動,被宿主咳出併吞咽。被吞咽後,L3幼蟲會進入小腸,並在那裡蛻皮進入成蟲階段,即L4。從皮膚穿透到成蟲發育的整個過程大約需要5至9周。雌成蟲會釋放卵(美洲板口線蟲大約每天9千至1萬個卵,十二指腸鉤口線蟲大約每天2.5萬至3萬個卵),並通過宿主的糞便排出體外。這些卵在幾天內就會在環境中孵化,然後開始新一輪的循環。[15][20][21]
病理生理學
鉤蟲感染通常被認為是無症狀的,但正如諾曼·斯托爾(Norman Stoll)在1962年所述,鉤蟲感染是一種極其危險的感染,因為其損害是「無聲且陰險的」。[22]個體在感染後不久可能會出現一般症狀。地痒疹,在感染美洲板口線蟲的患者中很常見,是寄生蟲穿透和進入身體部位時引起的過敏反應。[12]此外,當幼蟲開始侵入肺泡並沿氣管向上移動時,可能會導致咳嗽和肺炎。而一旦幼蟲到達宿主的小腸並開始成熟,感染者就會出現腹瀉和其他胃腸不適症狀。[12]然而,斯托爾所指的「無聲且陰險的」症狀與慢性、高強度的鉤蟲感染有關。鉤蟲感染最嚴重的併發症是由腸道出血、缺鐵性貧血和蛋白質營養不良引起的。[20]這主要是由寄生在小腸中的成蟲攝食血液、破懷紅血球並降解宿主的血紅蛋白引起的。[15]這種長期失血可以通過面部和周圍水腫在身體上表現出來。一些鉤蟲感染患者也會出現由缺鐵性貧血引起的嗜酸性粒細胞增多和異食癖(通常為食土癖)。[12]近年來,人們對鉤蟲感染的其他重要後果也越來越重視,這些後果在公共衛生中起著重要作用。現在人們普遍認為,患有慢性鉤蟲感染的兒童會出現生長遲緩,以及智力和認知障礙。[15][23]此外,也有研究重點關注孕婦在懷孕期間感染鉤蟲可能對母嬰產生不良後果。[來源請求]
鉤蟲感染是通過腸道內長度為0.85至1.27厘米的鉤蟲(十二指腸鉤口線蟲)引起的,這一發現主要歸功於西奧多·比爾哈茨(Theodor Bilharz)和威廉·葛利辛格(Wilhelm Griesinger)於1854年在埃及的研究工作。[24]
鉤蟲感染的症狀可能與腸道炎症有關,這種炎症是由鉤蟲在腸道中吸血引起的。感染症狀包括噁心、腹痛和間歇性腹瀉;在長期感染的情況下,鉤蟲會導致進行性貧血,其症狀如食慾無常、異食癖(通常為食土癖)、頑固性便秘伴隨腹瀉、心悸、絲脈、皮膚冰涼、黏膜蒼白、疲勞虛弱、氣短;在嚴重的病例中,還可能出現痢疾、出血和水腫。[24]這些鉤蟲吸血並損傷黏膜。然而,糞便中的失血並不明顯。[來源請求]
在早期感染中,血液檢查通常會顯示嗜酸性粒細胞的數量增加。嗜酸性粒細胞是一種白血球,最先受到組織中鉤蟲感染的刺激(局部炎症反應中也存在大量嗜酸性粒細胞)。在長期感染引發貧血的情況下,血液中的血紅蛋白水平會下降。[來源請求]
與大多數腸道蠕蟲病相比,鉤蟲的患病率和強度在成年男性中可能更高(蠕蟲病感染最嚴重主要發生在兒童中)。對此的解釋是,鉤蟲感染往往是職業性的,由同事和其他親密群體通過污染他們的工作環境來維持高感染率。然而,在大多數流行地區,成年女性受貧血影響最嚴重,主要是因為她們對鐵的生理需求更高(月經、重複懷孕等)。值得注意的是,在十二指腸鉤口線蟲感染的情況下,幼蟲會通過母乳傳播傳染給嬰兒。該物種的幼蟲穿透皮膚後並不會全部立即通過肺部進入腸道,而是通過循環系統傳播到全身,並在肌肉纖維中休眠。在孕婦分娩後,部分或全部幼蟲會受到刺激並重新進入循環系統(可能是由於荷爾蒙突然變化所致),然後進入乳腺,使嬰兒通過母乳攝入大量的感染性幼蟲。這解釋了在中國、印度和澳大利亞北部等地區出現的一些難以解釋的嬰兒感染情況,即出生約一個月左右的嬰兒出現了非常嚴重甚至致命的鉤蟲感染。同樣的現象在犬類的犬鉤口線蟲感染中更為常見,新生的幼崽甚至可能因大量攝入鉤蟲引發的腸道出血而死亡。這也反映了人類和犬類寄生蟲之間密切的進化聯繫,它們可能有一個共同的祖先,可以追溯到人類和狗最初開始緊密生活在一起的時期。絲狀幼蟲是寄生蟲的感染階段,當土壤中的幼蟲穿透皮膚,或者在穿透皮膚後通過受污染的食物和水攝入時,就會發生感染。[來源請求]
診斷

診斷依賴於在糞便顯微鏡檢查中發現特徵性的蟲卵,雖然這在早期感染中是不可能的。大多數狗的早期感染症狀包括跛行和肛門瘙癢。鉤蟲的卵呈卵形或橢圓形,長約60微米,寬約40微米,無色,不被膽汁染色,並具有薄而透明的殼膜。當鉤蟲將卵釋放到腸道中時,卵中的卵子還未分節。在沿著腸道向下移動的過程中,卵子發育,因此通過糞便排出的卵是具有分段的卵子,通常有4至8個卵裂球。由於鉤口線蟲和板口線蟲(以及大多數其他鉤蟲物種)的卵難以區分,為了鑑別它們的屬,必須在實驗室中培養它們。如果糞便樣本在熱帶條件下放置一天或更長時間,幼蟲就會孵化出來,因此卵可能不再明顯。在這種情況下,有必要區分鉤蟲和類圓蟲幼蟲,因為後者的感染具有更嚴重的影響並且需要不同的處理方法。兩種鉤蟲的幼蟲也可以通過顯微鏡來區分,雖然通常不會常規進行,而是為了研究目的。成蟲很少見(除非通過內窺鏡檢查、手術或屍檢),但如果發現,將可以明確識別該物種。可根據頰腔的度(即口腔開口與食道之間的空間)進行分類,鉤蟲橫杆狀幼蟲具有長頰腔;而類圓蟲橫杆狀幼蟲具有短頰腔。[12]
最近的研究側重於開發基於DNA的工具,以用於診斷感染、鉤蟲的特異性鑑定以及分析鉤蟲種群內的遺傳變異。[25]由於鉤蟲卵往往難以與其他寄生蟲卵進行區分,因此PCR檢測可以作為準確診斷糞便中鉤蟲的分子方法。[25][26]
預防
感染性幼蟲在潮濕的土壤環境中發育和生存,尤其是沙土和壤土。它們無法在黏土或泥漿中存活。主要的預防措施是遵循良好的衛生行為:
- 不要露天排便,而應在廁所內排便。
- 不得使用未經處理的人類排泄物或未經處理的污水作為農業肥料。
- 不要在已知的感染地區赤腳行走。
- 對寵物狗和貓進行驅蟲。犬類和貓類的鉤蟲很少會在人體中發育成為成蟲。但有些常見的犬鉤蟲如犬鉤口線蟲偶爾會在人體中發育成為成蟲,引起嗜酸性粒細胞性胃腸炎,其侵入性幼蟲會引起瘙癢性皮疹,稱為皮膚幼蟲移行症。
在美國,莫西菌素以(吡蟲啉+莫西菌素)的局部溶液形式供狗和貓使用。它利用莫西菌素來控制和預防蛔蟲、鉤蟲、心絲蟲和鞭蟲感染。

大部分公共衛生問題的焦點都集中在感染鉤蟲的兒童身上。這種對兒童的關注很大程度上是因為大量證據表明鉤蟲感染與學習障礙、缺勤增加和未來經濟生產力下降之間存在密切聯繫。[15]2001年,第54屆世界衛生大會通過了一項決議,要求成員國在2010年前實現至少75%的有風險學齡兒童定期驅蟲的最低目標。[27]2008年,世界衛生組織發表了一篇關於治療有風險學齡兒童的努力的報告。其中一些統計數據如下:[28]
- 130個流行國家中只有9個能夠達到75%的目標
- 在總共8.78億有風險兒童中,只有不到7700萬人受到治療,這意味著只有8.78%的有風險兒童接受了鉤蟲感染的治療。
校本大規模驅蟲計劃一直以來都是解決兒童鉤蟲感染問題最流行的策略。校本計劃極具成本效益,因為學校已經擁有可用、廣泛且可持續的基礎設施,而且學校還配備了與社區關係密切的熟練勞動力。[27]接受當地衛生系統的少量培訓,教師就可以輕鬆地管理藥物,而這些藥物的費用通常每個兒童每年不到0.50美元。[29]
然而,許多人開始質疑校本計劃是否一定是最有效的方法。校本計劃的一個重要問題是,該計劃往往無法惠及未上學的兒童,從而忽視了大量有潛在風險的兒童。2008年,Massa等人的一項研究進一步深化了關於校本計劃的爭論。他們在坦尚尼亞的坦噶地區研究比較了社區導向治療與校本治療的效果。一個重要的結論是,採用社區導向治療方法的村莊中,鉤蟲平均感染強度明顯低於採用校本治療方法的村莊。在該特定研究中採用的社區導向治療模式允許村民通過自行選擇社區藥物分發員來管理抗蠕蟲藥物,以控制兒童的治療。此外,村民還組織並實施了自己的方法,將藥物分發給所有兒童。[30]這種新模式所取得的積極成果凸顯了在驅蟲活動中大規模社區參與的必要性。[來源請求]
許多大規模驅蟲計劃還會將自身的努力與公共衛生教育相結合。這些衛生教育計劃通常強會調重要的預防技巧,例如:飯前洗手,遠離被人類糞便污染的水源或區域。這些計劃可能還會強調必須穿鞋,但這些計劃本身也有健康風險,而且可能效果不佳。[31]全球各地城鎮和村莊的鞋子穿著習慣是由文化信仰和社會教育水平決定的。穿鞋可以防止周圍土壤中的鉤蟲穿透皮膚(如腳趾之間的區域)而引起鉤蟲感染。[32]
1943年至1947年在密西西比州和佛羅里達州進行的鉤蟲防治運動表明,鉤蟲感染的主要原因是衛生條件差,這可以通過興建和維護廁所來解決。儘管這些任務看似簡單,它們卻帶來了重要的公共衛生挑戰。大多數感染者來自衛生條件惡劣的貧困地區。因此,有潛在風險的兒童很可能無法獲得乾淨的水來洗手,並且生活在沒有適當衛生基礎設施的環境中。因此,衛生教育必須在資源有限的情況下提出可行且可持續的預防措施。[來源請求]
對許多公共衛生干預措施的評估普遍表明,通常歸因於貧困的各個方面的改善(例如衛生設施、健康教育和基本營養狀況)往往對傳播的影響有限。例如,一項研究發現,在資源有限的社區引入廁所僅將鉤蟲感染的患病率降低了4%。[33]然而,巴西薩爾瓦多的另一項研究發現,改善排水和污水處理(下水道)對鉤蟲感染的患病率有顯著影響,但對鉤蟲感染的強度沒有任何影響。[34]這似乎表明,僅通過環境控制對鉤蟲傳播的影響非常有限。因此,有必要進行更多的研究,以了解整合多種預防方法(包括教育、衛生設施和治療)的綜合計劃的有效性和可持續性。
治療
鉤蟲最常見的治療藥物是苯並咪唑,特別是阿苯達唑和甲苯咪唑。苯並咪唑通過與線蟲的β-微管蛋白結合,抑制寄生蟲內的微管的聚合作用,從而殺死成蟲。[20]在某些情況下,也可以使用左旋咪唑和噻嘧啶。[15]2008年的一項研究發現,用於治療鉤蟲感染的單劑量治療的療效如下:阿苯達唑為72%,甲苯咪唑為15%,噻嘧啶為31%。[35]這證實了此前的觀點,即阿苯達唑對於鉤蟲感染比甲苯達唑更有效。另外值得注意的是,世界衛生組織確實建議孕婦在妊娠三個月後進行驅蟲治療。[20]同時,如果患者還患有貧血,應在驅蟲治療的同時每天服用硫酸亞鐵(200毫克)3次,直至血紅蛋白值恢復正常,這可能需要長達3個月的時間。[12]
當鉤蟲仍在皮膚中時,可以通過局部冷凍療法治療鉤蟲感染。[36]
阿苯達唑對於在腸道中的成蟲,或是在皮膚下遷移的幼蟲均有效。[36]
如果出現缺鐵性貧血,補充鐵劑可以緩解的症狀。然而,隨著紅血球水平的恢復,可能會出現葉酸或維生素B12等其他必需物質的不足,因此這些物質也可能需要進行補充。
1910年代,治療鉤蟲感染的常見藥物包括百里酚、2-萘酚、氯仿、汽油和桉樹油。[37]到了1940年代,治療方法選擇使用四氯乙烯[38],在空腹狀態下給予3至4cc,然後再服用30至45克硫酸鈉。據統計,四氯乙烯對板口線蟲感染的治癒率為80%,但對鉤口線蟲感染的治癒率僅為25%,並且常常使患者產生輕度中毒。
與鉤蟲感染治療相關的其他重要問題是再感染和耐藥性。研究表明,治療後的再感染率極高。一些研究甚至表明,在接受治療的社區,30至36個月內鉤蟲感染率可達到治療前的80%。[20]雖然可能會發生再感染,但仍然建議進行定期治療,因為這將最大限度地減少慢性後果的發生。此外,鉤蟲耐藥性問題也越發受關注。家畜線蟲已對一線驅蟲藥表現出了耐藥性。一般來說,人類線蟲由於繁殖時間較長、治療頻率較低且治療更具針對性,因此不太可能產生耐藥性。儘管如此,國際社會必須小心維持現有驅蟲藥的有效性,因為沒有新的驅蟲藥處於後期開發階段。[20]
流行病學

沒有數據
少於10
10–15
15–20
20–25
25–30
30–35
35–40
40–45
45–50
50–55
55–60
多於60
據估計,有5.76至7.4億人感染了鉤蟲。[39][20]在這些感染者中,約有8000萬人受到嚴重影響。[25]鉤蟲感染的主要原因是美洲板口線蟲,它分布於美洲、撒哈拉以南非洲和亞洲。[15]十二指腸鉤口線蟲分布於更分散的焦點環境中,即歐洲和地中海。大多數感染者集中在撒哈拉以南非洲和東亞/太平洋島嶼,分別估計有1.98億和1.49億感染者。其他受影響地區包括:南亞(5000萬)、拉丁美洲和加勒比地區(5000萬)以及中東/北非(1000萬)。[20]這些感染者大多數生活在衛生條件差的貧困地區。鉤蟲感染最為集中的地區是世界上最貧困的人群,他們每天的生活費不足2美元。[15]
雖然鉤蟲感染可能不會直接導致死亡,但其對發病率的影響需要得到立即關注。在考慮失能調整生命年(DALY)時,包括鉤蟲感染在內的被忽視的熱帶疾病,與腹瀉病、缺血性心臟病、瘧疾和結核病一起成為開發中國家最重要的健康問題之一。
據估計,鉤蟲感染導致損失了多達2210萬個失能調整生命年。近年來,人們越來越關註解決與鉤蟲感染相關的公共衛生問題。例如,比爾及梅琳達·蓋茨基金會捐贈了3400萬美元,用於對抗包括鉤蟲感染在內的被忽視的熱帶疾病。[40]美國前總統柯林頓還在2008年柯林頓全球倡議(CGI)年會上宣布了一項為1000萬兒童驅蟲的重大承諾。[41]
有關鉤蟲感染患病率的許多數字都是估計值,因為目前沒有國際監測機制來確定其患病率和全球分布情況。[15]一些患病率是通過世界各地流行地區的調查數據來衡量的。以下是關於鉤蟲流行地區患病率的一些發現。
印度西孟加拉邦胡格利縣大吉嶺(Pal等人,2007)[42]
- 43%的感染率主要為美洲板口線蟲,但也有一些十二指腸鉤口線蟲感染
- 鉤蟲感染量和貧血程度均在輕度範圍內
中國海南省秀龍坎村(音譯)(Gandhi等人,2001)[43]
- 60%的感染率主要為美洲板口線蟲
- 值得注意的趨勢是,患病率隨著年齡的增長而增加(約41歲的平台期),並且女性的患病率高於男性
- 總共526個測試家庭中有52%被感染
- 無法識別物種,但之前在北越的研究報告稱,超過95%的鉤蟲幼蟲中有美洲板口線蟲
- 63%的感染率主要為美洲板口線蟲
- 內陸地區美洲板口線蟲患病率為9%
- 沿海平原地區美洲板口線蟲患病率為63%
- 35%的感染率主要為美洲板口線蟲
技術的發展也可能有助於更準確地繪製鉤蟲患病率圖表。一些研究人員已經開始使用地理信息系統(GIS)和遙感(RS)來研究蠕蟲的生態學和流行病學。Brooker等人 利用這項技術創建了撒哈拉以南非洲的蠕蟲分布圖。通過將衛星獲取的環境數據與學校調查的患病率數據聯繫起來,他們能夠創建詳細的患病率圖表。該研究重點關注多種蠕蟲,但特別是鉤蟲方面有一些有趣的結論。與其他蠕蟲相比,鉤蟲能夠在更熱的條件下生存,並且在溫度範圍的上限中廣泛分布。[49]
改進的分子診斷工具是另一項技術進步,可以幫助改善現有的患病率統計數據。近年來的研究重點是開發一種基於DNA的工具,該工具可用於感染診斷、鉤蟲特異性鑑定以及分析鉤蟲種群的遺傳變異。這也可以作為針對鉤蟲感染的各種公共衛生措施的重要工具。目前,大多數有關診斷工具的研究都集中在創建一種快速且具有成本效益的檢測方法,用於鉤蟲感染的特異性診斷。許多人希望它的開發可以在未來五年內實現。[何時?][25]
歷史
現在被歸因於鉤蟲感染的症狀在古埃及的莎草紙獻中出現(約公元前1500年),被描述為一種以貧血為特徵的精神錯亂。伊本·西那(Ibn Sina,也稱Avicenna)是十一世紀的波斯醫生,他在他的幾位患者身上發現了鉤蟲,並將其與他們的疾病聯繫起來。後來,這種情況在英國、法國、德國、比利時、北昆士蘭和其他地方的採礦業中明顯普遍。[24]
1838年,義大利醫生[[安吉洛·杜比尼|安吉洛·杜比尼]](Angelo Dubini)在對一名農婦進行屍檢後發現了鉤蟲。杜比尼於1843年發表了詳細信息,並將該物種鑑定為十二指腸鉤口線蟲。1852年,在埃及醫療系統工作的德國醫生西奧多·比爾哈茨在借鑑同事威廉·葛利辛格的研究成果的基礎上,在屍檢過程中發現了鉤蟲,並進一步將它們與當地流行的低色素性貧血(今天可能被稱為缺鐵性貧血)聯繫起來。
25年後,義大利聖哥達鐵路隧道工地爆發了一次腹瀉和貧血流行病。[24]在1880年的一篇論文中,醫生卡米洛·博佐洛(Camillo Bozzolo)、愛德華多·佩龍西托(Edoardo Perroncito)和路易吉·帕利亞尼(Luigi Pagliani)正確地假設鉤蟲與工人必須在15公里長的隧道內排便以及許多人穿著破舊的鞋子有關。[50]工作環境經常積水,有時深及膝蓋,幼蟲能夠在水中存活數周,使它們能夠感染許多工人。1897年,確定了皮膚是感染的主要途徑,並闡明了鉤蟲的生物生命周期。
1899年,美國寄生蟲學家查爾斯·沃德爾·斯泰爾斯(Charles Wardell Stiles)發現美國南部出現的進行性惡性貧血是由十二指腸鉤口線蟲引起的。1900年代的測試顯示,學齡兒童中感染情況非常嚴重。在波多黎各,美國陸軍醫生貝利·阿什福德(Bailey K. Ashford)在1903年至1904年期組織並開展了寄生蟲治療活動,治癒了約30萬人(占波多黎各人口的三分之一),並將貧血症死亡率降低了90%。

1909年10月26日,由於老約翰·洛克菲勒(John D. Rockefeller, Sr.)捐贈100萬美元,成立了洛克菲勒根除鉤蟲病衛生委員會。這個為期五年的計劃取得了巨大成功,為美國公共衛生做出了巨大貢獻,在美國南部十一個州進行了公共教育、藥物治療、實地工作和現代政府衛生部門建設。[51]鉤蟲展覽是1910年密西西比州博覽會的重要組成部分。
該委員會發現,平均40%的學齡兒童感染了鉤蟲。在根除計劃實施前,鉤蟲感染水平較高的地區在干預後入學率、出勤率和識字率都有較大提高。計量經濟學研究表明,這種影響無法用多種替代因素來解釋,包括各地區的差異趨勢、農產品價格的變動、某些教育和衛生政策的變化以及根除瘧疾的影響。[52]對於成年人來說,由於他們先前的感染率低得多,沒有發現顯著的同期結果,因此他們從干預中受益較少。該計劃幾乎消滅了鉤蟲,並在之後得到了新的資金支持,由洛克菲勒基金會國際衛生部門管理。[53]
洛克菲勒基金會在墨西哥開展的鉤蟲防治運動展示了科學和政治如何在制定衛生政策中發揮作用。該運動匯集了政府官員、衛生官員、公共衛生工作者、洛克菲勒官員和社區人員。這項運動的發起目的是為了根除墨西哥的鉤蟲。儘管該運動沒有著重長期治療,但它確實確定了墨西哥與洛克菲勒基金會之間的關係條款。該運動背後的科學知識有助於制定公共衛生政策,改善公共衛生並在美國和墨西哥之間建立牢固的關係。[54]
1920年代,根除鉤蟲運動擴展到了加勒比海和拉丁美洲。18世紀末,西印度群島報導了大量的鉤蟲感染死亡病例,巴西和其他熱帶及亞熱帶地區也有相關描述。[24]
20世紀初的治療方法是使用瀉利鹽來減少保護性黏液,然後使用百里酚來殺死鉤蟲。[55][37]到了1940年代,四氯乙烯成為主要方法。[38]直到20世紀中期,新的有機藥物化合物才被開發出來。[17]
研究
據估計,開發中國家有三分之一的孕婦感染鉤蟲,56%的孕婦患有貧血,所有孕產婦死亡中有20%與貧血直接或間接相關。這樣的數字引起了人們對懷孕期間鉤蟲相關貧血這一話題產生了更多的興趣。[56]由於慢性鉤蟲感染通常會導致貧血,許多人質疑鉤蟲治療是否會影響嚴重貧血率的變化,從而影響母嬰的健康。大多數證據表明,鉤蟲導致孕產婦貧血,因此生活在流行地區的所有育齡婦女都應定期接受驅蟲治療。世界衛生組織甚至建議受感染的孕婦在妊娠早期接受治療。[20]不管這些建議如何,只有馬達加斯加、尼泊爾和斯里蘭卡將驅蟲納入其產前護理計劃。[57]
沒有對孕婦進行驅蟲治療的原因在於大多數人仍然擔心驅蟲治療會導致不良的分娩結果。但是,2006年Gyorkos等人的一項研究發現,將一組接受甲苯咪唑治療的孕婦與一個接受安慰劑的對照組進行比較時,兩組的不良分娩結果率相當相似。治療組的不良分娩結果為5.6%,而對照組的不良分娩結果為6.25%。[56]此外,Larocque等人的研究表明,治療鉤蟲感染實際上給嬰兒帶來了積極的健康效果。這項研究的結論是,與安慰劑對照組相比,在產前護理期間使用甲苯咪唑加鐵劑治療可顯著降低極低出生體重嬰兒的比例。[58]迄今為止的研究已經驗證了在懷孕期間治療感染鉤蟲的孕婦這一建議。
一項研究發現,在第二個孕期服用單劑驅蟲藥可能在高寄生蟲患病率地區減少孕婦貧血和寄生蟲患病率。[59]
關於鉤蟲感染的嚴重程度以及鉤蟲的種類與孕期的鉤蟲相關性貧血之間的關係尚未進行研究。此外,還需要在世界不同地區進行更多研究,以查看已完成研究中發現的趨勢是否持續存在。[60]
鉤蟲和惡性瘧原蟲的共同感染在非洲很常見。[61]儘管確切數字尚不清楚,但初步分析估計,多達四分之一的非洲學齡兒童(1780至3210萬名5至14歲兒童)可能同時面臨感染惡性瘧原蟲和鉤蟲的風險。[62]雖然最初的假設認為多種寄生蟲的共同感染會損害宿主對單一寄生蟲的免疫反應,並增加患臨床疾病的易感性,但研究卻得出了相反的結果。例如,在塞內加爾的一項研究表明,與沒有寄生蟲感染的兒童相比,有寄生蟲感染的兒童患臨床瘧疾感染的風險增加,而其他研究未能重複這樣的結果,即使在實驗室的小鼠實驗中,寄生蟲對瘧原蟲的影響也是多變的。
在非洲,鉤蟲和瘧原蟲的共感染是常見的。雖然確切的數字尚不清楚,初步分析估計多達四分之一的非洲學齡兒童(5-14歲的1,780-3,210萬兒童)可能同時面臨感染瘧原蟲和鉤蟲的風險。雖然最初的假設認為與多種寄生蟲的共感染將削弱宿主對單一寄生蟲的免疫反應,並增加患臨床疾病的易感性,但研究結果卻產生了不同的結論。例如,塞內加爾的一項研究顯示,與沒有寄生蟲感染的兒童相比,有寄生蟲感染的兒童患臨床瘧疾感染的風險增加,而其他研究未能重複這樣的結果[63],即使在實驗室的小鼠實驗中,寄生蟲對瘧原蟲的影響也是多變的。[64]
一些假設和研究表明,由於可能調節促炎症和抗炎症細胞因子反應,蠕蟲感染可能可以保護我們免受腦瘧疾。[65]此外,這種假定的疾病易感性增加的機制尚不清楚。例如,蠕蟲感染會引起強烈且高度極化的免疫反應,表現為輔助性T細胞2型(Th2)細胞因子和免疫球蛋白E(IgE)的產生增加。[66]然而,這種反應對人體免疫反應的影響尚不清楚。此外,瘧疾和蠕蟲感染均可引起貧血,但人們對同時感染和可能加劇貧血的影響知之甚少。[17]
衛生假說指出,缺乏與傳染性病原體的接觸的嬰兒和兒童更容易通過免疫系統發育的調節而患過敏性疾病。該理論最初由大衛·斯特拉坎(David P. Strachan)提出,他指出花粉熱和濕疹在大家庭的兒童中不太常見。[67]從那時起,研究就注意到胃腸道蠕蟲對開發中國家兒童過敏的影響。例如,在甘比亞的一項研究發現,一些村莊消滅蠕蟲導致兒童皮膚過敏反應增加。[68]
雖然每年或每半年進行大規模驅蠕蟲藥物分發是公共衛生干預的一個關鍵方面,但許多人已經意識到,由於貧困、高再感染率以及隨著重複使用藥物效力降低等因素,這種方法是不可持續的。因此,當前的研究重點是開發一種可以整合到現有控制計劃中的疫苗。疫苗開發的目標不一定是創造一種具有消除性免疫或完全抵抗免疫的疫苗。一種能夠降低接種者發生嚴重感染的可能性,從而減少血液和營養水平下降的疫苗,仍然可能對全世界的高疾病負擔產生重大影響。
目前的研究側重於針對蠕蟲發育的兩個階段,即幼蟲階段和成蟲階段。有關幼蟲抗原的研究主要集中在屬於病程相關蛋白超家族的蛋白質,即鉤蟲分泌蛋白(Ancylostoma Secreted Proteins)。[69]儘管最初時是在鉤口線蟲中被描述,但這些蛋白質也已成功地從美洲板口線蟲的分泌產物中分離出來。美洲板口線蟲ASP-2(Na-ASP-2)是目前領先的幼蟲階段鉤蟲疫苗候選藥物。已經進行了一項隨機、雙盲、安慰劑對照的研究,36名無鉤蟲感染史的健康成年人接受3次肌內注射不同濃度的Na-ASP-2,並在最後一次接種後觀察6個月。[70]該疫苗誘導了顯著的抗Na-ASP-2 IgG和細胞免疫反應。此外,它是安全的,不會產生使人衰弱的副作用。該疫苗目前正處於第一階段試驗,在巴西,已有先前感染記錄的健康成年志願者正在按照最初研究中使用的相同時間和劑量濃度接受接種。[69]如果這項研究成功,下一步將進行第二階段試驗,以評估疫苗接種者中鉤蟲感染的比率和強度。由於Na-ASP-2疫苗僅針對幼蟲階段,因此參與研究的所有受試者在接種疫苗之前都必須接受抗蠕蟲藥物治療以消除成蟲,這一點至關重要。
成蟲鉤蟲抗原也被確定為有潛力的疫苗候選者。當成蟲附著在人類宿主的腸黏膜上時,紅血球在蠕蟲的消化道中破裂,導致游離血紅蛋白釋放,隨後通過蛋白水解級聯降解。負責這種蛋白水解級聯的幾種蛋白質對於蠕蟲的營養和生存也至關重要。因此,能夠誘導這些抗原的抗體的疫苗可能會干擾鉤蟲的消化途徑,危害蠕蟲的生存。[71]已經確定了三種蛋白質,即天冬氨酸蛋白酶-血紅蛋白酶APR-1(Aspartic protease-hemoglobinase APR-1)、半胱氨酸蛋白酶-血紅蛋白酶CP-2(Cysteine protease-hemoglobinase CP-2)和穀胱甘肽S-轉移酶。[72][73][74]接種APR-1和CP-2可以減少狗的失血量和糞便蟲卵計數。[72][73]對於APR-1,疫苗接種甚至可以減少蠕蟲負擔。[72]目前的研究在至少開發其中一個抗原作為重組蛋白用於臨床試驗中的測試階段受到了阻礙。
術語
參見
- 人類寄生蟲列表
- 蠕蟲病
參考文獻
外部連結
Wikiwand - on
Seamless Wikipedia browsing. On steroids.