嚴重急性呼吸道症候群冠狀病毒2型 [ 4] severe acute respiratory syndrome coronavirus 2,SARS-CoV-2 )[ 6] 包膜 的正鏈單股RNA病毒 ,屬於冠狀病毒科 乙型冠狀病毒屬 嚴重急性呼吸道症候群相關冠狀病毒 種[ 10] SARS病毒 及MERS病毒 屬於同一譜系但不同進化枝 ,是已知的第七種可感染人類的冠狀病毒。病毒的宿主包括哺乳動物和禽類動物,它造成了於2019年底爆發 的嚴重特殊傳染性肺炎 (COVID-19)[ 11] ACE2 為受體達到感染;主要感染器官包括肺部、心臟、腎臟等多個主要器官[ 12] [ 13]
本條目存在以下問題 ,請協助
改善本條目 或在
討論頁 針對議題發表看法。
此條目
過於依賴第一手來源 。
(2021年5月18日 )
此條目需要
精通或熟悉醫學 的編者 參與及協助編輯。
(2021年3月17日 )
維基百科 中的醫學內容
僅供參考 ,並
不能 視作專業意見。如需獲取醫療幫助或意見,請諮詢專業人士。詳見
醫學聲明 。
Quick Facts 嚴重急性呼吸道症候群冠狀病毒2型, 病毒分類 ...
Close
2019年12月,這一病毒所導致的嚴重特殊傳染性肺炎 在中華人民共和國 湖北省 武漢市 首次被報告,2020年1月中旬在疫情 爆發期間,從一位陽性患者樣本的核酸檢測 以及基因組定序 發現此病毒[ 14] [ 15] [ 16] [ 17] [ 18] [ 19]
截至2023年12月6日,全球已累計報告772,138,818 名確診病例,其中逾6,985,964人死亡 [ 20]
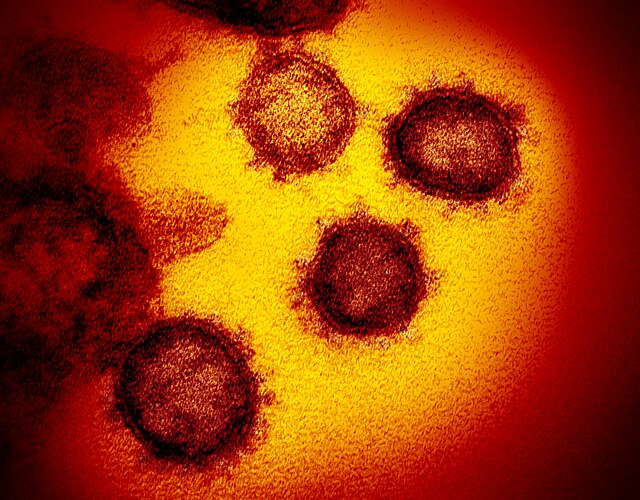
從細胞培養出來的SARS-CoV-2病毒電子顯微鏡 照片 在過往會將新發現的冠狀病毒暫時稱為新型冠狀病毒 ,包括在2012年發現引發中東呼吸症候群 (MERS )的冠狀病毒及其病症都曾被稱為「新型冠狀病毒」及「新型肺炎」[ 21] [ 22] [ 23] 世界衛生組織 暫時將其命名為Novel Coronavirus(即「新型冠狀病毒」),縮寫為2019-nCoV[ 24] [ 25] 國際病毒分類委員會 的冠狀病毒科研究小組確認該病毒與SARS-CoV 形成姊妹支 ,正式將該病毒依據分類學和已有慣例命名為「SARS-CoV-2」(全稱:Severe Acute Respiratory Syndrome Coronavirus 2)[ 6] [ 26] [ 5]
ICTV的CSG小組對命名進行了解釋,指出對病毒的命名是基於唯一可確定的特徵,即病毒的基因組序列。病毒保守蛋白的變異表明,它和SARS冠狀病毒種屬於同一簇,但與SARS和MERS具有顯著不同。由於遺傳學上有關聯,ICTV將病毒歸類於SARS相關冠狀病毒種,並產生出SARS-CoV-2這一名字。ICTV指出,儘管命名相似,對SARS-CoV和SARS-CoV-2病毒引發的疾病需要區別看待。[ 6] [ 27]
石正麗 等病毒學家於2020年2月19日對ICTV的命名提出異議,認為從生物學、流行病學及臨床資料上SARS-CoV和SARS-CoV-2有顯著區別,需要另行命名。[ 28]
國際病毒分類委員會 冠狀病毒科研究組(CSG)建議全球研究者對分離病毒株統一以「SARS-CoV-2/Host(宿主)/Location(分離地點)/Isolate/Date(日期)」之格式命名以便於交流[ 6]
另外,也有研究文獻使用「human coronavirus 2019」(人類冠狀病毒2019,HCoV-19 或hCoV-19 )[ 29] [ 30] [ 31] [ 32]
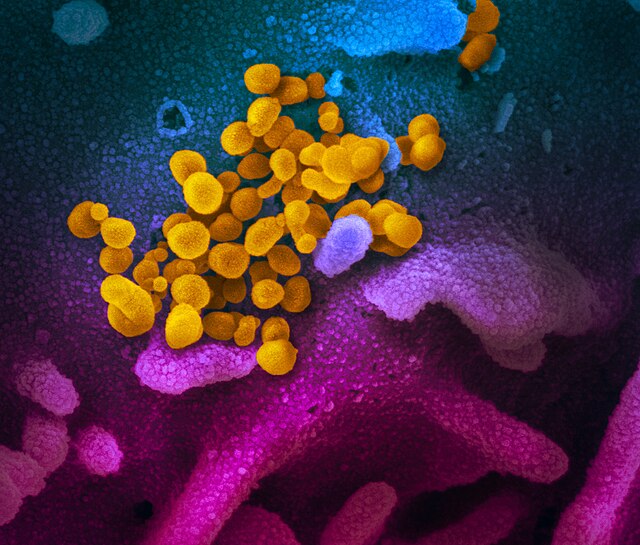
圖為SARS-CoV-2病毒(黃色)的常溫電鏡圖片 嚴重急性呼吸道症候群冠狀病毒2型是一種具有包膜的、不分節段的正鏈單股RNA病毒 ,顆粒呈圓形或橢圓形,直徑約80~120nm,屬於網巢病毒目 冠狀病毒科 乙型冠狀病毒屬 。[ 17] [ 33] [ 34] [ 35] [ 36] [ 33] 核苷酸 左右,[ 16] [ 37] [ 38] 基因 序列顯示嚴重急性呼吸道症候群冠狀病毒2型
屬於乙型冠狀病毒屬 譜系 β(Betacoronavirus Lineage β, Sarbecovirus )進化樹中分支較長的一種病毒,[ 39] 中華菊頭蝠 中發現的冠狀病毒相似,例如MERS-CoV 或SARS-CoV 。[ 16] [ 40] [ 41] [ 42] [ 43]
2020年1月27日,中國疾病預防控制中心 分離出第一株嚴重急性呼吸道症候群冠狀病毒2型
。[ 44] [ 註 1] [ 17] [ 註 2] [ 45] HKU9-1 。[ 46] [ 47] 中華菊頭蝠 。[ 48] 浙江 舟山 ,無除中華菊頭蝠外的來源。[ 49] [ 50] [ 48] [ 49]
有研究利用了SARS-CoV-2病毒WIV04 的基因 序列與另一類SARS 變種 蝙蝠冠狀病毒RaTG13 (Bat-CoV RaTG13)進行對比,發現兩者相似度有96%。作者利用Bat-CoV RaTG13和SL-CoV ZC45 為對照組,基本確認新型冠狀病毒同SARS一樣利用自己RBD(受體結合域:receptor binding domain)的S1蛋白與人體血管收縮素轉化酶2 (hACE2)進行結合。[ 12] HKU3-4 和自由結合能最強的rSHC014 之間,但弱於SARS-CoV。[ 50] ORF1a 、ORF1b 以及接近一半的RBD域有極高的同一性,NCoV和RaTG13在β屬CoV 中可以獨立再被分類為一譜系。另外的研究對2019年採集的來自中華人民共和國雲南 的蝙蝠冠狀病毒RmYN02 進行了對比,指出儘管基因組整體上與SARS-CoV-2的同一性不如RaTG13,但是在1ab基因的對比中同源性高達97%,推測了蝙蝠冠狀病毒轉化到人類冠狀病毒的過程中重組的可能性。[ 51]
SARS-CoV-2病毒的平面結構 圖為SARS-CoV-2的S蛋白建模。 多項研究指出,儘管RaTG13或RmYN02的變異難以造成2019年爆發的疫情,但支持新型冠狀病毒來源於蝙蝠的說法,且非嵌入產物。[ 52] [ 51] [ 53] [ 49] [ 51] [ 52]
SARS-CoV-2從蛋白組成上類似SARS-CoV和MERS-CoV,基因組都由結構蛋白、非結構蛋白和輔助蛋白編碼。[ 54] [ 55] pro )、木瓜蛋白酶樣蛋白酶(PLpro )、解旋酶(helicase)、和RNA依賴性RNA聚合酶(RdRp)。[ 54] [ 56] [ 57] pro 和PLpro 在病毒的1ab基因的多個位點上運轉,主要功能是幫助病毒RNA轉譯。[ 58] pro 晶體結構進行解析,指出這是可以抑制病毒複製的靶標之一。[ 54] [ 59] [ 59]
對乙型冠狀病毒屬譜系α中的OC43 和HKU1 的一項研究表明,儘管進化枝和其有限的宿主導性相符,在多重進化下,人類冠狀病毒的血球凝集素酯酶蛋白中的凝集素域幾乎全部被刪除,相反在動物冠狀病毒中這一蛋白域得到保留。[ 60] 血球凝集素 酯酶蛋白有受體結合的作用,但它在冠狀病毒中為受體破壞酶。[ 61] 呼吸道 唾液 醣蛋白 並成功在呼吸道上皮細胞 內進行複製的進化機制。[ 60] [ 62] [ 62] [ 63]
SARS-CoV-2病毒的棘蛋白(S蛋白)屬於三聚體I類融合蛋白,其中分S1和S2兩個亞基以及一個跨膜錨,表面刺突長度約23nm,寬7nm,S1解離時會造成S2的構象變化。[ 64] [ 33] [ 65] [ 65] [ 66] [ 67] [ 65]
圖為SARS-CoV-2的低溫電子斷層掃描電腦成像 對SARS-CoV-2的受體結合域(RBD)與ACE2 複合物的晶體結構進行測定後知,該晶體含C、N、O、S等元素,屬於四方P [ 68] 1 21 2空間群 。[ 33] [ 69] [ 70] 表面電漿共振 實驗中,hACE2對RBD的結合親和力為15.2nM;對S蛋白整體則為14.7nM。[ 70] [ 64] [ 71] [ 72] [ 71] [ 73]
圖為SARS-CoV-2的穿透式電子顯微鏡 影像,病毒表面的S蛋白結構清晰可見。 現有認知中,病毒的RBD突變是導致SARS-CoV-2與hACE2的親和力更高的原因。[ 52] [ 74] [ 75] [ 76] [ 77] [ 78] [ 79]
對相近的SARS病毒進行對比發現,SARS-CoV-2病毒在S蛋白內的23619-23632位點中有四個獨特的胺基酸插入:681-PRRA-684。[ 73] 弗林蛋白 )中創建了潛在裂解位點序列RXXR。[ 73] [ 73] [ 51] [ 80] [ 81] [ 79] [ 51] 齧齒類動物 、麝貓 等動物會具有更低的受體親和力。[ 74] [ 82] [ 83]
2020年4月,有實驗室成功合成SARS-CoV-2,這類病毒樣本可以被用於相關的動物模型、宿主分析、疫苗研發等多種研究。[ 84] [ 85]
SARS-CoV-2病毒現有的參考病毒基因為NC045512,[ 86] [ 87] [ 46] [ 88] [ 89]
圖為新型冠狀病毒分離株武漢—滬—1(Wuhan-Hu-1)的基因圖譜 在對SARS-CoV-2的進化分析中顯示,RmYN02和RaTG13 是在親緣關係上最相近的。對RBD單獨組建的進化樹則顯示,SARS-CoV-2在接觸人群前,經歷過多次S蛋白重組事件,MP789、RaTG13等穿山甲及蝙蝠病毒與SARS-CoV-2在這方面具有最密切的相關程度。[ 51] [ 90] [ 51]
在2020年的疫情中,對來自不同地區的SARS-CoV-2病毒毒株分析顯示出少量的同義及非同義突變。其中病毒的ORF8、ORF1a和ORF9的非同義突變率最高,包括S蛋白在內的其他基因則相對保守。[ 88] [ 88] [ 91] [ 92]
有研究針對病毒的部分位點突變,進行了分型,分為L型和S型[ 93] [ 94] [ 94] [ 95] [ 95] [ 95] [ 96] [ 95] [ 97]
在2020年初,一株致病性較弱的SARS-CoV-2曾流行於新加坡、澳洲、西班牙等地。這一分支的病毒的ORF8蛋白較標準樣本缺失382個核苷酸,影響了病毒的轉錄效率。這一特點造成患者在病毒載量 沒有顯著區別的情況下,呈現較輕的臨床體徵,相關的細胞因子水平也較低。[ 98] [ 63] [ 98] [ 99] [ 100]
2020年12月31日,世衛組織通報嚴重急性呼吸道症候群冠狀病毒2型自出現以來已出現四種變體,其中三種傳播力增強[ 101] 變異病毒 有Alpha 、Beta 、Gamma 、Delta 與Omicron 等。[ 102] [ 103]
上圖顯示了冠狀病毒的複製過程 根據現有認知,病毒具有熱敏感性,暴露在紫外線 下或處於56℃高溫環境下30分鐘可達到不活化效果。[ 19] [ 104] 乙醚 、75%乙醇 、含氯消毒劑、過氧乙酸 和氯仿 等脂溶劑均可有效不活化病毒,氯己定 不能有效不活化病毒。[ 17] [ 105] [ 106]
現在對SARS-CoV-2理化特性的認識多來自對SARS-CoV和MERS-CoV的研究。這一病毒能以動物為中介傳染給人類,且具有人傳人的能力。[ 107] [ 108] [ 109] [ 110] [ 111] [ 112] [ 113] [ 114] S蛋白 構象變化 ,使之RBD區域暴露後與hACE2相結合,接著透過促進S2蛋白介導與細胞的膜融合完成感染的全過程。[ 64] [ 115] [ 116] [ 51] [ 49] [ 73]
影片:病毒與標的細胞的結合過程 圖為病毒蛋白酶蛋白結構的三維表示 現已知SARS等冠狀病毒S蛋白進入標的細胞取決於與hACE2受體的結合作用以及細胞蛋白酶對S蛋白的啟動作用,SARS的S蛋白與其受體hACE2結合是靠細胞絲胺酸蛋白酶 TMPRSS2來引發的,與它有76%胺基酸同一性的新型冠狀病毒被發現有相似的機能。[ 82] [ 117] [ 118] [ 119] RBM ,懷疑其中負責和hACE2結合的序列與SARS相同,且在其餘無法透過hACE2結合的Bat-CoV中未發現同樣的序列。研究表示,在實驗新型冠狀病毒進入Caco-2細胞時,使用針對TMPRSS2的絲胺酸蛋白酶抑制因子卡莫司他 後,有效阻止了病毒的入侵;相反的,針對CatB/L的抑制因子E64d在293T細胞上無效果。這一實驗結果初步表明新型冠狀病毒的S蛋白也是由TMPRSS2引發的,並可在呼吸道上皮細胞上進行膜融合。[ 82] [ 120]
儘管SARS-CoV-2和hACE2的結合親和力相比較SARS-CoV高10-20倍,但還沒有研究確認SARS-CoV-2的膜融合能力。[ 121] [ 122] [ 123] [ 124] 弗林蛋白 介導,透過蛋白酶裂解來觸發膜融合。在SARS病毒中引入RXXR裂解位點後,會增加病毒的膜融合活性。[ 73]
在對冠狀病毒和hACE2受體進行結合的研究中,發現hACE2以二聚體形式存在,儘管同時有開放和關閉兩種構象,對與病毒的互相識別無影響。[ 125] [ 125] [ 126] [ 107] [ 110] 結腸 細胞 中的表現與人體免疫、調節病毒性感染正相關,會因被病毒下調表現而活化腎素-血管收縮素系統(RAS)。[ 126] [ 126] [ 113]
冠狀病毒普遍被認為在細胞質進行複製和轉錄,其中只有它的RdRp是完全保守的。[ 127] [ 128] [ 128] [ 129] [ 129] [ 128] [ 130] [ 130] [ 131] pro 。這類蛋白酶與RdRp同為藥物靶點之一。[ 132]
對SARS-CoV-2感染細胞的轉譯組和蛋白組分析顯示,人體內多條細胞通路的蛋白質水平都發生顯著變化。其中,與RNA修飾或碳代謝有關的蛋白水平顯著上升,而與膽固醇代謝相關的蛋白水平則顯著下降。[ 133] [ 134] + 巨噬細胞中發現,但無法在CD3+ T細胞或B220+ B細胞中發現。這一研究猜測病毒抗原誘導了Fas的加強,並因此介導了淋巴球減少症的產生。[ 134]
除人類外,貓和狗等寵物也會成為SARS-CoV-2的宿主,另外多種用於構造傳染模型的動物如老鼠、雪貂、倉鼠等都可以被感染。[ 135] [ 136] [ 137] [ 136] [ 135] [ 138] [ 135]
在包括狗、倉鼠等動物中所檢測到的SARS-CoV-2序列與在人群中傳播的病毒序列相比沒有差異。[ 137] [ 139] [ 140]
印度在六月發生首例亞洲獅感染後病死的事件。[ 141]
韓國疾控中心採集的SARS-CoV-2病毒樣本 SARS-CoV-2病毒進入人體後,會引起先天免疫系統 的免疫應答 。其中,免疫系統會在病毒複製過程中介入並抑制病毒的傳播,包括會產生特異性抗體等。[ 92] [ 151] [ 151]
SARS-CoV-2進入人體後,有研究者指出它會活化CD4+ T淋巴球,成為Th1輔助細胞。Th1分泌出顆粒球-巨噬細胞集落刺激因子(GM-CSF)導致IL6高表現的炎性因子CD14和CD16的出現,加速肺炎發展。對患有COVID-19的患者進行觀察發現,他們的肺部呈現出大量炎性細胞浸潤現象,研究猜測Th1在進入肺循環後會起到免疫破壞作用,導致肺功能障礙乃至臨床死亡。[ 152] + T細胞的比例。[ 153]
透過對免疫微環境的觀察可發現,具有不同程度臨床症狀的COVID-19患者的免疫學表現也極為不同。[ 153] [ 154] + 巨噬細胞逐漸增多並取代了原有的肺泡巨噬細胞,且其中mDCs和pDCs的相對比例較輕中症患者更低。單核球來源的巨噬細胞具有相對較高的發炎性,並產生出如IL-1β、6、8等炎性細胞因子。[ 154] + T細胞,從而產生更多的免疫效應分子:XCL1、ITGAE、CXCR6以及ZNF683。[ 153] + T細胞在輕症患者體內已知作用有細胞活化、遷移和上調細胞因子相關途徑的基因;在重症患者體內則具有轉譯啟動、細胞穩態以及核苷酸代謝等作用。[ 154] [ 13] [ 155] [ 156] [ 157] [ 157]
對病人的臨床分析顯示,血型對於病毒對人體的易感程度有影響。[ 158] [ 158] [ 159] FH 、CD4、8以及免疫球蛋白IgM、IgG,在臨床症狀消除一周後依舊有顯著的免疫反應。[ 160] [ 161] [ 162]
在Vero E6細胞中培養的SARS-CoV-2病毒(綠色)
人體對冠狀病毒的先天免疫訊息傳遞的機制是保守的,因此由於SARS-CoV-2與其他冠狀病毒的較高的同源性暗示它與宿主的互相作用類似於其他冠狀病毒。[ 163] [ 164] [ 165] [ 166] [ 167] [ 168] [ 168] [ 169]
針對免疫系統的IFN分泌,SARS-CoV-2有類似於SARS-CoV的免疫感應逃避機制。[ 163] [ 170] [ 171]
人體的免疫應答機制應對如SARS-CoV-2等RNA病毒有兩個途徑,分泌干擾素(IFN)以及趨化因子,分別用於抑制病毒增殖和召集白血球攻擊病毒。[ 172] [ 173] [ 174] [ 165] [ 165] [ 175]
有研究採用空間蛋白組學技術對SARS-CoV-2患者的樣本進行分析,繪製了多種免疫檢查蛋白受體的表現。這項研究發現,在具有高病毒載量 的區域,PD-L1、CTLA-4和IDO-1蛋白均較低載量區域有更多的表現。這些蛋白具有控制免疫反應,如阻止CD8+ T細胞增生等功能。[ 176]
有研究者發現,經過冷凍電鏡的觀察,SARS-CoV-2的S蛋白三聚體結構相對緊湊,透過多醣屏蔽表位,有助於病毒免疫逃避。[ 177] [ 178] [ 179] [ 66] [ 67]
人體免疫系統針對病毒轉錄的一種ISG為干擾素誘導蛋白(IFIT),IFIT可藉由與eIF3相結合來抑制病毒的轉錄。[ 180] [ 181] [ 181] [ 163]
在成功感染細胞後,被感染細胞會利用MHC-I分子傳遞資訊給CD8+ T細胞,以協助免疫系統清除受感染細胞。[ 182] [ 183] [ 182]
基於COVID-19的血清樣本橫斷面分析,感染SARS-CoV-2病毒的患者大約在20天後可完全檢測到IgG和IgM抗體。兩種血清的轉換時間大約在發病兩星期後出現,但與患者的臨床症狀輕重無顯著關聯。[ 184] [ 185] [ 186] [ 187] [ 186]
從患者體內提取的SARS-CoV-2病毒樣本,可見病毒顆粒(紫色)已經嚴重感染周邊細胞 對中和性抗體的初步研究顯示,患者體內產生的一種抗體可以結合在S蛋白與hACE2的交互面,其抗體表位經檢測為456-FRK-SN-460。[ 188] [ 189] [ 189] [ 190]
一項針對SARS-CoV的抗體研究顯示在SARS-CoV的S2亞基中,包含HR2但不包含HR1的免疫原性域在SARS-CoV-2樣本中高度保守。[ 191] [ 192] [ 193] [ 194] [ 195] [ 196] [ 192] [ 192] [ 197] [ 192]
現今,已經有多種針對病毒不同蛋白的高中和性的單株抗體被發現,並正在研發應用階段。[ 198] [ 199] [ 200] [ 201] [ 202]
人體經SARS-CoV-2感染後會在體內呈階段性發展,其中已康復患者的血漿因其免疫學特徵可有效治療其他患者。[ 203] + 單核球比例升高,並具有更高比重的CD14+ IL1β+ 單核球。相對於水平較低的CD4+ T細胞,NK細胞則顯著增加。[ 203] [ 203] [ 204] [ 203]
針對SARS-CoV的研究表明,動物模型和人體顯示短期內記憶B細胞和記憶T細胞都具有特異性免疫應答,但只有記憶T細胞的反應可延長至數年。[ 205] [ 206] [ 207] [ 208] [ 209] [ 186] [ 190] [ 210] [ 211] [ 212] [ 213] [ 110] [ 160] [ 213] [ 214] [ 215]
目前關於新型冠狀病毒的流行病學 認識受疫情變化影響,無完全確切的認知。新型冠狀病毒被認為對人群普遍易感。老年人及有基礎疾病者感染後病情較重,兒童及嬰幼兒等人群相對成年人有相似的被感染風險。[ 216] [ 217] [ 218] [ 17] [ 219] [ 112] [ 220] SARS病毒 所引發的臨床症狀一般更輕微但傳播性更強,且潛伏期可能極具有傳播力。[ 221] [ 222] [ 223] [ 50] [ 110]
圖為電鏡拍攝的SARS-CoV-2病毒(黃色) SARS-CoV-2在疫情爆發期間,會產生多種突變,在GISAID資料庫中被上傳的基因樣本已經超過一萬份。[ 224] [ 87] [ 225] [ 88] [ 226] [ 227] [ 88] [ 88] [ 226] [ 228] [ 226] 病毒載量 上具有顯著差異。[ 229]
最新的臨床結果顯示,對11名患者的病毒樣本分析中出現33個突變,其中超過一半是新出現的突變。研究認為,SARS-CoV-2的多樣性在之前被低估,且在複製能力上不同的毒株之間病毒載量的區別可以達到270倍。[ 229]
因在疫情期間,對基本傳染數 的估計無可統一說法,多方估測的R 0 指數從1.4-6.4不等,但都認為基本傳染數R 0 > 1。根據這一共識,在流行病學的定義下,新型冠狀病毒疫情初期會以指數增長 的趨勢形成常態分布,成為流行病 。[ 230] R 0 指數提出不同的傳播率看法,認為需要使用動態傳播的模型,而非傳統的以常數表現的傳染指數。[ 231]
在疫情爆發初期,基本傳染數 據先前預計為1.4到2.5之間[ 232] 香港中文大學 研究認為基本傳染數為3.30到5.47之間[ 233] 倫敦帝國理工學院 院根據截至2020年1月24日的資料,統計得出基本傳染數中位數 為2.6,95%置信區間 為2.1-3.5。[ 220] 蘭開斯特大學 研究人員Jonathan M Read所領導的研究小組於2020年1月28日發表的預印本認為,此病毒的R 0 係數為3.11(95%置信度區間(95%CI)為2.39-4.13),在武漢,此傳染係數確定為5.0。[ 234] 西安交通大學 Tang Biao領導的研究小組與2020年1月24日所發表的文章認為:R 0 係數可能高達6.47。[ 235] 哈佛大學 流行病學 專家 丁亮(Eric Ding)根據各方的公開資訊,估計傳染指數目前介於2.6與2.9之間[ 236]
基於至2020年1月22日的所有病例報告,中國疾病預防控制中心 的研究者認為R 0 係數應當為2.2,95%置信區間為1.4-3.9。[ 219] R 0 係數提升至2.68,95%置信區間則被縮小到2.47-2.86。[ 237] R 0 平均值為 3.28,中位數為2.79[ 238] [ 239]
新的研究提出,在疫情爆發過程中,封鎖城市、醫療水平的提高、預防方案的完善等各項要素對流行病動力學 模型 有很大的影響。[ 231] [ 240] [ 231] R 0 指數得出的幾種擴散數量統計,認為最終在感染人數於高峰期前緩慢增長,而非指數性增長。[ 231] 嚴重急性呼吸道症候群 )的R 0 係數在3左右。[ 241]
圖為從美國一名患者體內提取的SARS-CoV-2病毒(紅色)在實驗室培養皿中 目前一般認為新型冠狀病毒與蝙蝠冠狀病毒同源,在初步的基因對比中,有研究人員認為穿山甲 或為此次新型冠狀病毒潛在中間宿主,[ 242] [ 243] [ 244]
有實驗室對在疫情爆發前一年的中國大陸穿山甲和馬來西亞穿山甲的基因樣本進行了定序,顯示出其體內抗體可與新型冠狀病毒的S蛋白相結合。經對比發現,穿山甲體內存有的冠狀病毒的S蛋白、小包膜蛋白、基質蛋白 以及核衣殼蛋白與新型冠狀的蛋白擁有超過90%的同一性。對S蛋白RBD的對比指出,兩者RBD結構除一個胺基酸序列外完全一致。[ 245] [ 90] [ 246] [ 247]
在疫情初期,新型冠狀病毒接觸人群的傳播源被認定為是位於武漢的華南海鮮市場,但後續有研究根據疫情進展以及病毒基因溯源分析質疑了這一說法,認為武漢海鮮市場並非最初的暴露源。[ 248] [ 62] [ 87] [ 87] [ 249]
研究者透過流行病學模型分析認為,零號病人的出現,最早可以追溯到2019年10月初,也有其他研究傾向於11月下旬。[ 248] [ 249] [ 250] [ 251] [ 252] [ 253]
圖為已經被病毒(黃色)感染的凋亡細胞 。 有研究指出,病毒的主要感染途徑為侵入人體呼吸道 上皮 細胞。[ 46] [ 254] [ 255] [ 17] [ 256] [ 17] [ 34] [ 257] [ 258] [ 259]
溶於較大液滴中的SARS-CoV-2會透過人觸摸臉部的方式傳染,但多數會沉澱於上呼吸道或被鼻腔的分泌物清除。[ 258] [ 258] [ 218]
對確診攜帶病毒的患者分析指出,人體唾液、淚液、尿液、糞便等樣本中,均發現了有感染能力的病原體。[ 260] [ 261] [ 262] [ 263]
此前有一份研究構建了新型冠狀病毒的擴散模型,其中指出疫情爆發時值春節 時期,在預測受感染病患人數時需要納入因春運 而造成的出入境人流增多因素。[ 264] [ 265] [ 266] [ 267] [ 268] [ 268]
圖為正在進行增殖的SARS-CoV-2病毒 在更新的研究中發現,二代、三代病毒攜帶者的潛伏周期平均更長,且從出現症狀至入院的時間經觀察比早期的患者更長,研究者認為在患病早期確診病患並進行隔離治療會更加困難。研究指出,病毒潛伏期平均為5.2天,且每7.4天感染者就會翻倍。[ 219] [ 219] [ 237] 鍾南山 帶領的團隊發表了一項新的綜合性研究,將潛伏期的上限擴大至24天,並指出臨床資料支持受新型冠狀病毒的傳染後從放射學和裸眼觀察的角度上均相比SARS和MERS更難在感染初期發現病徵,這增加了病毒的擴散能力。[ 240] [ 269]
由於SARS-CoV-2病毒的爆發,促成多個疫情爆發地區施行社交隔離的方式來保障公共安全。[ 270] [ 270] [ 270] [ 271] 春運 期間)內的流動模型計算,與前述研究從流行病學角度分析成年人更容易受到感染的結果相符。[ 270] [ 271] [ 272] [ 272]
有研究指出,任何病毒在感染人類後,會選擇更高傳染力的方向進行突變,並在SARS疫情中得到了體現。[ 62] [ 273] [ 62] 病毒載量 進行了對比,發現新型冠狀病毒的核酸排出模式與感染流感病毒的患者類似。研究懷疑,無症狀以及輕症狀的新冠患者在傳播能力上不輸於有症狀患者。因此這一研究認為在構建傳播動力學模型時需要納入這一變量,並建議採取與控制SARS疫情不同的防疫策略。[ 274] [ 275] [ 276]
有研究利用已有的R0 係數對SARS-CoV-2的傳播鏈進行了分析。這一研究中採納的R0 為2.2-2.5,並得出病毒攜帶者感染他人的時間中位點為症狀出現前的2.3天左右。研究認為,主動採取包括抗病毒藥物等手段可以正面影響病例在治癒前的病毒排出動力學。[ 277] [ 278] [ 279]
而對病患體內病毒的一項分析指出,人體去胺酶參與了對SARS-CoV-2轉錄組的RNA編輯。研究指出,調節干擾素信號的ORF6基因的編輯率最高。[ 92] [ 280] [ 281]
新的研究將SARS-CoV-2與其他引發大規模流行病的病毒進行了對比。針對紐約市 分別在H1N1以及SARS-CoV-2流行期間的死亡率對比研究指出,儘管在COVID-19流行期間具有更完善的衛生措施,SARS-CoV-2對同期死亡率的影響尤甚於H1N1。[ 282]
圖為COVID-19的常見症狀 SARS-CoV-2病毒會造成一種感染性疾病COVID-19,由於SARS-CoV-2造成的疫情還在爆發中,現今的臨床多為初步性研究。[ 283] [ 19] [ 283] [ 109] [ 284] [ 285]
COVID-19的傳染依靠病毒為載體,一般會經由咳嗽或噴嚏產生。[ 286] 流行病學 調查,病毒潛伏期 為1-19天,多數患者居於為3-7天內,中位值為5天;少數患者潛伏期則長達19天至24天[ 240] [ 287] [ 288] [ 289] [ 290] CT )檢查。[ 291]
同時,SARS-CoV-2病毒被發現與兒童多系統發炎症候群(MIS-C)相關聯。這一病症特點為全身性發炎反應,更嚴重會患有多器官功能衰竭,與COVID-19的臨床表現相類似。MIS-C在免疫細胞水平的測試中表現與COVID-19相差無幾,較明顯可用於區分兩者的指標為免疫細胞嗜中性球水平。這一區別也用於區分MIS-C和川崎病 [ 292] [ 293]
公共衛生機構推薦群眾依靠常洗手、保持人際距離、少觸摸臉部來預防感染,同時疑似被感染者可透過戴口罩減少感染他人的機率。[ 294] [ 295] [ 295] [ 296] [ 297]
圖為美國疾控中心的SARS-CoV-2病毒檢測盒 針對感染SARS-CoV-2的病例,需要實時螢光RT-PCR 檢測病毒核酸呈陽性才能完全確診。但是在臨床實踐中,不排除測試結果呈虛假的反應 的可能出現,應結合流行病學接觸史和臨床特點進行綜合分析。[ 19] [ 19] [ 298] RT-PCR 檢測新型冠狀病毒核酸陽性者可以確診。在對呼吸道樣本或血液樣本進行病毒基因定序後,若與已知的新型冠狀病毒高度同源,即為確診病例。[ 17] 影像學檢查結果 等臨床特點綜合分析。[ 17]
RT-PCR測試是現有的對SARS-CoV-2病毒進行檢測的主流方式。[ 19] [ 299] [ 279] [ 300] + 巨噬細胞、CD20+ B細胞以及CD8+ T細胞。[ 279] [ 279]
針對RNA病毒,北京大學 和清華大學 的研究者聯合發表了一種新型確認病人感染新型冠狀病毒的定序手段SHERRY。這種手段透過基於Tn5轉座酶的轉錄組定序,相比傳統的smart-seq2技術有更好的效率,減少了樣本的需求量。新型冠狀病毒是SHERRY首次在臨床上進行應用的對象。[ 301]
2020年3月12日,瑞士製藥羅氏公司 宣布該公司基於核酸檢測 的商業化檢測方法得到了美國食品和藥物管理局(FDA)的緊急使用授權 [ 302] [ 303]
針對SARS-CoV-2常用的檢測手段為RT-PCR。[ 304] [ 305] [ 305]
More information 症狀, 百分比 ...
早期病例中患者出現不同症狀的比例[ 283]
症狀
百分比
發燒
87.9%
乾咳
67.7%
疲勞感
38.1%
積痰
33.4%
呼吸急促
18.6%
肌肉/關節痛
14.8%
咽喉酸痛
13.9%
頭痛
13.6%
寒顫
11.4%
噁心嘔吐
5.0%
鼻腔堵塞
4.8%
腹瀉
3.7%
咳血
0.9%
眼結膜充血
0.8%
Close
COVID-19患者因病毒特性,會患有病毒性肺炎。大多數患者表現以下呼吸道症狀為主,常見臨床表現包括發燒、四肢乏力、乾咳等症狀,其他表現包含咳痰、頭痛、咳血,或腹瀉等等。[ 110] [ 35] [ 107] 急性呼吸窘迫症候群 (ARDS)、敗血性休克、難以糾正的代謝性酸中毒、急性心肌損傷和出凝血功能障礙等。[ 19] [ 110] [ 218]
根據不同的臨床症狀,患者可被分為輕型、普通型、重型,以及危重型。[ 218] mmHg [ 218] [ 218]
對患者使用胸腔斷層掃描 檢查,可觀察到影像學異常。早期患者的肺部會呈現多發小斑片影及間質改變,以肺外帶明顯。經發展後,肺炎患者被觀察到雙肺多發毛玻璃狀影 肺實變 [ 45] [ 218] [ 306] C反應蛋白 (CRP)和紅血球沉降率 (ESR)升高,降鈣素原正常。嚴重者D-二聚體升高、周邊血淋巴球 進行性減少。[ 218] [ 307]
現今對COVID-19的病態生理學以及其微觀病變沒有完善的資料,但已有對死亡患者的解剖,展示了COVID-19的多個主要病理學特徵:[ 308] [ 309] [ 310]
光學檢查中,可發現包括胸膜炎、心包炎、肺實變和肺水腫在內的病徵。
屍體呈現不同程度的病毒性肺發炎狀,由輕至重如下:
輕度漿液性滲出、輕度纖維蛋白滲出
肺水腫、肺泡上皮細胞增生、非典型肺泡細胞、間質性發炎伴隨淋巴球浸潤及多核巨細胞的形成
後會出現擴散性肺泡損傷(DAD),導致在COVID-19患者中觀察到的急性呼吸窘迫症候群(ARDS)和嚴重的低氧血症。
還可觀察到肺泡腔內分泌物及肺間質纖維化
進行支氣管肺泡灌洗後可發現漿細胞
微泡性脂肪變性
目前,對COVID-19的病理的研究,主要來自於對SARS-CoV和MERS-CoV的理解。由於SARS-CoV-2和兩種病毒的相似性,研究者認為人體主動清除病毒的方式依然依靠免疫應答。[ 11] [ 311] + Th1細胞和CD8+ T細胞的抗病毒反應。[ 11] [ 311] [ 11] [ 312]
對人體不同器官的ACE2受體表現定序顯示,上呼吸道、肺部、迴腸、心臟、腎臟都是易損器官,有研究認為SARS-CoV-2造成的病毒血症對此有一定影響。[ 313] [ 314] [ 313] [ 315]
上圖為一名女性患者的CT影像,這名患者拍攝時已經經歷一周左右的鼻腔堵塞、乏力、厭食等初期症狀,血樣顯示較低水平的淋巴球。 上圖為一名典型男性患者的CT影像。 SARS-CoV-2感染人群後造成的COVID-19會先呈現上呼吸道症狀,並引起先天免疫系統的反擊。[ 316] [ 45] [ 311] [ 179]
相似於因SARS-CoV和MERS-CoV導致的重症患者,COVID-19患者目前常見的致死病因來自於細胞因子釋放症候群(CRS)。[ 317] 白血球 、淋巴球 減少,部分患者可以出現肝酶、乳酸去氫酶 (LDH)、肌酶和肌紅素 增高;部分危重者可見肌鈣蛋白 增高。[ 218] IL-2 、IL-7、IL-10、GCSF TNF-α 亦高於正常值[ 110]
患者由於被SARS-CoV-2感染,被活化的單核球、巨噬細胞等會分泌大量包括IL-6在內的炎性因子。[ 317] [ 318] 先天免疫系統 的方式被推測與SARS-CoV等同屬病毒有一樣的機制,IL-6可與IL-6R和gp130形成複合體,活化JAK-STAT通路,並引起CRS。[ 319] 細胞因子 ,同時IL-6在另一通路中會與sIL-6R結合,與gp130形成二聚體,利用下游的JAK-STAT3通路活化不表現mIL-6R的細胞。[ 317] 細胞因子風暴 和急性發炎反應 ,導致全身血管更為脆弱,引發急性呼吸窘迫症(ARDS)和多器官衰竭 。[ 110] [ 155] [ 317]
在進入重症的COVID-19患者中,很大比例的患者具有不同的心血管損傷如心律不整、血管栓塞、肺血管收縮等。[ 320] [ 321]
SARS-CoV-2結合的受體ACE2一般情況下會作用於Mas受體,發揮拮抗Ang II/AT1R效應,導致血壓降低、血管舒張並抑制發炎。受感染後由於ACE2的降低,RAS活化後向Ang II/AT1R偏移,從而使得組織擴大損傷。有研究表明,患有糖尿病、高血壓以及心衰的患者有顯著的高ACE2表現水平。[ 322] 99 。[ 320] [ 320] [ 321] [ 323]
受病毒感染後,患者有一定機率在血栓形成後引起大血管中風。[ 324] [ 325] [ 155] [ 156] [ 326] [ 326] [ 327]
病患的脾臟在被感染後也會具有不同程度的病變。包括脾臟及淋巴結,其內的CD4+ T細胞和CD8+ T細胞水平顯著下降。其他臨床症狀包括白髓萎縮、紅髓充血、灶性出血,脾臟內巨噬細胞增生並可見吞噬現象等。[ 328]
所有的COVID-19患者在入院後,都呈現出不同程度的胰臟、肝臟等器官的損傷。[ 110] [ 110] [ 329] [ 329] [ 330] [ 330]
儘管SARS-CoV-2在患者腸道內腔會被腸液不活化,有研究認為腸道也可能會被病毒感染且對疾病的發展有影響。[ 122] [ 313] [ 331] [ 240] [ 332] [ 333]
受SARS-CoV-2感染後,COVID-19患者的泌尿系統會受到不同程度的損傷。[ 334] [ 335] [ 336] [ 335] [ 335] [ 336] [ 336] [ 337]
有多個臨床研究報告了SARS-CoV-2也可以攻擊中樞神經。在多個報告中,不同比例的COVID-19患者有喪失嗅覺、味覺的症狀。一項病例報告指出從一名患有腦膜炎的患者的腦脊液中探測到了病毒的存在。[ 338]
SARS-CoV-2可透過眼結膜感染人體,也可因全身病毒性感染擴散至結膜[ 339] [ 340]
由於對病毒無特效的針對性治療方式,在臨床實踐中以維持患者生命指標為目標進行支持性治療。[ 35] α-干擾素 利巴韋林 等藥物抑制病症加重。[ 218] ECMO 等體外生命維持治療可臨床適用。[ 35]
一項研究發現,雄激素 剝奪療法是一種可能有效的預防病毒感染及治療COVID-19的手段。[ 341] [ 112] 前列腺癌 的患者經歷過雄激素剝奪療法後,感染病毒或因感染病毒死亡的比例均極大的低於其他類型的癌症患者。研究認為,由於雄激素具有調節TMPRSS2蛋白的功能,這一療法可以下調TMPRSS2表現,從而達到預防和治療的效果。[ 341]
較多COVID-19患者具有第2型糖尿病 ,初步的回顧性研究表明第2型糖尿病的主要治療藥物二甲雙胍仍可以應用於患有COVID-19的糖尿病患者。儘管二甲雙胍 在治療期間的酸中毒頻率與COVID-19的嚴重程度顯著相關,對患者死亡率沒有影響。[ 342]
COVID-19患者中症狀較重的一些病例需要在治療中採用機械通氣或其他類似手段來保證患者的正常呼吸功能。[ 343] [ 344] 插管 。[ 345] [ 344] [ 346]
在病患發展至出現ARDS 的階段,吸氧會更加困難。[ 347] [ 348] [ 349]
上圖為被認為當下最有效的抗新冠病毒藥瑞德西韋的分子結構 針對SARS-CoV-2的藥物研發自疫情初期的2020年1月底開始,中國科學院上海藥物研究所 與上海科技大學 的團隊羅列了已有的30種可能對病毒有效的藥物,其中包括蛋白酶抑制劑 因地那韋 沙奎那韋 、洛匹那韋 等抗病毒藥物 。[ 350] [ 351] [ 59]
由於針對COVID-19還沒有任何特效藥,在臨床實踐中的部分用藥屬於同情用藥,包括正在進行針對性臨床試驗的氯化奎寧、羥氯奎寧等藥物。[ 352] [ 353]
一種新型實驗性廣效抗病毒藥物瑞德西韋 [ 註 3] 呼吸道上皮細胞 中SARS和MERS病毒的複製。[ 354] [ 355] [ 356] [ 357] [ 358] [ 359] [ 360]
氯化奎寧類藥物因對SARS-CoV有一定抑制作用,也被一些研究者認為有可能可以有效抑制由SARS-CoV-2引發的COVID-19患者體內的病毒擴散。[ 361] [ 362] [ 363] [ 352] [ 364] 病毒載量 進行對比時發現,氯化奎寧藥物無法體現顯著的抑制效果。[ 352] FDA 也因此提醒不要使用氯化奎寧 或羥氯奎寧 。[ 365]
More information 藥品名稱, 效果 ...
下列為可能對SARS-CoV-2具有作用的藥物[ 366] [ 367]
藥品名稱
效果
有效範圍
備註
K22
抑制病毒的膜融合功能
對SARS-CoV及MERS-CoV有效,可能對SARS-CoV-2有效
[ 368]
雙鏈核糖核酸活化的細胞凋亡蛋白酶聚合體(DRACO)
針對病毒dsRNA並引起感染病毒的細胞凋亡
具有廣效抗病毒作用,可能對SARS-CoV-2有效
[ 369]
霉酚酸(MPA)
靶向核苷酸以抑制鳥苷一磷酸的合成
具有廣效抗病毒作用,可能可以結合IFN-β1b抑制SARS-CoV-2
[ 370]
洛匹那韋(Lopinavir)
抑制3CLpro
具有廣效抗病毒作用,包括SARS-CoV及MERS-CoV,可能對SARS-CoV-2有效
[ 371]
瑞德西韋(Remdesivir)
終止病毒RNA的轉錄
結合IFN-β可以抑制SARS-CoV-2感染
[ 356]
利巴韋林(Ribavirin)
靶向RdRp以抑制RNA合成
具有廣效抗病毒作用,包括SARS-CoV及MERS-CoV,低劑量用藥可能對SARS-CoV-2有效
[ 371]
加利地韋(Galidesivir)
靶向RdRp以抑制RNA合成
具有廣效抗病毒作用,包括SARS-CoV及MERS-CoV,可能對SARS-CoV-2有效
[ 372]
巴南寧(Bananins)
靶向病毒解旋酶蛋白以抑制解鏈及三磷酸腺苷酶活動
具有廣效抗病毒作用,可能對SARS-CoV-2有效
[ 373]
芳基二酮酸(ADK)
靶向病毒解旋酶蛋白以抑制解鏈
具有廣效抗病毒作用,包括SARS-CoV及MERS-CoV,可能對SARS-CoV-2有效
[ 373]
格瑞弗森凝集素(GRFT)
靶向病毒S蛋白上的低聚醣以阻止和宿主細胞結合
對SARS-CoV及MERS-CoV具有作用,可能對SARS-CoV-2有效
[ 374]
阿米洛利(Hexamethylene amiloride)
靶向病毒包膜蛋白並抑制離子通道
對數種冠狀病毒有效,可能適用於SARS-CoV-2治療。
[ 375]
親脂性噻唑烷衍生物JL103
靶向病毒脂膜,抑制病毒的膜融合
在多種病毒上有效,可能對SARS-CoV-2有效
[ 371] [ 373]
重組人工干擾素
誘導先天干擾素應答以應對病毒抗原
具有廣效抗病毒作用,可能對SARS-CoV-2有效
[ 371] [ 373]
硝唑尼特(Nitazoxanide)
誘導先天干擾素應答以應對病毒抗原
具有廣效抗病毒作用,可能對SARS-CoV-2有效
[ 376]
阿拉泊韋(Alisporivir)
抑制親環蛋白(CYP)以影響鈣調磷酸酶-T細胞細胞核因子通路
具有廣效抗病毒作用,更傾向於冠狀病毒,可能對SARS-CoV-2有效
[ 371]
雷帕黴素(Rapamycin)
抑制激酶資訊傳遞相關的通路以阻止病毒入侵
對SARS-CoV及MERS-CoV具有作用,可能對SARS-CoV-2有效
[ 377]
伊馬替尼(Imatinib)
抑制激酶資訊傳遞相關的通路以阻止病毒入侵
對SARS-CoV及MERS-CoV具有作用,可能對SARS-CoV-2有效
[ 371]
達沙替尼(Dasatinib)
抑制激酶資訊傳遞相關的通路以阻止病毒入侵
對SARS-CoV及MERS-CoV具有作用,可能對SARS-CoV-2有效
[ 371]
Close
由於2019年爆發的疫情影響,SARS-CoV-2病毒感染地區的人群呈現出不同程度的心理變化,有研究認為權力機構和醫療機構應當對病毒、病毒所引起的疾病和受疫情影響的群眾進行考慮,緩解心理壓力。[ 378]
在2019年爆發的疫情由於持續時間長,有評論認為,全球的醫護人員不是醫院的硬體設施可以24小時運轉,他們的身心健康需要得到關注。評論指出,對在疫情中治療COVID-19患者的醫生和護理師,需要提供足夠的家庭支持和心理疏導,這一評論將他們稱為當時「每一個國家最珍貴的資源」。[ 379] [ 380]
SARS-CoV-2於2019年底爆發時,病毒以及它所引發的疾病COVID-19的命名問題引起公眾討論。[ 381] [ 382] [ 383] [ 384]
利用SARS-CoV-2的不同稱呼,包括「中國病毒 」(Chinese Virus )、「武漢病毒 」(Wuhan Virus )、「冠狀病毒」(Coronavirus)、「新冠病毒」(Novel Coronavirus)等詞,有研究對人群的詞彙使用傾向和潛在心理機制進行了大資料分析。[ 385] [ 386] [ 385] [ 386] [ 385] [ 385] [ 386] [ 386] [ 386] [ 386]
2020年1月30日,一篇有關新型冠狀病毒在流行病學上的病例研究發表於新英格蘭醫學期刊 ,其中一項發現為德國有可能存在無症狀傳播者 。[ 387] Science 期刊刊登了一篇報道質疑了這項內容的準確和可靠性。[ 388] [ 388]
2020年1月31日,預印本網站BioRxiv 上刊登了一篇討論新型冠狀病毒基因構成的論文。論文稱,在病毒的S蛋白內發現4組和HIV-1 基因相似的序列。作者認為這樣的結果在自然中為偶然結果的可能性很小。[ 389] [ 390] [ 389] [ 391]
2020年2月18日,來自八個國家和多個不同科研機構的27名公共衛生領域的科學家於《刺胳針》上聯合發表聲明,指出對SARS-CoV-2病毒以及其引起的疾病COVID-19的謠言和陰謀論妨礙了疫情相關資料的共享。聲明的簽署人共同指出,他們想要促進科學的論證和團結,邀請更多的科學家加入這份聲明。[ 392]
Cheng-Tao. 武漢肺炎防疫手冊 . 國立嘉義大學嚴重特殊傳染性肺炎資訊平台. 2020-02-12 [2020-08-24 ] . (原始內容存檔 於2020-09-14). Gorbalenya, Alexander E.; Baker, Susan C.; Baric, Ralph S.; de Groot, Raoul J.; Drosten, Christian; Gulyaeva, Anastasia A.; Haagmans, Bart L.; Lauber, Chris; Leontovich, Andrey M. The species Severe acute respiratory syndrome-related coronavirus : classifying 2019-nCoV and naming it SARS-CoV-2 . Nature Microbiology. 2020-04, 5 (4): 536–544 [2020-03-24 ] . ISSN 2058-5276 doi:10.1038/s41564-020-0695-z 存檔 於2020-03-05) (英語) . Blake Oberfeld; Adi Achanta; Kendall Carpenter; Pamela Chen; Nicole Gilette; Pinky Langat; Jordan Said; Abigail Schiff; Allen Zhou; Amy Barczak; Shiv Pillai. SnapShot: COVID-19 (PDF) . Cell. 2020-04-13 [2020-04-19 ] . (原始內容存檔 (PDF) 於2020-04-19). Yang, Xiaobo; Yu, Yuan; Xu, Jiqian; Shu, Huaqing; Xia, Jia'an; Liu, Hong; Wu, Yongran; Zhang, Lu; Yu, Zhui. Clinical course and outcomes of critically ill patients with SARS-CoV-2 pneumonia in Wuhan, China: a single-centered, retrospective, observational study . The Lancet Respiratory Medicine. 2020-05-01, 8 (5): 475–481. ISSN 2213-2600 PMID 32105632 doi:10.1016/S2213-2600(20)30079-5 (英語) . 中國疾病預防控制中心 . www.chinacdc.cn. [2020-01-23 ] . (原始內容存檔 於2021-10-02).CoV2020 . platform.gisaid.org. [2020-01-12 ] . (原始內容存檔 於2020-01-12).Gorbalenya, Alexander E.; Krupovic, Mart; Mushegian, Arcady; Kropinski, Andrew M.; Siddell, Stuart G.; Varsani, Arvind; Adams, Michael J.; Davison, Andrew J.; Dutilh, Bas E. The new scope of virus taxonomy: partitioning the virosphere into 15 hierarchical ranks . Nature Microbiology. 2020-05, 5 (5): 668–674 [2020-05-01 ] . ISSN 2058-5276 doi:10.1038/s41564-020-0709-x 存檔 於2020-05-01) (英語) . Zhu, Na; Zhang, Dingyu; Wang, Wenling; Li, Xingwang; Yang, Bo; Song, Jingdong; Zhao, Xiang; Huang, Baoying; Shi, Weifeng. A Novel Coronavirus from Patients with Pneumonia in China, 2019 . New England Journal of Medicine. 2020-02-20, 382 (8): 727–733 [2021-01-19 ] . ISSN 0028-4793 PMC 7092803 PMID 31978945 doi:10.1056/NEJMoa2001017 存檔 於2020-07-12). Lu, Roujian; Zhao, Xiang; Li, Juan; Niu, Peihua; Yang, Bo; Wu, Honglong; Wang, Wenling; Song, Hao; Huang, Baoying. Genomic characterisation and epidemiology of 2019 novel coronavirus: implications for virus origins and receptor binding . The Lancet. 2020-02-22, 395 (10224): 565–574 [2021-01-19 ] . ISSN 0140-6736 PMID 32007145 doi:10.1016/S0140-6736(20)30251-8 存檔 於2020-05-19) (英語) . Zhang, Linlin; Lin, Daizong; Sun, Xinyuanyuan; Curth, Ute; Drosten, Christian; Sauerhering, Lucie; Becker, Stephan; Rox, Katharina; Hilgenfeld, Rolf. Crystal structure of SARS-CoV-2 main protease provides a basis for design of improved α-ketoamide inhibitors . Science. 2020-04-24, 368 (6489): 409–412 [2021-01-19 ] . ISSN 0036-8075 PMID 32198291 doi:10.1126/science.abb3405 存檔 於2021-08-18) (英語) . Yao, Hangping; Song, Yutong; Chen, Yong; Wu, Nanping; Xu, Jialu; Sun, Chujie; Zhang, Jiaxing; Weng, Tianhao; Zhang, Zheyuan. Molecular Architecture of the SARS-CoV-2 Virus . Cell. 2020-10, 183 (3): 730–738.e13 [2021-01-19 ] . PMC 7474903 PMID 32979942 doi:10.1016/j.cell.2020.09.018 存檔 於2021-11-12) (英語) . Gordon, David E.; Jang, Gwendolyn M.; Bouhaddou, Mehdi; Xu, Jiewei; Obernier, Kirsten; White, Kris M.; O』Meara, Matthew J.; Rezelj, Veronica V.; Guo, Jeffrey Z. A SARS-CoV-2 protein interaction map reveals targets for drug repurposing . Nature. 2020-07, 583 (7816): 459–468 [2020-05-01 ] . ISSN 1476-4687 doi:10.1038/s41586-020-2286-9 存檔 於2020-05-01) (英語) . Bakkers, Mark J. G.; Lang, Yifei; Feitsma, Louris J.; Hulswit, Ruben J. G.; Poot, Stefanie A. H. de; Vliet, Arno L. W. van; Margine, Irina; Groot-Mijnes, Jolanda D. F. de; Kuppeveld, Frank J. M. van. Betacoronavirus Adaptation to Humans Involved Progressive Loss of Hemagglutinin-Esterase Lectin Activity . Cell Host & Microbe. 2017-03-08, 21 (3): 356–366. ISSN 1931-3128 PMID 28279346 doi:10.1016/j.chom.2017.02.008 (英語) . Xiao, Kangpeng; Zhai, Junqiong; Feng, Yaoyu; Zhou, Niu; Zhang, Xu; Zou, Jie-Jian; Li, Na; Guo, Yaqiong; Li, Xiaobing; Shen, Xuejuan; Zhang, Zhipeng; Shu, Fanfan; Huang, Wanyi; Li, Yu; Zhang, Ziding; Chen, Rui-Ai; Wu, Ya-Jiang; Peng, Shi-Ming; Huang, Mian; Xie, Wei-Jun; Cai, Qin-Hui; Hou, Fang-Hui; Chen, Wu; Xiao, Lihua; Shen, Yongyi. Isolation of SARS-CoV-2-related coronavirus from Malayan pangolins. Nature. 2020-07-09, 583 (7815): 286–289. doi:10.1038/s41586-020-2313-x Wu, Aiping; Niu, Peihua; Wang, Lulan; Zhou, Hangyu; Zhao, Xiang; Wang, Wenling; Wang, Jingfeng; Ji, Chengyang; Ding, Xiao. Mutations, Recombination and Insertion in the Evolution of 2019-nCoV . bioRxiv. 2020-03-02: 2020.02.29.971101 [2020-03-06 ] . doi:10.1101/2020.02.29.971101 存檔 於2020-03-17) (英語) . Xie, Xuping; Muruato, Antonio; Lokugamage, Kumari G.; Narayanan, Krishna; Zhang, Xianwen; Zou, Jing; Liu, Jianying; Schindewolf, Craig; Bopp, Nathen E. An Infectious cDNA Clone of SARS-CoV-2 . Cell Host & Microbe. 2020-05, 27 (5): 841–848.e3 [2021-01-19 ] . PMC 7153529 PMID 32289263 doi:10.1016/j.chom.2020.04.004 存檔 於2021-12-07) (英語) . Thi Nhu Thao, Tran; Labroussaa, Fabien; Ebert, Nadine; V』kovski, Philip; Stalder, Hanspeter; Portmann, Jasmine; Kelly, Jenna; Steiner, Silvio; Holwerda, Melle. Rapid reconstruction of SARS-CoV-2 using a synthetic genomics platform . Nature. 2020-06, 582 (7813): 561–565 [2020-05-05 ] . ISSN 1476-4687 doi:10.1038/s41586-020-2294-9 存檔 於2020-05-04) (英語) . Zhang, Xiaonan; Tan, Yun; Ling, Yun; Lu, Gang; Liu, Feng; Yi, Zhigang; Jia, Xiaofang; Wu, Min; Shi, Bisheng. Viral and host factors related to the clinical outcome of COVID-19 . Nature. 2020-07, 583 (7816): 437–440 [2021-01-19 ] . ISSN 0028-0836 doi:10.1038/s41586-020-2355-0 存檔 於2021-12-15) (英語) . Tang, Xiaolu; Wu, Changcheng; Li, Xiang; Song, Yuhe; Yao, Xinmin; Wu, Xinkai; Duan, Yuange; Zhang, Hong; Wang, Yirong; Qian, Zhaohui; Cui, Jie; Lu, Jian. On the origin and continuing evolution of SARS-CoV-2 . National Science Review. 2020-03-03 [2020-03-06 ] . (原始內容存檔 於2020-03-06) (英語) . Young, Barnaby E.; Fong, Siew-Wai; Chan, Yi-Hao; Mak, Tze-Minn; Ang, Li Wei; Anderson, Danielle E.; Lee, Cheryl Yi-Pin; Amrun, Siti Naqiah; Lee, Bernett. Effects of a major deletion in the SARS-CoV-2 genome on the severity of infection and the inflammatory response: an observational cohort study . The Lancet. 2020-08-29, 396 (10251): 603–611. ISSN 0140-6736 PMID 32822564 doi:10.1016/S0140-6736(20)31757-8 (英語) . Su, Yvonne C. F.; Anderson, Danielle E.; Young, Barnaby E.; Linster, Martin; Zhu, Feng; Jayakumar, Jayanthi; Zhuang, Yan; Kalimuddin, Shirin; Low, Jenny G. H. Discovery and Genomic Characterization of a 382-Nucleotide Deletion in ORF7b and ORF8 during the Early Evolution of SARS-CoV-2 . mBio. 2020-08-25, 11 (4) [2020-08-21 ] . ISSN 2150-7511 PMID 32694143 doi:10.1128/mBio.01610-20 存檔 於2020-09-14) (英語) . Chan, Jasper Fuk-Woo; Yuan, Shuofeng; Kok, Kin-Hang; To, Kelvin Kai-Wang; Chu, Hin; Yang, Jin; Xing, Fanfan; Liu, Jieling; Yip, Cyril Chik-Yan. A familial cluster of pneumonia associated with the 2019 novel coronavirus indicating person-to-person transmission: a study of a family cluster . The Lancet. 2020-02-15, 395 (10223): 514–523. ISSN 0140-6736 PMID 31986261 doi:10.1016/S0140-6736(20)30154-9 (英語) . Hui, David S.; Azhar, Esam I.; Madani, Tariq A.; Ntoumi, Francine; Kock, Richard; Dar, Osman; Ippolito, Giuseppe; Mchugh, Timothy D.; Memish, Ziad A. The continuing 2019-nCoV epidemic threat of novel coronaviruses to global health — The latest 2019 novel coronavirus outbreak in Wuhan, China . International Journal of Infectious Diseases. 2020-02-01, 91 : 264–266 [2021-01-19 ] . ISSN 1201-9712 PMID 31953166 doi:10.1016/j.ijid.2020.01.009 存檔 於2020-04-01) (英語) . Huang, Chaolin; Wang, Yeming; Li, Xingwang; Ren, Lili; Zhao, Jianping; Hu, Yi; Zhang, Li; Fan, Guohui; Xu, Jiuyang. Clinical features of patients infected with 2019 novel coronavirus in Wuhan, China . The Lancet. 2020-02, 395 (10223): 497–506 [2021-01-20 ] . ISSN 0140-6736 PMC 7159299 PMID 31986264 doi:10.1016/s0140-6736(20)30183-5 存檔 於2020-01-27). Zhou, Jie; Li, Cun; Liu, Xiaojuan; Chiu, Man Chun; Zhao, Xiaoyu; Wang, Dong; Wei, Yuxuan; Lee, Andrew; Zhang, Anna Jinxia. Infection of bat and human intestinal organoids by SARS-CoV-2 . Nature Medicine. 2020-07, 26 (7): 1077–1083 [2020-05-13 ] . ISSN 1546-170X doi:10.1038/s41591-020-0912-6 存檔 於2020-05-14) (英語) . Chen, Nanshan; Zhou, Min; Dong, Xuan; Qu, Jieming; Gong, Fengyun; Han, Yang; Qiu, Yang; Wang, Jingli; Liu, Ying. Epidemiological and clinical characteristics of 99 cases of 2019 novel coronavirus pneumonia in Wuhan, China: a descriptive study . The Lancet. 2020-02-15, 395 (10223): 507–513. ISSN 0140-6736 PMID 32007143 doi:10.1016/S0140-6736(20)30211-7 (英語) . Ziegler, Carly G.K.; Allon, Samuel J.; Nyquist, Sarah K.; Mbano, Ian M.; Miao, Vincent N.; Tzouanas, Constantine N.; Cao, Yuming; Yousif, Ashraf S.; Bals, Julia. SARS-CoV-2 Receptor ACE2 Is an Interferon-Stimulated Gene in Human Airway Epithelial Cells and Is Detected in Specific Cell Subsets across Tissues . Cell. 2020-05, 181 (5): 1016–1035.e19 [2021-01-19 ] . ISSN 0092-8674 PMC 7252096 PMID 32413319 doi:10.1016/j.cell.2020.04.035 存檔 於2021-12-24). Kirchdoerfer, Robert N.; Cottrell, Christopher A.; Wang, Nianshuang; Pallesen, Jesper; Yassine, Hadi M.; Turner, Hannah L.; Corbett, Kizzmekia S.; Graham, Barney S.; McLellan, Jason S. Pre-fusion structure of a human coronavirus spike protein . Nature. 2016-03, 531 (7592): 118–121 [2020-04-20 ] . ISSN 1476-4687 doi:10.1038/nature17200 存檔 於2020-04-22) (英語) . Bertram, Stephanie; Heurich, Adeline; Lavender, Hayley; Gierer, Stefanie; Danisch, Simon; Perin, Paula; Lucas, Jared M.; Nelson, Peter S.; Pöhlmann, Stefan. Thiel, Volker , 編. Influenza and SARS-Coronavirus Activating Proteases TMPRSS2 and HAT Are Expressed at Multiple Sites in Human Respiratory and Gastrointestinal Tracts . PLoS ONE. 2012-04-30, 7 (4): e35876. ISSN 1932-6203 PMC 3340400 PMID 22558251 doi:10.1371/journal.pone.0035876 (英語) . Li, Wenhui; Moore, Michael J.; Vasilieva, Natalya; Sui, Jianhua; Wong, Swee Kee; Berne, Michael A.; Somasundaran, Mohan; Sullivan, John L.; Luzuriaga, Katherine. Angiotensin-converting enzyme 2 is a functional receptor for the SARS coronavirus . Nature. 2003-11, 426 (6965): 450–454 [2020-02-02 ] . ISSN 1476-4687 doi:10.1038/nature02145 存檔 於2020-02-05) (英語) . Glowacka, I.; Bertram, S.; Muller, M. A.; Allen, P.; Soilleux, E.; Pfefferle, S.; Steffen, I.; Tsegaye, T. S.; He, Y. Evidence that TMPRSS2 Activates the Severe Acute Respiratory Syndrome Coronavirus Spike Protein for Membrane Fusion and Reduces Viral Control by the Humoral Immune Response . Journal of Virology. 2011-05-01, 85 (9): 4122–4134 [2020-04-22 ] . ISSN 0022-538X PMC 3126222 PMID 21325420 doi:10.1128/JVI.02232-10 存檔 於2021-05-13) (英語) . Iwata-Yoshikawa, Naoko; Okamura, Tadashi; Shimizu, Yukiko; Hasegawa, Hideki; Takeda, Makoto; Nagata, Noriyo. Gallagher, Tom , 編. TMPRSS2 Contributes to Virus Spread and Immunopathology in the Airways of Murine Models after Coronavirus Infection . Journal of Virology. 2019-01-09, 93 (6): e01815–18, /jvi/93/6/JVI.01815–18.atom [2020-04-22 ] . ISSN 0022-538X PMC 6401451 PMID 30626688 doi:10.1128/JVI.01815-18 存檔 於2020-04-22) (英語) . Zhou, Peng; Yang, Xing-Lou; Wang, Xian-Guang; Hu, Ben; Zhang, Lei; Zhang, Wei; Si, Hao-Rui; Zhu, Yan; Li, Bei. A pneumonia outbreak associated with a new coronavirus of probable bat origin . Nature. 2020-03, 579 (7798): 270–273 [2020-03-15 ] . ISSN 1476-4687 doi:10.1038/s41586-020-2012-7 存檔 於2020-02-03) (英語) . Bosch, Berend Jan; Martina, Byron E. E.; Zee, Ruurd van der; Lepault, Jean; Haijema, Bert Jan; Versluis, Cees; Heck, Albert J. R.; Groot, Raoul de; Osterhaus, Albert D. M. E. Severe acute respiratory syndrome coronavirus (SARS-CoV) infection inhibition using spike protein heptad repeat-derived peptides . Proceedings of the National Academy of Sciences. 2004-06-01, 101 (22): 8455–8460 [2020-03-15 ] . ISSN 0027-8424 PMID 15150417 doi:10.1073/pnas.0400576101 存檔 於2020-03-10) (英語) . Wang, Jun; Zhao, Shanmeizi; Liu, Ming; Zhao, Zhiyao; Xu, Yiping; Wang, Ping; Lin, Meng; Xu, Yanhui; Huang, Bing. ACE2 expression by colonic epithelial cells is associated with viral infection, immunity and energy metabolism . medRxiv. 2020-02-07: 2020.02.05.20020545 [2020-02-10 ] . doi:10.1101/2020.02.05.20020545 存檔 於2021-11-05) (英語) . Wang, Quan; Wu, Jiqin; Wang, Haofeng; Gao, Yan; Liu, Qiaojie; Mu, An; Ji, Wenxin; Yan, Liming; Zhu, Yan. Structural Basis for RNA Replication by the SARS-CoV-2 Polymerase . Cell. 2020-07, 182 (2): 417–428.e13 [2021-01-19 ] . PMC 7242921 PMID 32526208 doi:10.1016/j.cell.2020.05.034 存檔 於2021-12-20) (英語) . Gao, Yan; Yan, Liming; Huang, Yucen; Liu, Fengjiang; Zhao, Yao; Cao, Lin; Wang, Tao; Sun, Qianqian; Ming, Zhenhua. Structure of RNA-dependent RNA polymerase from 2019-nCoV, a major antiviral drug target . bioRxiv. 2020-03-17: 2020.03.16.993386 [2020-03-20 ] . doi:10.1101/2020.03.16.993386 存檔 於2020-03-20) (英語) . Yin, Wanchao; Mao, Chunyou; Luan, Xiaodong; Shen, Dan-Dan; Shen, Qingya; Su, Haixia; Wang, Xiaoxi; Zhou, Fulai; Zhao, Wenfeng. Structural basis for inhibition of the RNA-dependent RNA polymerase from SARS-CoV-2 by remdesivir . Science. 2020-06-26, 368 (6498): 1499–1504 [2021-01-19 ] . ISSN 0036-8075 PMID 32358203 doi:10.1126/science.abc1560 存檔 於2021-08-26) (英語) . Jin, Zhenming; Du, Xiaoyu; Xu, Yechun; Deng, Yongqiang; Liu, Meiqin; Zhao, Yao; Zhang, Bing; Li, Xiaofeng; Zhang, Leike. Structure of M pro from SARS-CoV-2 and discovery of its inhibitors . Nature. 2020-06, 582 (7811): 289–293 [2020-05-22 ] . ISSN 1476-4687 doi:10.1038/s41586-020-2223-y 存檔 於2020-05-14) (英語) . Shi, Jianzhong; Wen, Zhiyuan; Zhong, Gongxun; Yang, Huanliang; Wang, Chong; Huang, Baoying; Liu, Renqiang; He, Xijun; Shuai, Lei. Susceptibility of ferrets, cats, dogs, and other domesticated animals to SARS–coronavirus 2 . Science. 2020-05-29, 368 (6494): 1016–1020 [2021-01-19 ] . ISSN 0036-8075 PMID 32269068 doi:10.1126/science.abb7015 存檔 於2021-08-11) (英語) . Kim, Young-Il; Kim, Seong-Gyu; Kim, Se-Mi; Kim, Eun-Ha; Park, Su-Jin; Yu, Kwang-Min; Chang, Jae-Hyung; Kim, Eun Ji; Lee, Seunghun. Infection and Rapid Transmission of SARS-CoV-2 in Ferrets . Cell Host & Microbe. 2020-05, 27 (5): 704–709.e2 [2021-01-19 ] . ISSN 1931-3128 PMC 7144857 PMID 32259477 doi:10.1016/j.chom.2020.03.023 存檔 於2021-11-30). Sit, Thomas H. C.; Brackman, Christopher J.; Ip, Sin Ming; Tam, Karina W. S.; Law, Pierra Y. T.; To, Esther M. W.; Yu, Veronica Y. T.; Sims, Leslie D.; Tsang, Dominic N. C. Infection of dogs with SARS-CoV-2 . Nature. 2020-10, 586 (7831): 776–778 [2020-05-14 ] . ISSN 1476-4687 doi:10.1038/s41586-020-2334-5 存檔 於2020-05-14) (英語) . Sia, Sin Fun; Yan, Li-Meng; Chin, Alex W. H.; Fung, Kevin; Choy, Ka-Tim; Wong, Alvina Y. L.; Kaewpreedee, Prathanporn; Perera, Ranawaka A. P. M.; Poon, Leo L. M. Pathogenesis and transmission of SARS-CoV-2 in golden hamsters . Nature. 2020-07, 583 (7818): 834–838 [2020-05-14 ] . ISSN 1476-4687 doi:10.1038/s41586-020-2342-5 存檔 於2020-07-11) (英語) . Murakami, Shin; Kitamura, Tomoya; Suzuki, Jin; Sato, Ryouta; Aoi, Toshiki; Fujii, Marina; Matsugo, Hiromichi; Kamiki, Haruhiko; Ishida, Hiroho; Takenaka-Uema, Akiko; Shimojima, Masayuki; Horimoto, Taisuke. Detection and Characterization of Bat Sarbecovirus Phylogenetically Related to SARS-CoV-2, Japan. Emerging Infectious Diseases. 2020, 26 (12): 3025–3029. ISSN 1080-6040 doi:10.3201/eid2612.203386 Hu, Dan; Zhu, Changqiang; Ai, Lele; He, Ting; Wang, Yi; Ye, Fuqiang; Yang, Lu; Ding, Chenxi; Zhu, Xuhui; Lv, Ruicheng; Zhu, Jin; Hassan, Bachar; Feng, Youjun; Tan, Weilong; Wang, Changjun. Genomic characterization and infectivity of a novel SARS-like coronavirus in Chinese bats. Emerging Microbes & Infections. 2018, 7 (1): 1–10. ISSN 2222-1751 doi:10.1038/s41426-018-0155-5 Xiao, Kangpeng; Zhai, Junqiong; Feng, Yaoyu; Zhou, Niu; Zhang, Xu; Zou, Jie-Jian; Li, Na; Guo, Yaqiong; Li, Xiaobing; Shen, Xuejuan; Zhang, Zhipeng; Shu, Fanfan; Huang, Wanyi; Li, Yu; Zhang, Ziding; Chen, Rui-Ai; Wu, Ya-Jiang; Peng, Shi-Ming; Huang, Mian; Xie, Wei-Jun; Cai, Qin-Hui; Hou, Fang-Hui; Chen, Wu; Xiao, Lihua; Shen, Yongyi. Isolation of SARS-CoV-2-related coronavirus from Malayan pangolins. Nature. 2020-07-09, 583 (7815): 286–289. doi:10.1038/s41586-020-2313-x Zhou, Hong; Chen, Xing; Hu, Tao; Li, Juan; Song, Hao; Liu, Yanran; Wang, Peihan; Liu, Di; Yang, Jing; Holmes, Edward C.; Hughes, Alice C.; Bi, Yuhai; Shi, Weifeng. A Novel Bat Coronavirus Closely Related to SARS-CoV-2 Contains Natural Insertions at the S1/S2 Cleavage Site of the Spike Protein. Current Biology. 2020, 30 (11): 2196–2203.e3. ISSN 0960-9822 doi:10.1016/j.cub.2020.05.023 Zhou, Peng; Yang, Xing-Lou; Wang, Xian-Guang; Hu, Ben; Zhang, Lei; Zhang, Wei; Si, Hao-Rui; Zhu, Yan; et al. A pneumonia outbreak associated with a new coronavirus of probable bat origin. Nature. 2020, 579 (7798): 270–273. ISSN 0028-0836 doi:10.1038/s41586-020-2012-7 Temmam, Sarah; Vongphayloth, Khamsing; Baquero, Eduard; Munier, Sandie; Bonomi, Massimiliano; Regnault, Béatrice; Douangboubpha, Bounsavane; Karami, Yasaman; Chrétien, Delphine; Sanamxay, Daosavanh; Xayaphet, Vilakhan; Paphaphanh, Phetphoumin; Lacoste, Vincent; Somlor, Somphavanh; Lakeomany, Khaithong; Phommavanh, Nothasin; Pérot, Philippe; Dehan, Océane; Amara, Faustine; Donati, Flora; Bigot, Thomas; Nilges, Michael; Rey, Félix A.; van der Werf, Sylvie; Brey, Paul T.; Eloit, Marc. Bat coronaviruses related to SARS-CoV-2 and infectious for human cells. Nature. 16 February 2022. doi:10.1038/s41586-022-04532-4 Zhao, Juanjuan; Yuan, Quan; Wang, Haiyan; Liu, Wei; Liao, Xuejiao; Su, Yingying; Wang, Xin; Yuan, Jing; Li, Tingdong. Antibody Responses to SARS-CoV-2 in Patients With Novel Coronavirus Disease 2019 . Clinical Infectious Diseases. 2020-11-19, 71 (16): 2027–2034 [2021-01-19 ] . ISSN 1058-4838 PMC 7184337 PMID 32221519 doi:10.1093/cid/ciaa344 存檔 於2021-12-06) (英語) . Zhou, Yonggang; Fu, Binqing; Zheng, Xiaohu; Wang, Dongsheng; Zhao, Changcheng; Qi, Yingjie; Sun, Rui; Tian, Zhigang; Xu, Xiaoling. Pathogenic T-cells and inflammatory monocytes incite inflammatory storms in severe COVID-19 patients . National Science Review. 2020-06-01, 7 (6): 998–1002 [2021-01-19 ] . ISSN 2095-5138 doi:10.1093/nsr/nwaa041 存檔 於2021-12-21) (英語) . Bost, Pierre; Giladi, Amir; Liu, Yang; Bendjelal, Yanis; Xu, Gang; David, Eyal; Blecher-Gonen, Ronnie; Cohen, Merav; Medaglia, Chiara. Host-Viral Infection Maps Reveal Signatures of Severe COVID-19 Patients . Cell. 2020-06-25, 181 (7): 1475–1488.e12. ISSN 0092-8674 PMID 32479746 doi:10.1016/j.cell.2020.05.006 (英語) . Liao, Mingfeng; Liu, Yang; Yuan, Jing; Wen, Yanling; Xu, Gang; Zhao, Juanjuan; Cheng, Lin; Li, Jinxiu; Wang, Xin. Single-cell landscape of bronchoalveolar immune cells in patients with COVID-19 . Nature Medicine. 2020-06, 26 (6): 842–844 [2020-05-12 ] . ISSN 1546-170X doi:10.1038/s41591-020-0901-9 存檔 於2020-05-13) (英語) . Wang, Qiming; Fang, Peining; He, Rui; Li, Mengqi; Yu, Haisheng; Zhou, Li; Yi, Yu; Wang, Fubing; Rong, Yuan. O-GlcNAc transferase promotes influenza A virus–induced cytokine storm by targeting interferon regulatory factor–5 . Science Advances. 2020-04-01, 6 (16): eaaz7086 [2020-04-19 ] . ISSN 2375-2548 doi:10.1126/sciadv.aaz7086 存檔 於2021-08-14) (英語) . Thevarajan, Irani; Nguyen, Thi H. O.; Koutsakos, Marios; Druce, Julian; Caly, Leon; van de Sandt, Carolien E.; Jia, Xiaoxiao; Nicholson, Suellen; Catton, Mike. Breadth of concomitant immune responses prior to patient recovery: a case report of non-severe COVID-19 . Nature Medicine. 2020-04, 26 (4): 453–455 [2020-03-20 ] . ISSN 1546-170X doi:10.1038/s41591-020-0819-2 存檔 於2020-03-20) (英語) . Chen, Xiangyu; Li, Ren; Pan, Zhiwei; Qian, Chunfang; Yang, Yang; You, Renrong; Zhao, Jing; Liu, Pinghuang; Gao, Leiqiong. Human monoclonal antibodies block the binding of SARS-CoV-2 spike protein to angiotensin converting enzyme 2 receptor . Cellular & Molecular Immunology. 2020-06, 17 (6): 647–649 [2020-04-20 ] . ISSN 2042-0226 doi:10.1038/s41423-020-0426-7 存檔 於2020-04-22) (英語) . Vabret, Nicolas; Britton, Graham J.; Gruber, Conor; Hegde, Samarth; Kim, Joel; Kuksin, Maria; Levantovsky, Rachel; Malle, Louise; Moreira, Alvaro. Immunology of COVID-19: Current State of the Science . Immunity. 2020-06, 52 (6): 910–941 [2021-01-19 ] . ISSN 1074-7613 PMC 7200337 PMID 32505227 doi:10.1016/j.immuni.2020.05.002 存檔 於2021-12-21). Channappanavar, Rudragouda; Fehr, Anthony R.; Zheng, Jian; Wohlford-Lenane, Christine; Abrahante, Juan E.; Mack, Matthias; Sompallae, Ramakrishna; McCray, Paul B.; Meyerholz, David K. IFN-I response timing relative to virus replication determines MERS coronavirus infection outcomes . The Journal of Clinical Investigation. 2019-09-03, 129 (9): 3625–3639 [2020-05-23 ] . ISSN 0021-9738 PMC 6715373 PMID 31355779 doi:10.1172/JCI126363 存檔 於2020-05-23) (英語) . Blanco-Melo, Daniel; Nilsson-Payant, Benjamin E.; Liu, Wen-Chun; Uhl, Skyler; Hoagland, Daisy; Møller, Rasmus; Jordan, Tristan X.; Oishi, Kohei; Panis, Maryline. Imbalanced Host Response to SARS-CoV-2 Drives Development of COVID-19 . Cell. 2020-05, 181 (5): 1036–1045.e9 [2021-01-19 ] . PMC 7227586 PMID 32416070 doi:10.1016/j.cell.2020.04.026 存檔 於2021-12-18) (英語) . Zhao, Xuesen; Zheng, Shuangli; Chen, Danying; Zheng, Mei; Li, Xinglin; Li, Guoli; Lin, Hanxin; Chang, Jinhong; Zeng, Hui. LY6E Restricts the Entry of Human Coronaviruses, including the currently pandemic SARS-CoV-2 . bioRxiv. 2020-04-05: 2020.04.02.021469 [2020-05-23 ] . doi:10.1101/2020.04.02.021469 存檔 於2020-07-26) (英語) . Cameron, Mark J.; Kelvin, Alyson A.; Leon, Alberto J.; Cameron, Cheryl M.; Ran, Longsi; Xu, Luoling; Chu, Yong-Kyu; Danesh, Ali; Fang, Yuan. Lack of Innate Interferon Responses during SARS Coronavirus Infection in a Vaccination and Reinfection Ferret Model . PLOS ONE. 2012-09-24, 7 (9): e45842 [2020-10-02 ] . ISSN 1932-6203 PMC 3454321 PMID 23029269 doi:10.1371/journal.pone.0045842 存檔 於2020-09-14) (英語) . Walls, Alexandra C.; Tortorici, M. Alejandra; Frenz, Brandon; Snijder, Joost; Li, Wentao; Rey, Félix A.; DiMaio, Frank; Bosch, Berend-Jan; Veesler, David. Glycan shield and epitope masking of a coronavirus spike protein observed by cryo-electron microscopy . Nature Structural & Molecular Biology. 2016-10, 23 (10): 899–905 [2020-03-09 ] . ISSN 1545-9985 doi:10.1038/nsmb.3293 存檔 於2020-02-24) (英語) . Long, Quan-Xin; Liu, Bai-Zhong; Deng, Hai-Jun; Wu, Gui-Cheng; Deng, Kun; Chen, Yao-Kai; Liao, Pu; Qiu, Jing-Fu; Lin, Yong. Antibody responses to SARS-CoV-2 in patients with COVID-19 . Nature Medicine. 2020-06, 26 (6): 845–848 [2020-05-01 ] . ISSN 1546-170X doi:10.1038/s41591-020-0897-1 存檔 於2020-05-01) (英語) . Grifoni, Alba; Weiskopf, Daniela; Ramirez, Sydney I.; Mateus, Jose; Dan, Jennifer M.; Moderbacher, Carolyn Rydyznski; Rawlings, Stephen A.; Sutherland, Aaron; Premkumar, Lakshmanane. Targets of T Cell Responses to SARS-CoV-2 Coronavirus in Humans with COVID-19 Disease and Unexposed Individuals . Cell. 2020-06-25, 181 (7): 1489–1501.e15 [2021-01-19 ] . ISSN 0092-8674 doi:10.1016/j.cell.2020.05.015 存檔 於2021-12-21) (英語) . Ni, Ling; Ye, Fang; Cheng, Meng-Li; Feng, Yu; Deng, Yong-Qiang; Zhao, Hui; Wei, Peng; Ge, Jiwan; Gou, Mengting. Detection of SARS-CoV-2-Specific Humoral and Cellular Immunity in COVID-19 Convalescent Individuals . Immunity. 2020-06-16, 52 (6): 971–977.e3. ISSN 1074-7613 PMID 32413330 doi:10.1016/j.immuni.2020.04.023 (英語) . Keng, Choong-Tat; Zhang, Aihua; Shen, Shuo; Lip, Kuo-Ming; Fielding, Burtram C.; Tan, Timothy H. P.; Chou, Chih-Fong; Loh, Chay Boon; Wang, Sifang. Amino Acids 1055 to 1192 in the S2 Region of Severe Acute Respiratory Syndrome Coronavirus S Protein Induce Neutralizing Antibodies: Implications for the Development of Vaccines and Antiviral Agents . Journal of Virology. 2005-03-15, 79 (6): 3289–3296 [2020-03-09 ] . ISSN 0022-538X PMID 15731223 doi:10.1128/JVI.79.6.3289-3296.2005 存檔 於2020-03-08) (英語) . Lip, Kuo-Ming; Shen, Shuo; Yang, Xiaoming; Keng, Choong-Tat; Zhang, Aihua; Oh, Hsueh-Ling Janice; Li, Zhi-Hong; Hwang, Le-Ann; Chou, Chih-Fong. Monoclonal Antibodies Targeting the HR2 Domain and the Region Immediately Upstream of the HR2 of the S Protein Neutralize In Vitro Infection of Severe Acute Respiratory Syndrome Coronavirus . Journal of Virology. 2006-01-15, 80 (2): 941–950 [2020-03-09 ] . ISSN 0022-538X PMID 16378996 doi:10.1128/JVI.80.2.941-950.2006 存檔 於2020-03-21) (英語) . Cao, Yunlong; Su, Bin; Guo, Xianghua; Sun, Wenjie; Deng, Yongqiang; Bao, Linlin; Zhu, Qinyu; Zhang, Xu; Zheng, Yinghui. Potent Neutralizing Antibodies against SARS-CoV-2 Identified by High-Throughput Single-Cell Sequencing of Convalescent Patients’ B Cells . Cell. 2020-07, 182 (1): 73–84.e16 [2021-01-19 ] . ISSN 0092-8674 PMC 7231725 PMID 32425270 doi:10.1016/j.cell.2020.05.025 存檔 於2021-11-06). Pinto, Dora; Park, Young-Jun; Beltramello, Martina; Walls, Alexandra C.; Tortorici, M. Alejandra; Bianchi, Siro; Jaconi, Stefano; Culap, Katja; Zatta, Fabrizia. Cross-neutralization of SARS-CoV-2 by a human monoclonal SARS-CoV antibody . Nature. 2020-07, 583 (7815): 290–295 [2020-05-19 ] . ISSN 1476-4687 doi:10.1038/s41586-020-2349-y 存檔 於2020-05-18) (英語) . Ju, Bin; Zhang, Qi; Ge, Jiwan; Wang, Ruoke; Sun, Jing; Ge, Xiangyang; Yu, Jiazhen; Shan, Sisi; Zhou, Bing. Human neutralizing antibodies elicited by SARS-CoV-2 infection . Nature. 2020-08, 584 (7819): 115–119 [2020-05-28 ] . ISSN 1476-4687 doi:10.1038/s41586-020-2380-z 存檔 於2020-05-27) (英語) . Wen, Wen; Su, Wenru; Tang, Hao; Le, Wenqing; Zhang, Xiaopeng; Zheng, Yingfeng; Liu, Xiuxing; Xie, Lihui; Li, Jianmin. Immune cell profiling of COVID-19 patients in the recovery stage by single-cell sequencing . Cell Discovery. 2020-05-04, 6 (1): 1–18 [2020-05-15 ] . ISSN 2056-5968 doi:10.1038/s41421-020-0168-9 存檔 於2020-05-17) (英語) . Tang, Fang; Quan, Yan; Xin, Zhong-Tao; Wrammert, Jens; Ma, Mai-Juan; Lv, Hui; Wang, Tian-Bao; Yang, Hong; Richardus, Jan H. Lack of Peripheral Memory B Cell Responses in Recovered Patients with Severe Acute Respiratory Syndrome: A Six-Year Follow-Up Study . The Journal of Immunology. 2011-06-15, 186 (12): 7264–7268 [2020-08-21 ] . ISSN 0022-1767 PMID 21576510 doi:10.4049/jimmunol.0903490 存檔 於2021-11-10) (英語) . Le Bert, Nina; Tan, Anthony T.; Kunasegaran, Kamini; Tham, Christine Y. L.; Hafezi, Morteza; Chia, Adeline; Chng, Melissa Hui Yen; Lin, Meiyin; Tan, Nicole. SARS-CoV-2-specific T cell immunity in cases of COVID-19 and SARS, and uninfected controls . Nature. 2020-08, 584 (7821): 457–462 [2020-08-21 ] . ISSN 1476-4687 doi:10.1038/s41586-020-2550-z 存檔 於2020-08-21) (英語) . Yang, Li-Tao; Peng, Hui; Zhu, Zhao-Ling; Li, Gang; Huang, Zi-Tong; Zhao, Zhi-Xin; Koup, Richard A.; Bailer, Robert T.; Wu, Chang-You. Long-lived effector/central memory T-cell responses to severe acute respiratory syndrome coronavirus (SARS-CoV) S antigen in recovered SARS patients . Clinical Immunology. 2006-08-01, 120 (2): 171–178 [2021-01-19 ] . ISSN 1521-6616 PMC 7106132 PMID 16781892 doi:10.1016/j.clim.2006.05.002 存檔 於2021-10-11) (英語) . Long, Quan-Xin; Tang, Xiao-Jun; Shi, Qiu-Lin; Li, Qin; Deng, Hai-Jun; Yuan, Jun; Hu, Jie-Li; Xu, Wei; Zhang, Yong. Clinical and immunological assessment of asymptomatic SARS-CoV-2 infections . Nature Medicine. 2020-08, 26 (8): 1200–1204 [2020-08-21 ] . ISSN 1546-170X doi:10.1038/s41591-020-0965-6 存檔 於2020-08-21) (英語) . Sekine, Takuya; Perez-Potti, André; Rivera-Ballesteros, Olga; Strålin, Kristoffer; Gorin, Jean-Baptiste; Olsson, Annika; Llewellyn-Lacey, Sian; Kamal, Habiba; Bogdanovic, Gordana. Robust T Cell Immunity in Convalescent Individuals with Asymptomatic or Mild COVID-19 . Cell. 2020-10, 183 (1): 158–168.e14 [2021-01-19 ] . PMC 7427556 PMID 32979941 doi:10.1016/j.cell.2020.08.017 存檔 於2021-12-28) (英語) . Wilk, Aaron J.; Rustagi, Arjun; Zhao, Nancy Q.; Roque, Jonasel; Martínez-Colón, Giovanny J.; McKechnie, Julia L.; Ivison, Geoffrey T.; Ranganath, Thanmayi; Vergara, Rosemary. A single-cell atlas of the peripheral immune response in patients with severe COVID-19 . Nature Medicine. 2020-07, 26 (7): 1070–1076 [2020-08-21 ] . ISSN 1546-170X doi:10.1038/s41591-020-0944-y 存檔 於2020-09-14) (英語) . Bi, Qifang; Wu, Yongsheng; Mei, Shujiang; Ye, Chenfei; Zou, Xuan; Zhang, Zhen; Liu, Xiaojian; Wei, Lan; Truelove, Shaun A. Epidemiology and Transmission of COVID-19 in Shenzhen China: Analysis of 391 cases and 1,286 of their close contacts . medRxiv. 2020-03-04: 2020.03.03.20028423 [2020-03-06 ] . ISSN 2002-8423 doi:10.1101/2020.03.03.20028423 存檔 於2020-03-07) (英語) . Li, Qun; Guan, Xuhua; Wu, Peng; Wang, Xiaoye; Zhou, Lei; Tong, Yeqing; Ren, Ruiqi; Leung, Kathy S. M.; Lau, Eric H. Y. Early Transmission Dynamics in Wuhan, China, of Novel Coronavirus–Infected Pneumonia . New England Journal of Medicine. 2020-01-29 [2020-09-28 ] . PMC 7121484 PMID 31995857 doi:10.1056/NEJMoa2001316 存檔 於2021-12-29) (英語) . COVID-19 . Imperial College London. [2021-01-20 ] (英國英語) .Stefanelli, Paola; Faggioni, Giovanni; Lo Presti, Alessandra; Fiore, Stefano; Marchi, Antonella; Benedetti, Eleonora; Fabiani, Concetta; Anselmo, Anna; Ciammaruconi, Andrea. Whole genome and phylogenetic analysis of two SARS-CoV-2 strains isolated in Italy in January and February 2020: additional clues on multiple introductions and further circulation in Europe . Eurosurveillance. 2020-04-02, 25 (13) [2020-04-21 ] . ISSN 1560-7917 PMC 7140597 PMID 32265007 doi:10.2807/1560-7917.ES.2020.25.13.2000305 存檔 於2020-04-22) (英語) . James Holland Jones. Notes On R0 (PDF) . Stanford University. [2020-01-27 ] . (原始內容存檔 (PDF) 於2020-01-04). Zhao, Shi; Lin, Qianyin; Ran, Jinjun; Musa, Salihu S.; Yang, Guangpu; Wang, Weiming; Lou, Yijun; Gao, Daozhou; Yang, Lin. Preliminary estimation of the basic reproduction number of novel coronavirus (2019-nCoV) in China, from 2019 to 2020: A data-driven analysis in the early phase of the outbreak . International Journal of Infectious Diseases. 2020-03, 92 : 214–217 [2021-01-20 ] . PMC 7110798 PMID 32007643 doi:10.1016/j.ijid.2020.01.050 存檔 於2021-10-21) (英語) . Lam, Tommy Tsan-Yuk; Jia, Na; Zhang, Ya-Wei; Shum, Marcus Ho-Hin; Jiang, Jia-Fu; Zhu, Hua-Chen; Tong, Yi-Gang; Shi, Yong-Xia; Ni, Xue-Bing. Identifying SARS-CoV-2-related coronaviruses in Malayan pangolins . Nature. 2020-07, 583 (7815): 282–285 [2020-03-27 ] . ISSN 1476-4687 doi:10.1038/s41586-020-2169-0 存檔 於2020-03-27) (英語) . 衛生福利部疾病管制署. 新型冠狀病毒:疾病介紹 . [2020-01-28 ] . (原始內容存檔 於2020-01-27) (中文(臺灣)) . van Doremalen, Neeltje; Bushmaker, Trenton; Morris, Dylan H.; Holbrook, Myndi G.; Gamble, Amandine; Williamson, Brandi N.; Tamin, Azaibi; Harcourt, Jennifer L.; Thornburg, Natalie J. Aerosol and Surface Stability of SARS-CoV-2 as Compared with SARS-CoV-1 . New England Journal of Medicine. 2020-04-16, 382 (16): 1564–1567 [2021-01-20 ] . ISSN 0028-4793 PMC 7121658 PMID 32182409 doi:10.1056/NEJMc2004973 存檔 於2020-06-05). Zheng, Shufa; Fan, Jian; Yu, Fei; Feng, Baihuan; Lou, Bin; Zou, Qianda; Xie, Guoliang; Lin, Sha; Wang, Ruonan. Viral load dynamics and disease severity in patients infected with SARS-CoV-2 in Zhejiang province, China, January-March 2020: retrospective cohort study . BMJ. 2020-04-21, 369 [2020-04-22 ] . ISSN 1756-1833 PMID 32317267 doi:10.1136/bmj.m1443 存檔 於2020-04-22) (英語) . Sood, Neeraj; Simon, Paul; Ebner, Peggy; Eichner, Daniel; Reynolds, Jeffrey; Bendavid, Eran; Bhattacharya, Jay. Seroprevalence of SARS-CoV-2–Specific Antibodies Among Adults in Los Angeles County, California, on April 10-11, 2020 . JAMA. 2020-06-16, 323 (23): 2425 [2020-05-20 ] . ISSN 0098-7484 doi:10.1001/jama.2020.8279 存檔 於2020-05-20) (英語) . Liu, Yuan; Ning, Zhi; Chen, Yu; Guo, Ming; Liu, Yingle; Gali, Nirmal Kumar; Sun, Li; Duan, Yusen; Cai, Jing. Aerodynamic analysis of SARS-CoV-2 in two Wuhan hospitals . Nature. 2020-06, 582 (7813): 557–560 [2020-04-27 ] . ISSN 1476-4687 doi:10.1038/s41586-020-2271-3 存檔 於2020-04-27) (英語) . 、Zhang, Juanjuan; Litvinova, Maria; Liang, Yuxia; Wang, Yan; Wang, Wei; Zhao, Shanlu; Wu, Qianhui; Merler, Stefano; Viboud, Cécile. Changes in contact patterns shape the dynamics of the COVID-19 outbreak in China . Science. 2020-06-26, 368 (6498): 1481–1486 [2021-01-20 ] . ISSN 0036-8075 PMID 32350060 doi:10.1126/science.abb8001 存檔 於2021-08-20) (英語) . Zou, Lirong; Ruan, Feng; Huang, Mingxing; Liang, Lijun; Huang, Huitao; Hong, Zhongsi; Yu, Jianxiang; Kang, Min; Song, Yingchao. SARS-CoV-2 Viral Load in Upper Respiratory Specimens of Infected Patients . New England Journal of Medicine. 2020-03-19, 382 (12): 1177–1179. ISSN 0028-4793 PMC 7121626 PMID 32074444 doi:10.1056/NEJMc2001737 Lavezzo, Enrico; Franchin, Elisa; Ciavarella, Constanze; Cuomo-Dannenburg, Gina; Barzon, Luisa; Del Vecchio, Claudia; Rossi, Lucia; Manganelli, Riccardo; Loregian, Arianna. Suppression of a SARS-CoV-2 outbreak in the Italian municipality of Vo’ . Nature. 2020-08, 584 (7821): 425–429 [2020-08-21 ] . ISSN 1476-4687 doi:10.1038/s41586-020-2488-1 存檔 於2020-08-18) (英語) . He, Xi; Lau, Eric H. Y.; Wu, Peng; Deng, Xilong; Wang, Jian; Hao, Xinxin; Lau, Yiu Chung; Wong, Jessica Y.; Guan, Yujuan. Temporal dynamics in viral shedding and transmissibility of COVID-19 . Nature Medicine. 2020-05, 26 (5): 672–675 [2020-04-18 ] . ISSN 1546-170X doi:10.1038/s41591-020-0869-5 存檔 於2020-04-19) (英語) . Yao, Xiao-Hong; He, Zhi-Cheng; Li, Ting-Yuan; Zhang, Hua-Rong; Wang, Yan; Mou, Huaming; Guo, Qiaonan; Yu, Shi-Cang; Ding, Yanqing. Pathological evidence for residual SARS-CoV-2 in pulmonary tissues of a ready-for-discharge patient . Cell Research. 2020-06, 30 (6): 541–543 [2020-04-29 ] . ISSN 1748-7838 doi:10.1038/s41422-020-0318-5 存檔 於2020-04-30) (英語) . Sama, Iziah E.; Ravera, Alice; Santema, Bernadet T.; van Goor, Harry; ter Maaten, Jozine M.; Cleland, John G. F.; Rienstra, Michiel; Friedrich, Alex W.; Samani, Nilesh J. Circulating plasma concentrations of angiotensin-converting enzyme 2 in men and women with heart failure and effects of renin–angiotensin–aldosterone inhibitors . European Heart Journal. 2020-05-14, 41 (19): 1810–1817 [2021-01-20 ] . ISSN 0195-668X doi:10.1093/eurheartj/ehaa373 存檔 於2021-12-21) (英語) . Jin, Ying-Hui; Cai, Lin; Cheng, Zhen-Shun; Cheng, Hong; Deng, Tong; Fan, Yi-Pin; Fang, Cheng; Huang, Di; Huang, Lu-Qi. A rapid advice guideline for the diagnosis and treatment of 2019 novel coronavirus (2019-nCoV) infected pneumonia (standard version) . Military Medical Research. 2020-02-06, 7 (1): 4. ISSN 2054-9369 PMC 7003341 PMID 32029004 doi:10.1186/s40779-020-0233-6 Carter, Michael J.; Fish, Matthew; Jennings, Aislinn; Doores, Katie J.; Wellman, Paul; Seow, Jeffrey; Acors, Sam; Graham, Carl; Timms, Emma. Peripheral immunophenotypes in children with multisystem inflammatory syndrome associated with SARS-CoV-2 infection . Nature Medicine. 2020-11, 26 (11): 1701–1707 [2020-08-19 ] . ISSN 1546-170X doi:10.1038/s41591-020-1054-6 存檔 於2021-11-15) (英語) . Di, Lin; Fu, Yusi; Sun, Yue; Li, Jie; Liu, Lu; Yao, Jiacheng; Wang, Guanbo; Wu, Yalei; Lao, Kaiqin. RNA sequencing by direct tagmentation of RNA/DNA hybrids . Proceedings of the National Academy of Sciences. 2020-02-11, 117 (6): 2886–2893 [2021-01-20 ] . ISSN 0027-8424 PMID 31988135 doi:10.1073/pnas.1919800117 存檔 於2021-01-23) (英語) . Broughton, James P.; Deng, Xianding; Yu, Guixia; Fasching, Clare L.; Servellita, Venice; Singh, Jasmeet; Miao, Xin; Streithorst, Jessica A.; Granados, Andrea. CRISPR–Cas12-based detection of SARS-CoV-2 . Nature Biotechnology. 2020-07, 38 (7): 870–874 [2020-04-21 ] . ISSN 1546-1696 doi:10.1038/s41587-020-0513-4 存檔 於2020-04-20) (英語) . Cascella, Marco. Features, Evaluation, and Treatment of Coronavirus (COVID-19). 2023.
Sungnak, Waradon; Huang, Ni; Bécavin, Christophe; Berg, Marijn; Queen, Rachel; Litvinukova, Monika; Talavera-López, Carlos; Maatz, Henrike; Reichart, Daniel. SARS-CoV-2 entry factors are highly expressed in nasal epithelial cells together with innate immune genes . Nature Medicine. 2020-05, 26 (5): 681–687 [2020-04-24 ] . ISSN 1546-170X doi:10.1038/s41591-020-0868-6 存檔 於2020-04-24) (英語) . Burrell, Louise M.; Risvanis, John; Kubota, Eiji; Dean, Rachael G.; MacDonald, Peter S.; Lu, Sai; Tikellis, Christos; Grant, Sharon L.; Lew, Rebecca A. Myocardial infarction increases ACE2 expression in rat and humans . European Heart Journal. 2005-02-01, 26 (4): 369–375 [2020-04-24 ] . ISSN 0195-668X doi:10.1093/eurheartj/ehi114 存檔 於2020-04-24) (英語) . Chen, Guang; Wu, Di; Guo, Wei; Cao, Yong; Huang, Da; Wang, Hongwu; Wang, Tao; Zhang, Xiaoyun; Chen, Huilong. Clinical and immunological features of severe and moderate coronavirus disease 2019 . The Journal of Clinical Investigation. 2020-05-01, 130 (5): 2620–2629 [2020-04-18 ] . ISSN 0021-9738 doi:10.1172/JCI137244 存檔 於2020-04-19) (英語) . Shi, Shaobo; Qin, Mu; Shen, Bo; Cai, Yuli; Liu, Tao; Yang, Fan; Gong, Wei; Liu, Xu; Liang, Jinjun; Zhao, Qinyan; Huang, He; Yang, Bo; Huang, Congxin. Association of Cardiac Injury With Mortality in Hospitalized Patients With COVID-19 in Wuhan, China . JAMA Cardiology. 2020-03-25 [2020-04-20 ] . doi:10.1001/jamacardio.2020.0950 存檔 於2020-04-20) (英語) . Klok, F. A.; Kruip, M. J. H. A.; van der Meer, N. J. M.; Arbous, M. S.; Gommers, D. A. M. P. J.; Kant, K. M.; Kaptein, F. H. J.; van Paassen, J.; Stals, M. A. M. Incidence of thrombotic complications in critically ill ICU patients with COVID-19 . Thrombosis Research. 2020-07-01, 191 : 145–147 [2021-01-20 ] . ISSN 0049-3848 doi:10.1016/j.thromres.2020.04.013 存檔 於2021-12-04) (英語) . Wang, Tao; Chen, Ruchong; Liu, Chunli; Liang, Wenhua; Guan, Weijie; Tang, Ruidi; Tang, Chunli; Zhang, Nuofu; Zhong, Nanshan. Attention should be paid to venous thromboembolism prophylaxis in the management of COVID-19 . The Lancet Haematology. 2020-05-01, 7 (5): e362–e363. ISSN 2352-3026 PMID 32278361 doi:10.1016/S2352-3026(20)30109-5 (英語) . 、Oxley, Thomas J.; Mocco, J.; Majidi, Shahram; Kellner, Christopher P.; Shoirah, Hazem; Singh, I. Paul; De Leacy, Reade A.; Shigematsu, Tomoyoshi; Ladner, Travis R. Large-Vessel Stroke as a Presenting Feature of Covid-19 in the Young . New England Journal of Medicine. 2020-05-14, 382 (20): e60 [2021-01-20 ] . ISSN 0028-4793 PMC 7207073 PMID 32343504 doi:10.1056/NEJMc2009787 存檔 於2021-12-16) (英語) . Li, Yanan; Li, Man; Wang, Mengdie; Zhou, Yifan; Chang, Jiang; Xian, Ying; Wang, David; Mao, Ling; Jin, Huijuan. Acute cerebrovascular disease following COVID-19: a single center, retrospective, observational study . Stroke and Vascular Neurology. 2020-09, 5 (3): 279–284. ISSN 2059-8688 PMC 7371480 PMID 32616524 doi:10.1136/svn-2020-000431 (英語) . Zhao, Bing; Ni, Chao; Gao, Ran; Wang, Yuyan; Yang, Li; Wei, Jinsong; Lv, Ting; Liang, Jianqing; Zhang, Qisheng. Recapitulation of SARS-CoV-2 infection and cholangiocyte damage with human liver ductal organoids . Protein & Cell. 2020-10-01, 11 (10): 771–775. ISSN 1674-8018 PMC 7164704 PMID 32303993 doi:10.1007/s13238-020-00718-6 (英語) . Wu, Di; Shu, Ting; Yang, Xiaobo; Song, Jian-Xin; Zhang, Mingliang; Yao, Chengye; Liu, Wen; Huang, Muhan; Yu, Yuan. Plasma metabolomic and lipidomic alterations associated with COVID-19 . National Science Review. 2020-07-01, 7 (7): 1157–1168 [2021-01-20 ] . ISSN 2095-5138 doi:10.1093/nsr/nwaa086 存檔 於2021-10-02) (英語) . Lamers, Mart M.; Beumer, Joep; van der Vaart, Jelte; Knoops, Kèvin; Puschhof, Jens; Breugem, Tim I.; Ravelli, Raimond B. G.; Paul van Schayck, J.; Mykytyn, Anna Z. SARS-CoV-2 productively infects human gut enterocytes . Science. 2020-07-03, 369 (6499): 50–54. ISSN 0036-8075 PMC 7199907 PMID 32358202 doi:10.1126/science.abc1669 (英語) . Diao, Bo; Wang, Chenhui; Wang, Rongshuai; Feng, Zeqing; Tan, Yingjun; Wang, Huiming; Wang, Changsong; Liu, Liang; Liu, Ying; Liu, Yueping; Wang, Gang; Yuan, Zilin; Ren, Liang; Wu, Yuzhang; Chen, Yongwen. Human Kidney is a Target for Novel Severe Acute Respiratory Syndrome Coronavirus 2 (SARS-CoV-2) Infection . medRxiv. 2020-04-10 [2020-05-18 ] . doi:10.1101/2020.03.04.20031120 存檔 於2020-05-20) (英語) . Moriguchi, Takeshi; Harii, Norikazu; Goto, Junko; Harada, Daiki; Sugawara, Hisanori; Takamino, Junichi; Ueno, Masateru; Sakata, Hiroki; Kondo, Kengo. A first case of meningitis/encephalitis associated with SARS-Coronavirus-2 . International Journal of Infectious Diseases. 2020-05, 94 : 55–58 [2021-01-20 ] . PMC 7195378 PMID 32251791 doi:10.1016/j.ijid.2020.03.062 存檔 於2021-12-25) (英語) . Deng, Wei; Bao, Linlin; Gao, Hong; Xiang, Zhiguang; Qu, Yajin; Song, Zhiqi; Gong, Shunran; Liu, Jiayi; Liu, Jiangning; Yu, Pin; Qi, Feifei; Xu, Yanfeng; Li, Fengli; Xiao, Chong; Lv, Qi; Xue, Jing; Wei, Qiang; Liu, Mingya; Wang, Guanpeng; Wang, Shunyi; Yu, Haisheng; Liu, Xing; Zhao, Wenjie; Han, Yunlin; Qin, Chuan. Ocular conjunctival inoculation of SARS-CoV-2 can cause mild COVID-19 in Rhesus macaques . bioRxiv. 2020-03-30 [2020-04-21 ] . doi:10.1101/2020.03.13.990036 存檔 於2020-04-22) (英語) . Montopoli, M.; Zumerle, S.; Vettor, R.; Rugge, M.; Zorzi, M.; Catapano, C. V.; Carbone, G. M.; Cavalli, A.; Pagano, F. Androgen-deprivation therapies for prostate cancer and risk of infection by SARS-CoV-2: a population-based study (N = 4532) . Annals of Oncology. 2020-08-01, 31 (8): 1040–1045. ISSN 0923-7534 PMID 32387456 doi:10.1016/j.annonc.2020.04.479 (英語) . Cheng, Xu; Liu, Ye-Mao; Li, Haomiao; Zhang, Xin; Lei, Fang; Qin, Juan-Juan; Chen, Ze; Deng, Ke-Qiong; Lin, Lijin. Metformin Is Associated with Higher Incidence of Acidosis, but Not Mortality, in Individuals with COVID-19 and Pre-existing Type 2 Diabetes . Cell Metabolism. 2020-10-06, 32 (4): 537–547.e3. ISSN 1550-4131 PMID 32861268 doi:10.1016/j.cmet.2020.08.013 (英語) . Richardson, Safiya; Hirsch, Jamie S.; Narasimhan, Mangala; Crawford, James M.; McGinn, Thomas; Davidson, Karina W.; and the Northwell COVID-19 Research Consortium; Barnaby, Douglas P.; Becker, Lance B. Presenting Characteristics, Comorbidities, and Outcomes Among 5700 Patients Hospitalized With COVID-19 in the New York City Area . JAMA. 2020-05-26, 323 (20): 2052 [2020-04-24 ] . ISSN 0098-7484 PMC 7177629 PMID 32320003 doi:10.1001/jama.2020.6775 存檔 於2020-04-24) (英語) . Diaz, Raiko; Heller, Daniel. Barotrauma And Mechanical Ventilation. StatPearls . Treasure Island (FL): StatPearls Publishing. 2020 [2021-01-20 ] . PMID 31424810 存檔 於2021-03-08). Briel, Matthias; Meade, Maureen; Mercat, Alain; Brower, Roy G.; Talmor, Daniel; Walter, Stephen D.; Slutsky, Arthur S.; Pullenayegum, Eleanor; Zhou, Qi. Higher vs Lower Positive End-Expiratory Pressure in Patients With Acute Lung Injury and Acute Respiratory Distress Syndrome: Systematic Review and Meta-analysis . JAMA. 2010-03-03, 303 (9): 865 [2021-12-29 ] . ISSN 0098-7484 doi:10.1001/jama.2010.218 存檔 於2021-11-13) (英語) . Borba, Mayla Gabriela Silva; Val, Fernando Fonseca Almeida; Sampaio, Vanderson Souza; Alexandre, Marcia Almeida Araújo; Melo, Gisely Cardoso; Brito, Marcelo; Mourão, Maria Paula Gomes; Brito-Sousa, José Diego; Baía-da-Silva, Djane. Effect of High vs Low Doses of Chloroquine Diphosphate as Adjunctive Therapy for Patients Hospitalized With Severe Acute Respiratory Syndrome Coronavirus 2 (SARS-CoV-2) Infection: A Randomized Clinical Trial . JAMA Network Open. 2020-04-24, 3 (4): e208857 [2021-01-20 ] . ISSN 2574-3805 doi:10.1001/jamanetworkopen.2020.8857 存檔 於2021-12-20) (英語) . Sheahan, Timothy P.; Sims, Amy C.; Graham, Rachel L.; Menachery, Vineet D.; Gralinski, Lisa E.; Case, James B.; Leist, Sarah R.; Pyrc, Krzysztof; Feng, Joy Y. Broad-spectrum antiviral GS-5734 inhibits both epidemic and zoonotic coronaviruses . Science Translational Medicine. 2017-06-28, 9 (396) [2020-01-29 ] . ISSN 1946-6234 PMID 28659436 doi:10.1126/scitranslmed.aal3653 存檔 於2021-08-16) (英語) . Sheahan, Timothy P.; Sims, Amy C.; Leist, Sarah R.; Schäfer, Alexandra; Won, John; Brown, Ariane J.; Montgomery, Stephanie A.; Hogg, Alison; Babusis, Darius. Comparative therapeutic efficacy of remdesivir and combination lopinavir, ritonavir, and interferon beta against MERS-CoV . Nature Communications. 2020-01-10, 11 (1): 222 [2020-01-29 ] . ISSN 2041-1723 doi:10.1038/s41467-019-13940-6 存檔 於2020-01-20) (英語) . Holshue, Michelle L.; DeBolt, Chas; Lindquist, Scott; Lofy, Kathy H.; Wiesman, John; Bruce, Hollianne; Spitters, Christopher; Ericson, Keith; Wilkerson, Sara. First Case of 2019 Novel Coronavirus in the United States . New England Journal of Medicine. 2020-03-05, 382 (10): 929–936. ISSN 0028-4793 PMC 7092802 PMID 32004427 doi:10.1056/NEJMoa2001191 Wang, Manli; Cao, Ruiyuan; Zhang, Leike; Yang, Xinglou; Liu, Jia; Xu, Mingyue; Shi, Zhengli; Hu, Zhihong; Zhong, Wu. Remdesivir and chloroquine effectively inhibit the recently emerged novel coronavirus (2019-nCoV) in vitro . Cell Research. 2020-03, 30 (3): 269–271 [2020-04-27 ] . ISSN 1748-7838 doi:10.1038/s41422-020-0282-0 存檔 於2020-02-05) (英語) . Rosenberg, Eli S.; Dufort, Elizabeth M.; Udo, Tomoko; Wilberschied, Larissa A.; Kumar, Jessica; Tesoriero, James; Weinberg, Patti; Kirkwood, James; Muse, Alison. Association of Treatment With Hydroxychloroquine or Azithromycin With In-Hospital Mortality in Patients With COVID-19 in New York State . JAMA. 2020-06-23, 323 (24): 2493 [2020-05-14 ] . ISSN 0098-7484 PMC 7215635 PMID 32392282 doi:10.1001/jama.2020.8630 存檔 於2020-05-14) (英語) . Khan, Suliman; Siddique, Rabeea; Shereen, Muhammad Adnan; Ali, Ashaq; Liu, Jianbo; Bai, Qian; Bashir, Nadia; Xue, Mengzhou. Kraft, Colleen Suzanne , 編. Emergence of a Novel Coronavirus, Severe Acute Respiratory Syndrome Coronavirus 2: Biology and Therapeutic Options . Journal of Clinical Microbiology. 2020-03-11, 58 (5): e00187–20, /jcm/58/5/JCM.00187–20.atom [2020-05-05 ] . ISSN 0095-1137 PMC 7180238 PMID 32161092 doi:10.1128/JCM.00187-20 存檔 於2020-05-04) (英語) . Barton, Christopher; Kouokam, J. Calvin; Lasnik, Amanda B.; Foreman, Oded; Cambon, Alexander; Brock, Guy; Montefiori, David C.; Vojdani, Fakhrieh; McCormick, Alison A. Activity of and Effect of Subcutaneous Treatment with the Broad-Spectrum Antiviral Lectin Griffithsin in Two Laboratory Rodent Models . Antimicrobial Agents and Chemotherapy. 2014-01-01, 58 (1): 120–127 [2020-05-05 ] . ISSN 0066-4804 PMID 24145548 doi:10.1128/AAC.01407-13 存檔 於2021-05-08) (英語) . Pervushin, Konstantin; Tan, Edward; Parthasarathy, Krupakar; Lin, Xin; Jiang, Feng Li; Yu, Dejie; Vararattanavech, Ardcharaporn; Soong, Tuck Wah; Liu, Ding Xiang. Baric, Ralph S. , 編. Structure and Inhibition of the SARS Coronavirus Envelope Protein Ion Channel . PLoS Pathogens. 2009-07-10, 5 (7): e1000511. ISSN 1553-7374 PMC 2702000 PMID 19593379 doi:10.1371/journal.ppat.1000511 (英語) . Lai, Jianbo; Ma, Simeng; Wang, Ying; Cai, Zhongxiang; Hu, Jianbo; Wei, Ning; Wu, Jiang; Du, Hui; Chen, Tingting. Factors Associated With Mental Health Outcomes Among Health Care Workers Exposed to Coronavirus Disease 2019 . JAMA Network Open. 2020-03-23, 3 (3): e203976 [2020-04-21 ] . ISSN 2574-3805 PMC 7090843 PMID 32202646 doi:10.1001/jamanetworkopen.2020.3976 存檔 於2020-04-21) (英語) . Rothe, Camilla; Schunk, Mirjam; Sothmann, Peter; Bretzel, Gisela; Froeschl, Guenter; Wallrauch, Claudia; Zimmer, Thorbjörn; Thiel, Verena; Janke, Christian. Transmission of 2019-nCoV Infection from an Asymptomatic Contact in Germany . New England Journal of Medicine. 2020-03-05, 382 (10): 970–971 [2021-01-20 ] . ISSN 0028-4793 PMC 7120970 PMID 32003551 doi:10.1056/NEJMc2001468 存檔 於2020-06-13). Calisher, Charles; Carroll, Dennis; Colwell, Rita; Corley, Ronald B.; Daszak, Peter; Drosten, Christian; Enjuanes, Luis; Farrar, Jeremy; Field, Hume. Statement in support of the scientists, public health professionals, and medical professionals of China combatting COVID-19 . The Lancet. 2020-03-07, 395 (10226): e42–e43. ISSN 0140-6736 PMID 32087122 doi:10.1016/S0140-6736(20)30418-9 (英語) .