Loading AI tools
canlılarda hastalıklara karşı koruma sağlayan biyolojik savunma sistemi bütünü Vikipedi'den, özgür ansiklopediden
Bağışıklık sistemi, bir canlıdaki hastalıklara karşı koruma yapan, patojenleri ve tümör hücrelerini tanıyıp onları yok eden işleyişlerin toplamıdır. Sistem, canlı vücudunda geniş bir çeşitlilikte, virüslerden parazitik solucanlara, vücuda giren veya vücutla temasta bulunan her yabancı maddeye kadar tarama yapar ve onları, canlının sağlıklı vücut hücrelerinden ve dokularından ayırt eder. Bağışıklık sistemi, çok benzer özellikteki maddeleri bile birbirinden ayırabilir, örneğin; bir amino asidi farklı olan proteinleri bile birbirinden ayırabilecek özelliğe sahiptir. Bu ayrım, patojenlerin konak canlıdaki savunma sistemine rağmen enfeksiyon yapmaları için yeni yollar bulmalarına, bazı uyumlar sağlamalarına neden olacak kadar karmaşıktır. Bu mücadelede hayatta kalmak için patojenleri tanıyan ve onları etkisizleştiren bazı mekanizmalar gelişmiştir. Doğadaki tüm canlılar kendilerinden olmayan doku, hücre ve moleküllere karşı savunma sistemlerine sahiptirler. Hatta bakteriler gibi basit tek hücreli canlılarda da onları viral enfeksiyonlara karşı koruyan enzim sistemleri bulunur. Yüksek canlılardaysa çok daha karmaşık bir bağışıklık sistemi vardır. Omurgalılarda bağışıklık sistemi özel işlevlere sahip çok sayıda farklı hücre ve molekül içermektedir.
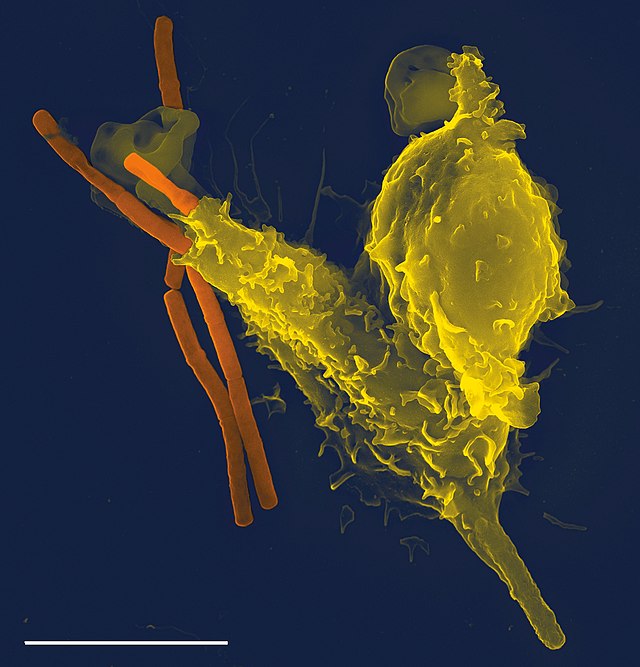
Geçmiş çağlardaki ökaryotik canlılarda diğer basit bağışıklık mekanizmaları gelişmiş ve günümüzdeki bitkiler, balıklar, sürüngenler ve böcekler gibi torunlarına miras kalmıştır. Bu mekanizmalar, defensinler olarak adlandırılan antimikrobiyal peptidleri, fagositleri ve kompleman sistemi kapsar. Daha tecrübeli sistemler omurgalıların evrimiyle, nispeten yakın zamanda gelişmiştir.[1] İnsan gibi omurgalılardaki bağışıklık sistemleri dinamik işleyiş sırasında birbirlerini etkileyen, seçilmiş proteinlerin, hücrelerin, organların ve dokuların bazı çeşitlerinden oluşur. Daha karmaşık bağışıklık yanıtının bir parçası olan omurgalıların sistemi, zamanla patojenleri daha etkili tanımaya uyum sağlamıştır. Uyum süreci bağışıklık belleğini yaratmış ve bu da patojenlerle gelecek karşılaşmalarda daha etkili bir koruma sağlamaya izin vermiştir. Edinilmiş bağışıklığın bu süreci aşılamanın temelini oluşturmaktadır.
Bağışıklık sistemindeki bozukluklar hastalıklara neden olabilir. Bağışıklık yetmezliği hastalıkları, bağışıklık sistemi normalden daha az etkin olduğunda meydana gelir, tekrarlayan ve yaşamı tehdit eden enfeksiyonlarla sonuçlanır. Bağışıklık yetmezliği ayrıca X-SCID gibi genetik hastalıkların bir sonucu ya da farmosötikler veya HIV retrovirüsünün neden olduğu AIDS gibi bir enfeksiyonun sonucu olarak da görülebilir. Buna zıt olarak, kendinebağışık (otoimmün) hastalıklar, normalden fazla etkin olan bir bağışıklık sisteminin, vücudun kendi dokularını yabancı olarak algılayıp, onlara saldırmasıyla sonuçlanır. Yaygın kendine bağışık hastalıklar; romatoid artrit, diyabet tip 1 ve sistemik lupus eritematozus'dur.
Bağışıklık sistemi, eski çağlardan bu yana ilgi çeken bir konu olmuş, insanlar tarih boyunca bazı bağışıklık yöntemleri bile geliştirilmiştir.
Günümüzde bağışıklık sisteminin çok geniş ölçüde aydınlatılabildiği söylenebilir, bu sistemi oluşturan unsurlardan, hastalıkların tanı ve tedavisinde geniş ölçüde yararlanılmaktadır. Günümüzde "bağışıklık bilimi" olarak bilinen "immünoloji", Eski Roma'da askerlikten muaf (korunmuş) asillere denilen immunitas sözcüğünden gelmektedir. İmmünoloji günümüzdeki rolüyle bilimsel çalışmalarının oldukça önemli alanlarını oluşturmaktadır.
Bağışıklık sisteminin organları lenfoid dokulu organlardır. Bu organlar, birincil lenfoid organlar ve ikincil lenfoid organlar olarak iki grup halinde incelenseler de birbirleriyle sürekli ilişki halindedirler. Birincil lenfoid organlarda, lenfositlerin üretim işleri yapılırken; ikincil organlarda lenfositler ilk defa antijenlerle yüzleşirler.

Canlı vücudu oldukça farklı moleküllerden, hücrelerden ve dokulardan oluşan birçok savunma sistemi tarafından korunmaktadır. Canlıların bağışıklık sistemlerini uyaran ve canlı için kendinden-olmayan tüm moleküllere "antijen" veya "immunojen" denir. Canlı koruyucu elemanlarıyla öncelikle yapısına yabancı olan "antijen"lerin vücuda girmesini engeller. Bu koruma, tabaka tabaka arttırılmış bir sistemdir, üyeleri; yüzey engelleri, doğuştan gelen ve edinilmiş bağışıklık sistemidir. İlk engel olan deri, solunum ve sindirim sistemi gibi yüzey bariyerlerini herhangi bir antijen aşabilir ve canlıyla dahil olursa, ikinci savunma sistemi hemen harekete geçer.
Yüzey bariyerlerini aşan bir madde karşısında, doğuştan gelen sistemin elemanlarından kemik iliği, timus, lenf bezleri ve dalak gibi özelleşmiş merkezlerde yer alan fagositler, makrofajlar, lenfositler gibi savunma hücreleri ve molekülleri devreye girerler. İlk aşamada, öncü hücreler olan fagositler ve makrofajlar antijenleri yok etmeye çalışırlar. Kendinden-olmayan yapıların vücut tarafından bu şekilde yok edilmeleri sürekli devam eden bir olaydır, vücudun açıklıklarından girebilen birçok molekül bu şekilde yok edilir.[2]
Bu ikinci koruma sistemi de başarılı olamazsa, edinilmiş bağışıklık sisteminin temel hücreleri olan B ve T lenfositler devreye girerler. Böylece oldukça karmaşık olan bir zincir sistemi tetiklenir. Antijen varlığını haber alan T hücreleri, diğer savunma hücrelerini bunlara bağlı gelişen birçok biyokimyasal kaskadı tetiklerler.[3]
T hücrelerinin alt gruplarından öldürücü T hücreleri antijenleri yok etmeye çalışırken, edinilmiş sistemin bir diğer önemli hücreleri olan B hücreleri de "bağışıklığın akıllı molekülleri" olarak adlandırılan "antikor"ları (immünoglobulinler) sentezlemeye başlarlar. Glikoprotein yapılı bu moleküller, anahtar-kilit uyumu şeklinde özgül antijenlere bağlanarak antijenleri ya etkisiz hale getirirler ya da kompleman sistemi ve diğer savunma hücrelerini harekete geçirerek antijenlerin yok edilmelerini sağlarlar.
Savunma sisteminde çok önemli bir rolü olan antikorlar, Y şeklindedir ve ağır zincir ve hafif zincir olmak üzere 2 çift protein zincirinden yapılmışlardır. Ağır ve hafif zincirler üzerinde, değişken (V/variable) ve sabit (C/constant) bölgeler bulunur. Değişken bölge, antijeni tanıyan kısmı oluşturmak üzere özelleşmiştir ve bir çift halinde bulunur. Buradaki aminoasit dizilimlerindeki farklılıklar, farklı antijen bağlanmasına yol açar.[4]
Antikor molekülünde ağır ve hafif zincirler, farklı DNA bölümlerinden meydana gelmiş genler tarafından kodlanır. Bu gen parçaları, her B hücresinde farklı olan zincirleri meydana getirecek genleri yapmak üzere, yeniden düzenlenir. Gen parçalarının düzenlenmesi değişkendir ve bu nedenle vücudun yapabildiği 100 milyon kadar farklı antikor, az sayıda gen parçası tarafından oluşturulur. Yani bağışıklık sisteminin başarısının temeli, immünoglobulinin ağır ve hafif zincirlerindeki değişken bölgelerin, çok çeşitli sayıda üretilebilmesidir. Bu çeşitliliğin üretimi, çoğul genlerin varlığı, (vücut hücrelerini içeren) somatik hipermutasyonlar, somatik rekombinasyonlarla (kromozomlar arası gen değiş-tokuşuyla) sağlanır ki tüm bu olaylar B hücre gelişimi sırasında ortaya konur. Böylece B hücreleri, vücuda giren antijenleri durduracak antikorları, antijenik özelliklerine göre ayrı ayrı sentezler.[5]
Bağışıklık sistemi, gittikçe artarak özelleşen katmanlı savunmalarla canlıları enfeksiyonlardan korur. En basitiyle; fiziksel engeller bakteri veya virüs gibi patojenlerin vücuda girmelerini engeller. Eğer bir patojen bu engellerden birini aşarsa, doğuştan gelen bağışıklık sistemi hemen devreye girer fakat özgül bir yanıt oluşturmaz. Doğuştan gelen bağışıklık sistemi bütün bitki ve hayvan gruplarında bulunur.[6] Bununla beraber, patojenler doğuştan gelen yanıttan kaçabilirler. Omurgalılarda üçüncü bir koruma engeli olarak doğuştan gelen yanıtla etkinleştirilen edinilmiş bağışıklık sistemi gelişmiştir. Burada bağışıklık sistemi, bir enfeksiyon sırasında patojeni tanımasını geliştirecek cevaplara uyum sağlar. Bu gelişmiş yanıt, patojen ortadan kaldırıldıktan sonra da bir bağışıklık belleği şeklinde hatırlanır ve bu, aynı patojenle bir daha karşılaşıldığında daha hızlı ve güçlü bir yanıt verilmesini sağlar.[7]
Bağışıklık sistemi genelde iki bölüm halinde incelenir:
| Doğuştan gelen bağışıklık sistemi | Edinilmiş bağışıklık sistemi |
|---|---|
| Yanıt özgül değil | Patojen ve antijene özgül yanıt verilir |
| Bulunana hızlıca en büyük düzeyde yanıt verilir | bulunmayla yanıt arasında gecikme vardır |
| Hücre aracılı ve humoral bileşenler | Hücre aracılı ve humoral bileşenler |
| Bağışıklık belleği bulunmaz | Bağışıklık belleği oluşturulur |
| Neredeyse yaşamdaki bütün canlı şekillerinde bulunur | Sadece Gerçekçenelilerde bulunur |
Doğuştan ve edinilmiş bağışıklıkların her ikisi de kendinden olan ve kendinden olmayan moleküllerin ayrımına bağımlıdır. İmmünolojide kendinden olan moleküller, bir canlının vücudunda bulunan ve bağışıklık sistemince yabancı moleküllerden ayrılabilen bileşenlerdir.[8] Kendinden olmayanlar ise yabancı moleküller olarak tanımlanabilir. Kendinden olmayan moleküllerin bir sınıfı antijenler olarak bilinir ve özgül bağışıklık almaçlarına bağlanıp bir bağışıklık yanıtının oluşmasına neden olan maddeler olarak tanımlanabilirler.[9]
Mekanik, kimyasal ve biyolojik engeller gibi bazı bariyerler canlıları enfeksiyonlardan korur. Bitkilerin mumlu yaprakları, böceklerin dış iskeletleri, yumurtaların koruyucusu yumurta kabukları ve deri, enfeksiyon karşısında ilk hatta bulunan mekanik engellerin örnekleridir.[9] Bununla birlikte canlılar etraflarındaki çevreye karşı tamamen korunamazlar; canlılar diğer sistemlerini ve vücudun akciğerler, bağırsak ve idrar deliği gibi açıklıklarını korumak zorundadırlar.

Akciğerlerde öksürük ve hapşırma, solunum yollarını tehdit oluşturan patojenlerin ve diğer maddelerin dışarı atılmasını sağlayan mekanik korumalardandır. Gözyaşıyla yıkama, idrar, solunum ve sindirim yolundaki mukus salgıları da mikroorganizmaları mekanik olarak dışarı atma yollarındandır.[10]
Kimyasal engeller de enfeksiyona karşı koruma yaparlar. Deri ve solunum alanı, ß-defensinler olarak bilinen antimikrobiyal peptidleri salgılar.[11] Tükürükteki lizozim, fosfolipaz A2 gibi enzimler, gözyaşı ve göğüs sütü de antibakteriyal vücut salgılarındadır.[12][13] Vajinal salgılar hafif asidik özellikteyken; meni patojenleri öldürmek üzere çinko ve defensinleri içermektedir.[14][15] Midede gastrik asit ve proteaz salgıları, yutulmuş patojenlere karşı oldukça güçlü koruma yapan kimyasallardandır.
Bağırsaklarda ve gastrointestinal alanlarda bulunan kommensal flora da, ortama yerleşmek isteyen patojenik bakterilerle mücadeleye girerek, bazı hallerde ortamın pH ve ulaşılabilir demir miktarı gibi şartlarını değiştirerek biyolojik bir engel olarak görev görür.[16] Bu, patojenlerin hastalığa neden olacak kadar yeterli sayıya ulaşma ihtimalini azaltır. Bununla beraber antibiyotiklerin çoğu bakterilere özgül olarak hedeflenmezler, bu yüzden kullanıldıklarında bu florayı yok edebilirler, ayrıca mantarlara karşı da işlev görmezler bu yüzden bakterileri florasının azalmasıyla vajina gibi bazı bölgelerde mantarların çoğalmasına yol açabilirler.[17] Burada, normalde yoğurtta bulunan Lactobacillus gibi canlılardaki probiyotik floranın tekrar gündeme gelmesinin iyi bir kanıtı bulunmaktadır; bu flora çocukların intestinal enfeksiyonlarındaki mikrobiyal populasyonların sağlıklı bir şekilde dengelenmesine yardımcı olur ve bakteriyal gastroenteritis, enflamasyonlu bağırsak hastalığı, idrar yolu hastalıkları ve ameliyat-sonrası enfeksiyonlar için yapılan çalışmalarda öncü olan verilerdendir.[18][19][20]
Bir canlıya başarıyla girebilen mikroorganizmalar doğuştan gelen bağışıklık sisteminin mekanizmaları ve hücreleriyle karşılaşırlar. Doğuştan olan yanıt genellikle mikroorganizmaların geniş gruplarında saklı olan bileşenleri tanıyan örnek tanıma reseptörlerince mikroplar tanımlandıklarında tetiklenir.[21] Doğuştan gelen bağışıklık sistemi özgül değildir; yani bu sistem patojenleri soysal olarak tanır ve yanıtlar.[9] Sistem, bir patojen karşısında uzun süreli bağışıklık kazandırmaz. Doğuştan gelen bağışıklık sistemi, çoğu canlıda konağın korunmasında baskın olan sistemdir.[6]

Yangı, bağışıklık sisteminde enfeksiyona karşı gösterilen ilk tepkilerden birisidir.[22] Enflamasyonun belirtileri, dokudaki kan artışı sonucu olan kızarıklık ve şişmedir. Yangı, yaralanmış ya da enfekte olmuş hücrelerce salınan eikosanoidler ve sitokinlerce oluşturulur. Eikosanoidler, ateşi üreten, yangıyla ilişkili olarak kan damarlarının genişlemesine neden olan prostaglandinleri ve beyaz kan hücreleri lökositleri çeken lökotrienleri kapsar.[23][24] Yaygın sitokinler; beyaz kan hücreleri arasında iletişimden sorumlu olan interlökinleri, kemotaksiyi ilerleten kemokinleri ve konak hücrede protein sentezini kapatmak gibi anti-viral etkileri olan interferonları kapsar.[25] Büyüme faktörleri ve sitotoksik faktörler de ayrıca salınabilir. Bu sitokinler ve diğer kimyasallar bağışıklık hücrelerini enfeksiyon alanına toplar ve patojenlerden kurtulma sonrasında hasarlı dokunun iyileşmesini ilerletirler.[26]
Kompleman sistemi, yabancı hücrelerin yüzeylerine saldıran bir biyokimyasal kaskaddır. 20 farklı protein içerir ve patojenleri antikorlarla öldürmesini "tamamlayıcı" (komplemanter) yeteneğinden dolayı bu şekilde isimlendirilmiştir. Tamamlayıcı sistem, doğuştan gelen bağışıklık yanıtının ana humoral bileşenidir.[27][28] Bitkiler, balıklar ve bazı omurgasızlar gibi memeli olmayan bazı türler de kompleman sistemleri bulundururlar.[29] Bu yanıt insanlarda, bu mikroplara ilişmiş antikorların tamamlanıp bağlamasıyla veya kompleman proteinlerinin mikropların yüzeylerindeki karbonhidratlara bağlanmasıyla etkinleştirilir. Bu tanıma sinyali bir hızlı öldürme yanıtını tetikler.[30] Bu yanıtın hızı, ayrıca proteazlar olan kompleman moleküllerinin bir dizi proteolitik etkinleşmesini izleyen sinyal büyümesinin bir sonucudur. Kompleman proteinlerinin ilk olarak mikroba bağlanmalarından sonra, sırayla diğer proteazları tamamlayan ve devam eden proteaz aktivitelerini etkinleştirirler. Bu üretim pozitif geribeslemeyle kontrol edilen ilk sinyali yükselten katalitik bir kaskaddır.[31] Kaskad bağışıklık hücrelerini çeken peptidlerin üretimiyle sonuçlanır, damarsal geçirgenliği arttırır ve patojenlerin yüzeylerini kaplayarak (opsonizasyon) onları yıkım için işaretler. Komplemanın kalıntıları ayrıca hücre zarlarını yırtmak suretiyle hücreleri de doğrudan öldürebilir.[27]

Lökositler (beyaz kan hücreleri) tek hücreli canlılar gibi bağımsız davranabilirler ve doğuştan gelen bağışıklık sisteminin ikinci kollarıdırlar.[9] Doğuştan gelen lökositler; fagositleri, makrofajları, nötrofilleri, dendritik hücreleri, mast hücrelerini, eozinofilleri, bazofilleri ve doğal öldürücü hücreleri kapsar. Bu hücreler bütün patojenleri hatta büyük patojenleri bile tanımlar, yutarak ya da temasa geçerek onları öldürürler.[29] Doğuştan gelen hücreler ayrıca edinilmiş bağışıklık sistemini etkinleştiren aracı moleküller olarak da önemlidirler.[7]
Fagositler doğuştan gelen hücresel bağışıklığın önemli biçimleridir; patojenleri veya parçacıkları yutmalarından (fagosite etmelerinden) ya da yemelerinden dolayı böyle isimlendirilmişlerdir. Fagositler genellikle patojenleri arayarak vücutta dolaşırlar ve özelleşmiş bölgelere sitokinler tarafından çağırılabilinirler.[9] Bir patojen bir fagosit tarafından yutulduğunda, hücre içinde bir kümeye konur ve bu küme fagozom olarak isimlendirilir, fagozom sonradan hücre içinde bulunan lizozom denilen bazı kümelerle birleşir ve "fagolizozom" olarak isimlendirilir. Patojen, fagolizozom içinde sindirim enzimlerinin etkinliğiyle ya da solunumsal (oksidatif) tepkimeyi izleyen serbest radikallerin fagolizozom içine bırakılmasıyla öldürülür.[32][33] Fagositler gerekli besinlerini bu şekilde almak için evrilmişlerdir fakat bu rolleri fagositlere patojenleri bir savunma mekanizması şeklinde yutmalarını da sağlamıştır.[34] Fagositler ev sahibi savunmasındaki muhtemelen en eski şekilleri teşkil ederler ve omurgasızların ve omurgalıların her ikisinde de bulunurlar.[35]
Nötrofiller ve makrofajlar da vücutta saldırgan patojenleri takip eden fagositlerdir.[36]
Nötrofiller normalde dolaşım sisteminde bulunurlar ve fagositlerin en çok bulunan tipleridir; toplam kanda dolaşan lökositlerin %50-60'ını oluştururlar.[37] Kısmen bakteriyal enfeksiyonun sonucu olan yangının akut fazlarında, nötrofiller yangının olduğu bölgeye doğru kemotaksi olarak bilinen süreçle göç ederler ve genellikle enfeksiyon bölgesine ilk ulaşan hücrelerdir.
Makrofajlar ise, dokularda bulunan ve çok yönlü hücrelerdir, enzimler, kompleman proteinleri ve interlökin 1 gibi düzenleyici faktörleri kapsayan kimyasalların geniş çeşitliliğini üretirler.[38] Makrofajlar ayrıca çöpçüler gibi de davranıp, etkin edinilmiş bağışıklık sisteminin antijen sunan hücrelerinin atıklarını veya vücudun parçalanmış hücreleri gibi döküntülerini de temizlerler.[7]
Dendritik hücreler, dış çevreyle ilişkide bulunan dokularda bulunan fagositlerdir; bu yüzden ana olarak deride ("Langerhans hücreleri" olarak isimlendirilirler), burunda, akciğerlerde, midede ve bağırsaklarda bulunurlar.[39] Sinir hücreleri nöronların dendritlerine benzemelerinden dolayı böyle isimlendirilmiş olsalar da, sinir sistemiyle ilgileri yoktur. Dendritik hücreler antijen sunumu sürecinde doğuştan gelen ile edinilmiş bağışıklık sisteminde arasında T hücrelerine antijen sunmaları gibi bir rolle bağlantı oluşturduklarından edinilmiş bağışıklık sisteminin anahtarlarından biridirler.[39]
Mast hücreleri, bağ dokuda ve muköz membranlarda yerleşik olarak bulunurlar ve yangı yanıtını düzenlerler.[40] Mast hücreleri, patojenlere karşı savunmayla ve sıcaklıkla yakından alakalı, fakat daha çok alerji ve anafilaksi ile ilişkilendirilen doğuştan gelen bağışıklık sistemi hücrelerinin bir çeşididir.[37]
Bazofiller ve Eozinofiller nötrofillerle bağlantılı hücrelerdir. Bir patojence etkinleştirildiklerinde, parazitlere karşı savunmada ve (astım gibi) alerjik reaksiyonlarda önemli rolü olan histamini salarlar.[41] Bu yüzden herhangi bir doku harabiyetinin önlenmesiyle oldukça ilişkilidirler.[37]
Doğal öldürücü hücreler (NK ya da DÖH hücreler), tümör hücreleri veya virüslerce enfekte edilmiş hücrelere saldırıp onları yokeden lökositlerdir.[42] İsimleri olan 'doğal öldürücü', etkinleştirilmeye ihtiyaç duymadan "kendini-kaybetmiş" hücreleri öldürdüklerinden verilmiştir.
Edinilmiş bağışıklık sistemi, ilkel omurgasızlarda evrimleşmiş ve bağışıklık belleği gibi daha güçlü bir yanıtın verilmesine olanak sağlayan, her patojenin antijen imzasıyla hatırlandığı bir bağışıklık sistemidir.[43] Edinilmiş bağışıklık yanıtı antijene özgüdür ve kendinden-olmayan antijenleri, "antijen sunumu" diye bilinen süreçte tanımayı gerektirir. Antijen özgüllüğü, özgül patojenler veya patojen-enfeksiyonlu hücrelere uydurulmuş yanıtların doğuşuna izin verir. Bu uygun yanıtların vücutta uygun şekilde kalması ise bellek hücreleriyle sağlanır. Eğer bir patojen vücuda tekrar girerse, bu bellek hücreleri sayesinde daha hızlı ve güçlü bir cevap alarak yok edilir.
Edinilmiş bağışıklık sisteminin hücreleri lökositlerin özel tipleri lenfositler olarak isimlendirilir. Periferik kanda lenfositlerin %20-50'sini dolaşır, kalanı lenfatik sistemle hareket eder.[9]

B ve T hücreleri lenfositlerin kemik iliğindeki hematopoietik kök hücrelerinden köken alan iki temel tipidir.[29] B hücreleri humoral bağışıklık yanıtını oluştururken, T hücreleri hücresel bağışıklığı oluştururlar. B ve T hücrelerinin her ikisi de özgül hedefleri tanıyan reseptör molekülleri taşırlar. "MHC" olarak bilinen 'kendinden olan' reseptör kombinasyonlarıyla antijenler işlenip, sunulduktan sonra T hücreleri, patojenler gibi kendinden-olmayan hedefleri tanırlar.
T lenfositler kanda dolaşan bütün lenfositlerin % 80'ini oluştururlar. T lenfositlerin iki ana alt tipi bulunmaktadır: yardımcı ve öldürücü T lenfositler. Öldürücü T lenfositler sadece MHC sınıf I ile eşlenmiş molekülleri tanırken, yardımcı T lenfositler MHC sınıf II ile ilişkili molekülleri tanır. Antijen sunumunun bu iki mekanizması T hücrelerinin iki tipinin farklı rollerde olmasıyla sonuç verir. Üçüncü bir alt grup olan γδ T hücreleri ise MHC reseptörlerine bağlı olmayan tam antijenleri tanır.[44] Zıt olarak, B hücresinin antijene özgü reseptörü, B hücresi yüzeyinde bulunan bir antikor molekülüdür ve antijen işlemesine gerek duymadan bütün patojenleri tanır. B hücrelerinin her soyu farklı bir antikoru ifade eder, bu yüzden B hücresi antijen reseptörünün tüm takımları vücudun üretebildiği bütün antikorları sunarlar.[29]
Öldürücü T hücreleri virüslerle veya diğer patojenlerle enfekte olmuş ya da işlev göremeyen veya hasarlanmış hücreleri öldüren T hücrelerinin alt gruplarından biridir.[45] B hücreleri gibi T hücrelerinin her tipi de farklı antijenleri tanır. Öldürücü T hücreleri, kendi T reseptörlerini (TCRler), özgül antijenlerini başka bir hücrenin MHC sınıf I reseptörüne bağlayarak bir kompleks oluşturduğunda etkinleşirirler. Bu MHC'nin antijen kompleksini tanımasına, T hücresindeki "CD8" diye adlandırılan yardımcı bir ko-reseptörle yardım edilir. Sonrasında T hücresi bu antijeni taşıyan MHC I reseptörlerini aramak için vücutta dolaşır. T hücresi böyle hücrelerle iletişime geçip etkinleştiğinde, perforin gibi hedef hücrenin hücre zarı porlarından iyonların, suyun ve toksinlerin geçmesine izin veren sitotoksinleri salar. Bir proteaz olan granülizin de hücreyi apoptozise götüren başka bir toksindir.[46] Konağın T hücrelerinin öldürme özelliği, virüslerin replikasyonunun önlenmesinde kısmen önemlidir. T hücresi etkinleştirilmesi sıkıca kontrol altında tutulur ve genellikle çok güçlü MHC/antijen aktivasyon sinyalini gerektirir ya da ek sinyaller yardımcı T hücreleri ile sağlanır.[46]
Yardımcı T hücreleri doğuştan ve edinilmiş bağışıklık yanıtlarını düzenler ve belirli bir patojene vücudun bağışıklık yanıtı tiplerinden hangisinin verileceğine karar verirler.[47][48] Bu hücrelerin öldürücü (sitotoksik) işlevselliği yoktur, enfekte hücreleri öldürmezler veya patojenleri doğrudan temizlemezler. Bunun yerine bu hizmetlerdeki diğer hücreleri yönlendirerek bağışıklık yanıtını kontrol ederler. Yardımcı T hücreleri, MHC sınıf II moleküllerine bağlanan antijenleri tanıyan T hücresi reseptörlerini ifade ederler. MHC-antijen kompleksi ayrıca, T hücresinin etkinleştirilmesinden sorumlu olan (Lck gibi) molekülleri T hücresinin içinde toplayan, yardımcı T hücresinin CD4 yardımcı reseptörü tarafından tanınır. Yardımcı T hücrelerini MHC-antijen kompleksleriyle, öldürücü T hücreleri için toplananlardan daha zayıf ilişkidedirler, yani öldürücü T hücreleri tekli bir MHC-antijen molekülüyle ilişkilenip etkinleştirilebilirlerken, T hücresi üzerinde bulunan bazı reseptörler (200-300 civarında) yardımcı hücrenin etkinleştirilmesi için MHC-antijeni tarafından bağlanmalıdırlar. Yardımcı T hücrelerinin etkinleştirilmesi ayrıca antijen sunan bir hücreyle ilişkilenmesi nedeniyle daha uzun süreye gereklilik duyar.[49] Dinlenen bir T hücresinin etkinleştirilmesi, bazı hücre tiplerinin hareketlerini etkileyen sitokinlerin salınmasına neden olur. Sitokin sinyalleri makrofajların mikrobisidal fonksiyonunu ve öldürücü T hücrelerinin etkinliğini geliştiren yardımcı T hücreleri tarafından üretilir.[9] Ek olarak, yardımcı T hücrelerinin etkinleştirilmesi, T hücresinin yüzeyinde ifade edilen, antikor üreten B hücrelerinin etkinleştirilmesinde tipik olarak gerek duyulan, fazladan uyarı sinyalleri sağlayan CD40 (CD154) zinciri gibi moleküllerin düzenlenmesine (upregülasyonuna) neden olur.[50]
T hücreleri, CD4+ ve CD8+ (γδ) T hücrelerinden farklı bir T hücresi reseptörüne (TCR) sahiplerdir ve öldürücü T hücreleri, yardımcı T hücreleri ve doğal öldürücü hücrelerin özelliklerini paylaşırlar. γδ T hücrelerinden yanıt oluşturan şartlar henüz tam olarak aydınlanmamıştır. Diğer alışılagelmemiş T hücresi altkümelerindeki benzer olarak CD1d-bağlı doğal öldürücü hücreler gibi değişmeyen TCRler, γδ T hücreleri doğştan ve edinilmiş bağışıklık arasındaki hatta bulunurlar.[51] Diğer taraftan γδ T hücreleri, edinilmiş bağışıklığın reseptör çeşitliliğini üretmek ve ayrıca hatırlanabilir bir fenotipi geliştirmek için TCR genlerini düzenleyen bileşenleridir. Öteki taraftan çeşitli altkümeler ayrıca doğuştan gelen bağışıklık sisteminin örnek tanıma reseptörleri gibi kullanılan TCRlerini ya da DÖH reseptörlerini bağlayan parçalarıdır. Örneğin insan Vγ9/Vδ2 T hücrelerinin büyük miktarları, mikroplar tarafından üretilen
peptidik olmayan antijenlere saatler içinde karşılık verir ve epiteldeki yüksek oranda bağlanmış Vδ1+ T hücreleri stres altındaki epitel hücrelerini yanıtlar.[52]
Bir B hücresi bir patojeni, yüzeyindeki antikorlara özgü yabancı antijenler bağlandığında tanımlar.[53]
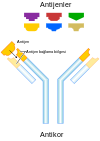
Bu antijen/antikor kompleksi B hücresi tarafından kabul edilir ve proteolizis tarafından peptidlerin içine işlenir. B hücresi o zaman bu antijenik peptidleri yüzeyindeki MHC sınıf II moleküllerinde gösterir. MHC'nin bu kompleksi ve antijen, lenfokinleri salan ve B hücrelerini etkinleştiren eşlenik bir yardımcı T hücresini çeker.[54] Etkin B hücresi böylece bölünmeye başladığında, ürünleri (plazma hücreleri), antijenleri tanıyan antikorların milyonlarca kopyalarını salgılar. Bu antikorlar kan plazmasında ve lenfde dolaşır, antijen sunan patojenleri bağlar ve onları kompleman sisteminin ya da fagositlerin yıkımı ve kaldırması için işaretler. Antikorlar ayrıca bakteriyal toksinleri bağlayarak veya virüslerin ve bakterilerin enfekte hücrede kullandıkları reseptörlere müdahalede bulunarak istilacıları doğrudan etkisizleştirebilirler.[55]CD20 antijeni ayrıca B lenfositlerinde de bulunur.
Edinilmiş bağışıklık sisteminin klasik molekülleri (örn. antikorlar ve T hücre reseptörleri), sadece Gerçekçenelilerde bulunmasına karşın, farklı bir lenfosit benzeri molekül yılan balığı ve Myxine cinsi gibi ilkel omurgasızlarda da keşfedilmiştir. Bu hayvanlar, çeneli omurgalılardaki antijen reseptörlerine benzeyen sadece bir ya da iki gen tarafından üretilen, "çeşitli lenfosit reseptörü (VLRler)" olarak adlandırılan moleküllerinin geniş bir dizisine sahiptirler. Bu moleküllerin patojenik antijenleri, antikorlara benzer yollarla ve aynı özgüllükte bağladığına inanılır.[56]
B ve T hücreleri etkinleştirilip, kendilerini eşlemeye başladıklarında, ürünlerinin bazıları uzun-yaşamlı bellek hücreleri haline gelir. Bir hayvanın hayatı boyunca bu bellek hücreleri her özgül saldıran patojeni hatırlayabilir ve eğer patojen tekrar saldırırsa daha güçlü bir yanıtı sergileyebilir. Bu kazanılmıştır çünkü canlının hayatı boyunca bu patojenlerle enfeksiyonlara uyum sağlama devam eder ve bağışıklık sistemi gelecek salıdırılar için kendini hazırlar.
Bağışıklık belleği, aktif veya pasif şekillerde görülebilir:
Yeni doğanların mikroplarla daha önce tecrübesi olmamıştır ve enfeksiyonla hasarlanmaları kısmen mümkündür. Pasif bağışıklığın bazı tabakaları anne tarafından sağlanır. Gebelik sırasında, IgG olarak adlandırılan antikorların bir kısmı anneden bebeğe plesanta yoluyla geçer ve böylece insan bebekleri doğduklarında bile annelerininki kadar aynı düzeyde antijen özgüllüğüne ve antikorların büyük kısmına sahiplerdir.[57]
Göğüs sütü ayrıca yenidoğanın sindirim sistemine de geçen antikorları içerir ve yenidoğan kendi antikorlarını sentezleyince kadar bebeği bakteriyal enfeksiyonlardan korur.[58] Bu pasif bağışıklıktır çünkü fetüs aslında hiç bellek hücresi ya da antikor üretemez, onları sadece ödünç alır.
Bu pasif bağışıklık genellikle kısa sürelidir, birkaç gün ila birkaç ay sürer. Tıpta, koruyucu pasif bağışıklık ayrıca, bir canlıdan diğerine antikor zengini serum verilerek yapay olarak sağlanabilir.[59]
Uzun süreli aktif bellek enfeksiyon sonrası B ve T hücrelerinin etkinleştirilmesine gerek duyar. Aktif bağışıklık ayrıca yapay olarak aşılamayla da sağlanabilir. Aşılamanın (bağışıklama) arkasında yatan temel kural, patojenden gelen bir antijenle bağışıklık sistemini uyarmak ve bu patojen karşısında özgül bağışıklığı ev sahibinde hastalığa neden olmadan geliştirmektir.[9] Bu önceden planlanmış bağışıklık yanıtı başarılıdır çünkü bağışıklık sisteminin doğal özgüllüğünü kullanır. İnsan populasyonun ölüm nedenlerinden önde gelen nedenlerden enfeksiyon hastalıklarında, bağışıklık sisteminin insanlıkla gelişiminden beri en etkili uygulamayı "aşılama" sunmaktadır.[29][60]
Çoğu viral aşı yaşayan zayıflatılmış virüslerden elde edilirken, bakteriyal aşılar mikroorganizmaların zararsız toksinlerini de içeren aselüler (hücresiz) bileşenlerine dayanır.[9]
Bazı antijenler aselüler aşlılardan elde edildiklerinden beri edinilmiş yanıtın çok güçlü olmasına neden olmadıklarından beri, bazı bakteriyal aşılar bağışıklığı yükselten ve doğuştan gelen bağışıklığın antijen sunan hücrelerini etkinleştiren ek yardımcılar da taşımaktadırlar.[61]
Bağışıklık sistemi fark edilebilir derecede özgüllüğün, toplanmanın ve uyumun birleştirilmesi gibi etkileyici bir yapıya sahiptir. Ev sahibinin savunmasında hatalar oluşabilir ve bunlar üç kategori altında incelenir: bağışıklık yetmezlikleri, kendine bağışıklık ve aşırı duyarlılık.
Bağışıklık yetmezliği, bağışıklık sisteminin bileşenlerinden biri ya da birkaçı inaktif duruma geldiğinde meydana gelir. Bağışıklık sisteminin patojenlere olan yanıtı genç ve yaşlıların her ikisinde de, 50'li yaşlarda belirgin olarak "bağışıklık yaşlılığıyla" ilişkili olarak azalır.[62][63] Gelişmiş ülkelerde obezite, alkolizm ve yasal olmayan ilaçlar bağışıklık işlevlerinin zayıflamasına neden olan başlıca sebeplerdir.[63] Bununla beraber iyi beslenmeme de gelişmiş ülkelerde bağışıklığı düşüren önemli nedenler arasındadır.[63] Protein fakiri beslenme hücre-aracılı bağışıklığının azalması, tamamlama etkinliği, fagositik işlevsellik, IgA antikor yoğunluğu değişimi ve sitokin üretimiyle ilişkilendirilir. Şunlar gibi tekli besinlerin eksiklikleri de; demir, bakır, çinko, selenyum, vitaminler, A vitamini, C vitamini, E vitamini ve B6 ve folik asit (vitamin B9) ayrıca bağışıklık yanıtlarını azaltır.[63] Ek olarak, timusun erken yaşlarda genetik mutasyonlar veya operasyonlar sonucu kaybedilmesi bazı bağışıklık yetmezliklerine neden olabilir ve yüksek enfeksiyon kapma olasılığıyla sonuçlanır.[64] Bağışıklık yetmezlikleri ayrıca kalıtılabilir ya da edinilebilir.[9] Fagositlerin patojenleri yok etmek için indirgenmiş bir yetenek kazandıkları kronik granülomatus hastalığı kalıtılmış ya da konjenital bir bağışıklık yetmezliği örneğidir. AIDS ve kanserlerin bazı tipleri de edinilmiş bağışıklık yetmezliklerine neden olur.[65][66]
Aşırı etkin bağışıklık yanıtları bağışıklık sisteminin işlevsizliğinin başka bir sonucunu; özellikle "kendine bağışık" yetmezlikleri kapsar. Burada bağışıklık sistemi kendinden ve kendinden-olmayanı uygun şekilde ayırmakta hataya düşer ve vücudun kendi parçalarına saldırır. Normal şartlar altında bile bazı T hücreleri ve antikorlar kendinden-olan peptidlerle tepkimeye girerler.[67] Timus ya da kemik iliğinde özelleşmiş hücrelerin fonksiyonlarından biri, genç lenfositleri kendi antijenleriyle vücudun içine üretip sunmak ve bu hücrelerin kendinden-antijenleri, kendine bağışıklığı engelleyerek seçmesidir.[53]
Aşırı duyarlılık, vücudun kendi dokularına zarar veren bir bağışıklık yanıtıdır. Aşırı duyarlılık reaksiyon zamanı ve uyarlandıkları karmaşık mekanizmalara göre 4 sınıfa ayrılır: Tip I aşırı duyarlılık; sıkı sık alerjiyle ilişkili olan derhal ya da anaflaktik olan reaksiyondur. Semptomlar orta düzey rahatsızlıktan ölüme kadar gidebilir. Tip I aşırı duyarlılığa mast hücrelerinden ve bazofillerden salınan IgE ile aracılık eder.[68] Tip II aşırı duyarlılık; antikorlar hastanın kendi hücrelerindeki antijenlere bağlanıp, onları yıkım için işaretlediklerinde meydana gelir. Bu ayrıca antikor-bağımlı (ya da sitotoksik) aşırı duyarlılık olarak isimlendirilir ve IgG ve IgM antikorları tarafından aracılık edilir.[68] Çeşitli dokularda bulunan bağışıklık kompleksleri (antijenlerin yapışmaları, kompleman proteinler ve IgG ve IgM antikorları) tip III aşırı duyarlılık reaksiyonlarını tetikler.[68] Tip IV aşırı duyarlılık; (hücre-aracılı ya da gecikmiş tip aşırı duyarlılık olarak da bilinir); genellikle gelişmesi iki ya da üç gün süren aşırı duyarlılık tipidir. Type IV reaksiyonları bazı kendine bağışık ve enfeksiyonöz hastalıklarıyla ilişkilidir, fakat bunlardan başka kontakt dermatitis (zehirli sarmaşık) ile de ilişkili olabilir. Bu reaksiyonlara T hücreleri, monositler ve makrofajlarca aracılık edilir.[68]
Edinilmiş bağışıklık sistemleri şeklinde bağışıklık yanıtı ilk kez omurgalılarda ortaya çıkmıştır çünkü omurgasızlarda lenfositler veya antikora-dayalı humoral yanıtlar görülmez.[1] Bununla beraber bazı türler omurgalı bağışıklığına bakışta öncü olarak görülen bazı mekanizmaları kullanırlar. Bakteriler ve (belki bazı diğer prokaryotik organizmalar) kendilerini bakteriyofaj gibi viral patojenlerden korumak için restriksiyon-modifikasyon sistemi olarak bilinen eşsiz bir savunma mekanizması geliştirmişlerdir.[69] Patern tanıma reseptörleri, neredeyse bütün organizmalarca, mikrobiyal patojenlerle ilişkili molekülleri tanımlamak için kullanılan proteinlerdir. "Defensinler" olarak adlandırılan antimikrobiyal peptidler, bütün hayvanlar ve bitkilerde bulunan ve omurgasızlarda sistemik bağışıklığın ana şekillerini gösteren evrimsel olarak korunmuş doğuştan gelen bağışıklığın bileşenleridir.[1] Kompleman sistemi ve fagositik hücreler de ayrıca omurgasızların çoğu hayat formlarınca kullanılırlar. Ribonükleaz ve RNA interferans yolları bütün ökaryotlarda saklıdır ve virüslere karşı bağışıklık yanıtının oluşmasında rol aldıkları düşünülmektedir.[70]
Hayvanlardan farklı olarak, bitkiler fagositik hücrelerden yoksunlardır ve çoğu bitkinin bağışıklık yanıtları, bitkinin tamamına yayılan sistemik kimyasal sinyaller gönderir.[71]
Bitkinin bir parçası enfekte edildiğinde, bitki sınırlı bir hipersensivite yanıtı (HR) oluşturur, enfeksiyonun olduğu bölgede bitkinin diğer parçalarına yayılmasını engelleyen hızlı programlanmış hücre ölümü gerçekleştirilir. Sistemik kazanılmış dayanıklılık (SAR), tüm bitkiyi birçok enfeksiyon ajanına karşı dirençli hale getiren bir savunma yanıtı tipidir.[71] RNA interferans mekanizmaları özellikle bu sistemik yanıtlarda virüs replikasyonunu önleyebildikleri için önemlidir.[72]

Bağışıklık sisteminin başka bir önemli rolü de tümörleri tanıması ve yok etmesidir. Tümörlerin değişime uğramış hücreleri, normal hücrelerde bulunmayan tümör antijenlerini ifade ederler. Bağışlıklık sistemine bu antijenler yabancı olarak görünür, sunumları bağışıklık sistemini hücrelerinin değişmiş tümör hücrelerine saldırmasına neden olur. Tümör hücrelerince ifade olunan antijenlerin bazı kaynakları vardır;[74] bazıları servikal kansere neden olan insan papillomavirüsü gibi onkojenik virüslerden köken alırken,[75] diğerleri düşük seviyelerde normalken yüksek seviyelerde kansere neden olan canlının kendi proteinleridir. Enzimlerden tirosinaz olarak bilineni yüksek seviyelerinde olağan deri hücrelerini (örn. melanositleri) melanoma diye bilinen tümörlere değiştirir.[76][77] Tümör antijenlerinin üçüncü bir olası kaynağı hücre büyümesi ve yaşamasını düzenleyen, çoğunlukla onkogen diye adlandırılan moleküllerin kansere dönüşmesini sağlayan proteinlerdir.[74][78][79] Bağışıklık sisteminin tümörlere ana yanıtı; yardımcı T hücrelerinin yardımıyla öldürücü T hücrelerini kullanarak anormal hücreleri yok etmesidir.[77][80] Tümör antijenleri viral antijenlere benzer yollarla MHC sınıf I molekülleri üzerinden sunulur. Bu, öldürücü T hücrelerinin tümör hücrelerini "anormal" olarak tanımasına izin verir.[81] Doğal öldürücü hücreler de ayrıca tümörlü hücreleri benzer yollarla, özellikle tümörlü hücreler yüzeylerinde normalden biraz daha az MHC sınıf I molekülünü taşıyorlarsa öldürür, bu tümörlerde yaygın bir durumdur.[82] Antikorlar bazen kompleman sistemince yıkılmalarına izin veren tümör hücreleri karşısında üretilir.[78] Açıkçası, bazı tümörler bağışıklık sisteminden kaçabilir ve yaşamaya devam edebilirler.[83] Tümör hücreleri çoğunlukla yüzeylerindeki MHC sınıf I moleküllerinin bir kısmını indirgemişlerdir, bu yüzden öldürücü T hücrelerinin taramasından kaçabilirler.[81] Bazı tümör hücreleri ayrıca bağışıklık yanıtını baskılayan ürünler de salarlar; örneğin lenfositlerin ve makrofajların etkinliğini baskılayan TGF-β sitokini gibi.[84] Ek olarak, bağışıklıksal dayanıklılık (tolerans) tümör antijenleri karşısında gelişebilir ve böylece bağışıklık sistemi artık tümör hücrelerine saldırmaz olur.[83] Birbirine ters olarak, tümör hücrereleri makrofajları çeken sitokinleri ve tümör gelişimini besleyen gelişme faktörlerini bıraktıklarında, makrofajlar tümör gelişimini desteklerler.[85] Ayrıca tümördeki hipoksinin bir kombinasyonunda ve makrofajlarca bir sitokin üretildiğinde, tümör hücrelerinin metastazını bloklayan bir proteinin üretimini azaltır ve bu suretle kanser hücrelerinin yayılmasına yardımcı olunur.
Hormonlar, bağışıklık sisteminin duyarlılığını değiştirerek bağışıklık aracıları (immünomodülatörler) gibi görev alabilirler. Örneğin, dişi eşey hormonları edinilmiş ve[86] doğuştan gelen bağışıklık yanıtının uyarıcıları (immünostimulatörleri) olarak bilinirler.[87] Lupus erythematosus gibi bazı kendine bağışık hastalıklar, tercihen kadınları bulur ve başlangıçları kıllanmayla aynı zamana denk gelir. Zıt olarak, testosteron gibi erkek eşey hormonları bağışıklık baskılayıcı olarak görünmektedirler.[88] Diğer hormonlar, en çok prolaktin, büyüme hormonu ve D vitamini bağışıklık sistemini düzenliyor gibi görünmektedirler.[89][90] Yaşla değişen hormon seviyelerinin, yaşlanmada kısmen zayıflamış bağışıklık yanıtlarından sorumlu olduğu farzedilmektedir.[91] Ters olarak, bazı hormonlar bağışıklık sistemince düzenlenirler; örneğin; tiroid hormonu etkinliği gibi.[92] Bağışıklık sistemi uyku ve dinlenmeyle güçlenir,[93] stresle zayıflar.[94] Beslenme de bağışıklık sistemini etkileyebilir; örneğin taze meyveler, sebzeler ve yağ asitlerince güçlü yiyecekler sağlıklı bir bağışıklık sistemini destekleyebilir.[95] Başka bir deyişle, fetal iyi beslenememe, hayat boyu süren bağışıklık sistemi zayıflığına neden olabilir.[96] Geleneksel tıpta ekinezya, meyan kökü, ginseng, geven, adaçayı, sarımsak, mürver meyvesi, şitaki ve lingzhi mantarları, zufa otu gibi bazı bitkilerin ve balın bağışıklık sistemini uyardığına inanılmaktadır. Çalışmalar, eylemleri karmaşık ve tanımlanmaları zor olsa da bitkilerin gerçekten de bağışıklık sistemini uyarabileceğini göstermektedir.[97]
Bağışıklık yanıtı, kendine bağışıklıklık, alerji, doku nakli redleri sonucu istenmeyen yanıtları baskılamak için geliştirilebilir ve çoğunlukla bağışık sisteminden kaçan patojenler karşısında koruyucu yanıtları uyarabilir (bknz. bağışıklama).
Bağışıklık baskılayıcı ilaçlar büyük doku harabiyetleri oluştuştuğunda kendine bağışık düzensizlikleri ya da yangıyı kontrol etmek için ve bir organ nakli sonrası nakil reddini önlemek için kullanılırlar.[29][98]
Yangı-önleyici (anti-enflamatör) ilaçlar sıkça yangının etkilerini kontrol etmek için kullanılır. Glukokortikoidler bu ilaçların en güçlüleridir, bununla beraber bu ilaçların bazı yan etkileri olabilir (örn. merkezi obezite, hiperglisemi, osteoporoz) ve sıkı kontrol altında kullanılmalıdırlar.[99] Bu yüzden yangı-önleyici ilaçların düşük dozları sıkça sitotoksik ya da metotreksat ya da azathioprin gibi bağışıklık baskılayıcı ilaçlarla birleştirilerek kullanılırlar.
Sitotoksik ilaçlar etkin T hücreleri gibi bölünen hücreleri öldürerek bağışıklık yanıtını engellerler. Bununla birlikte, öldürme rastgeledir ve diğer sürekli bölünen hücreleri ve organları da etkiler ve zehirli yan etkilere neden olur.[98]
Siklosporin gibi bağışıklık baskılayıcı ilaçlar sinyal iletim yollarını engelleyerek T hücrelerinin sinyallere tam olarak doğru yanıt vermesini önlerler.[100] Daha büyük ilaçlar (>500 Da) özellikle tekrar tekrar veriliyorlarsa ya da daha yüksek dozdaysalar etkisiz (nötralize) bir bağışıklık yanıtını harekete geçirebilirler.
İlaçların etkileyiciliklerinin sınırları (6000 Da'dan daha büyük olan) peptidlere ve proteinlere bağlıdır. Bazı hallerde, ilacın kendisi immünojenik değildir fakat yardımcı bir immünojenik bileşikle güçlenebilir; Taxol zaman zaman bu roldedir. Sayısal yöntemler, terapötik antikorların taslaklanmasında kısmen yararlı olan, viral kapsül parçacıkları mutasyonlarının zararını tayin etmek ve peptid-bazlı ilaç tedavi tekliflerinin onaylanmasına peptidlerin ve proteinlerin immünojenikliğini öngörmek için geliştirilebilirler.
Erken dönem teknikleri büyük ölçüde hidrofilik amino asitlerin epitop bölgelerinde hidrofobik amino asitlere göre çok daha fazla bulunmasina dayanmaktaydı;[101] bununla birlikte daha gelişmiş yeni teknikler, bilinen epitopların, özellikle de üzerinde çok çalışma yapılmış virüs proteinlerinin veritabanlarını alıştırma kümeleri olarak kullanan öğrenme kabiliyeti bulunan makinesel tekniklere yani özdevimli öğrenme tekniklerine dayanmaktadır.[102] B hücreleri tarafından tanınanbildiği bilinen patojenlerin epitoplarının kataloğundan oluşan ve kamuya açık bir veritabanı kurulmuştur.[103]
İmmünojenik çalışmaların biyoenformatiğe dayalı yardımcı alanı "immunoenformatiğe" karşılık gelmektedir.[104]
Herhangi bir patojende başarı, onun konağın bağışıklık yanıtlarından kaçmabilme kabiliyetine bağlıdır. Bu yüzden patojenler bağışıklık aracılı yıkımdan kaçabilirlerken ev sahibini başarıyla enfekte edebilmelerine izin veren bazı metotlar geliştirmişlerdir.[105] Bakteriler sıklıkla bariyerleri eriten enzimler salgılayarak - örneğin tip II salgılama sistemi kullanarak- fiziksel engellerin üstesinden gelirler.[106] Farklı olarak, tip III salgılama sistemi kullanarak, patojenden konağa proteinlerini doğrudan aktarmayı sağlayan ev sahibinin hücresine içi boş bir tüp yerleştirebilirler; bu proteinler tüp boyunca ilerler ve genellikle konağın savunmalarını kapatırlar.[107] Doğuştan gelen sistemini kandıran bazı patojenlerce kullanılan birkaçma stratejisi de (intraselüler patogenez olarak da isimlendirilen) hücreiçi replikasyondur. Burada patojen hayat döngüsünün çoğunu, bağışıklık hücreleri antikorlar ve tamamlayıcılarla doğrudan temasdan korunduğu konak hücrelerde geçirir. Hücre içi patojenlerin bazı örnekleri; virüsler, besin bozucu bakterilerden Salmonella ve malarya etkeni olan ökaryotik parazit Plasmodium falciparum ve leishmania etkeni Leishmania spp.dir. Mycobacterium tuberculosis gibi diğer bakteriler tamamlayıcıların lizisinden korundukları koruyucu bir kapsül içinde yaşarlar.[108] Bazı patojenler konağın bağışıklık yanıtını yanlış yönlendiren veya etkisini azaltan bileşenler salarlar.[105] Bazı bakteriler kendilerini bağışıklık sisteminin hücrelerinden ve proteinlerinden koruyan biyofilmler şekillendirirler. Böyle biyofilmler bazı enfeksiyonlarda başarılı olabilirler; örneğin, kronik kistik fibrozisin karaktersitik enfeksiyonözleri Pseudomonas aeruginosa ve Burkholderia cenocepacia.[109] Diğer bakteriler antikorları bağlayan ve etkisizleştiren yüzey proteinleri üretirler; örneğin Streptococcus (protein G), Staphylococcus aureus (protein A) ve Peptostreptococcus magnus (protein L).[110] Virüsleri edinilmiş bağışıklık sisteminden koruyan mekanizmalar ise daha karmaşıktır. En basit yakınlaşma da saldırganın yüzeyindeki temelli-olan epitoplar saklanırken temelli-olmayan epitoplar (amino asitler ve/veya şekerler) hızlıca değiştirilir. Örneğin HIV, konak hedef hücreye girmesi için gerekli olan viral kapsülündeki proteinleri düzenli olarak değiştirir. Antijenlerdeki bu sık değişimler bu proteinlere yönlenen aşıların neden başarısız olduğunu açıklayabilir.[111] Antijenleri konağın molekülleriyle maskeleme de yaygın olarak kullanılan başka birkaçınma stratejisidir. HIV'deki vironu kaplayan kapsül konağın en dış membranından şekillenir; kendini-kaplayan virüsler böylece bağışıklık sistemininin "kendinden-olmayan"ı tanımasını zorlaştırır.[112]

İmmünoloji, bağışıklık sisteminin yapısını ve fonksiyonlarını açıklayan bilim dalıdır. Tıptan köken alır ve erken dönem çalışmaları hastalıkların bağışıklık nedenlerini üzerinedir. Bağışıklığın en erken anıldığı dönem MÖ. 430'da Atina veba salgınıdır. Thucydides daha önce bir nöbet geçirip iyileşmiş insanların ikinci defa hastalığa yakalanmadıklarını belirtmiştir.[113] Edinilmiş bağışıklığa bu bakış daha sonra Louis Pasteur tarafından aşıyı geliştirmede ve hastalık-germ teorisini ileri sürmede kullanılmıştır.[114] Pasteur'ün teorisi hastalıkların miasma teorisi gibi çağdaşı teorilere doğrudan karşıttı. Mikroorganizmaların enfeksiyon hastalıklarının nedeni olduğu, 1905'te Nobel Ödülü alan Robert Koch'un 1891'de yayımladığı Koch postülatlarına kadar kanıtlanmadı.[115] 1901'de virüslerin insan patojeni oldukları sarıhumma virüsünün Walter Reed tarafından keşfiyle doğrulandı.[116]
İmmünoloji 19. yüzyılın sonlarına doğru humoral ve hücresel bağışıklığın hızlı gelişmeleriyle büyük ilerleme kaydetti.[117]
Özellikle antijen-antikor reaksiyonunun özgüllüğünü açıklayan yan-zincir teorisini ileri süren Paul Ehrlich'in çalışmaları oldukça önemliydi; Ehrlich, humoral bağışıklığın tanımlanmasına olan katkılarıyla 1908'de hücresel bağışıklığın bulucusu Elie Metchnikoff ile birlikte Nobel Ödülü aldı.[118]
Seamless Wikipedia browsing. On steroids.
Every time you click a link to Wikipedia, Wiktionary or Wikiquote in your browser's search results, it will show the modern Wikiwand interface.
Wikiwand extension is a five stars, simple, with minimum permission required to keep your browsing private, safe and transparent.