Паулијев принцип
From Wikipedia, the free encyclopedia
Паулијев принцип искључења је принцип у квантној механици, који је 1925. формулисао Волфганг Паули. Гласи да ниједна два идентична фермиона не могу да се налазе у истом квантном стању симултано. Ригорозније тврђење овог принципа је да је, за два идентична фермиона, укупна таласна функција антисиметрична. За електроне у једном атому, гласи да ниједна два електрона не могу да имају иста четири квантна броја, то јест ако су , , и једнаки, мора бити различит тако да електрони имају супротне спинове. Ово је кључни принцип за разумевање и изградњу Периодног система елемената. Волфганг Паули, је за формулисање овог принципа 1945. добио Нобелову награду за физику.
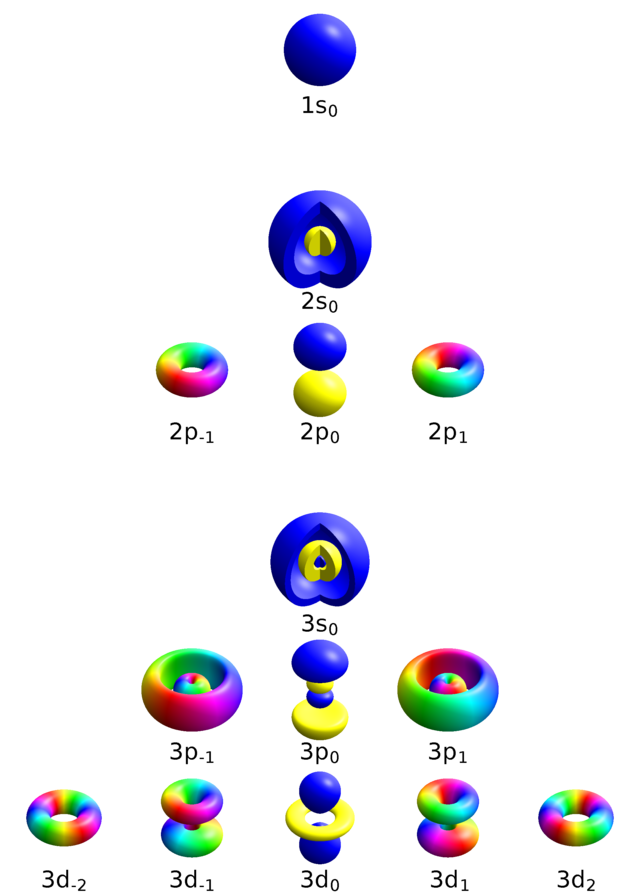

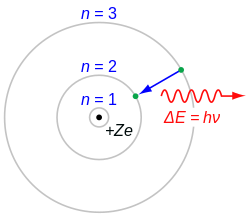

Паулијев принцип искључења објашњава електронска конфигурација, то јест смештај електрона у љускама атомског омотача, а тиме и периодичност својстава хемијских елемената. Њему се подвргавају и електрони у електронском плину у металима, на чему почива теорија електричне проvoдљивости, а објашњава и многа механичка, електрична, магнетска, оптичка и хемијска својства чврстих материја. Паули је то начело објаснио (формулирао) 1925. за електроне, а 1940. га је проширио од електрона на све фермионе, честице с полуцелим спином. У општем објашњењу, Паулијево начело изриче да таласна функција мора бити антисиметрична при замени двају фермиона, односно симетрична при замени пара бозона. То се начело показује важним за стабилност атома и хемијских материја генерално.[1]
Једна од последица принципа искључења јесте чињеница да постоје разни хемијски елементи, јер када он не би вредео, тада би сви електрони у атому заузели најниже енергетско стање, те би по хемијским својствима били једнаки. Електрони атома тежих од хелијумових не заузимају најниже енергетско стање, јер два електрона у истом атому не могу имати сва четири квантна броја ( и ) једнака, што значи да не могу бити описана једнаком таласном функцијом.