Млечна киселина
From Wikipedia, the free encyclopedia
Млечната киселина е органско соединение со хемиска формула CH3CH(OH)COOH. Таа е бела, кристална супстанца, со кисел вкус и растворлива е во вода. Кога е во течна агрегатна состојба, таа е безбојна. Се добива по природен и синтетски пат. Бидејќи има хидроксилна група во непосредна близина на карбоксилната група, млечната киселина се класифицира како алфа-хидрокси киселина. Кога е во форма на својата конјугирана база, наречена лактат, таа игра значајна улога во разни биохемиски процеси.
| |||
Претпочитано име по МСЧПХ: 2-хидроксипропанска киселина | |||
| Назнаки | |||
|---|---|---|---|
| 50-21-5 79-33-4 (L) 10326-41-7 (D) | |||
| ChEBI | CHEBI:422 | ||
| ChEMBL | ChEMBL330546 | ||
| ChemSpider | 96860 | ||
IUPHAR/BPS |
2932 | ||
| 3Д-модел (Jmol) | Слика | ||
| |||
| UNII | 33X04XA5AT | ||
| Својства | |||
| Хемиска формула | |||
| Моларна маса | 0 g mol−1 | ||
| Точка на топење | |||
| Точка на вриење | |||
| Киселост (pKa) | 3.86,[1] 15.1[2] | ||
| Термохемија | |||
| Ст. енталпија на согорување ΔcH |
1361.9 kJ/mol, 325.5 kcal/mol, 15.1 kJ/g, 3.61 kcal/g | ||
| Pharmacology | |||
| ATC код | G01AD01 QP53AG02 | ||
| Опасност | |||
| GHS-ознаки: | |||
Пиктограми |
 [3] [3] | ||
Изјави за опасност |
H315, H318[3] | ||
Изјави за претпазливост |
P280, P305+P351+P338[3] | ||
| Слични супстанци | |||
| Други анјони | лактат | ||
| Дополнителни податоци | |||
| Освен ако не е поинаку укажано, податоците се однесуваат на материјалите во нивната стандардна состојба (25 °C, 100 kPa) | |||
| Наводи | |||
Во раствор, протонот од карбоксилната група може да се јонизира, што резултира со добивање на лактатен анјон CH3CH(OH)COО-. Во споредба со оцетната киселина, нејзината pKa вредност е за една единица помала, што значи дека млечната киселина се депротонира десет пати полесно отколку оцетната киселина. Повисоката киселост е последица на меѓумолекулската водородна врска помеѓу α-хидроксилната група и карбоксилната група.
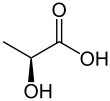
Млечната киселина е хирална супстанца, која се состои од два оптички изомери. Едниот изомер е познат како L-(+)-млечна киселина или (S)-млечна киселина, а другиот како D-(-)-млечна киселина или (R)-млечна киселина. Смесата од двата изомери со еднакви количини се нарекува DL-млечна киселина или рацемска млечна киселина.

Млечната киселина е хигроскопна. DL-млечната киселина се меша со вода и со етанол над точката на топење, која е околу 17 или 18 °C. Чистите D-млечна киселина и L-млечна киселина имаат повисоки точки на топење.
Кај животните, L-лактатот постојано се произведува од пируват со помош на ензимот лактат дехидрогеназа (LDH) во процес на ферментација, за време на нормалниот метаболизам и при вежбање. Концентрацијата не се зголемува сѐ додека стапката на продукција не ја надмине стапката на елиминација на лактатот, што е регулирано од бројни фактори, вклучувајќи ги монокарбоксилатните транспортери, концентрацијата и изоформата на LDH и оксидативниот капацитет на ткивата. Концентрацијата на лактат во крвта обично изнесува 1-2 mmol/L во мирување, но може да се зголеми над 20 mmol/L за време на интензивен физички напор,[4] па дури до 25 mmol/L после физичкиот напор.[5]
Во индустријата, ферментацијата на млечната киселина се прави со бактерии на млечно-киселинско вриење, кои ги претвораат простите јаглехидрати, како што се гликоза, сахароза или галактоза, во млечна киселина. Овие бактерии можат да се најдат и во усната празнина, а млечната киселина која ја продуцираат е одговорна за појава на кариес.[6][7][8][9]
Во медицината, лактатот е една од главните компоненти на лактатниот Рингеров и Хартманов раствор.[10] Овие интравенозни раствори содржат катјони на натриум и калиум, заедно со лактатни и хлоридни анјони растворени во дестилирана вода, во концентрации изотонични со човечката крв. Најчесто се користи за замена на течности по губење на крв поради траума, изгореници или при хируршки интервенции.