Ossido di trifenilfosfina
composto chimico Da Wikipedia, l'enciclopedia libera
L'ossido di trifenilfosfina è il composto organofosforico con formula OP(C6H5)3, usualmente scritta come OPPh3 o Ph3PO. Disponibile in commercio, in condizioni normali è un solido cristallino incolore, scarsamente solubile in acqua ma solubile in solventi organici polari. Si ottiene in genere come prodotto finale di scarto in numerose reazioni organiche coinvolgenti la trifenilfosfina.[3] Trova applicazione come reagente per facilitare la cristallizzazione di composti chimici.[4]
| Ossido di trifenilfosfina | |
|---|---|
 | |
 | |
| Nome IUPAC | |
| Trifenil-λ5-fosfanone | |
| Nomi alternativi | |
| trifenilfosfinossido | |
| Caratteristiche generali | |
| Formula bruta o molecolare | C18H15OP |
| Aspetto | solido |
| Numero CAS | |
| Numero EINECS | 212-338-8 |
| PubChem | 13097 |
| SMILES | C1=CC=C(C=C1)P(=O)(C2=CC=CC=C2)C3=CC=CC=C3 |
| Proprietà chimico-fisiche | |
| Densità (g/cm3, in c.s.) | 1,2[1] |
| Solubilità in acqua | poco solubile |
| Temperatura di fusione | 155–158 °C (428–431 K)[1] |
| Temperatura di ebollizione | >360 °C (633 K)[1] |
| Proprietà termochimiche | |
| C0p,m(J·K−1mol−1) | 312,5[2] |
| Indicazioni di sicurezza | |
| Punto di fiamma | 180°[1] |
| Simboli di rischio chimico | |

| |
| Frasi H | 302 - 412 [1] |
| Consigli P | 273 [1] |
Struttura
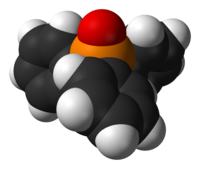
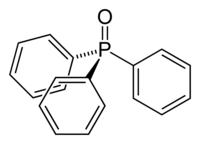
OPPh3 è una molecola tetraedrica, con l'atomo di fosforo in posizione centrale.[5][6] Dal punto di vista cristallografico si conoscono più polimorfi.[7][8][9][10] I più noti sono:
- una struttura monoclina, gruppo spaziale P21/c, con costanti di reticolo a = 1506,6 pm, b = 903,7 pm, c = 1129,6 pm, β = 98,47° e quattro unità di formula per cella elementare, distanze P–O 148,4 pm e P–C 180 pm.[9]
- una struttura ortorombica, gruppo spaziale Pbca, con costanti di reticolo a = 2908,9 pm, b = 913,47 pm, c = 1126,1 pm, quattro unità di formula per cella elementare, distanze P–O 147,9 pm e P–C 180 pm.[10]
Sintesi

L'ossido di trifenilfosfina fu ottenuto per la prima volta da August Michaelis nel 1882.[11] Il legame P=O è molto forte, e di conseguenza il composto si ottiene facilmente dalla trifenilfosfina trattandola con ossidanti vari quali acido nitrico, diossido di manganese, permanganato di potassio, perossido di idrogeno, e anche con il semplice ossigeno atmosferico.[3][5][6] Per questo campioni di trifenilfosfina lasciati all'aria risultano contaminati da OPPh3.
Reattività
Riepilogo
Prospettiva
L'ossido di trifenilfosfina è un composto molto stabile. La rigidità della molecola e la relativa basicità dell'atomo di ossigeno fanno sì che OPPh3 sia comunemente usata per la cristallizzazione di molecole di cui sia altrimenti difficile ottenere cristalli. Questo perché OPPh3 è un buon accettore di protoni e forma complessi con numerose sostanze organiche che abbiano protoni acidi.[4]
Come sottoprodotto in chimica organica
In chimica organica OPPh3 si forma in quantità stechiometrica come sottoprodotto in molte reazioni, tra le quali la reazione di Wittig, di Staudinger e di Mitsunobu. Separare il sottoprodotto OPPh3 dalla miscela di reazione può in vari casi risultare difficile. Se il prodotto desiderato è facilmente solubile in solventi come esano o etere dietilico si può ottenere una buona separazione per semplice triturazione in questi solventi, dove OPPh3 è insolubile. Un'altra possibilità è usare Mg(II) che con OPPh3 forma un complesso insolubile in toluene o diclorometano, separabile per filtrazione.[12] In solventi polari come etanolo, acetato di etile e tetraidrofurano l'aggiunta di ZnCl2 provoca la precipitazione di un complesso insolubile che può essere filtrato.[13] Sono anche stati studiati vari metodi per recuperare la OPPh3 di scarto rigenerando trifenilfosfina. Esistono vari agenti deossigenanti, come fosgene e triclorosilano.[14]
Come legante in chimica di coordinazione

OPPh3 può fungere da legante e preferisce coordinarsi a ioni metallici classificati duri secondo la teoria HSAB. Un esempio è il complesso tetraedrico NiCl2(OPPh3)2.[15]
Note
Bibliografia
Altri progetti
Wikiwand - on
Seamless Wikipedia browsing. On steroids.
