From Wikipedia, the free encyclopedia
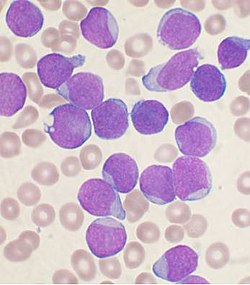
Սուր լիմֆոբլաստային լեյկոզ, արյան բջիջների լիմֆոիդ ճյուղի քաղցկեղ, որը բնութագրվում է արյան մեջ մեծ քանակի ոչ հասուն լիմֆոցիտներով[3]։ Ախտանիշներն են հոգնացության զգացողությունը, մաշկի գունատությունթյունը, տենդը, դյուրին արյունահոսումը, մեծացած ավշային հանգույցները կամ ոսկրային ցավերը[3]։ Որպես սուր լեյկոզ արագ հարաճում է և սովորաբար մի քանի շաբաթվա կամ ամսվա ընթացքում հանգեցնում է մահվան, եթե չի կատարվում բուժվում[4]։
| Սուր լիմֆոբլաստային լեյկեմիա | |
|---|---|
 | |
| Տեսակ | հիվանդության կարգ |
| Հիվանդության ախտանշաններ | տենդ[1], Աստենիա[1], հոգնածություն[1], մարմնի քաշի կորուստ[1], անորեքսիա[1], ոսկրացավ[1], որովայնային ցավ[1] և հևոց[1] |
| Բժշկական մասնագիտություն | ուռուցքաբանություն |
| Բուժում | արյան փոխներարկում[1], immunotherapy?[1] և hematopoietic stem cell transplantation?[2] |
Շատ դեպքերում պատճառը մնում է անհայտ[5]։ Ժառանգական ռիսկի գործոններն իրենց մեջ ներառում են Դաունի համամախտանիշը, Լի-Ֆրաումենի համախտանիշը կամ առաջին տիպի նեյրոֆիբրոմատոզը[6]։ Արտաքին ռիսկի գործոններին են պատկանում զգալի ճառագայթումը, քիմիոթերապիան[6]։ Էլեկտրամագնիսական ճառագայթների և թունաքիմիկատների դերը ապացուցված չէ[7]։ Կա վարկած, որ հասարակ վարակի հանդեպ ոչ նորմալ իմունային պատասխանը կարող է լեյկոզի պատճառ հանդիսանալ[7]։ Մեխանիզմի հիմքում ընկած է բազմաթիվ գենային մուտացիաները, որոնց հետևանքով բջիջները սկսում են արագ կիսվել[5]։ Առաջացած հավելյալ լիմֆոցիտները խանգարում են նոր էրիթրոցիտների, լեյկոցիտների և թրոմբոցիտների առաջացմանը[7]։ Ախտորշումը կատարվում է արյան քննության և ոսկրածուծի պունկցիայի հիման վրա[8]։
Սովորաբար բուժումը սկսվում է քիմիոթերապիայով, որն ուղղված է դեպի ախտադադար հաստատելը[5]։ Հետո լինում է մի քանի տարի առանց քիմիոթերապիայի[5]։ Լրացուցիչ բուժումը իր մեջ ներառում է ներողնուղեղային քիմիոթերապիա կամ ճառագայթային թերապիա՝ եթե տեղի է ունեցել տարածում ուղեղի վրա[5]։ Ցողունային բջիջների փոխպատվաստումը կարող է կիրառվել, եթե հիվանդությունը ենթարկվում է ստանդարտ բուժմանը[5]։ Լրացուցիչ բուժուները ինչպիսին իմունոթերապիան է դեռ ուսումնասիրվում են[5]։
2015 թվականի բոլոր ախտահարված մարդկանց թիվը կազմել է մոտ 876,000 որոնց մոտ 111,000 մահվան ելքով[9]։ Այն գերազանցապես հանդիպում է երեխաների մոտ, մասնավորապես, երկուսից հինգ տարեկանների շրջանում[10][11]։ Միացիալ նահանգներում դա երեխաների քաղցկեղի և մահվան ամենաշատ հանդիպող պատճառն է[5]։ Պետք է նշել, որ սա առաջին տարածուն քաղցկեղն է, որը ենթարկվել է բուժման[12]։ Ապրելիությունը երեխաների մոտ 1960-ականների 10%-ից 2015 թվականին աճել է միչև 90%[5]։ Ապրելիության ցուցանիշները մինչև 2 տարեկանների (50%[13]) և մեծահասակների մոտ (35%[14]) մնում են ցածր։
Սկցբնական ախտանշանները ոչ սպեցիֆիկ են, մասնավորապես, երեխաների մոտ։ Ավելի քան 50% լեյկոզով հիվանդ երեխաներ կարող են ունենալ թվարկվացներից մեկը կամ մի քանիսը. մեծացած լյարդ (64%), մեժացած փայծաղ (61%), գունատություն (54%), տենդ (53%), արյունազեղումներ (52%)[15]։ Կարող են ունել նաև կրկնվուղ վարակներ, հոգնածության զգացուղություն, վերջույթների ցավ, և մեծացած ավշային հանգույցներ, որն ուղեկցում է վերոնշյալներին։ Այնպիսի ախտանիշներ ինչպիսին է տենդը, գիշերային քրտնարտադրությունը և քաշի կորուստը նույնպես հաճախ են լինում։
Կենտրոնական նյարդային համակարգի ախտանշանները ինչպես գանգային նևրոպաթիան բերում է մենինգեալ ինֆիլտրացիայի, որը հայտնաբերվում է մեծահասակների մոտ ավելի պակաս քան 10% և երեխաների մոտ 5%-ից պակաս, մասնավորապես ներկայացվում է B լիմֆոցիտներով (Բերկետի լիմֆոմա)[16]։
Ախտանիշները և ախտանշանները տարբեր են և ներառում են[17].

Քաղցկեղային բջիջները ամբողջովին ներկայացված են լիմֆոբլաստներով։ Նորմալ լիմֆոբլաստը զարգանալուց հետո դառնում է հասուն, վարակի դեմ պաայքարող T և B բջիջներ, նաև կոչվում են լիմֆոցիտներ։ Օրգանիզմի ազդանշանները կարգավորում են լիմֆոցիտների թիվը այնպես, որ լինի ո՛չ շատ, ո՛չ քիչ։ Հիվանդության ժամանակ և՛ զարգացումը, և՛ թվի կարգավուրումը դառնում են թերի[7][20]։
Ամեն ինչ առաջանում է, երբ մի լիմֆոբլաստ ձեռք է բերում գեների շատ մուտացիաներ, որոնք ազդում են բջջի զարգացման և պրոլիֆերացիայի վրա։ Երեխաների մոտ այս գործընթացը սկսվում այս գեներից որոշների ժառանգումից։ Այս գեները իրենց հերթին բարձրացնում են ավելի շատ մուտացիաների ռիսկը, որով տեղի է ունենում լիմֆատիկ բջիջների զարգացումը։ Որոշ գենետիկ համախտանիշներ, ինչպես Դաունի համախտանիշն է՝ ունեն որոշակի ազդեցություն։ Շրջակա միջավայրի ռիսկի գործոնները նույնպես պետք է նպաստեն բավարար քանակի գենետիկական մուտացիաների առաջացմանը։ Շրջակա միաջավայրի ազդեցությունը երևում է բոլոր երկվորյակ երեխաների մոտ, որտեղ միայն 10-15%-ն են՝ երկուսն էլ գենետիկորեն համանման երկվորյակներն են, երկուսն էլ հիվանդանում են։ Քանի որ նրանք ունեն նույն գեները, արտաքին գործոնների տարբերությունը ցույց են տալիս, թե ինչու է երկվորյակներից մեկը հիվանդանում, իսկ մյուսը՝ ոչ[7]։
Նորածինների մոտ ավելի հազվագյուտ է լինում քան՝ մեկ տարեկան երեխաների մոտ։ KMT2A (նախկինում MLL) գենի վերադասավորումները առավել բնորոշ են և տեղի են ունենում էմբրիոնի կամ պտղի մոտ մինչև ծնունդը[7]։ Այս վերադասավորումների արդյունքում ավելանում է բջջի զարգացման գեների էքսպրեսիան, որի հետևանքով գեների տրանսկրիպցիան խթանվում է էպիգենետիկ փոփոխությունների միջոցով[21][22]։ Ի տարբերություն մեծահասակների, երեխաների մոտ արտաքին գործոնները չեն կարող զգալի ազդեցություններ ունենալ։ Բացի KMT2A-ի վերադասավորումից, սովորաբար միայն մեկ լրացուցիչ մուտացիա է հայտնաբերվում[11]։ Արտաքին գործոնները անհրաժեչտ չեն այլ մուտացիաներ առաջացնելու համար։
Ընդհանուր ժառանգած ռիսկի գործոնները ներառում են ARID5B, CDKN2A/2B, CEBPE, IKZF1, GATA3, PIP4K2A գեների և ավելի հազվադեպ TP53 գենի մուտացիաները։ Այս գեները կարևոր դեր են խաղում բջջի հասունացման, պրոլիֆերացիայի և տարբերակման մեջ[5][11][23]։ Անհատականապես, այս մուտացիաներից շատերը ցածր ռիսկի գործոն են հանդիսանում։ Էական հիվանդության ռիսկ է լինում, երբ այս մուտացիաները տեղի են ունենում միևնույն անձի մոտ և հանդիպում են իրար[11]։
Գենետիկ ռիսկերի անհավասար բաշխումը կարող է օգնել բացատրել հիվանդության հաճախության տարբերությունները էթնիկ խմբերի մեջ։ Օրինակ՝ ARID5B մուտացիան ավելի քիչ է հանդիպում աֆրիկական պոպուլացիաներում[11]։
Մի շարք գենետիկական համախտանիշներ իրենց մեջ բարձր ռիսկ են պարունակում։ Դրանք ներառում են Դաունի համախտանիշը, Ֆանկոնի սակավարյունությունը, Բլումի համախտանիշը, X-ի հետ շղթայակցված ագամմագլոբուլինեմիան, մի շարք համակցված իմունոդեֆիցիտներ, Շվախման-Դայմոնդի համախտանիշը, Կոստմանի համախտանիշը, առաջին տիպի նեյրոֆիբրոմատոզը, ատաքսիա-տելեանգիեկտազիան, պարոքսիզմալ գիշերային հեմոգլոբինուրիան և Լի-Ֆրաումանի համախտանիշը[12]։ Ավելի քիչ քան 5% դեպքերում հիվանդքւթյունը ասոցացվում է նշված համախտանիշների հետ։
Հազվագյուտ մուտացիաները ETV6 և PAX5 ասոցացվում են ընտանեկան ձևի հետ, ծնողներից աուտոսոմ դոմինանտ ժառնգումով[5]։
Շրջակա միջավայրի ազդեցությունը հիվանդության առաջացման վրա մշտական վեճերի և խոսակցությունների պատճառ է[11][23]։
Բջջի կորիզի բարձր դոզաներով ճառագայթումը լեյկոզի զարգացման ռիսկի հայտնի պատճառ է[24]։ Ապացույցներ կան, որ նույնիսկ քիչ քանակով ճառագայթումը, ինչպես ռենտգեն նկարահանումը հղիության ժամանակ բարձրացնում են հիվանդության առաջացմանվ հավանականությունը[23]։ Բայց հետազոտությունները ցույց են տվել, որ ռիսկը ճառագայթվածների և չճառագայթվածների մոտ չնչին քանակով է տարբերվում[11]։ Էլեկտրական հոսանքի հաղորդալարերի հզոր էլեկտրամագնիսական ճառագայթումը նույնպես շատ քիչ ազդեցություն է թողնում։ Այս արդյունքները դիտված են որպես ոչ պատճառահետևանքային մեխանիզմներ ըստ էլեկտրամագնիսական ճառագայթման հետևանքով առաջացած քաղցկեղի[11][23]։
Նորածնի մեծ քաշը նույնպես իր մեջ պարունակում է փոքր քանակի ռիսկ։ Բայց ավել քաշի և մեխանիզմի միջև կապը հայտնի չէ[23]։
Ապացույցները վկայում են, որ երկրորդաբար առաջացած լեյկոզը կարող է զարգանալ անահտական բուժումներից որոշակի քիմիոթերապիայի հետևանքով, ինչպես էպիպոդոֆիլոտոքսինից և ցիկլոֆոսֆամիդից[23][25]։
Կան որոշ ապացույցներ, որ սովորական ինֆեկցիան, ինչպիսին է գրիպի վիրուսը, կարող է անուղղակիորեն նպաստել հիվանդության առաջանալուն[11][23]։ Ուշացած վարակի վարկածը նշում է արդյունքներ ոչ նորմալ իմունային պատասխանի մասին վարակի հանդեպ գենետիկական ռիսկի գործոններ ունեցող մարդու մոտ։ Իմունային պատասխանի ուշացած զարգացումը կարող է լինել սահմանափակ հիվնդությունների դեպքում, որոնց ժամանակ լինում է լիմֆոցիտների ավելորդ արտադրություն և դրանով իսկ բարձրացնում հիվանդության առաջացման ռիսկը։ Շատ փոքր երեխաները, որոնց հանդեպ ավելի շատ է հսկողությունը, հավանականությունը ավելի է փոքրանում։ Շատ այլ ուսումնասիրություններից կան ապացույցներ, որ վարակների ազդեցությունը անհերքելի է լեյկոզի առաջացման մեջ[23]։
Մի քանի բնորոշ գենային փոփոխություններ բերում են նրան, որ առաջանում է լեյկեմիկ լիմֆոբլաստ։ Այս փոփոխությունները ներառում են քրոմոսոմալ տրանսլոկացիաները, ներքրոմոսոմային վերադասավորումները, քրոմոսոմների թվի փոփոխությունները լեյկոզային բջիջների մեջ և լրացուցիչ առանձնահատուկ գեների մուտացիանները[5]։ Քրոմոսոմային տրանսլոկացիաները ենթադրում են ԴՆԹ-ի ընդարձակ հատվածների տեղափոխումը այլ քրոմոսոմի վրա։ Այս տեղափոխության արդյունքը կարող է լինել գենի տեղադրումը մի քրոմոսոմում, որը խթանում է բջջի բաժանումը՝ ստեղծելով տրանսկրիպցիայի առավել ակտիվ շրջան։ Արդյունքը մի բջիջ է, որն ավելի հաճախ է բաժանվում։ Սրա օրինակը C-MYC գենի տրանսլոկացիան է, այն կոդավորում է տրանսկրիպցիայի գործոնը, որը ապահովում է բջջի արագացած բաժանումը։ Գտնվում է իմունոգլոբուլինների թեթև և ծանր շղթաների գենի ուժեղացնող գործոնի հարևանությամբ, բերում է ուժեղացած C-MYC էքսպրեսիային և ուժեղացած բջջի բաժանմանը[5]։ Այլ մեծ փոփոխություններ քրոմոսոմի կառուցվածքում լինում են երկու գեների միմյանց մոտ տեղակայվելու հետևանքով։ Արդյունքը երկու առանձին սպիտակուցների միաձուլումն է, որի հետևաբքով առաջանում է մեկ նոր սպիտակուց։ Այս նոր սպիտակուցը ունի նոր գործառույթ, որը խթանում է քաղցկեղի զարգացումը։ Սրա օրինակն է ETV6-RUNX1 գեների միաձուլումը, որը համակցում է երկու գործոնները, որոնք խթանում են բջջի զարգացումը և BCR-ABL1 գենի միաձուլումը և վերածվելը Ֆիլադելֆյան քրոմոսոմի։ BCR-ABL1 կոդավորում է մշտական ակտիվ թիրոզինկինազա ֆերմենտը, որը բջջի հաճախ բաժանման պատճառն է։ Այս մուտացիաները նպաստում են բջջի առավել հաճախ բաժանմանը, նույնիսկ աճի գործոնների բացակայության պայմաններում[5][11]։
Այլ գենային փոփոխություններ B բջիջներում ներառում է քրոմոսոմների թվի փոփոխություններ լեյկոզային բջիջների մեջ։ Ձեռք բերելով 5 լրացուցիչ քրոմոսոմ, դառնում են հիպերդիպլոիդ, որը տեղի է ունենում ավելի հաճախ։ Ավելի քիչ հաճախ քրոմոսոմները անհետանում են, դառնալով հիպոպլոիդ, որը ունի ավելի վատ պրոգնոստիկ նշանակություն։ B բջիջների լրացուցիչ գենային մուտացիաներից է ոչ ժառանգական մուտացիաները PAX5 and IKZF1[5]։ T բջիջների մեջ կարող են հանդիպել LYL1, TAL1, TLX1, ևTLX3 վերադասավուրումները[11]։
Հիվադությունը սկսվում է, երբ կա բավարար քանակությամբ գենետիկական փոփոխություններ լիմֆոբլաստի մեջ։ Օրինակ երեխաների մոտ լինում է մեկ միաձուլված գենի տրանսլոկացիա, որը հայտնաբերվում է 6-8 այլ նման գենային փոփոխությունների հետ[11]։ Սկզբնական լեյկեմիկ լիմֆոբլաստը կրկնօրինակում է ինքն իրեն, առաջացնելով նոր հավելյալ լիմֆոբլաստներ, որոնցից ոչ մեկ չի կարող հասունանալ և դառնալ ֆունկցիոնալ լիմֆոցիտ։ Այս լիմֆոբլաստները առաջանում են ոսկրածուծում և կարող են տարածվել ամբողջ օրգանիզմով՝ ավշային հանգույցներ, միջնորմ, փայծաղ, ամորձիներ և ուղեղ՝ ուղեկցվելով հիվանդության հիմնական ախտանշանների հետ[5]։
Ախտորոշումը սկսվում է հիվանդության պատմության մանրակրկիտ ուսումնասիրմամբ, ֆիզիկական զննությամբ, արյան ընդհանուր քննությամբ և արյան քսուքի ուսումնասիրմամբ։ Չնայած շատ ախտանշաններ կարող են լինել նաև այլ հիվանդությունների ժամանակ։ Հարատև և անբացատրելի ախտանշանները մեծացնում են քաղցկեղի կասկածը։ Քանի որ շատ հատկանիշներ բժշկական պատմության մեջ և հետազոտություններում սպեցիֆիկ չեն, հաճախ լրացուցիչ հետազոտությունների կարիք է լինում։ Արյան մեջ սպիտակ բջիջների և լիմֆոբլաստների մեծ քանակը կասկածելի է, քանի որ այն ցույց է տալիս ոսկրածուծում նրանց մեծ քանակներով արտադրությունը։ Շատ մեծ քանակների դեպքում սովորաբար պրոգնոստիկ վատ նշան է։ Արյան սպիտակ բջիջները լինում են զգալի քանակով, և ծայրամասային արյան քսուքում հանդիպում են կլինիկական դեպքերի մեծամասնության մոտ։
Ոսկրածուծի բիոպսիան տալիս է վերջնական ապացույցները, սովորաբար 20%-ից շատ լեյկեմիկ լիմֆոցիտներ։ Գոտկային պունկցիայից ստացված տվյալներով կարելի է տարբերակել արդյոք ողնուղեղը և գլխուղեղը ընդգրկված են պրոցեսի մեջ, թե ոչ։ Գլխուղեղի և ողնուղեղի ներգրավվածությունը կարող է ախտորոշվել կամ հերքվել ողնուղեղային հեղուկում լեյկեմիկ բջիջներ հայտնաբերվելու դեպքում, կամ եթե կլինիկապես առկա է ԿՆՀ-ի ախտահարման նշաններ։ Լաբորատոր քննությունները կարող են ցույց տալ նորմայից շեղված արյան պատկերը, երիկամների ֆունկցիան, էլեկտրոլիտները և լյարդի ֆերմենտների քանակը։
Ախտաբանական, բջջագենետիկական (մասնավորապես ֆիլադելֆյան քրոմոսոմի հայտնաբերում) հետազոտությունները, իմունոֆենոտիպավորումը հաստատում են արդյո՞ք լեյկեմիկ բջիջները միելոբլաստային (նեյտրոֆիլ, էոզինոֆիլ, բազոֆիլ) են, թե՞ լիմֆոբլաստային (B լիմֆոցիտ, T լիմֆոցիտ)։ Ոսկրածուծի բջջագենետիկական հետազոտությունը կարող է օգնել դասակարգել և կանխատեսել, թե ինչքան ագրեսիվ կլինի հիվանդության ընթացքը։ Տարբեր մուտացիաներ ունեն տարբեր ապրելիության ժամկետներ։ Իմունոհիստոքիմիական քննությունը կարող է հայտնաբերել TdT կամ CALLA հակածինները լեյկեմիկ բջիջների մակերեսներին։ TdT-ն դա սպիտակուց է, որը սինթեզվել է վաղ շրջանում նախա-T և նախա-B բջիջների վրա, մինչդեռ CALLA հակածինը հայտնաբերվում է բոլոր դեպքերի 80%-ի մոտ, ինչպես նաև քրոնիկ միելոլեյկոզի բլաստային կրիզի ժամանակ։
Համակարգչային շերտագրությունը կարող է հայտնաբերել լիմֆոբլաստների դեպի այլ օրգաններ ներթափանցում՝ թոքեր, լյարդ, փայծաղ, ավշային հանգույցներ, գլխուղեղ, երիկամներ և սեռական օրգաններ։
Որպես լրացում մորֆոլոգիային և բջջագենետիկային, իմունոֆենոտիպավորումը լաբորատոր տեխնիկա է բջջի մակերեսին էքսպրեսված սպիտակուցները հայտնաբերելու համար, այն ՍԼԼ-ի (սուր լիմֆոբլաստային լեյկոզ) ախտորոշման առանցքային բաղադրիչն է։ Իմունոֆենոտիպավորման նախընտրելի մեթոդը հոսանքային ցիտոմետրիան է։ Չարորակ դարձած ՍԼԼ-ի լիմֆոբլաստների մեջ տերմինալ դեօքսինուկլեոտիդի տրանսֆերազի (TdT) էքսպրեսիան բջջի մակերեսի վրա կարող է օգնել տարբերակել չարորակ դարձած լիմֆոցիտը ռեակտիվ լիմֆոցիտից։ Արյան սպիտակ բջիջները նորմալ են արձագանքում օրգանիզմում եղած վարակին։ Մյուս կողմից միելոպերօքսիդազան, որը միելոիդ ճյուղի մարկեր է, սովորաբար չի էքսպրեսվում։ Քանի որ T և B բջիջների նախորդները նման են միմյանց, իմունոֆենոտիպավորումը կարող է օգնել տարբերակել ՍԼԼ-ի ենթատեսակը և չարորակացած բջիջների հասունության աստիճանը։ ՍԼԼ-ի ենթատեսակները տարբերակվում են իմունոֆենոտիպավորումով և ըստ էության մուտացիաների աստիճանը։
| B Լիմֆոցիտ | T Լիմֆոցիտ |
|---|---|
| նախա-նախա-B ՍԼԼ (pro-B-ՍԼԼ) | նախորդող T ՍԼԼ |
| Սովորական ՍԼԼ | հասուն T-բջիջ ՍԼԼ |
| նախա-B ՍԼԼ | |
| Հասուն B-բջջային ՍԼԼ (Բերկետի լիմֆոմա - FAB L3) |
Բջջի մակերեսային մարկերների հանդեպ մոնոկլոնալ հակամարմինների ընդարձակ աղյուսակ, մասնավորապես CD կամ մարկերների տարբերակման կլաստեր, որոնք դասակարգվում են ըստ ճյուղերի։ Ստորև ՍԼԼ-ի T և B բջիջների հետ կապված իմունոլոգիական մարկերներն են։
| Իմունոլոգիական մարկերներ | B բջջային | T բջջային |
|---|---|---|
| B բջջային | ||
| CD19, CD22, CD79a | + | - |
| CD10 | - կամ + (սովորական ՍԼԼ) | |
| ցիտոպլազմատիկ Ig | - կամ + (նախա-B ՍԼԼ) | |
| մակերեսային Ig | - կամ + (հասուն B-բջջայինl Սլլ) | |
| TdT | + | + |
| T բջջային | ||
| CD2, CD3, CD4, CD5, CD7, CD8 | - | + |
| TdT | + | + |
Բջջագենետիկական հետազոտությունը ՍԼԼ-ով հիվանդ տարբեր տարիքային խմբերի մարդկանց մոտ ցույց է տվել գենետիկական անոմալիաների տարբեր համամասնություններ և հաճախություններ։ Այս տեղեկությունը մասնակի արժեք ունի դասակարգման մեջ և կարող է մասամբ բացատրել այս խմբերի տարբեր կանխատեսումները։ Դեպքերը ըստ էության շերտավորվում են ըստ քրոմոսոմային հավաքակազմի, բջջի մեջ քրոմոսոմային հավաքակազմերի թվի և յուրահատուկ գենային անոմալիաների, ինչպիսին են օրինակ տրանսլոկացիաները։ Հիպերդիպլոիդ բջիջները սահմանված են որպես բջիջներ, որոնք ունեն ավելի քան 50 քրոմոսոմ, մինչդեռ հիպոպլոիդը սահմանվում է որպես բջիջներ, որոնք ունեն ավելի քիչ, քան 44 քրոմոսոմ։ Հիպերդիպլոիդ դեպքերը հակված են պահպանելու լավ կանխատեսումը, այն ինչ հիպոպլոիդները` ոչ[26]։ Օրինակ, ամենայուրահատուկ անոմալիան երեխաների մոտ B բջջային ՍԼԼ-ի ժամանակ t(12;21) ETV6-RUNX1 տրանսլոկացիան է, որում RUNX1 գենը կոդավորում է մեկ սպիտակուց՝ ներգրավված արյունագոյացման տրանսլոկացիոն կառավարման մեջ և որը ճնշվում է ETV6-RUNX1 ձուլված սպիտակուցով[27]։
Ստորև տրված է բջջագենետիկական տրանսլոկացիաների և գենային անոմալիաների հաճախությունների աղյուսակը։
| Բջջագենետիկական տրանսլոկացիա | Գենային անոմալիաներ | % |
|---|---|---|
| կրիպտային t(12;21) | TEL–AML1 միաձուլում[28] | 25.4%[29] |
| t(1;19)(q23;p13) | E2A–PBX (PBX1) միաձուլում | 4.8%[29] |
| t(9;22)(q34;q11) | BCR-ABL միաձուլում(P185)[30] | 1.6%[29] |
| t(4;11)(q21;q23) | MLL–AF4 միաձուլում[31] | 1.6%[29] |
| t(8;14)(q24;q32) | IGH-MYC միաձուլում[32] | |
| t(11;14)(p13;q11) | TCR–RBTN2 միաձուլում[33] |
Ֆրանսիական-ամերիկյան-բրիտանական
Պատմականորեն՝ 2008 թվականից առաջ, ՍԼԼ-ն դասակարգվել է մորֆոլոգիորեն, օգտագործելով ֆրանս-ամերիկա-բրիտանական (ՖԱԲ) համակարգը, որը մեծ մասամբ հիմնվում էր մորֆոլոգիական գնահատականի վրա։ ՖԱԲ համակարգը տեղեկություն է տալիս չափի, ցիտոպլազմայի, կորիզակի, բազոֆիլիայի (ցիտոպլազմայի գույն) և վակուոլների (պղպջակի նման ներառումներ) մասին[34][35]։
| ՖԱԲ ենթատիպ | Բջջի տեսակ | Բնորոշում | Մեկնաբանություն |
|---|---|---|---|
| ՍԼԼ - L1 | T կամ նախա-B բջիջներ | փոքր և հոմոգեն (բազմաձև) բջիջներ | |
| ՍԼԼ - L2 | T կամ նախա-B բջիջներ | մեծ և հետերոգեն (բազմազան) բջիջներ | |
| ՍԼԼ - L3 | B բջիջ | մեծ և բազմազան բջիջներ վակուոլներով | ՍԼԼ-ի հասուն B բջիջներ, որը կոչվում է նաև Բերկետի լիմֆոմա. Սովորաբար լավ կանխատեսում՝ ստանդարտ բուժումով |
Որոշ կլինիցիստներ դեռ օգտագործում են ՖԱԲ սխեման ուռուցքային բջջի տեսքի նկարագրման համար։ Այս դասակարգումներից շատերը մոռացվել են պրոգնոստիկ արժեքի և բուժման ընտրության վրա սահմանափակ ազդեցության պատճառով[36]։
Առողջապահության համաշխարհային կազմակերպություն
2008 թվականին Առողջապահության համաշխարհային կազմակերպության ստեղծել է սուր լիմֆոբլաստային լեյկոզի դասակարգման համակարգ, որը կլինիկապես ավելի համապատասխան է և կարող է տալ պրգնոստիկ և բուժական որոշումներ։ Այս համակարգը ճանաչում է գենային, իմունոֆենոտիպային, մոլեկուլյար և մորֆոլոգիական հատկությունների տարբերությունները, որոնք հայտնաբերվում են բջջագենետիկական և մոլեկուլյար ախտորոշման միջոցով[37][38]։ Այս ենթատեսակավորումը օգնում է կանխատեսմանը և ամենահամապաատասխան բուժման կիրառմանը ՍԼԼ-ի ամեն դեպքի համար։
ՍԼԼ-ի ենթատեսակները ըստ ԱՀԿ-ի[39]։

Բուժման նպատակը տևական ռեմիսիայի ստացումն է՝ սահմանված որպես քաղցկեղային բջիջների բացակայություն օրգանիզմում (սովորաբար 5%-ից քիչ բլաստ բջիջ ոսկրածուծում)։
Մինչև վերջին մի քանի տասնամյակները, կատարվում են քայլեր բուժման ռեժիմի արդյունավետության բարձրացման ուղղությամբ, որի արդյունքը ապրելիության բարձրացման հաճախացումն է։ Սուր լիմֆոբլաստային լեյկոզի հնարավոր բուժումները ներառում են քիմիոթերապիան, ստերոիդները, ճառագայթային բուժումը, համակցված ինտենսիվ բուժում(ներառում է ոսկրածուծի կամ ցողունային բջիջների փոխպատվաստում), և/կամ աճման գործոններ[40]։
Քիմիոթերապիան նախնական ընտրության բուժում է, և շատ ՍԼԼ-ով հիվանդներ ստանում են համակցված դեղեր։ Չկան վիրաբուժական ցուցումներ կապված չարորակ բջիջների սերմնացրման վտանգի հետ։ ՍԼԼ-ի ցիտոտոքսիկ քիմիոթերապիան գերազանցապես ներառում է բազմաթիվ համակցված հակալեյկեմիկ դեղեր, որոնք համապատասխանեցված են ամեն հիվանդին։ ՍԼԼ-ի քիմիոթերապիան պարունակում է 3 փուլ՝ ախտադադարի ինդուկցիա, ինտենսիվացում, ընթացիկ բուժում։
| Փուլ | Նկարագրություն[41][42] | Բաղադրիչներ[41][42] |
|---|---|---|
| Ախտադադարի ինդուկցիա | Նպատակը՝
Պետք է հետևել ուռուցքի քայքայման համախտանիշին սկզբնական բուժումից հետո։ Առաջնային բուժման պատասխանին հետևելը կարևոր է, քանի որ որպես բուժման ձախողում արյան և ոսկրածուծի մեջ երևում են բլաստ բջիջներ բուժման առաջին 2 շաբատնեիրի ընթացքում։ Դա կապված է հիվանդության կրկնության բարձր ռիսկի հետ։
Սկսել ԿՆՀ պրոֆիլակտիկ ներողնուղեղային քիմիոթերապիա կամ բազմակի ողնուղեղային պունկցիաներ
|
համակցում՝
Կենտրոնկան նյարդային համակարգի պրոֆիլակտիային կարելի է հասնել[43]՝
Ֆիլադելֆյան քրոմոսոմ դրական ՍԼԼ, սկզբնական բուժման ինտենիվությունը կարող է ավելի քիչ քան սովորաբար տրվողը[44][45]։ |
| Համախմբում / ինտենսիվացում | Օգտագործել բարձր դոզայով քիմիոթերապիա ուռուցքայինն բջիջների ոչնչացման նպատակով։ | Տիպային գործելակերպերում օգտագործվում են վերոնշյալներից կազված բլոկներով (տատանվում է 1-3 բլոկների մեջ կախված հիվանդի ռիսկի խմբից) տարբեր դեղերի համակցումներով՝
Կենտրոնական նյարդային համակարգը բուժվում է ներողնուղեղային հիդրոկորտիզոնի, մեթոտրեքսատի և ցիտառաբինի ներմուծումով։ |
| Աջակցող բուժում | Քայքայել ամեն մնացորդային բջիջ, որը չի քայքայվել նախորդ փուլերի ընթացքում
|
Տիպիկ գործելակարգԹ պետք է ներառի՝
|
Քանի որ 10-40% մեծահասակների մոտ աղտորոշվում է ԿՆՀ-ի ներգրավվածություն, շատ մասնագետներ սկսում են կենտրոնական նյարդային համակարգի(ԿՆՀ) պրոֆիլակտիկ բուժում սկզբնական փուլում և շարունակում են բուժումը ինտենսիվ թերապիայի փուլում։
Մեծահասակների քիմիոթերապիաի ռեժիմը նմանակում է երեխաներին, սակայն ավելի բարձր է հիվանդության կրկնության ռիսկը միայն քիմիոթերապիայով։ Պետք է իմանալ, որ ՍԼԼ-ի 2 ենթատեսակները(B-բջջային ՍԼԼ և T-բջջային ՍԼԼ) պահանջում են հատուկ նկատառումներ, երբ համապատասխանեցում են ճիշտ բուժման ռեժիմը մեծահասակների մոտ։ B-բջջային ՍԼԼ-ը հաճախ կապված է բջջագենետիկական անոմալիաների հետ (հատկապես, t(8;14), t (2;8) և t(8;22)), որը պահանջում է ագրեսիվ թերապիաների կարճ դրվագներ, մեծ հաճախությամբ։ T-բջջային ՍԼԼ-ի վրա ազդում են ցիկլոֆոսֆամիդ պարունակող պրեպարատներ[42]։
Քիմիոթերապևտիկ ռեժիմը կարող է լինել ինտենսիվ և երկարատև։ Շատ հիվանդներ ունեն ներերակային կաթետերներ տեղադրված մեց երակի վրա(կոչվում է կենտրոնական երակային կաթետեր կամ Հիքմանի ուղի), կամ պորտակաթ, սովորաբար տեղակայվում է անրակի շրջանում, վարակի առավել ցածր ռիսկի և երկար օգտագործման համար։
Տղամարդիկ սովորաբար ավելի երկար բուժվում քան կանայք, քանի վոր ամորձիները կարող են հանդիսանալ քաղցկեղի ռեզերվուար։
Ճառագայթային օգտագործվում է ցավոտ ոսկրերի շրջանում, հիվանդության ծանր ընթացքի դեպքւմ, կամ որպես պատրաստություն ոսկրածուծի փոխպատվաստման համար։ Անցյալում, բժիշկները սովորաբար օգտագործում էին ճառագայթումը ամբողջ գլխուղեղի ճառագայթման տեսքով, որպես կենտրոնական նյարդային համակարգի պրոֆիլակտիկա և/կամ գլխուղեղում կրկնվող լեյկոզի բուժում։ Վերջերս ուսումնասիրությունները ցույց են տվել,որ ԿՆՀ-ի քիմիոթերապիաից ստացված արդյունքները բարենպաստ են, բայց ավելի քիչ կողմնակի էֆեկտներով։ Որպես հետևանք ամբողջ գլխուղեղի ճառագայթումը սահմանափակված է։ Շատ մասնագետներ մեծահասակների լեյկեմիաների ժամանակ դադարեցին կիրառել ճառագայթային բուժումը ԿՆՀ-ի պրոֆիլակտիկայի նպատակով, փոխարենը օգտագործելով ներողնուղեղային քիմիոթերապիա[46][47]։
Կենսաբանական թիրախների ընտրությունը՝ լեյկոզային լիմֆոբլաստների վրա ունեցած համակցական ազդեցության հիմքի վրա, կարող է ուղղորդել կլինիկական փորձերի բարելավումը ՍԼԼ-ի բուժման մեջ[48]։ Թիրոզինկինազայի ինհիբիտորները, ինչպես իմատինիբը, հաճախ ներառվում են բուժման պլանի մեջ այն հիվամդմերի մոտ որոնք ունեն Bcr-Abl1+ (Ֆիլադելֆյան+) ՍԼԼ։ Բայց ՍԼԼ-ի այս ենթատեսակը հաճախ կայուն է քիմիոթերապիաի և թիրոզին կինազայի ինհիբիտորների համակցմանը, և ալոգենային ցողունային բջիջների փոխպատվաստումը հաճախ խորհուրդ է տրվում ախտադարձությունից հետո[46]։
Բլինատումոմաբը CD19-CD3 երկսպեցիֆիկ մոնոկլոնալ մկնային հակամարմին է, և ներկայումս բավականին խոստումնալից է, որպես նոր դեղային բուժում։ Կապելով CD3 T-բջիջները B բջիջների CD19 ռեցեպտորներ հետ, այն խթանում է բորբոքային ցիտոկինների և բջջատոքսիկ սպիտակուցներ արդադրությունը, ինչպես նաև T բջիջների պրոլիֆորացիան CD19 B բջիջներին քայքայելու համար[42][47]։
Խիմերիկ անտիգենային ռեցեպտորները (ԽԱՌ) զարգացալ են որպես խոստումնալից իմունոթերապիա ՍԼԼ-ի համար։ Այս տեխնոլոգիան օգտագործում է միաշղթա փոփոխական ֆրագմենտ (մփվ), որը նախագծված է CD19 մակերեսային մարկեր ճանաչելու միջոցով ՍԼԼ-ի բուժման մեթոդ[49]։
CD19 մոլեկուլը հայտնաբերվում է բոլոր B բջիջների մոտ և կարող է օգտագործվել որպես չարորակացած B բջիջների տարբերակիչ։ Այս բուժման խամանակ մկները իմունիզացվում են CD19 անտիգենով և սկսում են արտադրել հակա-CD19 հակամարմիններ։ Հիբրիդոմաները զարգանում են մկան փայծաղում, որը հարուստ է միելոմային բջիջներով, որն էլ իր հերթին CD19 սպեցիֆիկ հակամարմիններ են ԴՆԹ-ով կոդավորված[50]։ ԴՆԹ-ն հաջորդականորեն կոդավորում է միմյանց կլոնավորող հակամարմինների փոփոխական ծանր և թեթև շղթաները օգտագործելով փոքր պեպտիդային ֆերմենտ։ Այս հաջորդականությամ կոդավորվում է մփվ-ն։ Սա կարող է կլոնաորվել տրանսգենի, որը կոդավորելով դառնում է ԽԱՌ-ի դոմեն։ Ենթակառուցվածքների տարբեր համաձայնեցումները ծառայում են որպես դոմեն, բայց նրանք հիմնականում պարունակում են դեպի մփվ կախված հատված, տրանսմեմբրանային հատված, ներբջջային խթանող մոլեկուլի հատված ինչպիսին է CD28-ը, և CD3-զետա պարունակող ներբջջային դոմեն որը պարունակում է իմունոռեցեպտոր թիրոզինային խթանիչի կրկնություններ։ Այլ հաջորդականությունների մեջ հաճախ ներառված են 4-1bb և OX40[51]։ Վերջնական տրանսգենային հաջորդականությունը պարունակում է մփվ և դոմենային հաջորդականությունը, որը հետո ներառվում է իմունային էֆեկտոր բջիջների բջիջների մեջ, որոնք ձեռք են բերվել հիվանդից և ընդլայնվված են լաբորատոր պայմաններում(in vitro): Փորձարկումներում դրանք ցիտոտոքսիկություն ընդունած T բջիջներ եղել[52]։
ԴՆԹ-ի ներմուծումը ազդող բջջի մեջ կարող է իրականացվել մի քանի եղանակներող։ Շատ հաճախ, այն կատարվում է օգտագործելով լենտիվիրուս, որը կոդավորում է տրանսգենը։ Կեղծ տպված, ինքնաինակտիվացնող լենտիվիրուսը արդյունավետ մեթոդ է ցանկալի տրանսգենը թիրախ բջջի մեջ կայուն ներդնելու համար[53]։ Այլ մեթոդները ներառում են էլեկտրոպորացիա և տրանսֆեկցիա, բայց սրանք սահմանափակ են իրենց արդյունավետության մեջ, քանի որ շատ ժամանակ տրանսգենի էքսպրեսիան նվազում է։
Գեները փոփոխված ազդող բջիջները հետո հետ են փոխպատվաստվում հիվանդին։ Սովորաբար այս գործընթացը կատարվում է միացվում է պայմանական կուրսով, ինչպիսին է ցիկլոֆոսֆամիդը, որը ցույց է տրվել T բջիջների ազդեցությունները ուժեղացնելու համար։ Այս ազդեցությունը վերագրվում է իմունոլոգիական ծավալ պոպւլյացված բջիջների ներսում[51]։ Այս ամեն ինչի արդյունքը ազդող բջիջ է, սովորաբար T բջիջ, որը կարող է ճանաչել ուռուցքային բջջի հակածինը մեծ հյուսվածահամատեղելիության կոմպլեքսից անկախ և որը կարող է սկսել բջջատոքսիկ պատասխանը։
2017 թվականին tisagenlecleucel հաստատվեց դեղերի և սննդի վարչության(FDA) կողմից՝ որպես ԽԱՌ-T բուժում B բջջային լիմֆոբլաստային լեյկոզով այն հիվանդների համար, որոնք չեն չեն արձագանքում այլ բուժումների կամ հիվանդությունը կրկնվել է[54]։ 22 օրվա ընթացքում «դեղը» հարմարեցվում է ամեն հիվանդի համար։ T բջիջները զտվում են ամեն հիվանդի համար, որը մոդիֆիկացված է վիրուսի կողմից։ Ընդ որում վիրուսը ներդրել է խիմերիկ հակածնի ԴՆԹ-ն T բջջի մեջ,որը ճանաչում է լեյկոզային բջիջներին[55]։
Սովորաբար մարդիկ՝ ովքեր ունեցել են ՍԼԼ-ի կրկնություն իրեն սկզբնական բուժումից հետո, ունեն ավելի վատ կանխատեսում քան այն մարդիկ ովքեր մտել են լիարժեք ռեմիսիայի մեջ սկզբնական բուժումից հետո։ Սա ցանկալի չէ, քանի որ կրկնվող լեյկեմիան ստանդարտը քիմիոթերապիաի ռեժիմով արդեն իրականացվել է և փոխարենը հիվանդները պետք է ենթարկվեն քիմիոթերապիաին ալոգենային ոսկրածուծի տրանսպլանտացիայից հետո։ Այս հիվանդները կրկնության ժամանակ կարող են նաև ստանալ բինատումոմաբ,քանի որ նա ցույց է տալիս ռեմիսիաի հաճախականության աճ և ընդհանուր ապրելիության երկարում առանց թունավոր ազդեցության աճի[56]։
Ցածր դեղաչափերով պալիատիվ ճառագայթումը կարող է օգնել թեթևացնել ԿՆՀ-ի ախտահարման աստիճանը և մեղմացնել որոշ ախտանշաններ։
Վերջերս կան նաև շատ ակնհայտ և հաստատ օգտագործում են դասատինիբ՝ թիրոզին կինազայի ինհիբիտոր։ Այն արդյունավետ է եղել այն Ֆ1- դրական և իմատինիբ կայուն ՍԼԼ-ի ժամանակ, բայց ավելի շատ հետազոտությունների կարիք ունի, որպեսզի երկարի ապրելիությունը և ախտադար ժամկետը[42][57]։
Նախքան քիմիոթերապիայի և արյունաստեղծ ցողունային բջիջների տրանսպլանտացիայի զարգացումը, երեխաների ապրելիության միջին երկարությունը 3 ամիս էր, մեծ մասամբ ինֆեկցիայի արյունահոսության պատճառով։ Քիմիոթերապիայի հայտնվելը, մանկական լեյկոզի կանխատեսումը մեծապես բարելավվել է և ՍԼԼ-ով հիվանդ երեխաները ունեն 95% հավանականություն բարեհաջող ախտադադարի հասնել 4 շաբաթ սկզբնական բուժումից հետո։ ՍԼԼ-ով հիվանդ մանկահասակների 80%-ը զարգացած երկրներում ունեն 5 տարուց ավել ապրելիություն։ Մոտ 60-80% մեծահասակներ սկզբնական քիմիոթերապիայից հետ հասնում են ախտադադարի 4 շաբաթ անց, և նույնիսկ 70 տարեկան հասակում կան 5% բուժվածներ[41][58]։

Սակայն ՍԼԼ-ի համար կան շատ տարբեր կանխատեսումներ կախված տարբեր գործոննրից՝
| Գործոն | Անբարենպաստ | Բարենպաստ |
|---|---|---|
| Տարիք | <2 կամ >10 տարեկան | 3–5 տարեկան |
| Սեռ | արական | իգական |
| Ռասսա | սևամորթ | կովկասցիներ |
| Օրգանի չափի մեծացում | առկա է | առկա չէ |
| Միջնորմային զանգված | առկա է | առկա չէ |
| ԿՆՀ-ի ներգրավվածություն | առկա է | առկա չէ |
| Լեյկոցիտների թիվ | B-ՍԼԼ >30,000մմ3 T-ՍԼԼ >100,000մմ3 | ցածր |
| Hemogblobin concentration | >10դ/դլ | <10գ/դլ |
| Բջջի տիպ | ոչ լինֆոիդ | լիմֆոիդ |
| Բջջի նախորդ | նախա B բջիջ +
T-ՍԼԼ (երեխաներ) |
վաղ նախա-B բջիջ |
| Կարիոտիպ | տրանսլոկացիա | հիպերդիպլոիդիա |
| Բուժման նկատմամբ պատասխանն | դանդաղ
>1 շաբատից շատ արյան միջից բլաստների մաքրում |
արագ
<1 շաբատից քիչ արյան միջից բլաստների մաքրում |
| Մինչև ախատադադարի ժամանակը | >4 շաբաթ | <4 շաբաթ |
| Նվազագույն ախտադադարի տևողություն | Դրական է 3-6 ամիսների դեպքում | Բացասական է 1 ամիս(երեխաների) և 3 ամիս (մեծահասակների) դեպքում |
Բջջագենետիկան ուսմունք է քրոմոսոմներին բնորոշ մեծ փոփոխություններով քաղցկեղային բջիջներում և շատ կարևոր ելքի կանխատեսում է[63]։ Որոշ բջջագենետիկական ենթտեսակներ ունեն շատ ավելի վատ կանխատեսումներ քան մնացածը։ Դրանք ներառում են[17]՝
| բջջագենետիկական փոփոխություն |
Ռիսկի կատեգորիա |
|---|---|
| Ֆիլադելֆյան քրոմոսոմ | վատ կանխատեսում |
| t(4;11)(q21;q23) | վատ կանխատեսում |
| t(8;14)(q24.1;q32) | վատ կանխատեսում |
| Կոմպլեքս կարոտիպ (ավելի քան 4 անոմալիաներ) | վատ կանխատեսում |
| Ցածր հիպոդիպլոիդիա կամ տրիպլոիդիա | վատ կանխատեսում |
| 7-րդ քրոմոսոմի կորուստ | վատ կանխատեսում |
| 8-րդ քրոմոսոմի տրիսոմիա | վատ կանխատեսում |
| Բարձր հիպերդիպլոիդիա(4-րդի, 7-րդի,10-րդի տրիսոմիաներ ) | լավ կանխատեսում |
| del(9p) | լավ կանխատեսում |
| Կանխատեսում | Բջջագենետիկայի արդյունքներ |
|---|---|
| Բարենպաստ | հիպերդիպլոիդիա > 50 ; t (12;21) |
| Միջանկյալ | հիպերդիպլոիդիա 47–50; նորմալ(դիպլոիդիա); del (6q); 8q24-ի վերադասավորումներ |
| Անբարենպաստ | Հիպերդիպլոիդիա- գրեթե հապլոիդիա; գրեթե տետրապլոիդիա; del (17p); t (9;22); t (11q23) |
Չդասակաորգվող ՍԼԼ-ն համարվում է միջանկյալ պրոգնոստիկ ռիսկ[64], լավ և վաատ կանխատեսումնորի միջև։
2015 թվականի սուր լիմֆոբլաստային լեյկոզով ախտահարված էր շուրջ 876,000 մարդ և նրանցից 111,000-ը մահվան ելքով[9]։ Այն հանդիպում է երեխաների և մեծահասակների մոտ և հաճախ 3ից 7 տարեկան հասակում․ Շուրջ 75% դեպքում հանդիպում է մինչև 6 տարեկանը, հաջորդ ռիսկի աճման շրջանը լինում է 40 տարեկանից հետո[41]։ Ամեն 1500 երեխայից մեկը ախտահարվում է։
Հաշվարկելով ամենամյա ախտահարվածների տարիքային ընդարձակ խումբը՝ ՍԼԼ-ն հանդիպում է 1,7 դեպքերում 100,000-ից։ ՍԼԼ ներկայացվում է մոտավորապես 20% մեծահասակների և 80% երեխաների մոտ, հանդիսանալով առավել հաճախ որպես մանկական քաղցկեղ։ Չնայած 80-ից 90%-ը երեխաների կունենա երկարաժամկետ ռեմիսիայի շրջան[37], այն կմնա քաղցկեղ ուղղորդված մանկական մահերի առաջատար պատճառը[65]։ Դեպքերի 85%-ը B բջջային տիպի է և հավասար են դեպքերը տաղաների և աղջիկների համար։ Մնացած 15%-ը T բջջային է և գերակշռողը տղաներն են։
Լեյկոզը հազվադեպ է միացած լինում հղիության հետ ախտահարելով շուրջ 1 հղիի 10000 հղիների միջից[66]։ Լեյկոզների վարումը հղիությաան ընթացքում առաջին հերթին կաղված է լեյկոզի տիպից։ Սուր լեյկոզները նորմայում պահանջում են արագ և ագրեսիվբուժում, չնայած հղիության ընդհատման և հետծննդյան արատների էական ռիսկին, հատկապես երբ քիմիոթերապիան կատարվում է զարգացման առաջին զգայուն եռամսյակում[66]։
Seamless Wikipedia browsing. On steroids.
Every time you click a link to Wikipedia, Wiktionary or Wikiquote in your browser's search results, it will show the modern Wikiwand interface.
Wikiwand extension is a five stars, simple, with minimum permission required to keep your browsing private, safe and transparent.