מלריה
מחלה זיהומית הנגרמת על ידי פלסמודיום מוויקיפדיה, האנציקלופדיה החופשית
מָלַרְיָה (בלטינית: Malaria; או קדחת הביצות) היא מחלה זיהומית הנפוצה בעיקר באזור הטרופי.
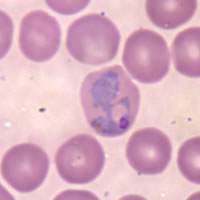 | |
| תא דם אדום נגוע ב-P.vivax | |
| תחום | מחלות זיהומיות |
|---|---|
| גורם | פתוגן, בפסקה זו 4 רשומות נוספות שטרם תורגמו |
| תסמינים | intermittent fever, צהבת, תרדמת, צמרמורת, splenomegaly, hepatomegaly, אנמיה, periodic fever, חום |
| טיפול |
|
| קישורים ומאגרי מידע | |
| eMedicine | article/221134 |
| DiseasesDB | 7728 |
| MeSH | D008288 |
| MedlinePlus | 000621 |
| OMIM | 248310 |
| סיווגים | |
| ICD-10 | B50 |

המלריה היא אחד מגורמי המוות העיקריים בעולם, בפרט בקרב ילדים בעולם השלישי. ב-2009 חלו במלריה 225 מיליון אנשים, וב-2010 מתו ממנה 655 אלף חולים. ב-2018 מעריכים כי חלו במלריה כ-228 מיליון בני אדם ומתוכם מתו כ-405,000, רובם בני פחות מ-15. רוב מקרי המוות ממלריה הם באפריקה שמדרום לסהרה[1].
המלריה מופצת על ידי יתושות אנופלס ופוגעת בעיקר בכדוריות הדם האדומות. במקרים קשים, נגרם נזק גם לאיברים חיוניים בגוף עקב אנמיה וחסימת כלי דם.
היצור החד-תאי הגורם למלריה, Plasmodium, נתגלה על ידי שארל לואי אלפונס לבראן (Charles Louis Alphonse Laveran), שהיה רופא בצבא הצרפתי, ועל גילוי זה הוענק לו פרס נובל לפיזיולוגיה ולרפואה ב-1907. פרס נובל נוסף לרפואה הוענק ב-1947 לפאול הרמן מילר, שגילה ב-1939 את תכונותיו של ה-די-די-טי כקוטל חרקים, לאחר שחומר זה שימש למניעת מלריה על ידי הדברת יתושים. בשנת 2015 הוענק עוד פרס נובל לפיזיולוגיה ולרפואה לטו יויו על גילוי החומר ארטמיסינין, המשמש תרופה למלריה.
אטימולוגיה
מקור המונח מלריה באיטלקית מימי הביניים: mala aria — "אוויר רע", חלק מתורת מיאזמה; המחלה נקראה בעבר קדחת ביצות בשל הקשר שלה עם ביצות ואדמות ביצות. המונח הופיע באנגלית לפחות כבר ב-1768. מלריה הייתה פעם שכיחה ברוב אירופה וצפון אמריקה, שם היא כבר לא אנדמית, אם כי מקרים מיובאים מתרחשים.
גורמי המחלה
המלריה בבני אדם נגרמת על ידי חמישה מינים של הפרוטיסט החד-תאי פלסמודיום (Plasmodium), ממערכת הנבגוניות. זוהי המחלה הקטלנית ביותר הנגרמת על ידי פרוטיסט.
שני המינים הנפוצים הם Plasmodium falciparum (המסוכן ביותר) ו-P. vivax; מינים נוספים, נפוצים פחות הם P. ovale, P. malariae ו-P. knowlesi. טפיל זה מועבר על ידי יתוש האנופלס. היתושה (תמיד נקבה) מוצצת דמו של אדם נגוע; אחרי שמונה ימים של התפתחות הפלסמודיום בגופה הוא מצוי בבלוטות הרוק שלה (שם ישכון עד מותה), זמין להעברה.
תסמינים
התסמינים של המלריה כוללים חום גבוה, רעד, כאבי מפרקים, כאב ראש עז, הקאות העשויות להכיל דם, הזעה מרובה, צמרמורת, שלשול, כאבי בטן והרגשה כללית לא טובה. עלולה גם להיות הרגשה של דקירות בעור וחוסר סוכר בדם, בעיקר במלריה הנגרמת מ-P. falciparum. תסמינים אלה מופיעים במחזוריות של יומיים עד ארבעה ימים.
סיבוכים של מלריה כוללים תרדמת, ובכ-20% מהמקרים של מלריה לא מטופלת - מוות. ילדים צעירים פגיעים במיוחד.
פתופיזיולוגיה
סכם
פרספקטיבה
יתושות אנופלס נושאות נבגי פלסמודיום בבלוטות הרוק שלהן. כאשר הן עוקצות אדם, דבר הנפוץ בעיקר בשעת בין הערביים ובלילה, הספורוזואיטים נכנסים לגוף דרך הרוק של היתושה, נודדים לכבד ומתרבים בתאי הכבד. בשלב המרוזיטי (merozoites) הם מגיעים לתאי הדם האדומים, שם הם מתרבים, ניזונים מהמוגלובין ומפרישים רעלנים. ומזמן לזמן פורצים אל תוך הגוף. הקדחת מתפרצת מדי שלושה או ארבעה ימים, עם יציאת המרוזויטים מתאי הדם. כאשר יתושה עוקצת אדם הנגוע במלריה, הטפיל מגיע עם הדם אל קיבתה, מתרבה שם ועובר לבלוטות הרוק שלה.
הטפיל מוגן יחסית מתגובת הנגד של המערכת החיסונית כיוון שהוא נמצא בכבד ובתאי הדם האדומים. עם זאת, תאי דם שהודבקו במחלה ונעים בחופשיות מושמדים בטחול. למניעת גורל זה הטפיל מייצר ציפוי חלבוני המקשה על הפעולה החיסונית.
בשנת 2002 הודיע צוות חוקרים כי הצליח לפענח בו זמנית את הגנום של כל הגורמים למחלה. החוקרים פענחו את הגנום של סוג טפיל המלריה הנפוץ והמסוכן ביותר - P. falciparum - ואת זה של יתוש האנופלס גמביה, המשמש נשא המעביר את הטפיל באפריקה.
בשנת 2012 חוקרים מצאו כי הטפיל הגורם למלריה בבני אדם משפר את יכולות יתושות אנופלס לשרוד רעב ממושך ובכך מקנה ליתושות שנדבקו בו יתרון על פני אחרים. באותה השנה הצליחו חוקרים מהאוניברסיטה העברית להבין את מנגנון ההסוואה של הטפיל מהמערכת החיסונית[2], הטפיל מסוגל להציג למערכת החיסון חלבון אחד בעוד הוא תוקף את הגוף בחלבון אחר וכך מתחמק מגילויו.
תולדות המחלה
סכם
פרספקטיבה
המלריה תוארה כבר על ידי היפוקרטס במאה החמישית לפנה"ס. בימי הביניים ניתן לה השם "מלריה" - הֶלְחֵם של המילים באיטלקית של אותה תקופה: "מלה אריה" (mala aria) שפירושן: "אוויר רע", שכן חשבו שהיא נגרמת מהאוויר העולה מהביצות. כבר במאה הראשונה לספירה כתבו קולומלה וארו שמקור המחלה הוא דווקא מ"בעלי חיים קטנים" החיים בביצות, והמחלה מועברת דרך האוויר. בשנת 1897, גילה רונלד רוס כי מלריה מועברת באמצעות נקבת היתוש מהסוג אנופלס. הרופא הצרפתי שארל לואי אלפונס לבראן גילה בשנת 1880 כי המחלה נגרמת על ידי טפיל הנמצא בתאי הדם האדומים של החולים.
תרופת הכינין הומצאה בידי אינדיאנים מפרו, אשר למדו כי משקה מקליפת עץ הכינין מועיל לחולים. המידע עבר למערב באמצעות איש דת ישועי. בעבר חשבו שלכינין יש גם תועלת מניעתית, אך הדבר התברר כלא נכון.
במדינות המתועשות כבר כמעט שלא קיימת מלריה[3], אבל במדינות המתפתחות היא עדיין גורמת לסבל רב.
בספרות היהודית ההיסטורית ניתן למלריה בדרך כלל הכינוי "קדחת".
בנטיעת האקליפטוסים קיוו החלוצים בארץ ישראל לבער את הביצות ואת יתושי האנופלס נושאי המלריה, מתוך הנחה מוטעית כי המלריה נגרמת מ"אוויר רע" העולה מהביצות, שאותו יטהר העץ ואף יסייע לייבוש הביצות. מאוחר יותר נוכחו כי השפעת האקליפטוס על הביצות שולית והמלריה מופצת על ידי יתושות אנופלס, והוחל בניקוז הביצות[4].
בשנים הראשונות שאחרי קום המדינה דווח על 1,000 חולים חדשים בשנה (יותר מפרומיל מהאוכלוסייה). השימוש ב-DDT ובאמצעים אחרים הביא להקטנת התחלואה, וזה ארבעים שנה אין בישראל מלריה מקומית. כמעט אין יתושי אנופלס ואין חולים שמהם ירכשו היתושות את הטפיל. עם זאת, כמה עשרות חולים מאובחנים בישראל מדי שנה, רובם ישראלים שבאו מאפריקה, שם תיירו או משם היגרו. מיעוטם הם תרמילאים ששבו מהמזרח הרחוק, בדרך כלל כאלו שלא הקפידו על טיפול הולם בעת שהותם באזורים נגועים.
בוונצואלה אושר ב-1936 חוק ההגנה ממלריה[5]. באותה תקופה החל לנהל את הקמפיין נגד מלריה הרופא ארנולדו גבלודון (Arnoldo Gabaldón). במסגרת הקמפיין להדברת המלריה, שהתמקד תחילה באזורים העירוניים שבהם היה כלכלי יותר לבצעו, ערכו הרשויות טיפולים להדברת יתושים ובפרט הדברה באמצעות פירטרינים ובהמשך שימוש ב-DDT. הקמפיין הצליח לצמצם מאוד את ההידבקות במלריה, וב-1961 הכריז ארגון הבריאות העולמי על הדברתה של המלריה מ-68% מאזור המלריה בוונצואלה[5]. בעקבות המשבר הכלכלי שחוותה ונצואלה בעשור השני של המאה ה-21, ועימו גל הגירה פנימית, אירעה התפרצות של מלריה[6].
דרכי טיפול
התרופות לקדחת מבוססות על הכינין, המופק מקליפתו של עץ הכינין או על כינין המיוצר ייצור סינתטי. הכינין היה ידוע בעבר כטיפול הידוע היחיד למלריה. קשה לרפא באמצעות תרופות אלה את הפלסמודיום, ולשם כך נדרשות תרופות נוספות.
מניעת המחלה
סכם
פרספקטיבה

האמצעי היעיל ביותר להילחם במלריה המתפשטת בקרב האוכלוסייה הוא לחסל את הדגירה של יתושי האנופלס על ידי ריסוס מקומות הדגירה, ייבוש הביצות, החדרת דגי גמבוזיה למקווי המים על מנת שיטרפו את הרימות והביצים של היתושים או, כמוצא אחרון, כיסוי הביצות בשכבת נפט שאינה מאפשרת לרימות היתושים לנשום וקוטלת אותן.
מניעת הידבקות במלריה היא אחת המטרות המרכזיות של מערכות הבריאות באפריקה שמדרום לסהרה בגלל היקף התמותה ממלריה ובהיעדר חיסון כנגדה.
בשנת 2021, אישר ארגון הבריאות העולמי חיסון נגד מלריה[7]. לפני כן, החיסון אושר על ידי הסוכנות האירופית לתרופות בשנת 2015[8].
התגוננות אישית
דרכי התגוננות אישית לנמצאים באזורים נגועי מלריה כוללים:
- הקפדה על שינה מתחת לכילות, רישות חלונות, מריחת הגוף בחומר דוחה יתושים, לבישת בגדים ארוכים והימנעות מיציאה בלילה, מכיוון שהיתושים פעילים בעיקר בשעות הקרירות של הלילה.
- נטילת תרופות התגוננות ממלריה במהלך השהיה באזור הנגוע.
תרופות
הדרך היעילה ביותר להתגוננות אישית מפני מלריה באזורים נגועים היא נטילת תרופות המיועדות לכך. קיימות תרופות המקנות 90%-95% הגנה מפני כל סוג של מלריה. סוג התרופה הניתנת תלוי באזור השהות היות שבכל אזור קיים סוג שונה של הטפיל. תרופת המנע נלקחת החל מיום לפני הכניסה לאזור נגוע במלריה ועד ארבעה שבועות לאחר היציאה מהאזור. התרופה החדשנית והיעילה ביותר נקראת "מלרון" אשר מאופיינת במיעוט תופעות לוואי (נוסף על כך קיימות תרופות כגון מפלוקווין, מלרון, כלורוקווין, דוקסילין). מנגנון הפעולה של תרופות אלו פוגע ביכולת ההתרבות של הטפיל הגורם למלריה.
שימוש בתרופות הוא דרך יעילה להימנעות מהידבקות במחלה אצל מטיילים, שמשך שהייתם באזור הוא זמני ומוגבל. אולם תושבים באזורים נגועי מלריה אינם יכולים פרקטית וכלכלית ליטול את התרופות במשך כל ימי חייהם. נוסף על כך, טיפול תרופתי ארוך טווח של אוכלוסייה רחבה יגרום לטפיל לפתח עמידות לתרופה במרוצת הזמן[9].
מניעת היעקצות

הגנה נוספת מתרכזת בהקטנת הסיכוי לעקיצת היתושה. לפי מחקרים רבים שיטה זו מוכחת כיעילה ביותר באזורים נגועי מלריה באפריקה. שיטה זו כוללת:
- הדברה ביתית המתמקדת בריסוס בתי האב בחומרי הדברה כנגד היתושים. ידוע כי היתושה עוקצת בעיקר בשעות הערב והלילה ולכן ההדברה תיעשה בשעות הללו. ריסוס קירות הבית חשוב היות שהחומרים הרעילים פוגעים ברגלי היתושים והורגים אותם. נוסף על כך, הדברת הקירות יעילה גם במקרה שהיתושה עקצה את אחד מיושבי הבית, שכן לאחר העקיצה על היתושה לנוח כדי להתחיל את תהליך העיכול. בזמן מנוחתה על הקירות גוברים הסיכויים שתמות וכך לא תעביר את המחלה ליושבי הבית האחרים. קיימים חומרי הדברה שונים, אך הוכח כי היעיל מכולם הוא ה-DDT. עם זאת, השימוש ב-DDT עורר ביקורת. ארגון הבריאות העולמי ממליץ על שימוש ב-12 סוגים שונים של חומרי הדברה, אחד מהם הוא ה-DDT[10].
- רשתות נגד יתושים (כילות) - כפי שצוין לעיל, היתושה עוקצת בעיקר בשעות הערב והלילה, ולכן שימוש ברשתות (כילות) במהלך הלילה תורם למניעת העקיצות והעברת המחלה. השימוש ברשתות מקטין את הסיכוי להיעקץ ב-70% לערך. עם זאת, הוכח כי רשתות אלו אינן מחסום מוחלט מפני היתושים, ולכן החלו בריסוס הרשתות בחומרי הדברה אשר יקטלו את היתושים וימנעו את העקיצות. כספים רבים ותרומות הושקעו בקנייה ובהפצה של הרשתות באזורים מוכי המלריה באפריקה. עם זאת, קיים קושי באימוץ הרגלי שינה מתחת לרשתות, היות שהאקלים באזורים אלו הוא טרופי (חם ולח) והרשתות חוסמות את זרימת האוויר. השימוש ברשתות על ידי האוכלוסייה הוא בסדר גודל של רק 50%-70%, למרות יעילותן[11].
- אלמנטים פרסונליים נוספים - קיימות דרכים נוספות בהגנה פרסונלית מפני עקיצת היתושה, כגון לבישת בגדים ארוכים לכיסוי הגוף ומריחת חומר דוחה יתושים על חלקי הגוף החשופים.
מאבק אזורי
הדברה

הזרוע המרכזית במלחמה במלריה שואפת להקטין את מספר היתושות המסוגלות לשאת את הטפיל, בכמה דרכים:
- ייבוש ביצות וגופי מים עומדים המשמשים בתי גידול של היתוש. שיטה זו יעילה, אולם לא תמיד אפשרית, כי באזורים טרופיים כמות הגשמים גבוהה וכך נוצרים בכל פעם מקווי המים מחדש. זאת ועוד, הטיפול הזה יקר ולעיתים מסובך[12].
- הדברת שטחים בקרבת ביצות ומקווי מים באמצעות חומר הדברה (למשל DDT) - ברוב האזורים באפריקה שיטה זו שונתה לידי הדברה פרסונלית, כלומר ריסוס בבתי האב באזור הנגוע במלריה. שיטה זו נמצאה יעילה, אך ארגוני איכות הסביבה מתנגדים לה בטענה שחומרי ההדברה פוגעים בסביבה לטווח הארוך וכן כי חומרים אלו עלולים לפגוע בבני אדם. על אף התנגדות זו, השימוש ב-DDT נמשך מאחר שלא נמצאה חלופה יעילה יותר. כמו כן, מחקרים חדשים מראים כי באזורים שבהם השתמשו בחומרי הדברה, אחוז החולים במלריה קטן בהיקפו במידה ניכרת וכן אין נזקים לבני האדם ולחי באזור[13].
- טיפול במקווי המים (שאיננו ייבוש). במקומות מסוימים קיים ניסיון לפגוע בתהליכי ההתפתחות וההתרבות הביולוגיים של היתושים. ניסיונות אלו כוללים החדרת דגי גמבוזיה אשר אוכלים את הזחל שממנו היתושים מתפתחים. טיפול נוסף הוא כיסוי תחתית הביצות בשכבת נפט שאינה מאפשרת לזחל לנשום והורגת אותו. טיפול זה איננו נפוץ, מכיוון שיש להתחשב באזורים הגאוגרפיים ובאופייה הסוציו-אקונומי של האוכלוסייה באזור (הטיפול יקר). אמצעי זה סופג ביקורת מארגוני איכות סביבה בהתבסס על הטענות שלעיל[12].
מאמצים למניעת התפתחות המלריה על ידי חיסול היתושים נמצאו יעילים באזורים נרחבים בעולם אשר נחשבו בעבר מוכי מלריה (דוגמת ישראל). לעומת זאת, על אף מאמצים של ארגונים שונים ותרומות ממדינות ומגופים בין-לאומיים, היקף המלריה באפריקה רחב ביותר. למרות השימוש באמצעים השונים המלריה באפריקה עדיין נחשבת לגורם תמותה מרכזי ביבשת.
חינוך והסברה
ארגונים שונים ותוכניות בין-לאומיות משלבים יחד עם פעולות למניעת ההידבקות במחלה תוכניות של חינוך והסברה לקהילות המקומיות. הרעיון המרכזי שבבסיס גישה זו הוא כי הכתבת מדיניות התמודדות עם המחלה ומניעתה איננה יעילה ללא שיתוף הקהילות והקניית ידע וכלים לאוכלוסייה. שכן, באמצעות חינוך ניתן ליצור דור חדש של תושבים שיכירו בחשיבות האמצעים למניעת המחלה כדי ליצור מצב שבו שיעורי התמותה ממלריה באפריקה יקטנו בצורה ניכרת.
להגברת המודעות למחלה הוכרז על ידי ארגון הבריאות העולמי יום המלריה הבין-לאומי, החל בכל שנה ב-25 באפריל.
פיתוח חיסון
 ערך מורחב – חיסון נגד מלריה
ערך מורחב – חיסון נגד מלריה
משך שנים נכשלו הניסיונות לפיתוח חיסון כנגד מלריה, היות שאחד הטפילים הגורם למחלה הוא בעל מחזור חיים מורכב אשר מסייע לו להתחמק ממערכת החיסון המנסה לתקוף אותו ועל כן מקשה את ניסיונות פיתוח החיסון.
חיסון ה־RTS,S (אנ') הוא הראשון שהדגים הישגים קליניים בטיפול בטפיל, ובשנים 2009–2014 נכנס לניסוי שלב 3 בהיקף גדול יחסית[14][15], באזורים בהם העברת מלריה נחשבת גבוהה או בינונית. בשלב זה בוצע הניסוי בסמיות כפולה על כ־15,000 משתתפים[14]. הניסוי הראה כי מקרי המלריה בקרב המחוסנים ירדו ביותר ממחצית בשנה הראשונה לאחר החיסון, וירדו ב-40% במהלך 4 שנות המעקב[5].
לאחר תוצאות ניסוי שלב 3, קיבל החיסון מספר אישורים בינלאומיים, בין היתר של סוכנות הבריאות של האיחוד האירופי, ה־CHMP (אנ')[14][16], והחל פיילוט בהכנסת חיסון ה־RTS S למערכות הבריאות בגאנה, קניה ומלאווי. הפיילוט הביא להפחתה משמעותית במקרי מלריה שנחשבים לחמורים, ולירידה במקרי מוות של ילדים ובאשפוזים, כאשר על פי הערכת ארגון הבריאות העולמי הציל החיסון את חייהם של 1 מכל 200 ילדים שהתחסנו במסגרת הפיילוט[5].
הגנה מולדת מפני מלריה: המחלה כגורם ברירה טבעית
סכם
פרספקטיבה
 ערך מורחב – עמידות גנטית למלריה
ערך מורחב – עמידות גנטית למלריה
מחלת המלריה היא המחלה שהיוותה את גורם הברירה הטבעית החזק ביותר על הגנום האנושי בעת האחרונה[17]. זאת עקב העובדה כי מחלת המלריה גורמת לשיעורי תמותה ותחלואה גבוהים ביותר באזורים מוגבלים בעולם.
ההשפעה של טפיל מחלת המלריה על מבנה הגנום האנושי נלמדה במיוחד אצל חולי אנמיה חרמשית. במחלת האנמיה החרמשית קיימת מוטציה בגן המוגלובין B (HBB) המקודד את החלבון בטא גלובין. בעוד שאלל נורמלי מקודד חומצה גלוטמית במקטע השישי של הבטא גלובין, המוטציה גורמת לקידוד ולין. שינוי זה מחומצת אמינו הידרופילית לחומצת אמינו הידרופובית מעודד היקשרות בין מולקולות ההמוגלובין, עם פלמור ההמוגלובין נגרם עיוות לתא הדם האדום והוא מקבל צורה "חרמשית". תאים כאלה מפונים במהירות ממחזור הדם, במיוחד בטחול, שם הם נהרסים.
בשלב המרוזיטי במעגל החיים של הטפיל, הטפילים מתרבים בתוך תאי הדם האדומים והמטבוליזם של הטפיל גורם לשינויים כימיים בהרכב תא הדם. תאי דם בריאים (ללא המוטציה של אנמיה חרמשית) שורדים עד לסיום ההתרבות של הטפיל ופריצתו אל נוזל הדם, אולם אם התא האדום מכיל המוגלובין מעורב - נורמלי וכזה עם מוטציה של אנמיה חרמשית - רבים סיכוייו לעוות את מבנה התא ולכן הוא יהרס בטחול לפני שהטפיל יספיק להתרבות ולצאת מן התא למחזור הדם. לכן אנשים להם הטרוזיגוטיות לאלל בעל המוטציה - שהם נשאי המוטציה לאנמיה חרמשית - יחיו בדרך כלל עם אנמיה חסרת חשיבות מבחינת תפקוד הגוף, אולם ייהנו מהגנה טבעית כמעט מוחלטת מפני המלריה[18][19]. אנשים הומוזיגוטיים למוטציה של אנמיה חרמשית יסבלו ממלוא התסמינים של המחלה ובחברות לא מערביות תוחלת חייהם קצרה מאוד. אולם בחברות בהם מחלת המלריה אנדמית, שכיחות המוטציה לאנמיה חרמשית היא בשיעור של כ-10% מן האוכלוסייה. שכיחותה הגבוהה של מוטציית האנמיה החרמשית דווקא באזורים נגועי מלריה, מצביעה על קשר אבולוציוני בין השניים.
מוטציות ספציפיות בגנים המקודדים לשרשרות הגלובין, שמרכיבות את ההמוגלובין, נמצאות באוכלוסיית אפריקה שמדרום לסהרה בקורלציה ישרה לתפוצת המלריה. מוטציות אלה, אשר העיקריות בהן גורמות לאנמיה חרמשית, המוגלובין C ותלסמיה, משפיעות הן כמותית והן איכותית על תפקוד ההמוגלובין. תפקוד לקוי של המוגלובין משפיע על משך שרידות האריתרוציטים במחזור הדם, דבר אשר גורם להפרעה במחזור החיים של טפילי המלריה בתוכם[20][21][22][23].
זו דוגמה לשקלול תמורות אבולוציוני: האנמיה החרמשית פוגעת באיכות חייו של החולה ואף עשויה לקצר את חייו, אך מנגד מביאה לכך שתהיה לו עמידות מוגברת למלריה. כך הוא עשוי להגיע לגיל פוריות ולהעביר לצאצאיו את המוטציה בגן שנושאת את האנמיה החרמשית. יש לו עדיפות בהישרדות על פני בני סביבתו שלא נושאים את הגן לאנמיה חרמשית, כי אלה ימותו צעירים ממלריה, לפני שיתרבו, וכך לא יצליחו להעביר את הגנים שלהם לצאצאיהם. כך מתפשט הגן לאנמיה חרמשית באוכלוסיית אפריקה שמדרום לסהרה.
גם מחלות גנטיות אחרות הקשורות למוטציות בייצור המוגלובין, וכן חסר באנזים G6PD (הגורם לרגישות לפול), מקנות עמידות חלקית למלריה, ונפוצים בעיקר באזורים מוכי מלריה, ולפיכך משערים שזו הסיבה לתפוצתם[24].
מלריה באפריקה שמדרום לסהרה
 ערך מורחב – מלריה באפריקה שמדרום לסהרה
ערך מורחב – מלריה באפריקה שמדרום לסהרה
באפריקה שמדרום לסהרה, שבמדינות רבות בה שורר מצב תברואתי קשה, קיימת התפשטות של היתושים מעבירי המחלה, ויכולות המניעה והטיפול אינן גבוהות, שיעור התחלואה ושיעור התמותה ממחלת המלריה הם מהגבוהים בעולם.
באפריקה שמדרום לסהרה, מלריה היא גורם התמותה החמישי בקרב ילדים, והיא הגורם הראשון הנגרם על ידי מחולל מחלה יחידה.
המלריה בארץ ישראל
 ערך מורחב – המלריה בארץ ישראל
ערך מורחב – המלריה בארץ ישראל
עם פלישת הבריטים לצפון אפריקה וישראל במלחמת העולם הראשונה, נאלץ הצבא הבריטי להתמודד עם המלריה שהפילה חללים רבים. ב-1922[25] פרסמו רשויות הבריאות הבריטיות את דרכי הפעולה שנקטו למלחמה במלריה. הספר מזהה את המקורות המרכזיים של המלריה בבארות המים הרבות שחפרו הערבים באזור והביצות לאורך מישור החוף. עם התקדמות הצבא מוקדי מלריה רבים נוקזו והודברו בחומר הורג יתושים או טופלו בשמן אם היו בארות מים לצורך שתייה. רוב היישובים החקלאיים שנוסדו בשנים הראשונות של תחיית היישוב העברי בארץ ישראל נוסדו בשלושה אזורים שהיו קטנים יחסית ומישוריים - בבקעת הירדן, בעמק יזרעאל ובמישור החוף של חבל השרון. הקרקע הייתה טובענית ופורייה מאוד, אך עם זאת גם הייתה נתונה למכירה משום שבאותה העת שרצה בה מחלת המלריה ולכן לא ניתן היה לעבד אותה. באזורים הגבוהים יותר שבהם המים לא עמדו, היתושים לא יכלו להתרבות (כגון אזור יהודה ושומרון) והיו מעט יישובים יהודיים, אם היו בכלל. בכך, הייתה למלריה השפעה של ממש על גבולות ההתיישבות היהודית בארץ ישראל.
מחלת המלריה האנדמית הודברה סופית במדינת ישראל בשנת 1966 הודות למאמציהם של אישים דוגמת ג'ון קרופר, הלל יפה, ישראל קליגלר, צבי סליטרניק, גדעון מר ורודולף רייטלר. ייבוש הביצות תרם תרומה ניכרת לחיסול המלריה בארץ.
אטימולוגיה
פירוש שם המחלה באיטלקית הוא "אוויר רע" (mala aria), בשל האמונה שהייתה קיימת בעבר כי אוויר הביצות הרע הוא הגורם לה[26].
קישורים חיצוניים
- ארגון הבריאות העולמי
- המרכז האמריקאי למניעת הפצת מחלות מידבקות
- ארז גרטי, מחלת המלריה, במדור "מאגר המדע" באתר של מכון דוידסון לחינוך מדעי, 25 ביוני 2010
- דוגמה להסתגלות אבולוציונית בקרב נגיף המלריה, בכתבה של רשת ב (19.5.15) הדנה במחקר לשם פיתוח חיסון מפני המלריה.
 אקונומיסט, העולם מתקרב לניצחון סופי על מחלת המלריה, באתר הארץ, 23 באוקטובר 2015
אקונומיסט, העולם מתקרב לניצחון סופי על מחלת המלריה, באתר הארץ, 23 באוקטובר 2015 ניר חסון, כך קבעה המלריה את גבולות מפת החלוקה, באתר הארץ, 16 במרץ 2018
ניר חסון, כך קבעה המלריה את גבולות מפת החלוקה, באתר הארץ, 16 במרץ 2018- מלריה, באתר אנציקלופדיה בריטניקה (באנגלית)
 הקרב נגד המלריה בעמק חפר, 1937, באתר ארכיון הסרטים הישראלי בסינמטק ירושלים
הקרב נגד המלריה בעמק חפר, 1937, באתר ארכיון הסרטים הישראלי בסינמטק ירושלים קדחת, דף שער בספרייה הלאומית
קדחת, דף שער בספרייה הלאומית
הערות שוליים
Wikiwand - on
Seamless Wikipedia browsing. On steroids.
