From Wikipedia, the free encyclopedia
A triosa-fosfato isomerase (TPI ou TIM, tamén escrita triosa fosfato isomerase ou triosafosfato isomerase) é un encima do grupo das isomerases co Número EC:5.3.1.1 que cataliza a interconversión reversible entre as dúas triosas fosfato isómeras, que son a dihidroxiacetona fosfato e o D-gliceraldehido 3-fosfato. Intervén na glicólise e gliconeoxénese.
| Dihidroxiacetona fosfato | triosa-fosfato isomerase | D-Gliceraldehido 3-fosfato | |
 |
 | ||
 | |||
| triosa-fosfato isomerase | |||
| Triosa-fosfato isomerase | |||||||||
|---|---|---|---|---|---|---|---|---|---|
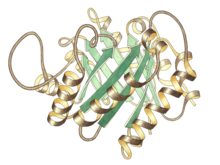 | |||||||||
| Vista lateral do monómero da triosa-fosfato isomerase co sitio activo na parte central superior. | |||||||||
| Identificadores | |||||||||
| Número EC | 5.3.1.1 | ||||||||
| Número CAS | 9023-78-3 | ||||||||
| Bases de datos | |||||||||
| IntEnz | vista de IntEnz | ||||||||
| BRENDA | entrada de BRENDA | ||||||||
| ExPASy | vista de NiceZyme | ||||||||
| KEGG | entrada de KEGG | ||||||||
| MetaCyc | vía metabólica | ||||||||
| PRIAM | perfil | ||||||||
| Estruturas PDB | RCSB PDB PDBe PDBj PDBsum | ||||||||
| Gene Ontology | AmiGO / EGO | ||||||||
| |||||||||
A triosa-fsofato isomerase xoga un importante papel na glicólise e é esencial para unha produción de enerxía eficiente. A triosa-fosfato isomerase atopouse en case todos os organismos en que se procurou, incluíndo animais como os mamíferos e os insectos e en fungos, plantas, e bacteriaa. Porén, algunhas bacterias que non realizan a glicólise, como Ureaplasma, carecen deste encima.
Nos humanos, as deficiencias en triosa-fosfato isomerase están asociadas cun trastorno neurolóxico grave progresivo chamado deficiencia de triosa-fosfato isomerase, que está caracterizada por unha anemia hemolítica crónica. Aínda que hai varias mutacións que causan esta doenza, a maioría inclúe unha mutación no ácido glutámico na posición 104 que cambia a ácido aspártico.[1]
A triosa-fosfato isomerase é un encima moi eficiente, que realiza a súa reacción miles de millóns de veces máis rápido do que ocorrería naturalmente en solución sen encima. A reacción é tan eficiente que se di que é perfecta cataliticamente, é dicir, está limitada só pola velocidade con que o substrato pode difundir dentro e fóra do centro activo do encima.[2][3]
O mecanismo catalítico implica a formación dun intermediato "enediol". A enerxía libre relativa de cada estado basal e estado de transición foi determinada experimentalmente, e móstrase na figura.[2]
A estrutura da triosa-fosfato isomerase facilita a conversión entre a dihidroxiacetona fosfato (DHAP) e o gliceraldehido 3-fosfato (GAP). O residuo glutamato 165 nucleofílico da triosa-fosfato isomerase desprotona o substrato,[4] e o residuo de histidina 95 electrofílico doa un protón para formar o intermediato enediol.[5][6] Cando se desprotona, o enediolato colápsase e, tomando un protón do glutamato 165 protonado, forma o produto gliceraldehido 3-fosfato. A catálise da reacción inversa procede analogamente, formando o mesmo enediol pero con colapso do enediolato desde o oxíxeno en C2.[7]
A triosa-fosfato isomerase está limitada pola difusión. En termos termodinámicos, a formación de dihidroxiacetona fosfato está favorecida nunha proporción de 20:1 sobre a produción de gliceraldehido 3-fosfato.[8] Porén, na glicólise o uso do gliceraldehido 3-fosfato nos seguintes pasos da ruta fai que a reacción se incline cara á súa produción. A triosa-fosfato isomerase é inhibida polos ións sulfato, fosfato, e arseniato, que se unen ao centro activo.[9] Outros inhibidores son o 2-fosfoglicolato, un análogo do estado de transición, e o D-glicerol 1-fosfato, un análogo do substrato.[10]
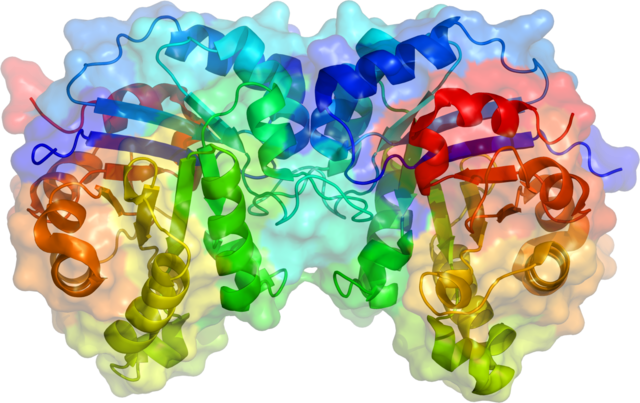
A triosa-fosfato isomerase é unha proteína dímera formada por dúas subunidades idénticas, cada unha das cales está formada por uns 250 residuos de aminoácidos. A estrutura tridimensional de cada subunidade presenta oito hélices α na parte externa e oito cadeas β paralelas no interior. Na ilustración, o modelo de fitas de cada subunidade está coloreado con cor degradada do azul ao vermello desde o N-terminal ao C-terminal. Este motivo estrutural denomínase barril αβ, ou barril TIM. O centro activo deste encima está no centro do barril. No mecanismo catalítico están implicados un residuo de ácido glutámico e unha histidina. A secuencia arredor dos residuos do centro activo está conservada en todas as triosas-fosfato isomerases coñecidas.
A estrutura da triosa-fosfato isomerase contribúe á súa función. Ademais dos residuos de glutamato e histidina situados con precisión para formar o enediol, ten unha cadea de dez ou once aminoácidos que actúa como un bucle que estabiliza o intermediato. O bucle, formado polos residuos 166 ao 176, péchase e forma un enlace de hidróxeno co grupo fosfato do substrato. Esta acción estabiliza o intermediato enediol e o outro estado de transición da reacción.[7]
Ademais de facer que a reacción sexa factible cineticamente, o bucle confina o intermediato enediol, que é moi reactivo, para impedir a descomposición de metilglioxal e fosfato inorgánico. O enlace de hidróxeno entre o encima e o grupo fosfato do substrato fai que esa descomposición sexa estereoelectronicamente desfavorable.[7] O metilglioxal é unha toxina e, en caso de que se forme, é eliminada por medio do chamado sistema glioxilase.[11] A perda dun enlace fosfato de alta enerxía e do substrato para o resto da glicólise fai que a formación de metilglioxal sexa ineficiente.
Os estudos suxiren que unha lisina próxima ao centro activo (na posición 12) é tamén fundamental para a función do encima. A lisina, protonada a pH fisiolóxico, pode axudar a neutralizar a carga negativa do grupo fosfato. Nos mutantes en que esta lisina está substituída por un aminoácido neutro, o encima deixa de funcionar, pero nos mutantes cun aminoácido diferente pero cargado positivamente mantén a súa funcionalidade.[12]
Seamless Wikipedia browsing. On steroids.
Every time you click a link to Wikipedia, Wiktionary or Wikiquote in your browser's search results, it will show the modern Wikiwand interface.
Wikiwand extension is a five stars, simple, with minimum permission required to keep your browsing private, safe and transparent.