From Wikipedia, the free encyclopedia
Unha biopelícula ou biofilme é un agregado de microorganismos no cal as células se adhiren unhas a outras sobre unha superficie, e xeralmente están incluídas dentro dunha matriz de substancias poliméricas extracelulares (SPE) producidas por elas mesmas. As biopelículas con matriz con estas substancias, tamén chamadas limos, son un conglomerado polimérico xeralmente composto principalmente por polisacáridos e proteínas. Unha biopelícula pode conter un 15% de células e o resto é matriz e outros compoñentes. As biopelículas poden formarse sobre superficies vivas ou non vivas e aparecen en medios naturais, industriais ou en hospitais.[1][2] As células microbianas que crecen nunha biopelícula son fisioloxicamente distintas das células de vida planctónica deses mesmos organismos, as cales son células separadas que nadan ou flotan nun medio líquido.
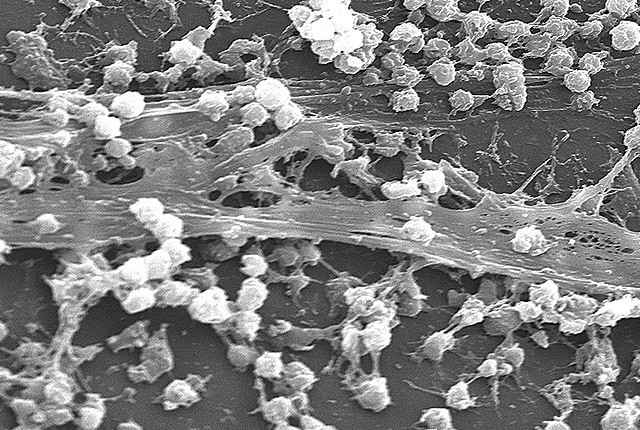
Os microbios forman biopelículas en resposta a moitos factores, que poden incluír o recoñecemento celular de sitios de fixación específicos ou non específicos nunha superficie, requirimentos nutricionais, ou nalgúns casos, a exposición de células planctónicas a concentracións de antibióticos subinhibitorias.[3][4]
Cando unha célula cambia ao modo de crecemento en biopelículas, sofre un cambio fenotípico no seu comportamento no cal moitos xenes son regulados diferencialmente.[5] Para adaptarse á biopelícula, as bacterias fan cambios importantes na súa estrutura e metabolismo. Os avances en proteómica e xenómica permitiron identificar xenes e proteínas que se activan e desactivan nas diferentes fases de desenvolvemento da comunidade. A expresión xénica das biopelículas é bastante distinta á das células planctónicas, xa que os requirimentos e organizacións son moi diferentes é cómpre unha sincronización de eventos para vivir en comunidade.
Como crecen en calquera superficie á que se adhiren, as biopelículas están asociadas á natureza crónica de infeccións como as que se presentan nos pulmóns de pacientes con fibrose quística, e unha proporción maioritaria das infeccións bacterianas é causada por biopelículas. Están implicadas por exemplo, na periodontite, carie, tuberculose, lexionelose, formación de cálculos renais, infeccións por Staphylococcus etc. Dificultan a acción dos antibióticos, do sistema inmunitario e doutros axentes.[6] Por este motivo, foron amplamente estudadas e considéranse unha ameaza clínica importante, xa que poden crecer en catéteres e implementos médicos e cirúrxicos.

A formación das biopelículas empeza coa fixación a unha superficie de microorganismos que flotan libremente. Estes primeiros colonizadores adhiren á superficie inicialmente por medio dunha adhesión feble e reversible por forzas de van der Waals. Se estes colonizadores non son separados inmediatamente da superficie, poden ancorarse a ela máis permanentemente utilizando estruturas de adhesión celular como os pili.[7] Algunhas especies non teñen a capacidade de fixarse á superficie por si mesmas pero a miúido poden facelo á matriz ou directamente aos primeiros microorganismos colonizadores. É durante esta colonización cando as células poden comunicarse por medio da percepción do quórum (quorum sensing). Por exemplo, Pseudomonas aeruginosa produce unhas substancias quimiotácticas chamadas homoserina lactonas.[6] Unha vez que a colonización empezou, a biopelícula crece pola combinación de divisións celulares e recrutamento de novos membros. A fase final da formación dunha biopelícula coñécese como desenvolvemento, e é a fase na cal se establece a biopelícula e xa só pode cambiar en forma e tamaño. O desenvolvemento dunha biopelícula pode permitir que unha colonia (ou colonias) de células agregadas se faga cada vez máis resistente aos antibióticos.
Hai cinco fases no desenvolvemento dun biofilme (ver ilustración á dereita):
A dispersión das células da colonia da biopelícula é unha fase esencial do ciclo de vida do biofilme. A dispersión permite que as biopelículas se espallen e colonicen novas superficies. Os encimas que degradan a matriz extracelular da biopelícula, como a dispersina B e a desoxirribonuclease, poden xogar un papel na dispersión da biopelícula.[8][9] Os encimas que degradan a matriz da biopelícula poden ser útiles como axentes antibiopelículas.[10][11] Atopáronse evidencias recentes de que un ácido graxo mensaxeiro (que actúa como molécula de comunicación célula-célula), o ácido cis-2-decenoico, pode inducir a dispersión e inhibir o crecemento das colonias das biopelículas. Este composto secretado por Pseudomonas aeruginosa actúa en varias especies de bacterias e no lévedo Candida albicans.[12] O óxido nítrico tamén activa a dispersión das biopelículas de varias especies bacterianas [13][14] a concentracións subtóxicas. O óxido nítrico ten o potencial de usarse no tratamento de pacientes que sofren de infeccións crónicas causadas polas biopelículas.[15]
Os biofilmes encóntranse xeralmente sobre substratos sólidos mergullados ou expostos a unha solución acuosa, aínda que poden formarse como capas flotantes en superficies líquidas e tamén na superficie de follas, especialmente en climas húmidos. Se ten recursos dabondo para poder crecer, unha biopelícula crece rapidamente ata facerse visible a simple vista. As biopelículas poden conter moitos tipos diferentes de microorganismos, como bacterias, arqueas, protozoos, fungos e algas, e cada grupo realiza funcións metabólicas especializadas. Porén, algúns organismos forman biopelículas dunha soa especie en certas condicións. A estrutura social (cooperación, competición) na biopelícula depende en grande medida das diferentes especies presentes nela.[16]
A biopelícula mantense unida e protexida por unha matriz de compostos poliméricos segregados chamada SPE, que é unha abreviación de substancia polimérica extracelular (EPS na literatura científica inglesa) ou exopolisacárido. Esta matriz protexe as células que están no seu seo e facilita a comunicación entre elas por medio de sinais bioquímicos. Algúns biofilmes conteñen canais de auga que axudan a distribuír nutrientes e moléculas sinalizadoras [17]. Esta matriz é o suficientemente forte como para que en certas condicións as biopelículas poidan quedar fosilizadas (ver estromatólitos).
As bacterias que viven nas biopelículas xeralmente teñen propiedades significativamente distintas das bacterias que viven flotando libremente da mesma especie, xa que o ambiente denso e protexido da película permítelles cooperar e interactuar de varios modos. Unha vantaxe que proporciona este ambiente é o incremento da resistencia aos deterxentes e antibióticos, xa que a mesta matriz extracelular e a capa externa de células protexe as células do interior da comunidade. Nalgúns casos a resistencia a antibióticos pode incrementarse mil veces.[18] A transferencia horizontal de xenes está moi facilitada nas biopelículas e acaba por orixinar unha estrutura da biopelícula máis estable.[19]
Porén, os biofilmes non son sempre menos susceptibles aos antibióticos. Por exemplo, a forma atopada nos biofilmes de Pseudomonas aeruginosa non presenta maior resistencia a axentes antimicrobianos do que as células planctónicas da fase estacionaria, aínda que cando a biopelícula se compara coas células planctónicas da fase logarítmica, a biopelícula mostra maior resistencia a antimicrobianos. Esta resistencia aos antibióticos nas células da fase estacionaria e nas biopelículas pode deberse á presenza de células persistentes[20] (estas células non son mutantes, senón células latentes que poden resistir ao tratamento antimicrobiano, xa que entraron nun estado fisiolóxico de crecemento lento ou moi lento, que as fai insensibles ou tolerantes ás drogas antimicrobianas).


As biopelículas son ubicuas. Case todas as especies de microorganismos, non só as bacterias e arqueas, teñen mecanismos polos cales poden adherirse a superficies e uns a outros. As biopelículas fórmanse en virtualmente todas as superficies que non se desprenden[21] en medios non estériles acuosos ou moi húmidos.
As biopelículas están implicadas nunha gran variedade de infeccións microbianas no corpo, que segundo unha estimación chegarían ao 80% de todas as infeccións.[27] Os procesos infecciosos nos cales foron implicados os biofilmes inclúen problemas comúns como as infeccións do tracto urinario, infeccións por catéter, otite media, formación da placa dental,[28] xinxivite,[28] recubrimento de lentes de contacto,[29] e procesos menos comúns pero máis graves como endocardites, infeccións propias da fibrose quística, e infeccións de dispositivos implantados permanentemente no corpo como próteses de articulacións e de válvulas cardíacas.[30][31] Máis recentemente indicouse que os biofilmes bacterianos poden ser prexudiciais para a curación das feridas cutáneas e reducir a eficiencia de antibacterianos tópicos na curación ou tratamenteo de feridas infectadas na pel.[32]
Recentemente viuse que os biofilmes están presentes no tecido extraído do 80% dos pacientes sometidos a cirurxía por sinusite crónica. Os pacientes con estas biopelículas carecían no tecido de cilios e células caliciformes, comparados cos individuos control sen biopelículas, que tiñan cilios normais e célula caliciformes de morfoloxía normal.[33] Os biofilmes tamén se encontraron en mostras de dous de cada 10 individuos de control sans.[34]
Os biofilmes poden tamén formarse nas superficies inertes de dispositivos implantados no corpo, como catéteres, válvulas cardíacas prostéticas ou dispositivos intrauterinos. [35]
Estanse a desenvolver novas técnicas de tinguidura para diferenciar as células bacterianas que crecen en animais vivos, por exemplo nos tecidos con inflamacións alérxicas.[36]
Investígase no descubrimento de novos antibióticos con capacidade de penetración nos biofilmes e de fármacos que interfiran na comunicación intercelular nos biofilmes, como as furamonas.[6]
A placa dental é o material que se adhire aos dentes e consiste en células bacterianas (principalmente Streptococcus mutans e Streptococcus sanguinis), polímeros da saliva e produtos bacterianos extracelulares. A placa é unha biopelícula situada sobre a superficie dos dentes. Esta acumulación de microorganismos somete aos dentes e enxivas a altas concentracións de metabolitos bacterianos, o que orixina enfermidades dentais.[28][37]
A bacteria Legionella en certas condicións crece nos biofilmes, nos cales está protexida contra os desinfectantes. Os traballadores das torres de refrixeración, as persoas que traballan en lugares con aire acondicionado e as que se duchan poden estar expostas á Legionella pneumophila por inhalación cando ditos sistemas non están ben deseñados, construídos ou mantidos.[38]
Entre 2021 e 2023 realizáronse probas na Estación Espacial Internacional para estudar a formación de biopelículas sobre metais nas condicións da estación, co obxectivo de estudar a proliferación bacteriana nese ambiente, que podería orixinar infeccións nos astronautas ou corrosións nos materias da nave, así como na Terra. Fixéronse probas para ver que metais evitaban máis doadamente a formación de biopelículas, entre eles o cobre, coñecido polas súas características xermicidas, debido á súa capacidade de romper as membranas celulares e interferir en procesos internos das células, causándolles graves danos.[39]
Seamless Wikipedia browsing. On steroids.
Every time you click a link to Wikipedia, Wiktionary or Wikiquote in your browser's search results, it will show the modern Wikiwand interface.
Wikiwand extension is a five stars, simple, with minimum permission required to keep your browsing private, safe and transparent.