Loading AI tools
sous-famille de virus De Wikipédia, l'encyclopédie libre
Orthocoronavirinae · Orthocoronavirinés, Orthocoronavirus
| Realm | Riboviria |
|---|---|
| Règne | Orthornavirae |
| Embranchement | Pisuviricota |
| Classe | Pisoniviricetes |
| Ordre | Nidovirales |
| Sous-ordre | Cornidovirineae |
| Famille | Coronaviridae |
Genres de rang inférieur

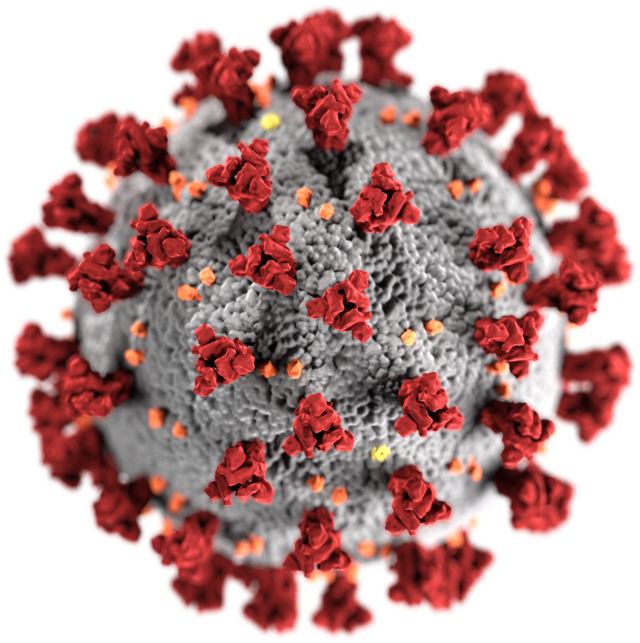
Les orthocoronavirus (CoV) sont des virus qui constituent la sous-famille Orthocoronavirinae de la famille Coronaviridae (les coronavirus). Le nom « coronavirus », du latin signifiant « virus à couronne », est dû à l'apparence des virions sous un microscope électronique, avec une frange de grandes projections bulbeuses qui évoquent une couronne solaire[2].
Ces coronavirus sont munis d'une enveloppe virale incluant une capside caractérisée par des protéines en forme de massue (appelées spicules). Ils ont un génome à ARN monocaténaire (c'est-à-dire à un seul brin), de sens positif (groupe IV de la classification Baltimore), de 26 à 32 kilobases (ce qui en fait les plus grands génomes parmi les virus à ARN)[3]. Ils se classent parmi les Nidovirales, ordre de virus produisant un jeu imbriqué d'ARNm sous-génomiques lors de l'infection. Des spicules, une enveloppe, membrane et capside contribuent à la structure d'ensemble de tous les coronavirus. Ils peuvent muter et se recombiner[4].
Les chauves-souris et les oiseaux, en tant que vertébrés volants à sang chaud, seraient les hôtes idéaux pour les coronavirus assurant l'évolution et la dissémination du virus[5]. Ces coronavirus sont normalement spécifiques à un taxon animal comme hôte, mammifères ou oiseaux selon leur espèce ; mais ils peuvent parfois changer d'hôte à la suite d'une mutation. Leur transmission interhumaine se produit principalement par contacts étroits via des aérosols respiratoires générées par les éternuements, la toux ou la phonation. Plus de 500 types de coronavirus ont été isolées chez la chauve-souris et il existerait plus de 5 000 types de coronavirus[6].
Sept principaux coronavirus sont généralement cités comme pouvant contaminer l'humain[7]. Un huitième a été identifié : le B814[8] (le premier coronavirus humain identifié), mais cette souche semble ne plus circuler.
Quatre coronavirus en circulation sont considérés comme sources d'infection bénignes : 229E, NL63, OC43 et HKU1. Ils seraient la cause de 15 à 30 % des rhumes courants.
Plus récemment ont été identifiés trois types de coronavirus responsables de graves pneumopathies :
Les coronavirus existent probablement depuis au moins des centaines de millions d'années, mais du point de vue de l'épidémiologie et de l'histoire médicale et en tant que zoonose c'est au XXIe siècle qu'ils ont pris de l'importance : « cinq des sept coronavirus humains ont été isolés au cours de ce siècle. Et malheureusement, les trois derniers sont entrés dans notre vie avec les craintes liées à une épidémie, une pandémie ou à la mort »[9].
C'est en 1930 aux États-Unis que la première maladie due à un coronavirus est observée, chez des volailles. L'année suivante, un médecin décrit dans un article la maladie qui cause une détresse respiratoire chez la poule et une diminution de la ponte et de la qualité des œufs. En 1937, l'agent infectieux, le virus de la bronchite infectieuse aviaire (IBV pour Infectious Bronchitis Virus) est isolé.[réf. nécessaire]
En 1946, un autre coronavirus est identifié, le Coronavirus de la gastro-entérite transmissible porcine (TGEV). Indépendamment, en 1949 à New York et 1951 à Londres, deux équipes découvrent le virus de l'hépatite murine chez une souris paralysée[10].
En 1965, le premier coronavirus infectant l'être humain (la souche B814) est découvert. Et rapidement, d'autres suivent : 229E en 1966 et OC43 en 1967[11], qui sont la cause de rhumes plus ou moins graves selon les personnes. L'année suivante, ils sont observés au microscope électronique par June Almeida et David Tyrrell qui mettent en évidence leur structure en couronne[12]. La relation est faite entre tous ces virus, et le terme de « coronavirus » est pour la première fois utilisé dans la revue Nature en 1968[2],[10].
Avec la découverte en 2018 de coronavirus infectant des amphibiens et classés dans une sous-famille à part (letovirus), les coronavirus infectant des amniotes (comme ses mammifères et des oiseaux) sont classées dans la sous-famille Orthocoronavirinae[1] et qualifiés plus précisément d'orthocoronavirus[13].
Le dernier coronavirus humain (ou récemment humanisé, très probablement à partir d'une ou plusieurs souches portées par des chauves-souris) semble avoir émergé à Wuhan en Chine en 2019 : le SARS-CoV-2. La maladie qu'il cause (Covid-19) a provoqué en quelques mois la première grande pandémie à coronavirus, caractérisée par un R0 élevé (2,3 en moyenne d'après les estimations disponibles en , mais qui semble pouvoir atteindre 5,7) ; avec un taux de létalité de 6,3 (très variable selon les âges et les contextes, pouvant parfois dépasser 15%)[9].
| Pandémie | Date | Cas confirmés | Décès | Guérisons | Sous-type impliqué |
|---|---|---|---|---|---|
| Épidémie de SRAS de 2002-2004 | 2002-2004 | 8 096 | 774 | - | Sars-Cov (SRAS) |
| Coronavirus du syndrome respiratoire du Moyen-Orient | 2012-2014 | 361 | 107 | - | MERS-CoV |
| Pandémie de Covid-19 (En cours) | 2019-2024 | + 250 847 494 ()[14] | + 5 064 350 ()[14] | + 220 905 435 ()[14] | SARS-CoV-2 (Covid-19) |
La taxonomie de ces nouveaux virus fait d'abord débat, pour finalement aboutir en 1975 à la création d'une nouvelle famille (Coronaviridae) et d'une nouvelle sous-famille (Orthocoronavirinae) par l'International Committee on Taxonomy of Viruses[10].
Le terme coronavirus (du latin corona et virus, littéralement « virus à couronne »[15]) provient de l'apparence des virions au microscope électronique, caractérisée par une frange de grandes protubérances entourant l'enveloppe avec l'apparence d'une couronne, par analogie avec la couronne solaire[2].
Les hôtes idéaux des coronavirus, en tant que vertébrés volants à sang chaud, sont les chauves-souris (pour les Alphacoronavirus et les Betacoronavirus) et les oiseaux (pour les Gammacoronavirus et les Deltacoronavirus). Ces espèces-réservoir assurent l'évolution et la dissémination des coronavirus[5]. Chez d'autres espèces, les symptômes varient (maladies des voies respiratoires supérieures chez la poule, diarrhée chez la vache ou le porc, des voies digestives chez le chat et le chien, etc.). Parfois, aucun symptôme n'est associé à leur présence (ex. : coronavirus du béluga).
L'être humain abrite naturellement quatre types de coronavirus bénins, qui provoquent des infections des voies respiratoires, comme le rhume, et plus rarement affectent les systèmes gastro-intestinaux, cardiaques et nerveux[16].
Les groupes de coronavirus ont normalement un hôte animal spécifique (mammifères ou oiseaux[17]) mais ils peuvent parfois changer d'hôte à la suite d'une mutation. Ce sont de telles mutations qui ont probablement conduit à l'apparition de souches causant de graves infections chez l'homme (SRAS, MERS et Covid-19).
On a longtemps pensé que les coronavirus avaient un tropisme uniquement respiratoire ou gastrointestinal (traduit par des pneumonies et entérocolites dans les cas graves), mais un nombre croissant d'études montrent un tropisme bien plus large, cardiovasculaire notamment, et neurologique également (dès les années 1980, on a montré que plusieurs coronavirus, dont en dernier cas le SARS-CoV-2 sont clairement aussi neuroinvasifs et neurotropes[18],[19],[20], au point que cette diversité de tropismes et de symptômes font des coronavirus (murins notamment, regroupées sous le sigle de MHV) un modèle animal pour l'étude de maladies humaines aussi variées que la sclérose en plaques, l’hépatite virale ou la pneumonie (S. R. Weiss et al. 2011). Le MHV pénètre le Système nerveux central (SNC) via les neurones du nerf olfactif, et peut causer une encéphalite aiguë ou une maladie démyélinisante chronique s'il y persiste (il peut aussi se propager jusqu’à la moelle épinière)[19],[21].
En 2002, l’apparition du Sars-CoV, un virus responsable d'une maladie infectieuse des poumons, pousse l’Union européenne à lancer plusieurs programmes afin de ne pas être prise au dépourvu en cas de nouvelles émergences. Dès 2004, l’équipe de Bruno Canard, directeur de recherche CNRS à Aix-Marseille, spécialiste des coronavirus, grâce aux réseaux collaboratifs européens, affiche des résultats prometteurs. « Nous avions eu cette idée qui s’est révélée fructueuse : les virus ont une capacité énorme à être différents, variés, avec de larges familles. Nous les avons donc étudiés tous en même temps, afin d’en avoir un modèle type qui nous permettrait, en cas de menace d’un virus inconnu, d’en trouver un proche, d’où nous pourrions extraire des données scientifiques[22]. »
Mais dès 2006, l’intérêt des politiques pour le Sars-CoV disparaît. La crise financière de 2008 accélère le désengagement de l’Europe et de la France pour la recherche, les stratégies de recherche fondamentale perdent leurs financements. Aussi, en 2015, Bruno Canard dénonce le désengagement européen et français dans le secteur des sciences et adresse avec ses collègues belges et hollandais, des lettres d’intention à la Commission européenne expliquant qu’il existe neuf familles de virus pour lesquelles une émergence est possible. « Le premier sur la liste était le flavivirus, explique-t-il. Le second, le coronavirus. Un an plus tard, apparaissait Zika, un flavivirus ». Or, la Commission européenne ne donnera jamais de réponse. Et en 2020 surgit le Sars-CoV-2, un coronavirus[22] engendrant la Covid-19.

Ce virus enveloppé est constitué d'une enveloppe virale entourant une capside hélicoïdale qui contient le brin d'ARN. La taille du génome de ces virus varie d'environ 26 à 32 kilobases, valeurs parmi les plus élevées chez les virus à ARN.
Les coronavirus ont en commun des protéines désignées par une lettre indiquant leur localisation : S (protubérances), E (enveloppe), M (membrane) et N (nucléocapside). Certains, notamment ceux du sous-groupe A du genre Betacoronavirus, ont une protéine HE (hémagglutinine estérase (en)) caractéristique. Le coronavirus du SRAS présente en outre sur la protéine S un site de liaison spécifique à l'enzyme de conversion de l'angiotensine 2[23] qui lui sert de point d'entrée dans la cellule hôte.
La taille physique du virion est classiquement donnée comme étant de 120 à 160 nm[24] ou comme étant de l'ordre de 125 nm[25]. Toutefois le SARS-CoV-2, responsable de la Covid-19 a été annoncé plus récemment comme mesurant approximativement de 60 à 140 nm, et comme étant de forme elliptique avec de nombreuses variations[26].

Tous les CoV ont un génome d'ARN non-segmentés (simple brin) organisé de la même manière : les deux tiers environ du génome contiennent deux grands « cadres de lecture ouverts » et se chevauchant (dits ORF1a et ORF1b). Ces deux cadres sont traduits en « polyprotéines réplicase » pp1a et pp1ab. « Ces polyprotéines sont ensuite traitées pour générer 16 protéines non structurales, désignées nsp1 ~ 16. La partie restante du génome contient des ORF pour les protéines structurales, y compris la pointe (S), l'enveloppe (E), la membrane (M) et la nucléoprotéine (N). Un certain nombre de protéines accessoires spécifiques à la lignée sont également codées par différentes lignées de CoV »[3],[27],[28],[29].

Elle se fait en six étapes successives (voir illustration) :
Les coronavirus sont nommés par un groupe d'étude[31] travaillant au sein de l'ICTV (International committee on Taxonomy of viruses)[32].
Les coronavirus (CoV) sont des virus à ARN monocaténaire de sens positif (groupe IV de la classification Baltimore) correspondant à la sous-famille Orthocoronavirinae de la taxonomie de l'ICTV[33], dans la famille Coronaviridae, et de l'ordre Nidovirales[34],[35].
Selon les caractéristiques de leurs séquences protéiques, les CoV sont classés en 4 genres (alpha-CoV, beta-CoV, gamma-CoV et delta-CoV), qui tous contiennent des virus pathogènes pour les mammifères[4] :

Remarques :
La sous-famille Orthocoronavirinae de la famille Coronaviridae est organisée en 4 genres, 22 sous-genres et une quarantaine d'espèces[39] :
Sept types de coronavirus infectent couramment l'homme[40], dont trois causent des infections graves.
Les quatre premiers types connus sont sans gravité : les coronavirus humains 229E, NL63, OC43 et HKU1, inconnus chez la chauve-souris. Ils causent des rhumes avec fièvre et des maux de gorge dus à des végétations adénoïdes gonflées, principalement en hiver et au début du printemps[41].
Les coronavirus seraient la cause de 15 à 30 % des rhumes courants[42].

Trois types de coronavirus qui ne se trouvent pas naturellement chez l'homme mais chez des mammifères ont été découverts plus récemment et ont été à l'origine d'infections graves des poumons (pneumopathie virale) :
Selon le virus en cause, les formes graves de la maladie ont leurs particularités. Par exemple, la diarrhée était très fréquente dans le SRAS mais rare dans la maladie à coronavirus 2019.
Trois principales sources sont utilisées : l'Institut Pasteur, l'OMS et les CDC américains[46].
| Syndrome respiratoire du Moyen-Orient (MERS)[47],[48] | Syndrome respiratoire aigu sévère (SRAS)[49],[50],[51] | Maladie à coronavirus 2019 (COVID-19) | |
|---|---|---|---|
| Agent pathogène | MERS-CoV | SARS-CoV | SARS-CoV-2 |
| Année d'apparition | 2012 | 2003 | 2019 |
| Nombre de cas | 1 219 | 8 098 dont 5 327 en Chine. | En cours, voir ici |
| Pourcentage de cas par transmission nosocomiale | 70 %[52] | 58 %[52] | |
| Nombre de décès | 449 | 774 (dont 349 en Chine) | En cours, voir ici |
| Réservoir | Dromadaire | Chauve-souris | Chauve-souris (probablement) |
| Transmission à l'homme par l'animal | Contact direct avec un animal infecté, consommation de lait cru de dromadaire. | Consommation de viande de civette palmiste masquée, animal sauvage vendu sur les marchés et consommé dans le Sud de la Chine. | Un pangolin[43] pourrait être l'hôte intermédiaire. |
| Transmission interhumaine | Oui | Oui | Oui |
| Transmission par objet | – | Oui | Risque très faible. |
| Transmission materno-fœtale | – | Aucun cas retrouvé chez les femmes enceintes infectées par ce virus[53]. | Aucune preuve[54]. |
| Transmission par le lait maternel | Un seul cas documenté[55] | RT-PCR négative sur 16 femmes testées[56] | |
| Incubation | Entre 5 et 15 jours. | Entre 2 et 7 jours. | Durée médiane d'incubation à 5,1 jours (5,5 jours en moyenne), 97,5 % des personnes seront malades 11,5 jours après le contact infectieux[57]. |
| Porteur sain | – | Probablement pas. | Oui (un seul cas publié) |
| Contagiosité | Taux de reproduction inférieur à 1[58]. | Taux de reproduction supérieur à 2[58]. | Médiane du taux de reproduction de base (R0) à 2,79[59]. |
| Durée de la contagiosité | – | – | Semble limitée à la période des signes cliniques. Possibilité disputée de contagion en phase asymptomatique[60]. |
| Début de la période de contagiosité | – | 3 à 4 jours après le début des signes cliniques. | Dès l'apparition des signes cliniques. Porteur asymptomatique prouvé[61]. |
| Fièvre | À 98% | À 99% | À 87.9%, mais peut apparaître plusieurs jours après la toux ou les difficultés à respirer. |
| Diarrhée | À 26% | À 20%[53]. | À 3.7%. |
| Transmission par les selles | Très probable mais a joué un rôle mineur[53]. | Cette possibilité est envisagée[62]. | |
| Létalité | 34,4 %[52] | 9,5 %[52], au-delà de 50 % chez les plus de 65 ans. | 3,4 %[63] |
| Traitement | Symptomatique | Symptomatique | Symptomatique |
| Vaccin | Aucun | Aucun | En cours |
| Statut | Résurgence possible. | Considéré comme éradiqué. | Épidémie en cours. |

Au vu des séquences génomiques disponibles, deux grands taxons animaux seraient le réservoir principal des CoVs :
Au vu des connaissances disponibles, les coronavirus semblaient avoir besoin d'hôtes intermédiaires (toujours des mammifères) pour s'« humaniser », c'est-à-dire muter pour pouvoir infecter l'Homme.
Des hôtes intermédiaires connus ont été :

La transmission interhumaine des coronavirus se fait principalement par les gouttelettes ou des aérosols respiratoires expectorées par une personne infectée (via la toux, les éternuements, des postillons, ou parfois par le simple fait de parler fort ou en criant) quand les particules virales sont inhalées par une personne se trouve à proximité. La transmission et la contagiosité varient aussi selon le coronavirus, et peut-être selon sa souche au sein d'une épidémie.
La prophylaxie passe par une prévention primaire visant à limiter la transmission du virus : éviter les contacts (surfaces potentiellement contaminées, poignées de main, embrassades), se laver les mains fréquemment, éviter de se toucher les yeux, le nez ou la bouche, par où le virus peut s'introduire dans l'organisme. En cas de symptômes de type toux ou rhume, se maintenir à au moins 1 mètre de toute personne et éviter d'émettre des particules contaminées[65].
D'autres recommandations comprennent[66] :
Dans le cas du SRAS, des médicaments ont été utilisés pour tenter d'enrayer l'épidémie : la ribavirine, un analogue de nucléotides, des anti-inflammatoires stéroïdiens et, après identification formelle de l'agent pathogène et des criblages de sensibilité, l'interféron-alpha et des inhibiteurs de protéases. Leur efficacité est encore sujette à caution. Aucun n'a fait l'objet d'une étude clinique adéquate : beaucoup d'études disponibles ne permettent pas de conclusions scientifiques claires car elles ont été réalisées sur de petits nombres de sujets ou alors sans protocole ou dose fixe. Certaines indiquent même que ces traitements pourraient avoir nui à l'éradication du virus[67].
Bruno Canard dénonce en l'emballement et publie une lettre ouverte Coronavirus : la science ne marche pas dans l’urgence ![68]. Il déclare : « Un vaccin demande au mieux 18 mois de recherches. Et pour des virus non prévisibles, qui changent, il n’est pas adapté. Mieux vaut faire des médicaments qui ont un large spectre dans une famille virale. Cela peut nécessiter 5 ans, parfois 10. D’où l’importance de l’anticipation scientifique[22]. »
Des vaccins à base de virus inactivé et d'autres fondés sur les protéines S et N sont à l'étude depuis plusieurs années[69] quand l'éradication rapide de l'épidémie de SRAS vient interrompre les essais cliniques. Cependant, les éléments viraux produisant l'immunité ne sont souvent pas assez conservés dans la même famille virale : « s'il y avait eu un vaccin contre le coronavirus de 2003, il est pratiquement certain qu'il n'aurait pas marché de manière satisfaisante contre [la] Covid-19 » (Bruno Canard)[70].
Bien que n'ayant pas abouti à leur certification, la recherche de vaccins contre le SRAS a rendu possible l'obtention rapide de vaccins contre la Covid-19. Ainsi, le vaccin de Pfizer et BioNTech est conçu en quelques heures dès [71], et autorisé au Royaume-Uni en décembre. En , 60 vaccins contre le SARS-CoV-2 sont autorisés ou en phase d'étude clinique, et 172 vaccins potentiels sont à l'étude[72].
En 2023, certains variants du SARS-CoV-2, et notamment le variant Omicron, échappent en partie aux différents vaccins administrés. Plusieurs équipes dans le monde cherchent à produire des vaccins conférant une immunité plus durable et plus efficace contre les variants existants et à venir, ainsi que contre d'autres coronavirus. Elles utilisent de nouvelles approches[73] : élargissement des cibles protéiniques et recherche de nouvelles cibles, emploi de nanoparticules, etc.
Un Romain dans la bande dessinée Astérix se nomme Coronavirus.
Seamless Wikipedia browsing. On steroids.
Every time you click a link to Wikipedia, Wiktionary or Wikiquote in your browser's search results, it will show the modern Wikiwand interface.
Wikiwand extension is a five stars, simple, with minimum permission required to keep your browsing private, safe and transparent.