رشد کنترلنشده سلول در بافتهای ریه From Wikipedia, the free encyclopedia
سرطان ریه (به انگلیسی: Lung cancer) نوعی بیماری است که مشخصه آن رشد کنترلنشده سلول در بافتهای ریه است. اگر این بیماری درمان نشود، رشد سلولی میتواند در یک فرایند به نام متاستاز به بیرون از ریه گسترش پیدا کند و به بافتهای اطراف یا سایر اعضای بدن برسد. اکثر سرطانهایی که از ریه شروع میشوند، به نام سرطانهای ابتدایی ریه، کارسینوماهایی هستند که از بافت پوششی نشات میگیرند. انواع اصلی سرطان ریه سرطانهای ریه سلول کوچک (SCLC)، که سرطان سلولی جو شکل نیز نامیده میشود، و سرطان ریه سلول غیر کوچک (NSCLC) هستند. شایعترین علائم عبارتند از سرفه (همراه با خلط خونی)، کاهش وزن و تنگی نفس.[1]
| سرطان ریه | |
|---|---|
 | |
| نمونهای از تومور موجود در ریه که توسط پیکانی بر روی رادیوگرافی قفسه سینه نشان داده شدهاست. | |
| تخصص | سرطانشناسی، پزشکی ریه |
| طبقهبندی و منابع بیرونی | |
| آیسیدی-۱۰ | C33-C34 |
| آیسیدی-۹-سیام | 162 |
| دادگان بیماریها | 7616 |
| مدلاین پلاس | 007194 |
| ئیمدیسین | med/۱۳۳۳ med/1336 emerg/335 radio/807 radio/405radio/406 |
| پیشنت پلاس | سرطان ریه |
| سمپ | D002283 |
شایعترین علت سرطان ریه قرار گرفتن در معرض دود دخانیات[2] برای مدتی طولانی دلیل ۹۰٪ سرطانهای ریه است.[1] درصد ابتلا به سرطان ریه در افرادی که سیگار نمیکشند ۱۵٪ است،[3] و دلیل این موارد اغلب ترکیبی از عوامل ژنتیکی،[4] گاز رادون،[4] آزبست،[5] و آلودگی هوا[4] از جمله دود سیگار فرد ثالث مربوط میشود.[6][7] ممکن است سرطان ریه در رادیوگرافی قفسه سینه و مقطعنگاری رایانهای (سیتی اسکن) قابل تشخیص باشد. تشخیص با یک بافتبرداری[8] که اغلب از طریق برونکوسکوپی یا راهنمای سیتی انجام میشود، قابل تأیید شدن است. درمان و نتایج طولانی مدت به نوع سرطان، مرحله (شدت گسترش) و سلامت کلی فرد، که از طریق وضعیت عملکرد سنجیده میشود، بستگی دارد.
درمانهای رایج، عبارتند از جراحی، شیمیدرمانی و پرتودرمانی. گاهی NSCLC با جراحی قابل درمان است، اما معمولاً SCLC به شیمی درمانی و پرتودرمانی بهتر پاسخ میدهد.[9] بهطور کل، ۱۵٪ از مردم ایالات متحده آمریکا که طبق تشخیص پزشک به سرطان ریه مبتلا بودهاند پنج سال بعد از تشخیص بیماری زنده ماندند.[10] در سراسر دنیا، سرطان ریه شایعترین دلیل مرگ و میر مربوط به سرطان در بین زنان و مردان بهشمار میرود، و مسئول ۱٫۳۸ میلیون مرگ و میر در سال، طبق گزارش سال ۲۰۰۸ است.[11]
سرطان ریه در مراحل اول خود اغلب هیچگونه علامتی ندارد. هنگامی که نخستین علائم ظاهر میشوند، اغلب بهصورت مشکلات تنفسیِ غیراختصاصی هستند: سرفه، خسخس سینه،[1] تنگی نفس یا درد قفسه سینه - که شدت و نوع آن از فردی به فرد دیگر متفاوت است.[12] در کسانی که سرفه دارند، این سرفه یا کلاً علامتی نوظهور است (یعنی قبلاً اصلاً سرفه نداشتهاند) یا آنکه سرفههای مزمن قبلیشان به دفعات بیشتر یا با شدت بیشتری از سرفههای پیشین روی میدهد.[12] سرفهها اغلب بیش از سه هفته باقی میماند.[13] تقریباً از هر چهار بیمارِ مبتلا، یک نفر سرفه با خلط خونی دارد، که میزان این خون از رگههای کوچک در خلط سینه تا مقادیر زیاد خون متغیر است.[14][12] حدود نیمی از مبتلایان به سرطان ریه دچار تنگی نفس میشوند و بین ۲۵ تا ۵۰ درصد نیز یک درد قفسه سینهٔ مبهم و مداوم[15] را تجربه میکنند که قطع نمیشود در همان محل باقی میماند (جایش عوض نمیشود).[12] دردِ سینه معمولاً با نفسِ عمیق، سرفه یا خنده تشدید میشود.[16] علاوه بر علائم تنفسی، برخی علائم سیستمیک دیگر شامل بیاشتهایی، کاهش وزن ناخواسته، ضعف عمومی بدن، تب و تعریق شبانه است.[12][17] باید توجه داشت که بسیاری از علائم سرطان ریه (کم اشتهایی، کاهش وزن، تب، خستگی و ضعف) مختص این بیماری نیستند.[8] و در بسیاری از بیماریهای دیگر هم ممکن است دیده شوند.
وجود تومور در مکانهای خاص ممکن است منجر به بروز برخی از علائم کمتر شایع گردد. تومورهای قفسه سینه میتوانند با انسداد نای یا اختلال در عصب دیافراگم باعث اشکال در تنفس شوند. اگر سرطان در راه تنفسی رشد کند، ممکن است جلوی جریان هوا را سد سازد، و علاوه بر مشکل در تنفس با تجمع ترشحات در پشت گرفتگی، فرد را مستعد سینهپهلو سازد.[1] مشکل در بلع بهسبب فشردن مری؛ گرفتگی صدا بهدلیل اختلال در اعصاب حنجره؛ و سندرم هورنر با ایجاد اختلال در دستگاه عصبی سمپاتیک پدیدار میگردند.[12][17] علاوه بر سندرم هورنر (افتادگی پلک و کوچک شدن مردمک در آن طرف)، تومور ریه ممکن است به شبکه بازویی آسیب بزند.[1] سندرم هورنر همچنین در تومورهای قلهٔ ریه، معروف به تومورهای پانکوست، شایع است، که همچنین باعث درد شانه میشود که دردش به سمت داخلی بازو (سمت انگشت کوچک دست) میزند و همچنین دندهٔ بالایی قفسه سینه را تخریب میکند.[17] تورم غدد لنفاوی بالای استخوان ترقوه ممکن است نشان دهنده توموری باشد که در قفسه سینه گسترش یافتهاست.[12] تومورهایی که جریانِ خون را به قلب مسدود میکنند میتوانند سبب بروز سندرم ورید اجوف فوقانی (تورم قسمت فوقانی بدن و تنگی نفس) شوند، در حالی که تومورهایی که به ناحیه اطراف قلب نفوذ میکنند، ممکن است سبب تجمع مایع در اطراف قلب، آریتمی قلب (ضربان قلب نامنظم) و نارسایی قلبی شوند.[17]
از هر سه نفری که دچار سرطان ریه میشوند، یک نفر دارای علائم ناشی از متاستاز به مکانهایی غیر از ریه است.[17] سرطان ریه قادر است به هر نقطه از بدن گسترش یابد و بسته به محلِ متاستاز، علائم متفاوتی دارد. متاستازهای مغزی میتوانند باعث سردرد، تهوع، استفراغ، تشنج و نقایص عصبی شوند. متاستازهای استخوانی باعث درد، شکستگی استخوان و فشردگی نخاع شوند. متاستاز به مغز استخوان ممکن است سبب کاهش شدید سلولهای خونی و سیتوپنی، کمخونی و حضور سلولهای نابالغ در گردش خون شوند.[17] متاستازهای کبدی میتوانند باعث بزرگ شدن کبد، درد در ربع فوقانی راست شکم، تب و کاهش وزن شوند.[17]
تومورهای ریه اغلب باعث ترشح هورمونهای دگرگونکنندهٔ بدن میشوند که علائمی غیرعادی به نام نشانگان پارانئوپلاستیک ایجاد میکنند.[17] ترشح نامناسب هورمون باعث تغییرات چشمگیر در غلظت مواد معدنی خون میشود. شایعترین نوع این اختلال یونی، هایپرکلسمی (کلسیم خون بالا) است که ناشی از تولید بیش از حد پروتئین مرتبط با هورمون پاراتیروئید یا خودِ هورمون پاراتیروئید است. هایپرکلسمی ممکن است به صورت تهوع، استفراغ، درد شکم، یبوست، پرنوشی، تکرر ادرار و تغییر وضعیت ذهنی ظاهر شود.[17] افراد مبتلا به سرطان ریه معمولاً هیپوکالمی (پتاسیم کم) را به دلیل ترشح نامناسب هورمون آدرنوکورتیکوتروپین و همچنین هیپوناترمی (سدیم کم) به دلیل تولید بیش از حد هورمون ضد ادراری یا پپتید ناتریورتیک دهلیزی تجربه میکنند.[17]
از هر سه بیمار مبتلا به سرطان ریه، یک نفر دچار چماقی شدن ناخن میشوند، در حالی که از هر ۱۰ نفر یک نفر دچار استئوآرتروپاتی هیپرتروفیک ریوی (چماقی شدن ناخن، درد مفاصل و ضخیم شدن پوست) میشود. انواعی از اختلالات خودایمنی ممکن است به شکل سندرمهای پارانئوپلاستیک در مبتلایان به سرطان ریه ایجاد شوند، از جمله سندرم میاستنی لامبرت-ایتون (که موجب ضعف عضلانی میشود)، نوروپاتی محیطی، التهاب ماهیچهها، انسفالیت (و زوالِ خودایمنیِ مخچه، دستگاه لیمبیک یا ساقه مغز).[17] از هر دوازده نفر بیمار مبتلا به سرطان ریه، یک نفر دچار لخته شدن پارانئوپلاستیک خون، از جمله ترومبوفلبیت وریدی مهاجر، تشکیل لخته در قلب و انعقاد درونرگی منتشر (تشکیل لخته در سراسر بدن) است.[17] سندرمهای پارانئوپلاستیک که پوست و کلیهها را درگیر میکنند نادر هستند و هر کدام در یک درصد یا کمتر از مبتلایان به سرطان ریه رخ میدهند.[17]
گاهی این سرطانها بهطور تصادفی و هنگام انجام رادیوگرافیهای منظم تشخیص داده میشوند.[10] در بسیاری از افراد، قبل از اینکه علائم مشخص شوند و فرد به دنبال درمان پزشکی برود، سرطان از محل اصلی خود فراتر رفته و گسترش پیدا کردهاست. محلهای شایع گسترش سرطان ریه عبارتند از مغز، استخوان، غدد فوق کلیوی، ریهٔ سمت مقابل، کبد، آبشامه، و کلیهها.[18] در حدود ۱۰٪ از افراد مبتلا به سرطان ریه در زمان تشخیص علائمی قابل مشاهده نیست؛ این سرطانها در زمان رادیوگرافی منظم قفسه سینه بهطور تصادفی تشخیص داده میشوند.[10]
سرطان پس از آسیب ژنتیکی به دیانای (ماده ژنتیکی وراثتی) گسترش مییابد. این آسیب ژنتیکی بر روی عملکرد طبیعی سلول، از جمله تکثیر سلولی، مرگ سلولی برنامهریزی شده (آپوپتوز) و ترمیم دی ان ای تأثیر میگذارد. هر چقدر آسیب بیشتر شود، خطر ابتلا به سرطان افزایش مییابد.[19]



استعمال دخانیات، به ویژه سیگار تاکنون دلیل اصلی ابتلا به سرطان ریه بودهاست.[20] دود سیگار حاوی بیش از ۶۰ ماده سرطانزا شناخته شدهاست[21] از جمله ایزوتوپ پرتوزا ناشی از فرایند تجزیه رادون، نیترو آمین و بنزوپیرین. به علاوه، نیکوتین واکنش ایمنی بدن را در مقابل رشد سلولهای سرطانی در بافتهای آسیب دیده سرکوب میکند.[22] در سراسر دنیای توسعه یافته، ۹۰٪ از مرگ و میرهای ناشی از سرطان ریه در مردان در طول سال ۲۰۰۰ به استعمال دخانیات مربوط بودهاست (۷۰٪ برای زنان).[23] کشیدن سیگار علت ۸۹–۹۰٪ از موارد ابتلا به سرطان ریه است.[1] به نظر متخصصان سیگار احتمال ابتلا به این بیماری را تا ۲۰ برابر و آلودگی هوا تا دو برابر افزایش میدهد.[24]
استنشاق دود سیگار —فروبردن دود زمانی که فرد دیگری سیگار میکشد -یکی از دلایل ابتلا به سرطان ریه در افرادی است که سیگار نمیکشند. فردی که دود سیگار استنشاق میکند در گروه فردی قرار میگیرد که با یک انسان سیگاری زندگی یا کار میکند. مطالعات بهدست آمده از ایالات متحده آمریکا،[25][26] اروپا،[27] انگلستان، ,[28] و استرالیا،[29] بهطور مداوم نشان دادهاند که خطر ابتلا به سرطان ریه در میان افرادی که در معرض دود سیگار دیگران هستند، بهطور چشمگیری افزایش داشتهاست.[30] احتمال خطر ابتلا به سرطان ریه در افرادی که با یک فرد سیگاری زندگی میکنند، ۳۰٪ بیشتر است درحالیکه افرادی که در محیطی کار میکنند که دود سیگار دیگران در آنجا وجود دارد، با ۱۹٪ افزایش خطر ابتلا مواجه هستند.[31] تحقیقات دربارهٔ دود جریان کناری نشان میدهد که این نوع دود از دود مستقیم خطرناک تر است.[32] استنشاق دود سیگار دلیل سالانه حدود ۳٬۴۰۰ مرگ و میر ناشی از سرطان ریه در ایالات متحده آمریکا است.[26]
رادون یک گاز بیرنگ و بیبو است که در اثر تجزیه رادیم رادیواکتیو که خود محصول تجزیه اورانیوم موجود در پوسته زمین است، به وجود میآید. محصولات تجزیه شده در اثر پرتو مواد ژنتیکی را یونیزه میکنند و موجب جهشهایی میشوند که گاهی سرطان زا هستند. رادون، بعد از استعمال دخانیات، دومین دلیل شایع سرطان ریه در ایالات متحده آمریکا است.[26] خطر سرطان درازای هر ۱۰۰ Bq/m³ افزایش در تجمع رادون، ۸–۱۶٪ افزایش مییابد.[33] میزان گاز رادون بسته به محل و ترکیب خاک و سنگهای زیرین متغیر است. برای نمونه، در مناطقی مانند کورنوال در انگلستان (که گرانیت لایه زیرین آنجا است)، گاز رادون یک مشکل اساسی است، و ساختمانها باید با فن کاملاً تهویه شوند تا تجمع گاز رادون کاهش یابد. آژانس حفاظت محیط زیست ایالات متحده آمریکا (EPA) برآورد کردهاست که از هر ۱۵ خانه در ایالات متحده آمریکا میزان رادون یک خانه بالای دستورالعمل توصیه شده ۴ کوری در لیتر (pCi/l) (148 Bq/m³) است.[34]
پنبه نسوز (پنبه نسوز یا آزبست) میتواند دلیل انواع مختلفی از بیماریهای ریه، از جمله سرطان ریه، باشد. استعمال تنباکو و آزبست روی ایجاد سرطان ریه تأثیر سینرژیک دارد.
آلودگی هوای بیرون تأثیر ناچیزی روی افزایش خطر ابتلا به سرطان ریه دارد.[4] ذرات (PM2.5) و ذرات گوگرد، که ممکن است از دود اگزوز خودروها ساطع شود، باعث میشوند خطر ابتلا به سرطان به میزان ناچیزی افزایش یابد.[4][35] در خصوص نیتروژن دیاکسید، افزایش تدریجی ۱۰ قسمت در میلیارد احتمال خطر سرطان ریه را ۱۴٪ افزایش میدهد.[36] آلودگی هوای بیرون ۱–۲٪ احتمال خطر ابتلا به سرطان ریه را افزایش میدهد.[4]
شواهد تجربی نشان میدهد که احتمال خطر ابتلا به سرطان ریه در اثر آلودگی هوا در فضای سرپوشیده مربوط به سوختن چوب، زغال چوب، کود یا مانده محصول برای پختوپز و گرم کردن بیشتر است.[37] خطر سرطان ریه در زنانی که در معرض دود زغال در فضای سرپوشیده هستند دو برابر بیشتر است و تعدادی از ضایعات ناشی از سوختن زیستتوده سرطان زا شناخته شدهاند یا مشکوک به آن هستند.[38] این خطر حدود ۲٫۴ میلیون نفر را در سراسر دنیا تحت تأثیر خود قرار دادهاست،[37] و ۱٫۵٪ از مرگ و میرهای ناشی از سرطان ریه به این دلیل اتفاق میافتند.[38]
اینگونه برآورد شدهاست که ۸ تا ۱۴٪ از موارد سرطان ریه به دلیل عوامل ارثی ایجاد میشوند.[39] احتمال خطر ابتلا به سرطان ریه در افرادی که خویشاوندان او به این بیماری مبتلا هستند، ۲٫۴ برابر بیشتر است. احتمال دارد دلیل این امر ترکیب ژنها باشد.[40]
مواد، مشاغل، و معرضگذاریهای بسیار دیگری با سرطان ریه ارتباط داده شدهاست. آژانس بینالمللی مطالعات سرطان (IARC) عنوان میکند که «شواهد کافی» برای سرطانزا بودن موارد زیر برای ریه در دست است:[41]
همانند بسیاری از سرطانهای دیگر، سرطان ریه نیز توسط فعال شدن آنکوژن یا غیرفعال شدن ژنهای سرکوبگر تومور آغاز میشود.[43] اعتقاد بر این است که انکوژنها (ژنهای تومورزا) انسانها را بیشتر مستعد سرطان میسازند. اعتقاد بر این است که پروتوانکوژنها در هنگام قرار گرفتن در معرض مواد سرطانزای خاص به انکوژنها (ژنهای تومورزا) تبدیل میشوند.[44] جهشهای ایجاد شده در پروتوانکوژن K-ras مسبب ۱۰–۳۰٪ از آدنوکارسینوماها میباشد.[45][46] پذیرنده عامل رشد روپوستی (EGFR) عملکردهای تکثیر سلولی، خزان یاختهای، رگزایی، و هجوم توموری را تنظیم میکند.[45] جهش و تقویت EGFR در سرطان ریهٔ از نوع «سلولهای غیرکوچک» رایج بوده و پایه و اساس درمان با مهارکنندههای EGFR را شکل میدهد. پروتئین Her2/neu کمتر مورد تأثیر قرار میگیرد.[45] آسیب کروموزومی میتواند به از دست رفتن هتروزیگوتی منجر شود. این موضوع میتواند به غیرفعال شدن ژنهای سرکوبگر تومور منجر شود. آسیبدیدگی کروموزومهای 3p، 5q، 13q، و 17p بهطور خاص در کارسینوم ریه سلول-کوچک رایج است. ژن سرکوبگر تومور پی۵۳، واقع بر روی کروموزوم 17p، در ۶۰–۷۵٪ موارد مورد تأثیر قرار میگیرد.[47] سایر ژنهایی که اغلب مورد جهش یا تقویت قرار میگیرند عبارتند از c-MET, NKX2-1، LKB1، PIK3CA، و BRAF.[45]
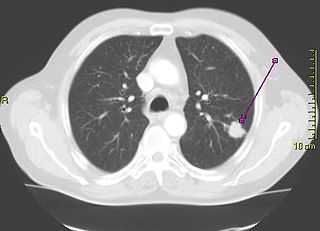
انجام یک رادیوگرافی قفسه سینه یکی از نخستین مراحل تحقیقی است که باید در صورت گزارش نشانههایی توسط فرد که ممکن است دال بر سرطان ریه باشد، صورت پذیرد. این کار میتواند یک توده مشخص، گشادگی میانسینه (که میتواند بیانگر گشادگی غدد لنفاوی واقع در آنجا باشد)، آتلکتازی (جمع شدن ریه)، التهاب ریه، یا ترشح پرده جنبی را آشکار نماید.[2] تصویربرداری سیتی نوعاً به منظور ارائه اطلاعات بیشتر در مورد نوع و درجهٔ بیماری مورد استفاده قرار میگیرد. نایژهبینی یا بافتبرداری هدایت شده توسط سیتی اغلب برای نمونهبرداری تومور برای بافتآسیبشناسی مورد استفاده قرار میگیرد.[10]
سرطان ریه اغلب به صورت یک توده ریوی منزوی بر روی یک پرتونگاری قفسه سینه ظاهر میشود. لیکن تشخیص افتراقی آن بسیار گستردهاست. بسیاری از بیماریهای دیگر نظیر سل، عفونتهای قارچی، سرطان دگردیس، یا التهاب سازماندهنده ریه نیز میتوانند چنین نمودی را نتیجه دهند. از جمله علل کمتر رایج «توده ریوی منزوی» میتوان به هامارتومها، کیستهای برونکوژنیکها، ورمهای غدهای، ناهنجاری شریانی و وریدی، انزوای ریوی، تودههای روماتیسمی، گرانولوماتوز وگنر یا لنفوم اشاره نمود.[48] سرطان ریه همچنین میتواند یک یافتن تصادفی باشد که به صورت یک توده ریوی منزوی بر روی یک پرتونگاری قفسه سینه یا سیتی اسکن انجام شده بنا بر یک دلیل ناشناخته ظاهر میگردد.[49] تشخیص قطعی سرطان ریه بر پایه یک بررسی بر پایهٔ بافتشناسی بافت مورد ظن از نظر ویژگیهای بالینی و ویژگیهای وابسته به پرتونگاری میباشد.[1]
| نوع وابسته به بافتشناسی | شیوع به ازای هر ۱۰۰٬۰۰۰ نفر در سال |
|---|---|
| همه انواع | ۶۶٫۹ |
| آدنوکارسینوما | ۲۲/۱ |
| کارسینوم سلول-فلسدار | ۱۴/۴ |
| کارسینوم سلول-کوچک | ۹/۸ |
سرطانهای ریه بر اساس نوع وابسته به بافتشناسی ردهبندی میشوند.[8] این ردهبندی برای تعیین نوع مدیریت بیماری و پیشبینی نتایج بیماری حائز اهمیت است. اکثریت قریب به اتفاق سرطانهای ریه کارسینوماها هستند —بدخیمیهایی که در نتیجه بافت پوششی پدید میآیند. — کارسینومهای ریه بر اساس اندازه و شکل سلولهای بدخیم دیده شده توسط یک متخصص هیستوپاتولوژی در زیر یک میکروسکوپ ردهبندی میشوند. دو رده گسترده آنها کارسینوم ریه سلول-غیرکوچک و کارسینوم ریه سلول-کوچک میباشد.[50]

سه نوع فرعی NSCLC عبارتند از آدنوکارسینوما، کارسینوم ریه سلول-فلسدار، و کارسینوم ریه سلول-بزرگ.[1]
حدود ۴۰٪ از سرطانهای ریه «آدنوکارسینوما» هستند که معمولاً در بافت ریوی جانبی شکل میگیرد.[8] اغلب موارد آدنوکارسینوما با سیگار کشیدن در ارتباط هستند؛ لیکن در میان افرادی که در طول عمر خود کمتر از ۱۰۰ نخ سیگار کشیدهاند (غیرسیگاریها)،[1] آدنوکارسینوما رایجترین شکل سرطان ریه است.[51] یک نوع فرعی از آدنوکارسینوما یعنی کارسینوم برونکیولوئالوئولار در زنهای غیرسیگاری رایجتر بوده و ممکن بقای طولانیمدت بهتری را به همراه داشته باشد.[52]
کارسینوم سلول-فلسدار حدود ۳۰٪ از سرطانهای ریه را تشکیل میدهد. آنها نوعاً در نزدیکی مجاری هوای بزرگ پدید میآیند. یک حفره توخالی و مرگ سلولی مرتبط با آن بهطور رایج در مرکز تومور یافت میشود.[8] حدود ۹٪ سرطانهای ریه «کارسینوم سلول-بزرگ» هستند. اینها به این دلیل اینگونه نام گرفتهاند که سلولهای سرطانی مرتبط با آنها بزرگ بوده و دارای سیتوپلاسم زیاد از حد، هستهها بزرگ و هستکهای گرد میانهسته بزرگ میباشند.[8]

در کارسینوم ریه سلول-کوچک (SCLC)، سلولها در بر گیرنده دانههای ترشح عصبی (کیسههای کوچک در بر گیرنده هورمونهای درونتراو عصبی) میباشند که این تومور را با سندروم درونتراو/پارانئوپلاستیک مرتبط ساختهاست.[53] اغلب موارد در مجاری هوای بزرگتر (نایژههای اولیه و ثانویه) پدید میآیند.[10] این سرطانها خیلی سریع رشد پیدا میکنند و خیلی زود در همان مراحل اولیه بیماری گسترش مییابند. شصت تا هفتاد درصد مبتلایان دچار بیماری دگردیس هستند. این نوع سرطان ریه بهشدت با سیگار کشیدن در ارتباط است.[1]
از لحاظ بافتشناسی چهار نوع فرعی اصلی شناخته شدهاست، درحالیکه برخی از سرطانها ممکن است ترکیبی از انواع فرعی مختلف را دربر گیرند.[50] از جمله انواع فرعی نادر میتوان به تومورهای غدهای، تومورهای کارسینوئیدی، و کارسینومهای نامتمایز اشاره نمود.[1]
| نوع وابسته به بافتشناسی | لکهگذاری ایمنی |
|---|---|
| کارسینوم سلول-فلسدار | CK5/6 مثبت CK7 منفی |
| آدنوکارسینوما | CK7 مثبت TTF-1 مثبت |
| کارسینوم سلول-بزرگ | TTF-1 منفی |
| کارسینوم سلول-کوچک | TTF-1 مثبت CD56 مثبت کروموگرانین مثبت سینپتوفیزین مثبت |
ریه محلی رایج برای گسترش تومور از سایر نقاط بدن است. ردهبندی سرطانهای ثانویه بر اساس محلی که از آن نشأت میگیرند صورت میپذیرد؛ برای مثال سرطان پستانی که به ریه گسترش یافته باشد سرطان پستان دگردیس نامیده میشود. دگردیسیها معمولاً دارای یک ظاهر مشخصه گرد بر روی پرتونگاری قفسه سینه هستند.[54]
خود سرطانهای ریه بهطور رایج به مغز، استخوانها، کبد، و غدد فوق کلیوی دگردیسی پیدا میکنند.[8] لکهگذاری ایمنی یک بیوپسی (زندهبینی) معمولاً برای تشخیص منشأ اصلی آن کارآمد است.[55]
ارزیابی مرحله پیشرفت سرطان ریه عبارت از ارزیابی درجهٔ گسترش سرطان از منشأ اصلی آن میباشد. این یکی از عوامل مؤثر بر پیشبینی روند بیماری و معالجهٔ احتمالی سرطان ریه بهشمار میرود.[1]
برای ارزیابی اولیه مرحلهٔ پیشرفت سرطان ریه سلول-غیرکوچک (NSCLC) از ردهبندی TNM استفاده میشود. این سیستم بر اساس تومور (tumor) اولیه، درگیری غده لنفاوی (lymph node)، و دگردیسی (metastasis) راه دور میباشد. پس از این، با استفاده از توصیفگرهای TNM یک گروه مرحلهٔ پیشرفت بیماری در محدوده بین سرطان پنهان تا مراحل ۰، IA (یک-A), IB, IIA, IIB, IIIA, IIIB و IV (چهار) تخصیص داده میشود. این گروه مرحلهٔ پیشرفت بیماری در انتخاب نوع معالجه و پیشبینی روند بیماری مؤثر است.[56] کارسینوم ریه سلول-کوچک (SCLC) بهطور سنتی به عنوان سرطان دارای «پیشرفت محدود» (محدود شده به نیمی از قفسه سینه و در محدوده یک تکمیدان پرتودرمانی تابآوردنی) یا سرطان دارای «پیشرفت گسترده» (سرطان دارای میزان پیشرفت بیشتر) ردهبندی شدهاست.[1] لیکن سیستم ردهبندی و گروهبندی TNM برای پیشبینی روند بیماری مؤثر است.[56]
هم برای NSCLC و هم برای SCLC، دو نوع کلی ارزیابی مرحلهٔ پیشرفت بیماری عبارت از «ارزیابی بالینی» و «ارزیابی توسط جراحی» میباشند. ارزیابی بالینی مرحلهٔ پیشرفت بیماری پیش از جراحی قطعی صورت میپذیرد. این روش بر مبنای نتایج مطالعات تصویربرداری (نظیر سیتی اسکن و اسکن PET) و نتایج بیوپسی (زندهبینی) میباشد. ارزیابی مرحلهٔ پیشرفت بیماری توسط جراحی چه در حین عمل و چه پس از آن صورت میپذیرد و بر مبنای ترکیب نتایج یافتههای جراحی و بالینی، شامل نمونهبرداری غدد لنفاوی قفسه سینه توسط جراحی، میباشد.[8]
پیشگیری، مقرونبهصرفهترین روش برای کاهش گسترش سرطان ریه است. با آنکه در اغلب کشورها مواد سرطانزای صنعتی و خانگی مورد شناسایی قرار گرفته و استفاده از آنها منع گردیدهاست، کشیدن تنباکو هنوز بسیار فراگیر است. حذف کشیدن تنباکو یک هدف اصلی در پیشگیری از سرطان ریه میباشد و توقف سیگار کشیدن یک ابزار پیشگیرانه مهم در این فرایند بهشمار میرود.[57]
تعیین مقررات به منظور کاهش آسیبپذیری از سیگار کشیدن دیگران در اماکن عمومی نظیر رستورانها و محلهای کار در بسیاری از کشورهای غربی از رواج بیشتری برخوردار گشتهاست.[58] کشور بوتان از سال ۲۰۰۵ مقررات منع کامل سیگار کشیدن را به اجرا درآورده است[59] در حالی که کشور هند سیگار کشیدن در اماکن عمومی را از ماه اکتبر ۲۰۰۸ منع کردهاست.[60] سازمان بهداشت جهانی از دولتها درخواست کردهاست تبلیغ تنباکو را بهطور کامل منع کنند تا از سیگاری شدن افراد جوان اجتناب گردد. آنها ارزیابی میکنند در جاهایی که چنین منعهایی به اجرا درآمدهاست مصرف تنباکو به میزان ۱۶٪ کاهش پیدا کردهاست.[61]
استفاده بلند مدت از مکمل ویتامین آ،[62][63] ویتامین ث،[62] ویتامین دی[64] یا ویتامین ای[62] احتمال ابتلا به سرطان ریه را کاهش نمیدهد. بعضی مطالعات نشان میدهد خطر ابتلا به این بیماری در افرادی که دارای رژیم غذایی محتوی سبزیجات و میوه جات زیاد میباشند کمتر است،[26][65] اما این امر به احتمال زیاد به دلیل اثر همزمان میباشد. مطالعات دقیق تر دیگر ارتباط واضحی بین این دو به دست نیامده است.[65]
آزمایشهای غربالگری به استفاده از آزمایش پزشکی به منظور تشخیص بیماری در افرادی که فاقد علائم بیماری هستند گفته میشود. آزمایشهایی که ممکن است برای تشخیص سرطان ریه به کار روند شامل آزمایش آسیبشناسی سلول خلط سینه، رادیوگرافی قفسه سینه (CXR) و مقطعنگاری رایانهای (CT) میباشند. برنامههای بیماریابی با استفاده از رادیوگرافی قفسه سینه یا آسیبشناسی سلول مفید واقع نشدند.[66] فرایند بیماریابی در مورد افراد دارای ریسک بالا (به عبارتی افراد بین سنین ۵۵ تا ۷۹ سال که بیش از ۳۰ پاکت-سیگار استفاده میکنند یا افرادی که سابقه سرطان ریه بودهاند) به صورت سالانه با استفاده از سی تی اسکن دوز پایین ممکن است باعث کاهش احتمال مرگ ناشی از سرطان ریه به میزان کاهش ریسک مطلق ۳درصد و کاهش ریسک نسبی ۲۰درصد شود.[67][68] با این وجود، نرخ بالایی از اسکنهای مثبت وجود دارد که ممکن است باعث شود به روشهای تهاجمی و نیز هزینههای مالی قابل توجه نیاز نباشد.[69] به ازای هر اسکن مثبت واقعی بیش از ۱۹ اسکن مثبت اشتباه وجود دارد.[70] قرار گرفتن در معرض تشعشع یکی از آسیبهای احتمالی بیمار یابی است.[71]
درمان سرطان به نوع سلول، وسعت گسترش آن و وضعیت عملکردی بیمار بستگی دارد. درمانهای رایج شامل مراقبت تسکینی،[72] جراحی، شیمیدرمانی و پرتودرمانی میباشد.[1]
سایبر نایف جدیدترین روش درمان تومورهای سرطانی به صورت جراحی بسته میباشد و کاملاً میتواند جایگزینی برای عمل جراحی باز باشد با این تفاوت که درمان با این روش بدون درد، خونریزی و کمترین عوارض جانبی برای بیماران سرطانی میباشد. علاوه بر این درصد موفقیت و نابود کردن تومورهای سرطانی با این روش بسیار بالاست.

در صورتی که بررسیها سرطان سلولهای غیر کوچک ریه را تأیید کنند، مرحله بندی سرطان مورد ارزیابی قرار میگیرد تا مشخص شود این بیماری به وسیله جراحی قابل درمان است یا پیشروی آن به حدی است که نمیتوان به وسیله جراحی آن را درمان کرد. سی تی اسکن و برشنگاری با گسیل پوزیترون به منظور تعیین این امر مورد استفاده قرار میگیرند.[1] در صورتی وجود غدد لنفاوی مدیاستن از مدیاستینوسکوپی به منظور نمونه برداری غدد و کمک به مرحله بندی استفاده میشود.[73] تست خون و آزمونهای عملکرد ریه مورد استفاده قرار میگیرند تا مشخص شود بیمار شرایط تحت عمل جراحی قرار گرفتن دارد یا خیر.[10] جراحی در صورتی صورت نمیگیرد که در آزمون عملکرد ریه مشخص شود بیمار دارای ظرفیت تنفسی پایین است.[1] در اکثر موارد سلولهای غیر کوچک ریه، برداشت ناحیه ریه لوبکتومی بهترین درمان میباشد. در بیمارانی که شرایط این گونه درمان را ندارند جداسازی قسمت کوچکتری از ریه برش گوهای انجام میشود. به هر حال، احتمال بازگشت بیماری در روش برش گوهای نسبت به روش لوبکتومی بیشتر است.[74]ید براکیتراپی رادیواکتیو در کنارههای محل جراحی میتواند احتمال بازگشت بیماری را کاهش دهد.[75] در موارد نادری برداشت تمام ریه نومونکتومی انجام میگیرد. روشهای جراحی از طریق ویدئو توراکوسکوپی و لوبکتومی تراسکوسکوپیک در جراحی سرطان ریه از فرایندی کم خطر تر در جراحی سرطان ریه بهره میبرند.[76] لوبکتومی تراسکوسکوپیک همان کارایی لوبکتومی باز معمول را دارد، ولی مزیت آن کاهش بیماریهای بعد از عمل جراحی است.[77] در سرطان سلول کوچک ریه، بهطور معمول از شیمی درمانی و/یا پرتو درمانی استفاده میشود.[78] با این وجود، نقش جراحی در سرطان سلول کوچک ریه در نظر گرفته میشود. جراحی ممکن است به همراه شیمی درمانی و پرتودرمانی در مراحل اولیه درمان سرطان سلول کوچک ریه بهبود قابل توجهی در وضعیت بیمار ایجاد کند.[79]
لوبکتومی- حذف لوب کامل ریه- روشی پذیرفتهشده برای از بین بردن سرطان ریه است، آنهمزمانی که ریه بهخوبی کار میکند. خطر مرگ بین ۳ تا ۴ درصد است و در بیماران سالمند، این درصد بالاتر است. اگر عملکرد ریه مانع لوبکتومی شود، سرطان کوچکی به منطقهای محدود، محدود میشود که میتوان با برداشتن برخش کوچکی از بافت حاشیه ریه، آن را حذف کرد. به این کار برداشتن سولوبار میگویند همچنین ممکن است به آن برداشت ناقص یا ناکامل نیز بگوید. برداشت سولوبار باعث کم شدن عملکرد ریه میشود. کل ریه لازم باشد که از طریق ریهبرداری حذف شود، میزان مرگومیر مورد انتظار، ۵ تا ۸ درصد میشود. بیماران سالمند درخطر بالاتری هستند.
پرتودرمانی در بیشتر موارد با شیمی درمانی همراه است و ممکن است به قصد درمان در مورد افرادی که دارای سرطان سلولهای غیر کوچک ریه هستند و شرایط جراحی را نداشته باشند به کار رود. این نوع پرتودرمانی را پرتودرمانی رادیکال مینامند.[80] نوع جدید این شیوه پرتودرمانی تسریع شده و بیش تفکیک شده مداوم (CHART) نام دارد که در آن پرتودرمانی زیاد در یک بازه زمانی کوتاه صورت میگیرد.[81] پرتودرمانی سینهای پس از عمل نباید بعد از جراحی سرطان سلولهای غیر کوچک ریه به کار رود.[82] این احتمال وجود دارد که پرتودرمانی بعد از عمل در بعضی از بیمارانی که دارای درگیری غده لنفاوی میان سینهای هستند مفید واقع شود.[83] درکنار شیمی درمانی، پرتودرمانی قفسه سینه در مواردی از که احتمال درمان سرطان ریه با یاختههای کوچک وجود دارد توصیه میشود.[8] اگر رشد سرطان بخش کوچکی از نایژه را مسدود کند، براکیتراپی (پرتودرمانی موضعی) در داخل لوله تنفسی صورت میگیرد تا این راه را باز کند.[84] برایکی تراپی در مقایسه با پرتودرمانی بیرونی باعث کاهش زمان درمان و نیز کاهش در معرض اشعه قرار گرفتن کارکنان مراکز درمانی میشود.[85] پرتودرمانی پیشگیرانه جمجمه (PCI) نوعی از پرتودرمانی مغز است که به منظور کاهش احتمال متاستاز مورد استفاده قرار میگیرد. این شیوه در اکثر موارد سرطان ریه با یاختههای کوچک مفید است. پرتودرمانی پیشگیرانه جمجمه در مواردی که بیماری پیشرفت نکرده احتمال بهبود فرد در طول سه سال را از ۱۵٪ به ۲۰٪ افزایش میدهد؛ در مواردی که بیماری پیشرفت داشته، این احتمال از ۱۳٪ به ۲۷٪ میرسد.[86] پیشرفتهای اخیر در هدف درمانی و عکس برداری منجر به پیشرفت پرتودرمانی استریوتاکتیک در درمان سرطان ریه شدهاست. در این نوع پرتودرمانی، با استفاده از هدف درمانی، پرتو زیادی در جلسههای کوتاه بر روی بیمار صورت میگیرد. استفاده از این روش در مرحله اول برای بیمارانی است که به علت همایندی مرضی شرایط جراحی را ندارند.[87] در بیمارانی که دچار سرطان ریه با یاختههای کوچک یا با یاختههای بزرگتر هستند، انجام میزان کمی پرتو به سینه میتواند برای کنترل نشانه مراقبت تسکینی مورد استفاده قرار گیرد.[88] پس از مدتی سلولهای سرطانی، به پرتو مقاوم میشوند. یکی از عوامل مقاوم کردن سلولها به پرتو، بیان بیش از حد آنزیم سیکلواکسیژناز-۲ است. سنجش سمیت و آنالیز وسترن بلات نشان داده که تیمار اولیه سلولها با دوزهای غیرکشنده از آسپرین، با حساس کردن سلولهای این نوع سرطان به اشعهٔ گاما باعث افزایش چشمگیر آپوپتوز و کاهش بقای سلولها میشود. با استفاده از تکنیک ثبت پیکربندی کروموزوم مشخص شدهاست که داروی آسپرین از طریق ایجاد اختلال در ساختار لوپ کروماتین آنزیم سیکلواکسیژناز-۲ منجر به افزایش حساسیت سلولهای ریه به پرتوی گاما و آپوپتوز میشود.[89]
چگونگی شیمیدرمانی به نوع تومور بستگی دارد.[8] در سرطان ریه با یاختههای کوچک، سیس پلاتین و اتیپوساید بیشتر مورد استفاده قرار میگیرد. ترکیب کربوپلاتین، جمسیتابین، پاکلیتاکسل، وینورلبین، توپوتکان و ایرینوتکان نیز مورد استفاده قرار میگیرد.[90][91] در سرطان ریه با یاختههای بزرگتر پیشرفته (NSCLC)، شیمی درمانی باعث بهبود بیمار میشود و به عنوان اولین درمان مورد استفاده قرار میگیرد، به این شرط که بیمار شرایط درمان را داشته باشد.[92] بهطور کلی، دو دارو مورد استفاده قرار میگیرد، که یکی از آنها بر پایه پلاتین (یا سیس پلاتین یا کربوپلاتین) میباشد. داروهای معمول دیگر جمسیتابین، پاکلیتاکسل، دوستاکسل،[93][94] پمترکسد،[95]اتیوپوساید یا وینورلبیبن میباشند.[94]
شیمیدرمانی کمکی به استفاده از شیمی درمانی پس از جراحی به ظاهر درمانی برای بهبود نتیجه اشاره دارد. در NSCLC، نمونهها در طول جراحی از غدد لنفاوی اطراف گرفته میشوند تا به مرحله بندی کمک کنند. در صورت تأیید مرحله ۲ یا ۳ بیماری، شیمی درمانی کمکی میتواند پس از پنج سال احتمال زنده ماندن فرد را ۵٪ درصد افزایش بدهد. .[96][97] ترکیب وینورلبین و سیس پلاتین از رژیمهای قدیمی مؤثرتر است.[97] شیمی درمانی کمکی برای افرادی که مبتلا به مرحله IB سرطان هستند بحثبرانگیز است، زیرا آزمایشهای بالینی بهطور واضح نشان ندادهاند که این امر مفید واقع خواهد شد.[98][99] آزمایشهای شیمی درمانی قبل از عمل (شیمی درمانی نئوادجوانتی) NSCLC قابل برداشت بینتیجه بودهاند. .[100]
ممکن است مراقبت تسکینی یا مدیریت بیمارستانی برای افراد مبتلا به بیماری ترمینال مناسب باشد.[10] این رویکردها فرصتی برای بحث و گفتگوی بیشتر دربارهٔ گزینههای درمان ایجاد میکنند و امکان میدهند تا تصمیمات سنجیده و مناسبی اخذ شود[101][102] و میتوانند از مراقبتهای بیفایده اما پرهزینه در پایان عمر افراد جلوگیری کنند.
در درمان NSCLC ممکن است شیمی درمانی با مراقبتهای تسکین دهنده همراه شود. در موارد پیشرفته، شیمی درمانی مناسب نسبت به استفاده تنها از مراقبتهای حمایتی متوسط بقای افراد را افزایش میدهد و نیز سطح کیفی زندگی را بالا میبرد.[103] در صورت وجود آمادگی جسمانی مناسب، شیمی درمانی مداوم در طول تسکین سرطان ریه ۱٫۵ تا ۳ ماه به عمر فرد میافزاید، سرطان را تسکین میدهد و سطح کیفی زندگی را بالا میبرد و با وجود عوامل مدرن نتایج بهتری بهدست آمدهاست. .[104][105] گروه مشارکتی تجزیه و تحلیل متا NSCLC پیشنهاد میدهد که اگر گیرنده میخواهد و میتواند درمان را تحمل کند، شیمی درمانی باید در مرحله پیشرفته NSCLC انجام شود.[92][106]
| مرحله بالینی | درصد افرادی که پنج سال زنده ماندهاند | |
|---|---|---|
| سرطان ریه بدون سلول ریز | سرطان ریه سلول ریز | |
| IA | ۵۰ | ۳۸ |
| IB | ۴۷ | ۲۱ |
| IIA | ۳۶ | ۳۸ |
| IIB | ۲۶ | ۱۸ |
| IIIA | ۱۹ | ۱۳ |
| IIIB | ۷ | ۹ |
| IV | ۲ | ۱ |
پیشآگهی این بیماری در کل ضعیف است. از بین تمام افراد مبتلا به سرطان ریه، ۱۵٪ به مدت پنج سال بعد از تشخیص بیماری زنده میمانند.[2] معمولاً مرحله بیماری در زمان تشخیص پیشرفتهاست. در زمان ارائه، ۳۰–۴۰٪ از موارد NSCLC در مرحله چهارم، و ۶۰٪ از SCLC در مرحله ششم هستند.[8]
عوامل پیش آگاهی در NSCLC عبارتست از وجود یا عدم وجود علائم ریوی، اندازه نئوپلاسم، بافتشناسی نوع سلول، شدت گسترش (مرحله) و متاستاز تا غدد لنفاوی چندگانه، و تهاجم عروقی. در خصوص افرادی که بیماری آنها جراحی نشدنی است، نتایج برای افرادی با وضعیت عملکرد ضعیف و کاهش وزن بیش از ۱۰٪ وخیم تر است.[107] عوامل پیش آگاهی در سرطان ریه سلول کوچک عبارتست از وضعیت عملکرد، جنسیت، مرحله بیماری، و درگیری دستگاه عصبی مرکزی یا کبد در زمان تشخیص.[108]
در خصوص NSCLC، بهترین پیشبینی بیماری از طریق برداشت کامل جراحی مرحله IA بیماری حاصل میشود، با حداکثر ۷۰٪ احتمال زنده ماندن برای پنج سال.[109] در خصوص SCLC، احتمال کلی زنده ماندن برای مدت پنج سال ۵٪ است.[1] احتمال زنده ماندن افراد مبتلا به SCLC مرحله شدید برای مدت پنج سال کمتر از ۱٪ است. میانگین مدت بقا برای بیماری که در مرحله محدود است ۲۰ ماه برآورد شدهاست و احتمال بقا به مدت پنج سال ۲۰٪ است.[2]
طبق دادههای ارائه شده از سوی انستیتو ملی سرطان ایالات متحده آمریکا، میانگین سنی در تشخیص سرطان ریه در ایالات متحده آمریکا ۷۰ سال است،[110] و میانگین سن فوت ۷۲ سال برآورده شدهاست.[111] در آمریکا، احتمال دارد افرادی که بیمه درمانی دارند به نتیجه بهتری دست یابند.[112]

no data
≤ ۵
5-10
10-15
15-20
20-25
25-30
|
30-35
35-40
40-45
45-50
50-55
≥ ۵۵
|
در سراسر دنیا، سرطان ریه شایعترین سرطان از لحاظ شیوع و مرگ و میر بهشمار میرود. در سال ۲۰۰۸، ۱٫۶۱ میلیون مورد جدید، و ۱٫۳۸ میلیون مرگ و میر ناشی از سرطان ریه گزارش شد. بالاترین نرخها در اروپا و آمریکای شمالی است.[11] جمعیتی که احتمال ایجاد سرطان ریه در آنها بیشتر است افراد بالای ۵۰ سال هستند که سابقه کشیدن سیگار دارند. برخلاف میزان مرگ و میر در مردان، که از بیش از ۲۰ سال پیش در حال کاهش است، نرخ مرگ و میر ناشی از سرطان ریه در زنان در طول دهههای گذشته افزایش یافتهاست، و اخیراً در حال تثبیت است.[114] در آمریکا، خطر مادامالعمر ابتلا به سرطان ریه در مردان ۸٪ و در زنان ۶٪ است.[1]
در ازای هر ۳–۴ میلیون سیگاری که روشن میشود، یک مرگ در اثر سرطان ریه اتفاق میافتد.[1][115] تأثیر صنعت توتون و تنباکو نقش مهمی را در فرهنگ استعمال دخانیات ایفا میکند.[116] افراد جوانی که سیگار نمیکشند، با مشاهده تبلیغات تنباکو بیشتر تشویق میشوند که سیگار بکشند. .[117] استنشاق دود سیگار بهطور روزافزون به عنوان یک عامل خطر ابتلا به سرطان ریه در حال شناخته شدن است[30] و منجر به دخالت سیاستی میشود تا میزان قرار گرفتن ناخواسته در معرض دود سیگار دیگران کاهش یابد.[118] دودی که از خودروها، کارخانجات، و نیروگاهها ساطع میشود نیز دارای خطرات بالقوه هستند.[4]
اروپای شرقی بالاترین آمار مرگ و میر ناشی از سرطان ریه را در بین مردان به خود اختصاص دادهاست، درحالیکه اروپای شمالی و آمریکا بالاترین آمار مرگ و میر را در میان زنان دارد. در آمریکا، مردان و زنان سیاهپوست بیشتر به این بیماری مبتلا میشوند.[119] نرخ سرطان ریه در حال حاضر در کشورهای در حال توسعه کمتر است.[120] با افزایش استعمال دخانیات در کشورهای در حال توسعه، انتظار میرود در چند سال آینده این نرخ به ویژه در چین[121] و هند بالا رود.
از دهه ۶۰، نرخ آدنوکارسینوم ریه نسبت به سایر انواع سرطانهای ریه افزایش یافت. این امر مقداری به معرفی سیگارهای فیلتردار مربوط میشود. استفاده از فیلتر ذرات بزرگتر را از دود تنباکو جدا میکند، بنابراین میزان رسوب در راههای تنفسی بزرگتر را کاهش میدهد. با این حال، فرد سیگاری باید بازدم عمیقتری داشته باشد تا همان میزان نیکوتین به بدن وی وارد شود، در نتیجه میزان رسوب ذرات در راههای تنفسی کوچک افزایش مییابد و در همانجا آدنوکارسینوم ایجاد میشود.[122] ابتلا به آدنوکارسینوم ریه همچنان اتفاق میافتد.[123]
قبل از پیدایش دود سیگار سرطان ریه یک بیماری نادر بود؛ حتی تا سال ۱۷۶۱ به عنوان یک بیماری مجزا شناخته نشده بود.[124] در سال ۱۸۱۰ توضیحات بیشتری دربارهٔ جنبههای مختلف سرطان ریه ارائه شد.[125] در سال ۱۸۷۸ تومورهای کشنده ریه فقط ۱٪ از تمام سرطانهای مشاهده شده در کالبدشکافی را تشکیل داده بود، اما تا اوایل دهه ۱۹۰۰ این میزان به ۱۰–۱۵٪ رسید.[126] طبق گزارشهای پروندهای در سوابق پزشکی تعداد افراد مبتلا به سرطان ریه در سال ۱۹۱۲ فقط ۳۷۴ تن در سراسر دنیا بودهاست،[127] اما مروری بر کالبدشکافیها نشان داد که سرطان ریه از ۰٫۳٪ در سال ۱۸۵۲ به ۵٫۶۶٪ در سال ۱۹۵۲ رسید.[128] در آلمان، در سال ۱۹۲۹ پزشکی به نام Fritz Lickint رابطه بین سیگار کشیدن و سرطان ریه را کشف کرد،[126] که منجر به یک کمپین ضد سیگار تهاجمی شد.[129] تحقیق پزشکان بریتانیا، منتشر شده در دهه ۱۹۵۰، اولین مدرک معتبر اپیدمیولوژیک دربارهٔ رابطه بین سرطان ریه و سیگار کشیدن بود.[130] در نتیجه، در سال ۱۹۶۴ جراح عمومی ایالات متحده آمریکا به افراد سیگاری توصیه کرد که باید سیگار را ترک کنند.[131]
ارتباط با گاز رادون برای اولین بار در میان معدن چیان در کوههای سنگ معدن در نزدیکی اشنیبرگ، ساکسونی مشخص شد. از سال ۱۴۷۰ از این معدنها نقره استخراج میشد، و این معادن غنی از اورانیوم همراه با رادیوم و گاز رادون بودند.[132] این معدن چیان به بیماری ریوی مبتلا شدند، و در نهایت در دهه ۱۸۷۰ مشخص شد که سرطان ریه دارند.[133] با وجود این اکتشاف، کار در معادن تا دهه ۱۹۵۰ و به دلیل درخواست USSR برای اورانیوم ادامه یافت.[132] در دهه ۱۹۶۰ تأیید شد که رادون یک عامل ابتلا به سرطان ریه است.[134]
اولین پنومونکتومی موفقیتآمیز برای سرطان ریه در سال ۱۹۳۳ انجام شد. پرتونگاری تسکین دهنده از دهه ۱۹۴۰ مورد استفاده قرار گرفت. پرتونگاری رادیکال، که در ابتدا در دهه ۱۹۵۰ از آن استفاده شد، تلاشی بود برای استفاده از دوزهای پرتویی بزرگتر در بیماران مبتلا به سرطان ریهای که کم و بیش در مرحله ابتدایی قرار دارند، اما با این حال برای جراحی مناسب نیستند. در سال ۱۹۹۷، پرتودرمانی هایپر فرکشن پرشتاب و مستمر نسبت به پرتودرمانی رادیکال معمول یک پیشرفت بهشمار میآمد. تلاشهای اولیه در خصوص سرطان ریه سلول کوچک در دهه ۱۹۶۰ دربرداشت جراحی و پرتودرمانی رادیکال ناموفق بود. در دهه ۱۹۷۰، رژیمهای پرتودرمانی موفقیتآمیزی ایجاد شدند.
Seamless Wikipedia browsing. On steroids.
Every time you click a link to Wikipedia, Wiktionary or Wikiquote in your browser's search results, it will show the modern Wikiwand interface.
Wikiwand extension is a five stars, simple, with minimum permission required to keep your browsing private, safe and transparent.