Top-Fragen
Zeitleiste
Chat
Kontext
Cyanidin
chemische Verbindung Aus Wikipedia, der freien Enzyklopädie
Remove ads
Cyanidin ist ein zur Gruppe der Anthocyanidine zählender kationischer Pflanzenfarbstoff. An unterschiedliche Kohlenhydrate (Zucker) glycosidisch gebunden ist Cyanidin Bestandteil zahlreicher Anthocyane, z. B. von Cyanidin-3-O-glucosid, die auch in pflanzlichen Lebensmitteln vorkommen. Es ist strukturell eng verwandt mit Peonidin und Rosinidin, bei denen einige Hydroxygruppen stattdessen als Methylether vorliegen.
Remove ads
Geschichte
Blaufarbene Blüten und Früchte waren für Naturforscher schon immer faszinierende Objekte. So untersuchten die französischen Chemiker E. Frémy und S. Cloëz die blauen Pflanzenfarbstoffe der Kornblume, des Veilchens und der Schwertlilie, und bezeichneten diese mit dem Namen Cyanin (gr. cyanos, κυανός, blau).[5] Richard Willstätter und Arthur E. Everest legten 1913 eine umfangreiche Abhandlung über Anthocyane vor, in der sie u. a. über den Farbstoff der Kornblume (Centaurea cyanus L.) berichteten. Sie fanden, dass Cyanin ein Glycosid ist, genauer ein Glucosid. Es wird durch Hydrolyse mit Mineralsäuren in Glucose und die eigentliche Farbstoffkomponente, das Aglykon, gespalten, das die Autoren als Cyanidin bezeichneten.[6] Das Aglykon wurde daraufhin auch in den Blütenblättern der Winteraster (Chrysanthemum indicum L.), der Stiefmütterchen (Viola species) sowie der Löwenmäulchen (Antirrhinum majus) – Klassikern der Pflanzengenetik – nachgewiesen und daraus isoliert. Die Autoren nannten es folglich Chrysanthemin bzw. Antirrhinin.[7][8][9]
Remove ads
Vorkommen
Abgesehen von der Kornblume und den obengenannten Pflanzen ist Cyanidin in Glycosidform als Anthocyan in vielen Pflanzen enthalten, darunter Rotkohl, roten Rosen, Hibiskus, Blaubeeren, Himbeeren, Pflaumen, Holunderbeeren, Brombeeren, Blutorangen und Rhabarber.[10]
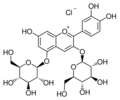
- Cyanin (Cyanidin-3,5-O-diglucosid)
- Chrysanthemin, Kuromanin (Cyanidin-3-O-glucosid)
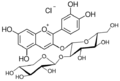
- Antirrhinin, Keracyanin, Prunicyanin, Sambucin (Cyanidin-3-O-rutinosid)
- Sambicyanin (Cyanidin-3-O-sambubiosid)
- Cyanidin-3-O-glycoside in Holunder
Remove ads
Gewinnung und Herstellung
Cyanidin wurde durch Extraktion und hydrolytische Abspaltung der Kohlenhydrat (Zucker)- Komponente gewonnen. Zur Isolierung wird das Chlorid – Cyanidinchlorid – hergestellt. Den Arbeitskreisen von Willstätter und Robinson gelangen Synthesen, die damals zum Strukturbeweis dienten (siehe auch Pelargonidin).

Das Chlorid des Cyanidins ließ sich aus verdünnter alkoholischer Salzsäure, d. h. einer Lösung von Chlorwasserstoff in 96-prozentigem Ethanol, in Kristallform als Monohydrat ausfällen.
Eigenschaften
Zusammenfassung
Kontext
Das Salz bildet braunrote Nadeln, die metallisch glänzen. Entfernt man das Kristallwasser durch Erhitzen, so schmilzt die wasserfreie Verbindung nicht unter 300 °C. Cyanidinchlorid ist praktisch unlöslich in Wasser.[3] Es löst sich gut in Ethanol mit violetter Färbung, in wässriger Natriumcarbonat-Lösung mit blauer Farbe (siehe unten). In verdünnter Salzsäure oder Schwefelsäure ist die Löslichkeit gering. In saurer Lösung absorbiert das Cyanidin-Kation Licht im Bereich von ca. 450–580 nm mit einem Absorptionsmaximum bei 535 nm.[11] Dies entspricht der roten Farbe des Flavylium-Kations. Bei einem pH-Wert von 6–6,5 wird es zu einem rotvioletten Produkt mit chinoider Struktur deprotoniert.[2] Bis pH 8 wandelt sich diese Farbe durch weitere Deprotonierung in königsblau. Bei noch höherem pH zeigen Extrakte von schwarzem Holunder oder Rotkohl auch Grünfärbungen.
Cyanidin als Indikator
Da sich die Struktur von Cyanidin je nach pH-Wert der Umgebung ändert und jede Struktur eine andere Farbe besitzt, kann eine Cyanidinhaltige Lösung zur Bestimmung des pH-Wertes über nahezu die gesamte pH-Skala benutzt werden, eignet sich daher als Indikator.[12] Die 3-O-Glycoside und 3,5-O-Diglycoside des Cyanidins verhalten sich prinzipiell genauso.



1 – 3 – 5 – 7 – 8 – 9 – 10 – 11 – 13
In den Pflanzen (Kornblume, Stiefmütterchen) liegt Cyanidin nicht als solches vor, sondern als Komplex mit Aluminium- und Eisen-Ionen. Seine Struktur ist kompliziert.[13] Der Farbstoff besteht aus einem Chelat-Komplex, in dessen Zentrum sich ein Al3+- und ein Fe3+-Ion befinden, die unter anderem von Cyanin- und Flavon-Molekülen umgeben sind. Der Komplex besteht aus sechs Anthocyan- (Cyanin und Succinylcyanin) und sechs Flavon-Molekülen sowie zwei Metall-Ionen (Fe(III) und Al(III)).[14]
Remove ads
Literatur
- Norbert Welsch und Claus Chr. Liebmann: Farben, Natur Technik. In: Kunst. 2. Auflage 2006, Spektrum Akademischer Verlag, ISBN 3-8274-1563-2.
Einzelnachweise
Wikiwand - on
Seamless Wikipedia browsing. On steroids.
Remove ads