proteïna globular que forma els microfilaments cel·lulars From Wikipedia, the free encyclopedia
L'actina és una proteïna globular que forma els microfilaments, un dels tres components fonamentals del citoesquelet de les cèl·lules eucariotes. S'expressa a totes les cèl·lules dels organismes pluricel·lulars, especialment a les fibres musculars, en les quals participa en la contracció muscular juntament amb la miosina i altres elements. Pot trobar-se en forma lliure, anomenada actina G, o formant part de polímers lineals anomenats microfilaments o actina F, que són essencials per a funcions cel·lulars tan importants com la mobilitat i la contracció de la cèl·lula durant la divisió cel·lular.
La importància capital de l'actina s'entén pel fet que un elevat percentatge del contingut proteic d'una cèl·lula és d'actina i que la seva seqüència està molt conservada, és a dir, ha canviat molt poc al llarg de l'evolució. Per ambdues raons es pot dir que la seva estructura ha estat optimitzada. Se'n poden destacar dos trets peculiars: és un enzim que hidrolitza ATP, la "moneda universal de l'energia" dels processos biològics, fent-ho molt lentament, però al mateix temps necessita aquesta molècula per mantenir la seva integritat estructural. Adquireix la seva forma eficaç en un procés de plegament gairebé dedicat. A més, és la proteïna que estableix més interaccions amb altres proteïnes de totes les conegudes, fet que li permet exercir funcions molt variades que arriben a gairebé tots els aspectes de la vida cel·lular. La miosina és un exemple de proteïna que uneix actina; un altre exemple és la vil·lina, que pot entrellaçar l'actina en feixos o bé pot tallar els filaments d'actina, depenent de la concentració de catió calci en el seu entorn.[3]
L'actina forma microfilaments en un procés dinàmic que proporciona una bastida que dota la cèl·lula d'una forma amb possibilitat de remodelar-se ràpidament en resposta al seu entorn o senyals de l'organisme, per exemple, augmentant la superfície cel·lular per a l'absorció o proporcionant suport a l'adhesió de les cèl·lules per a formar teixits. Sobre aquesta bastida es poden ancorar altres enzims, orgànuls com el cili, dirigir la deformació de la membrana cel·lular externa que permet la ingestió cel·lular o la citocinesi. També pot generar moviment, ja sigui per ella mateixa o ajudada per motors moleculars. D'aquesta manera contribueix a processos com el transport intracel·lular de vesícules i orgànuls i la contracció muscular, o la migració cel·lular, important en el desenvolupament embrionari, en la reparació de ferides o en la invasivitat del càncer. L'origen evolutiu d'aquesta proteïna es remunta a les cèl·lules procariotes, on poden trobar equivalents. Finalment, també és important en el control de l'expressió gènica.
Un bon nom de malalties tenen com a base alteracions genètiques en al·lels dels gens que governen la producció de l'actina o de les seves proteïnes associades, i també són essencials en el procés d'infecció d'alguns microorganismes patògens. Les mutacions en els diferents gens d'actina presents en humans ocasionen miopaties, variacions en la grandària i la funció cardíaca i sordesa. Els components del citoesquelet també tenen relació amb la patogenicitat de bacteris intracel·lulars i virus, especialment en processos relacionats amb l'evasió de la resposta del sistema immunitari.[4]

L'actina va ser observada experimentalment per primera vegada el 1887 per William D. Halliburton, qui va extraure una proteïna muscular que coagulava preparacions de miosina i la denominà «ferment de la miosina».[5] No obstant això, Halliburton va ser incapaç d'efectuar la caracterització de les seves observacions, i per això el descobriment s'atribueix a Brunó Ferenc Straub, que en aquells moments era un jove bioquímic que treballava al laboratori d'Albert Szent-Györgyi a l'Institut de química mèdica de la Universitat de Szeged, Hongria.
El 1942, Straub va desenvolupar una nova tècnica per a l'extracció de proteïnes musculars que li permetia aïllar quantitats substancials d'actina relativament pura. Aquest mètode és el mateix que essencialment s'utilitza en els laboratoris de l'actualitat. Szent-Györgyi havia descrit prèviament una forma més viscosa de miosina, produïda per extraccions lentes en músculs, com "miosina activada" i, ja que la proteïna de Straub produïa l'efecte activador, la va denominar «actina». La viscositat disminuïa si s'afegia ATP a la barreja d'ambdues proteïnes, coneguda com a actomiosina. El treball d'ambdós no va poder ser publicat en els països occidentals a causa de l'ambient bèl·lic de la Segona Guerra Mundial, i va sortir a la llum el 1945 quan va ser publicat com a suplement de l'Acta Physiologica Scandinavica.[6] Straub va continuar treballant amb l'actina fins al 1950, publicant que podia unir-se a l'ATP i que, durant la polimerització de la proteïna per a formar microfilaments, s'hidrolitzava a ADP + Pi, el qual romania unit al microfilament. Straub va suggerir que aquesta reacció ocupava un paper en la contracció muscular, però això només és cert en el cas del múscul llis i no va ser verificat experimentalment fins al 2001.[7][8]
La seqüència d'aminoàcids va ser completada per Elzinga i col·laboradors el 1973,[9] i l'estructura cristal·logràfica de l'actina G va ser determinada el 1990 per Kabsch i col·laboradors, tot i tractar-se d'un cocristall en el qual formava un complex amb la desoxirribonucleasa I;[10] es proposà un model el mateix any per a l'actina F per Holmes i els seus col·laboradors.[11] Aquest procediment de cocristal·lització amb diferents proteïnes va ser emprat repetidament durant els següents anys, fins que el 2001 s'aconseguí cristal·litzar la proteïna aïllada juntament amb ADP. Va ser possible gràcies a l'ocupació d'un conjugat de rodamina que impedia la polimerització bloquejant l'aminoàcid cys-374.[12] Aquell mateix any es va produir la defunció de Christine Oriol-Audit, la investigadora que el 1977 va aconseguir cristal·litzar per primera vegada l'actina en absència d'ABPs. Els cristalls van resultar massa petits per a la tecnologia de l'època.[13]
Tot i que actualment no existeix un model d'alta resolució de la forma filamentosa, l'equip de Sawaya va realitzar el 2008 una aproximació més exacta basant-se en múltiples cristalls dels dímers d'actina que contacten en diferents llocs.[14] Aquest model va ser refinat pel mateix autor i per Lorenz. Altres enfocaments, com l'ús de microscopia crioelectrònica o radiació per sincrotró han permès recentment augmentar el nivell de resolució i comprendre amb major profunditat la naturalesa de les interaccions i els canvis conformants implicats en la formació dels filaments d'actina.[15][16]
L'actina és una de les proteïnes més abundants entre els eucariotes i es troba present en tot el citoplasma.[3] De fet, en les fibres musculars representa el 20% en pes total de les proteïnes, i en altres cèl·lules animals està entre l'1 i el 5%. No obstant això, no existeix un únic tipus d'actina, sinó que els seus gens codificants estan definits per una família multigènica (família que, en plantes, alberga més de 60 elements, entre gens i pseudogens i, en humans, més de 30).[17] Això significa que la informació genètica de cada individu té instruccions per generar variants de l'actina (anomenades isoformes) que posseeixen funcions lleugerament diferents. D'aquesta manera, els organismes eucariotes expressen diferents gens que donen lloc a: l'actina α, que es troba en estructures contràctils; l'actina β, a la vora en expansió de les cèl·lules que empren la projecció d'estructures mòbils com a mètode de mobilitat; i l'actina γ, en els filaments de les fibres d'estrès.[18] A més de les similituds existents entre les isoformes d'un organisme, també hi ha una conservació evolutiva pel que fa a estructura i funció entre organismes de dominis diferents de l'eucariota: en bacteris es coneix l'homòleg MreB, una proteïna que és capaç de polimeritzar en microfilaments,[16] i en arqueus hi ha un representant (Ta0583) encara més semblant a les actines d'eucariotes.[19]
L'actina es presenta a la cèl·lula en dues formes: com a monòmers globulars denominats actina G i com a polímers filamentosos anomenats actina F (és a dir, filaments compostos de multitud de monòmers d'actina G). L'actina F també es pot denominar microfilament. A cada bri d'actina s'uneix una molècula d'adenosina trifosfat (ATP) o d'adenosina difosfat (ADP) al seu torn associada a un catió Mg2+. De les diferents combinacions possibles entre les formes d'actina i el nucleòtid trifosfat, en la cèl·lula predominen l'actina G-ATP i l'actina F-ADP.[20][21]
Pel que fa a la seva estructura molecular, l'actina G té una aparença globular al microscopi electrònic de rastreig, no obstant això, mitjançant la cristal·lografia de raigs X es pot apreciar que està composta de dos lòbuls separats per una esquerda, l'estructura conforma el plec ATPasa, un centre de catàlisi enzimàtica capaç d'unir l'ATP i Mg² i hidrolitzar el primer a ADP més fosfat. Aquest plec és un motiu estructural conservat que també està present en altres proteïnes que interaccionen amb nucleòtids trifosfat com l'hexoquinasa (un enzim del metabolisme energètic) o les proteïnes Hsp70 (una família de proteïnes que contribueixen que altres proteïnes tinguin estructures funcionals).[22] L'actina G només és funcional quan posseeix o bé ADP o bé ATP en la seva esquerda, no obstant això, en la cèl·lula predomina l'estat unit a l'ATP quan l'actina es troba lliure.[20]

L'actina cristal·litzada per Kabsch, que és la més utilitzada com a model en estudis estructurals (ja que va ser la primera a ser purificada) procedeix del múscul esquelètic del conill. Té unes dimensions aproximades de 67 x 40 x 37 Å, una massa molecular de 41785 UMA i un punt isoelèctric estimat en 4,8. La seva càrrega neta a pH = 7 és de -7.[23] [24]
La seqüència d'aminoàcids completa d'aquest tipus d'actina va ser determinada per Elzinga i col·laboradors el 1973 i afinada en treballs posteriors pel mateix autor. Conté 374 residus d'aminoàcids. El seu extrem N-terminal és molt àcid. Comença amb un aspartat acetilat en el seu grup amina, mentre que el seu C-terminal és bàsic, format per una fenilalanina precedida per una cisteïna de certa importància funcional. Tots dos extrems se situen en una posició molt propera dins del subdomini I. Pel que fa a aminoàcids anòmals, cal destacar una Nτ-metilhistidina en la posició 73.[23]
Està formada per dos dominis coneguts com a gran i petit, separats per una esquerda en el centre se situa el lloc d'unió a l'ATP-ADP + Pi. Per sota d'aquest hi ha una escotadura de menor profunditat anomenada solc. Quant es troben en forma nativa, malgrat el seu nom, tots dos tenen una mida equiparable.[9]
En els estudis topològics, per convenció, la proteïna s'orienta de manera que el domini major queda a l'esquerra, mentre que el menor se situa a la dreta. En aquesta posició, el domini petit es divideix al seu torn en el subdomini I (posició inferior, residus 1-32, 70-144 i 338-374) i subdomini II (posició superior, residus 33-69). El domini major també es divideix en dos, el subdomini III (inferior, residus 145-180 i 270-337) i el subdomini IV (superior, residus 181-269). La zona exposada dels subdominis I i III es denomina extrem "barbat", mentre que a la dels subdominis II i IV se l'anomena extrem "en punta de fletxa". Aquesta denominació fa referència al fet que a causa de la petita massa del subdomini 2, l'actina adquireix polaritat, que es discutirà posteriorment en parlar de la dinàmica d'acoblament. Alguns autors nomenen els subdominis com Ia, Ib, IIa i IIb, respectivament.[25]
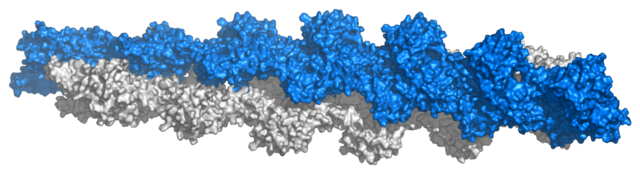
Una descripció clàssica afirma que l'actina F té una estructura filamentosa interpretable com una hèlix levogira monocatenaria amb gir de 166º i increment de 27,5 Å o bé com una hèlix dextrogira bicatenaria amb mig pas de rosca de 350-380 Å, estant cada actina envoltada de quatre.[27] La simetria del polímer d'actina, que és d'unes 2,17 subunitats per volta d'hèlix és incompatible amb la formació de cristalls, que només és possible quan aquestes són exactament 2, 3, 4 o 6 subunitats per volta. Per tant, s'han d'efectuar models que interpretin dades procedents de tècniques que salven aquests inconvenients, com la microscòpia electrònica, la criomicroscòpia electrònica, cristalls de dímers en diferents posicions o difracció de raigs X.[16] Parlar d'una "estructura" no és correcte per una cosa tan dinàmica com un filament d'actina: en realitat s'hauria de parlar de diferents estats estructurals, entre els quals la dada més constant és l'increment de 27,5 Å, mentre que la rotació de les subunitats mostra una considerable variabilitat, i és normal observar desplaçaments de fins al 10% de la seva posició ideal. Algunes proteïnes, com la cofilina, semblen incrementar l'angle de gir, però novament es pot interpretar que, en lloc d'això, estabilitzen alguns "estats estructurals" normals. Aquests podrien ser importants en el procés de la polimerització.[28]
Pel que fa al radi de gir o gruix del filament, les mesures són més controvertides: mentre que els primers models li assignaven una longitud de 25 Å, dades actuals de difracció de raigs X recolzats per criomicroscòpia electrònica coincideixen en uns 23,7 Å. Aquests mateixos estudis han determinat amb força precisió els punts de contacte entre monòmers. Uns s'estableixen amb unitats de la mateixa cadena, entre l'extrem "barbat" d'un monòmer i l'extrem "en punta de fletxa" del següent, mentre que els monòmers de cadenes adjacents fan contacte lateralment mitjançant projeccions del subdomini 4, sent les més importants la formada pel C-terminal i un enllaç hidròfob format per tres cossos en els quals intervenen els residus 39-42, 201-203 i 286. Per formar part d'un filament, segons aquest model, els monòmers estarien en una configuració anomenada "plana", en què els subdominis giren entre si, i que també sembla trobar-se a l'homòleg bacterià de l'actina MreB.[16]
Ja que totes les subunitats d'un microfilament apunten cap al mateix extrem, es diu que el polímer presenta polaritat en la seva estructura. Aquest fet ha creat una convenció: l'extrem que posseeix una subunitat d'actina exposant el lloc pel qual uneix ATP al medi se l'anomena «extrem (-)» mentre que l'oposat, en el qual l'esquerda està dirigida a un altre monòmer adjacent, rep el nom d'«extrem (+)».[18] La denominació «en punta de fletxa» i «barbat» dels extrems dels microfilaments es deu al seu aspecte al microscopi electrònic de transmissió quan es processen mitjançant una tècnica anomenada «decoració». Aquest mètode consisteix en l'addició d'elements S1 de la miosina en teixits fixats amb àcid tànnic, aquesta miosina s'uneix de forma polar als monòmers d'actina, cosa que dona lloc a una configuració semblant a fletxes amb plomes al llarg de tot el seu fust, on el fust correspondria a l'actina i les plomes a la miosina. D'aquesta manera, l'extrem del microfilament que queda sense miosina sobresortint s'interpreta com la punta de la fletxa, mentre l'oposat s'anomena barbat.[29]
Al múscul, el filament helicoidal de l'actina F conté també una molècula de tropomiosina, una proteïna d'una longitud de 40 nanòmetres que s'enrotlla al voltant de l'hèlix d'actina F. Durant l'estat de repòs cel·lular, la tropomiosina recobreix els llocs actius de l'actina de manera que no s'aconsegueix la interacció actina-miosina que produeix la contracció muscular. Unides al llarg del fil de tropomiosina hi ha altres molècules proteiques, les troponines, complexos de tres polímers: troponina I, troponina T i troponina C.[30]

L'actina pot adquirir espontàniament una gran part de la seva estructura terciària.[32] No obstant això, mostra un comportament molt especial i gairebé únic en la forma en què adquireix la seva forma plenament funcional a partir de la seva forma nativa acabada de sintetitzada. La raó d'una ruta tan especial podria ser la necessitat d'evitar la presència de monòmers d'actina mal plegats, que serien tòxics, ja que podrien actuar com a terminadors inadequats de la polimerització. En qualsevol cas, és clau per a l'estabilitat del citoesquelet, i no només això, sinó que podria ser un procés essencial per a la coordinació del cicle cel·lular.[33][34]
Per això empra obligadament un tipus de xaperonina (proteïna que ajuda a altres a plegar-se) citosòlica del grup II, la CCT, formada per un doble anell de vuit subunitats diferents (heterooctamèric) que es distingeix de les altres xaperones moleculars, i en especial de la seva homòloga arqueobactèria GroEL en el fet que no necessita una co-xaperona que actuï com a tapadora sobre la cavitat central catalítica. Accepta substrats unint-se a ells mitjançant dominis específics, de manera que en principi es va pensar que era exclusiva d'actina i tubulina, encara que actualment s'ha vist per immunoprecipitació que almenys interacciona amb un gran nom de polipèptids, possiblement com a substrats. Actua mitjançant canvis conformacionals dependents d'ATP, necessitant a vegades diverses rondes d'alliberament i catàlisi per completar el seu treball.[35]
Per al seu correcte plegament, l'actina i la tubulina també necessiten específicament el concurs d'una altra proteïna, la prefoldina, un complex heterohexamèric (format per sis subunitats diferents), i tan específicament que fins i tot hi ha coevolucionat. En el cas de l'actina, se li uneix immediatament mentre encara s'està traduint, aproximadament quan té una longitud de 145 aminoàcids, que són els corresponents al domini N-terminal.[36]
S'empren subunitats de reconeixement diferent per l'actina i la tubulina, encara solapades. Probablement en el cas de l'actina es tracta de les subunitats PFD3 i PFD4 que s'uneixen a l'actina en dos llocs, l'I, entre els residus 60-79 i el II, entre els residus 170-198. L'actina es reconeix, es carrega i es lliura a la CCT en conformació oberta per la part interna de l'extrem dels "tentacles" de la prefoldina (vegeu imatge i nota al peu).[n. 1] El contacte en el moment del lliurament és tan breu que no s'arriba a formar un complex ternari, alliberant la prefoldina immediatament.[31]

Posteriorment, la xaperonina citosòlica (CCT) efectua el plegament de l'actina de forma seqüencial, i formant unions amb les subunitats, en comptes de tancar-la en la seva cavitat.[n. 2] Per a això té zones específiques de reconeixement en el seu domini β apical. La primera etapa del plegament consistiria en el reconeixement dels residus 245-249. Posteriorment, altres determinants hi establirien contacte.[37] Tant l'actina com la tubulina s'uneixen a la CCT en conformacions obertes en absència d'ATP. En el cas de l'actina, a cada canvi conformacional s'uneix a dues subunitats, a diferència de la tubulina, que ho fa a quatre. L'actina té seqüències d'unió específiques, interaccionant amb les subunitats CCTδ i β o bé amb CCTδ i CCTε. Després de la unió d'AMP-PNP a la CCT, els substrats van movent-se per la cavitat de la xaperonina. Sembla també que en el cas de l'actina fa falta la proteïna CAP com un possible cofactor en els estadis finals del plegament de l'actina.[34]
Encara no es coneix amb exactitud la regulació d'aquest procés, però se sap que la proteïna PhLP3 (proteïna semblant a la fosducina) regula la seva activitat inhibint-la, mitjançant la formació d'un complex ternari.[35]
L'actina és una ATPasa, és a dir, un enzim que hidrolitza ATP. Aquest conjunt d'enzims es caracteritzen per actuar amb extrema lentitud. Se sap que aquesta ATPasa és "activa" o, cosa que és el mateix, la seva velocitat augmenta unes 40.000 vegades quan l'actina forma part d'un filament.[28] Un valor de referència per a aquesta taxa d'hidròlisi sota certes condicions ideals seria de 0,3 s-1. Posteriorment, el Pi romandria molt de temps unit a l'actina costat de l'ADP, alliberant-se a prop de l'extrem del filament.[38]
Avui dia no es coneixen els detalls moleculars concrets del mecanisme catalític. Encara que hi ha molta polèmica sobre aquest tema, sembla clar que per a la hidròlisi d'ATP cal una conformació "tancada", i es creu que apropa els residus implicats a la distància adequada.[28] Un dels residus clau seria Glu137, situat al subdomini 1. La seva funció seria ancorar la molècula d'aigua que produeix un atac nucleofílic a l'enllaç del fosfat γ de l'ATP, mentre el nucleòtid s'uneix fortament als subdominis 3 i 4. La lentitud del procés catalític es deuria a la gran distància i posició esbiaixada d'aquesta molècula d'aigua que fa al seu reactant. Amb molta probabilitat, el canvi conformacional que es produeix per rotació de dominis entre les formes G i F de l'actina apropa la Glu137, permetent la seva hidròlisi. Segons aquest model, la polimerització i la funció ATPasa estarien desacoblades en un primer moment.[16]

L'actina F combina les qualitats de ser resistent i dinàmica. A diferència d'altres polímers, com l'ADN, que mantenen units els seus elements constitutius mitjançant enllaços covalents, en els filaments d'actina els monòmers s'acoblen per enllaços més febles de tipus no covalent. Això, que en principi debilita l'estructura, ja que es podria trencar per agitació tèrmica, se soluciona mitjançant els enllaços laterals amb els monòmers veïns. Al mateix temps, els enllaços febles mantenen l'avantatge que els extrems del filament poden alliberar o incorporar fàcilment monòmers, de manera que es poden remodelar ràpidament i canviar l'estructura cel·lular de la qual són responsables en resposta a estímuls ambientals. Això últim i el mecanisme bioquímic pel qual s'efectua és el que es coneix com a "dinàmica d'acoblament".[4]
Els estudis de la dinàmica d'addicció i pèrdua de subunitats dels microfilaments s'han realitzat in vitro (és a dir, al laboratori, fora de sistemes mòbils), ja que el polímer d'actina resultant dona lloc a la mateixa actina F produïda in vivo, on aquest procés està controlat per multitud de proteïnes per respondre a les necessitats mòbils, de manera que seria molt difícil observar les seves condicions bàsiques.[39] In vitro, aquest fet es produeix de forma seqüencial: primer, es dona una «fase d'activació», on la unió i intercanvi de cations divalents en llocs específics de l'actina G, unit a ATP, produeixen un canvi conformacional, conegut a vegades com Actina G o monòmer d'actina F, ja que és més semblant a les unitats que se situen en el filament.[25] Això la prepara per a la següent «fase de nucleació», en la qual l'actina G dona lloc a petits fragments inestables d'actina F capaços de polimeritzar-se. Inicialment es formen dímers i trímers de manera inestable. Quant el nom d'aquests és prou gran, té lloc la «fase d'elongació», on el filament es forma i creix ràpidament mitjançant l'addició reversible de nous monòmers a ambdós extrems.[40] Finalment, en l'«equilibri estacionari», els monòmers d'actina G s'intercanvien en els extrems del microfilament sense que variï la longitud total del polímer.[3] En aquesta última fase es defineix la «concentració crítica Cc» com la relació entre les constants d'acoblament i desacoblament (es tracta, doncs, d'una constant de dissociació), i representa la concentració d'actina G en la qual la dinàmica d'addició i eliminació de monòmers no produeix una modificació en la longitud del microfilament. En les condicions usuals in vitro, Cc és de 0,1 μM,[41] cosa que significa que a valors grans es dona una polimerització ja valors menors, una despolimerització.[42]
Un assumpte important que introduït en l'apartat anterior és el fet que, encara que l'actina hidrolitza ATP, tot sembla indicar que això no intervé en l'acoblament, ja que, d'una banda, la hidròlisi es produeix en gran manera a l'interior del filament, i de l'altra, l'ADP també pot polimeritzar-se. Això planteja la qüestió de comprendre quin és el procés termodinàmicament desfavorable que requereix una despesa d'energia tan ingent. L'anomenat "cicle de l'actina", que lliga la hidròlisi a la polimerització, consisteix en l'addició de monòmers d'actina G-ATP preferentment a l'extrem barbat, creant un flux de monòmers cap a l'extrem en punta de fletxa en el qual es coneix com "trenament" (threadmilling, en anglès), on els monòmers estarien en forma d'actina F-ADP i serien alliberats, intercanviant posteriorment aquest ADP per ATP i tancant d'aquesta manera el cicle.
Poc després de l'addició, es produeix la hidròlisi de l'ATP de forma relativament ràpida. Hi ha dues hipòtesis sobre com es produeix, l'estocàstica, en la qual la hidròlisi es produiria a l'atzar influïda en certa manera per les molècules veïnes, i la vectorial, en la qual només es produiria en el límit amb altres molècules que ja han hidrolitzat el seu ATP. En qualsevol cas, no s'allibera el Pi resultant, sinó que roman un temps unit no de manera covalent a l'actina ADP, de manera que existirien tres espècies d'actina en un filament: ATP-actina, ADP + Pi-actina i ADP-actina.[38] El contingut d'un filament en cadascuna d'aquestes espècies depèn de la seva longitud i estat: al començament de l'elongació, el filament té una composició aproximadament equivalent de monòmers amb ATP i ADP + Pi i una petita quantitat al costat de l'extrem (-) d'actina ADP. A mesura que s'assoleix l'estat estacionari, la situació s'inverteix, estant la major part del filament amb ADP i l'extrem (+) pràcticament només amb ADP + Pi, amb l'ATP reduït a l'extrem.[43]
Si es comparen els filaments d'actina-ADP purs amb aquells que incorporen ATP, en els primers les constants crítiques són similars en ambdós extrems, mentre que en els altres dos nucleòtids la Cc són diferents, sent major en l'extrem (+), amb la qual es donen les següents situacions:[18]
Per tant, es pot deduir que l'energia de la hidròlisi s'utilitza per a crear un veritable "estat estacionari", és a dir, d'un flux en lloc d'un simple equilibri, la qual cosa dota de dinamisme, polaritat i força de tracció al filament, cosa que justifica la despesa pel guany de funcions biològiques essencials.[38] A més, la configuració dels diferents tipus de monòmers és detectada per les proteïnes d'unió a l'actina que controlen aquest dinamisme, com es veurà en la propera secció.[44]

In vivo, el citoesquelet d'actina no està compost exclusivament d'actina, sinó que per la seva generació, permanència i funció requereix altres proteïnes, que es denominen proteïnes d'unió a l'actina (ABP, actin binding proteins) i intervenen en la seva polimerització i despolimerització, en la seva estabilitat, en la seva organització en feixos o xarxes, en la seva fragmentació i en la seva destrucció.[3] La diversitat d'aquestes proteïnes és tal, que es considera que l'actina és la proteïna que participa en la majoria d'interaccions proteïna-proteïna de quantes es coneixen.[46] Per exemple, hi ha elements que segresten l'actina G, impedint la seva incorporació als microfilaments. De la mateixa manera, hi ha proteïnes que estimulen la seva polimerització o que doten de complexitat a les xarxes en síntesis.[18]

Altres proteïnes d'unió a actina regulen la longitud dels microfilaments realitzant talls en ells, la qual cosa dona lloc a nous extrems actius per a la polimerització. És a dir, si un microfilament, que posseeix dos extrems els quals poden unir-se o dissociar monòmers, és tallat dues vegades, resulten tres nous microfilaments amb sis extrems, la nova situació afavoreix la dinàmica d'acoblament i desacoblament. Entre aquestes proteïnes destaquen la gelsolina i la cofilina. Cal ressaltar que primer realitzen el tall mitjançant canvis en la conformació del monòmer d'actina al que s'uneixen en el polímer, quedant després recobrint el nou extrem (+) generat, el que impedeix l'agregat o l'intercanvi de noves subunitats d'actina G i, ja que els extrems (-) queden sense recobrir, afavoreixen la despolimerització dels filaments.[51]
Un altre tipus de proteïnes d'unió a l'actina recobreixen els extrems de l'actina F per tal d'estabilitzar-los, sense capacitat de trencar-los. Exemples d'aquestes proteïnes són CapZ (que uneix els extrems (+) segons els nivells de Ca2 + / calmodulina de la cèl·lula, nivells que depenen de senyals externs i internes de la cèl·lula i que intervenen en la regulació de les seves funcions biològiques)[52] o la tropomodulina (que uneix els extrems (-)). La tropomodulina és essencial com estabilitzador de l'actina F present en les miofibrilles dels sarcòmers del múscul, estructures caracteritzades per la seva gran estabilitat.[53]

El complex Arp2/3 es troba àmpliament difós en tots els organismes eucariotes.[55] Està compost per set subunitats, algunes de les quals tenen una topologia clarament relacionada amb la seva funció biològica: dues de les seves subunitats, anomenades «ARP2» i «ARP3», tenen una estructura molt semblant als mateixos monòmers d'actina. Aquesta homologia permet a ambdues unitats comportar-se com a agents nucleants de la polimerització dels monòmers d'actina G a actina F. A més, aquest complex és necessari per establir estructures dendrítiques i en anastomosi (és a dir, bifurcades o en xarxa), per tant més complexes, d'actina F.[56]

Existeixen diverses toxines que interfereixen amb la dinàmica de les actines, tant despolimerizant-les (latrunculina i citocalasina D) com estabilizant-les (faloidina):
L'actina com a proteïna es troba tant en el citoplasma com al nucli cel·lular.[61] Aquesta localització està regulada per les vies de transducció de senyals que integren els estímuls que la cèl·lula rep i que permet la reestructuració de les xarxes d'actina en resposta a aquells. En Dictyostelium, s'ha referit la intervenció de la ruta de fosfoinosítits intervinguda per la fosfolipasa D.[62] Els filaments d'actina són especialment abundants i estables en les fibres musculars. Dins del sarcòmer (la unitat morfològica i fisiològica de les fibres musculars) l'actina es disposa en les bandes I i A, en aquesta última, es presenta conjuntament amb la miosina.[63]

Els microfilaments intervenen en el moviment de totes les cèl·lules mòbils, fins i tot les no musculars, ja que s'ha descrit que els fàrmacs que desorganitzen l'actina F (com les citocalasines) afecten l'activitat d'aquestes cèl·lules. Com a proteïna, l'actina suposa el 2% del total de proteïnes en hepatòcits, el 10% en fibroblasts, el 15% a amebes i fins al 50-80% en plaquetes activades.[64] Existeixen diferents grups d'actina, amb estructura i funció lleugerament diferents. D'aquesta manera, l'actina α és exclusiva de fibres musculars, i la present en altres cèl·lules sol ser del tipus β i γ. A més, l'actina de diferent tipus de la α sol posseir una alta taxa de recanvi que provoca que la major part d'ella no formi part d'estructures permanents. Així, els microfilaments en les cèl·lules no musculars apareixen de dues formes:[65]
En llevats, el citoesquelet d'actina és clau durant els processos d'endocitosi, citocinesi, determinació de la polaritat cel·lular i durant la morfogènesi. Aquests fets, a més de dependre de l'actina, impliquen de 20 a 30 proteïnes associades, altament conservades evolutivament, així com multitud de molècules de senyalització; aquests elements permeten, en combinació, un assemblatge especialment i temporalment modulat que defineix la biologia cel·lular en resposta a estímuls interns i externs.[66]
Els llevats posseeixen tres grans tipus d'elements productes de l'associació de l'actina: pegats, cables i anells que, tot i detectar durant llargs períodes, es veuen sotmesos a un equilibri dinàmic a causa de la contínua polimerització i despolimerització. Com proteïnes accessòries, tenen una cofilina/ADF de 16 kDa (codificiada per un únic gen, denominat COF1), Aip1, un cofactor de la cofilina que afavoreix el desencadellat dels microfilaments, Srv2/CAP, un regulador de la dinàmica relacionat amb proteïnes adenilat ciclases, una profilina d'aproximadament 14 kDa que s'associa als monòmers d'actina, i tinfilina, una proteïna de 40 kDa implicada en l'organització de les estructures tipus pedaç.[66]
Els estudis de genòmica de plantes han revelat l'existència d'isovariants proteiques dins de la família de gens de l'actina, dins d'Arabidopsis thaliana, una magnoliòpsida emprada com a organisme model, hi ha almenys deu tipus d'actines, nou de tubulines α, sis de tubulines β, sis de profilines i dotzenes de miosines. Tal diversitat s'explica d'acord amb la necessitat evolutiva de posseir variants lleugerament diferents en la seva pauta d'expressió temporal i espacial, no obstant això, la majoria d'elles s'expressen conjuntament en els teixits analitzats. L'entramat de xarxes d'actina es distribueix per tot el citoplasma de les cèl·lules cultivades in vitro, amb un reforç entorn del nucli que es connecta, mitjançant radis, a l'escorça cel·lular; aquest entramat és altament dinàmic, amb un polimeritzat i despolimerizat continu.[67]

Si bé les cèl·lules vegetals posseeixen generalment una paret que defineix la seva morfologia i impedeix el seu moviment, els seus microfilaments generen les forces necessàries per a diverses activitats cel·lulars, per exemple, els corrents citoplasmàtics generats pels microfilaments i les miosines. A més, l'actina intervé en el moviment d'orgànuls i morfogènesi cel·lular, processos que inclouen la divisió cel·lular, l'elongació i la diferenciació.[69]
Pel que fa a les proteïnes associades al citoesquelet d'actina presents en plantes cal esmentar:[69] la vil·lina, una proteïna de la família de la gelsolina/severina, capaç de tallar microfilaments i unir monòmers d'actina en presència del catió calci; la fimbrina, un element capaç de reconèixer i unir monòmers d'actina i que intervé en la formació d'entramats (mitjançant una regulació diferent de la pròpia de cèl·lules animals i llevats);[70] les formines, proteïnes capaces d'actuar com a agent nucleant de la polimerització a actina F; la miosina, típic motor molecular propi d'eucariotes que, en Arabidopsis thaliana, està codificat per 17 gens classificats en dues classes diferents; CHUP1, capaç d'unir actina i implicat en la distribució espacial dels cloroplasts en la cèl·lula; KAM1/MUR3, una proteïna que defineix la morfologia del complex de Golgi així com la composició en xiloglucans de la paret cel·lular; NtWLIM1, proteïna que faculta l'aparició d'estructures aovillades d'actina; i ERD10, que participa en l'associació entre orgànuls delimitats per membranes i els microfilaments i que sembla tenir un paper especialment rellevant en presència de l'estrès.

Al múscul, el filament helicoidal de l'actina F conté també una molècula de tropomiosina, una proteïna d'una longitud de 40 nanòmetres que s'enrotlla al voltant de l'hèlix d'actina F. Durant l'estat de repòs cel·lular, la tropomiosina recobreix els llocs actius de l'actina de manera que no s'aconsegueix la interacció actina-miosina (aquesta interacció dona lloc a un lliscament entre tots dos que, per coordinació de moltes còpies d'aquests elements disposats en els músculs, produeix la seva contracció). Unides al llarg del bri de tropomiosina hi ha altres molècules proteiques, les troponines, complexos de tres polímers: troponina I, troponina T i troponina C.[30] La funció moduladora de la tropomiosina depèn de la interacció amb la troponina en presència d'ions de Ca2+.[71]
L'actina, juntament amb la miosina, intervé en la contracció i relaxació dels músculs, constituint les dues al voltant del 90% de les proteïnes musculars.[72] El procés global es dispara mitjançant un senyal extern, típicament mitjançant un potencial d'acció excitador del múscul que alberga les cèl·lules especialitzades riques en filaments d'actina i miosina en el seu interior. El cicle de contracció-relaxació respon als següents passos:[73]
L'estudi clàssic de la funció de l'actina el circumscriu el manteniment del citoesquelet i, per això, a l'organització i moviment dels orgànuls i determinació de la forma cel·lular.[65] Tanmateix, el paper de l'actina és bastant més ampli en la fisiologia cel·lular eucariota; més encara, existeixen elements semblants en procariotes.

En la majoria dels mamífers existeixen sis gens diferents d'actina. Dos d'ells estan relacionats amb el citoesquelet (ACTB i ACTG1) mentre que les quatre restants ho estan amb el múscul esquelètic (ACTA1), el múscul llis (acta2), el múscul llis entèric (ACTG2) i amb el múscul cardíac (ACTC1). Les mutacions que afecten a aquests gens eren desconegudes fins al 1998, i s'ha vist que produeixen miopaties, variacions en la grandària i la funció cardíaca i sordesa. Així mateix, l'actina del citoesquelet està implicada en el mecanisme de patogenicitat de múltiples agents infecciosos, inclòs el VIH. La immensa majoria de les mutacions que afecten a l'actina són de tipus puntual i tenen un efecte dominant, excepte almenys sis mutacions de miopatia nemalínica. Això és a causa que en molts casos la varietat mutant del monòmer d'actina actua fent de "capping", és a dir, com a terminador de l'elongació de l'actina F.[25]
L'ACTA1 és el gen que codifica la isoforma α de l'actina humana present principalment en el múscul esquelètic, tot i que també s'expressa en el múscul cardíac i en la glàndula tiroides.[88] La seva seqüència consta de set exons, que produeixen cinc transcrits coneguts.[89] El 2006, l'ENMC (European Neuromuscular Centre) havia publicat 116 mutacions relacionades amb patologies, conegudes com a actinopaties. La major part d'elles consisteixen en substitucions puntuals d'aminoàcids, que en molts casos poden ser associats amb el fenotip que determina la severitat i el curs de l'afecció.[25][89]

Es manifesten alterant l'estructura i la funció del múscul esquelètic produint tres formes de miopatia: miopatia nemalínica tipus 3, miopatia congènita amb excés de microfilaments (CM) i miopatia congènita amb desproporció de tipus de fibra (CFTDM). També s'ha detectat mutacions que produeixen miopatia amb cores (zones desproveïdes d'activitat oxidativa).[91] Encara que els seus fenotips són similars, a més de la miopatia nemalínica típica i la de bastons intranuclears, alguns especialistes distingeixen un tipus de miopatia anomenada actínica de la miopatia nemalínica. A la primera s'acumulen agregats d'actina en lloc dels típics bastons. És important assenyalar que un pacient pot mostrar més d'un d'aquests fenotips en la biòpsia.[92] Els símptomes més habituals consisteixen en una morfologia facial típica (fàcies miopàtica), debilitat muscular i retard en el desenvolupament motor i dificultats respiratòries. El curs, la gravetat i l'edat d'aparició són molt variables, i es troben formes de miopatia solapades. A la miopatia nemalínica apareixen unes estructures no patognomòniques en diverses localitzacions de les fibres musculars tipus 1 conegudes com a "bastons nemalínics", amb una composició similar als discos z del sarcòmer.[93]
La patogènesi és molt variada. Moltes mutacions es donen a la zona d'esquerda de l'actina, properes al lloc d'unió per nucleòtids, mentre que altres es donen en domini 2, o bé a les zones d'interacció amb les proteïnes associades, la qual cosa explica la gran varietat d'agregats que es formen en aquests casos, com cossos nemalínics, intranuclears o cossos zebra.[25] A la miopatia nemalínica es produeixen canvis en el plegament i en les propietats d'agregació de l'actina, i també en l'expressió d'altres proteïnes associades. En algunes variants en les quals es troben cossos intranuclears, el canvi en el plegament oculta el senyal d'exportació nuclear, de manera que l'agregació de la forma mutant d'actina es produeix en el nucli cel·lular.[94] En canvi, sembla que en les mutacions d'ACTA1 que donen lloc a CFTDM està més afectada la funció sarcomèrica que l'estructura en si.[95] Treballs recents tracten d'aclarir l'aparent paradoxa que no existeixi una correlació clara entre l'abundància de bastons i la debilitat muscular. Sembla que algunes mutacions particulars són capaces d'induir una major taxa d'apoptosi en les fibres musculars tipus II.[33]

Existeixen dues isoformes que codifiquen actines del múscul llis:
L'ACTG2 codifica la isoforma més llarga d'actina, amb nou exons, un d'ells, el situat en l'extrem 5', que no es tradueix.[96] Es tracta d'una γ actina que s'expressa en el múscul llis entèric. No s'han trobat mutacions que es corresponguin a patologies amb aquest gen, tot i que s'ha vist mitjançant microarrays que és la proteïna que, amb diferència, més augmenta la seva expressió en els casos de resistència a la quimioteràpia amb cisplatí.[97]
L'ACTA2 codifica una actina α localitzada en el múscul llis, i també en el múscul llis vascular. S'ha vist que una mutació, la MYH11, podria ser responsable d'almenys un 14% dels casos d'aneurismes d'aorta toràcica hereditària, concretament el tipus 6, ja que la variant mutada produeix un mal acoblament dels filaments i una reducció de la capacitat de contracció del múscul llis vascular. S'observa en aquests individus degeneració aòrtica medial, amb àrees de desorganització i hiperplàsia, i estenosi de les vases vasorum de l'aorta.[98] El nom d'afeccions en què podria estar implicat aquest gen està en augment. Se li ha relacionat amb la malaltia de Moyamoya, i sembla que algunes mutacions en heterocigosi podrien conferir predisposició a moltes patologies vasculars, com l'aneurisma d'aorta toràcica i la cardiopatia isquèmica.[99] L'actina α de múscul llis també és un interessant marcador per avaluar la progressió de la cirrosi hepàtica.[100]
L'ACTC1 és el gen que codifica la isoforma de l'actina α present en el múscul cardíac. Es va seqüenciar per primera vegada per Hamada i col·laboradors el 1982, observant-se que estava interromput per cinc introns.[101] Va ser el primer gen dels sis on es van trobar al·lels implicats en processos patològics.[102]

S'han descrit diversos trastorns estructurals que comporten una disfunció cardíaca associada a mutacions puntuals en aquest gen, com miocardiopatia dilatada tipus 1R i la miocardiopatia hipertròfica tipus 11. Recentment s'ha vist que alguns defectes atrials septals també podrien estar relacionats.[104][105]
En el cas de la cardiomiopatia dilatada, s'han estudiat dos casos en els quals en ambdós es produeix una substitució en aminoàcids molt conservats pertanyents als dominis que s'uneixen als discos Z i intercalats, la qual cosa porta a la hipòtesi que la dilatació es produeix per un defecte de transmissió de la força contràctil en els miòcits.[27][102]
Les alteracions de l'ACTC1 són responsables de menys del 5% de les cardiomiopaties hipertròfiques.[106] S'han demostrat també l'existència de diverses mutacions puntuals:[107]
La patogènesi sembla obeir a un mecanisme compensatori: les proteïnes mutants actuarien com un "tòxic" amb un efecte dominant, disminuint la capacitat de contracció amb un rendiment mecànic anormal, de manera que la hipertròfia, que sol ser tardana, seria conseqüència d'una resposta normal del múscul cardíac a l'estrès.[108]
Recentment s'han trobat mutacions d'ACTC1 implicades en dos processos patològics: la miocardiopatia restrictiva idiopàtica infantil,[109] i el miocardi ventricular esquerre no compacte.[110]
L'ACTB és un locus molt complex. Hi ha multitud de pseudogens repartits per tot el genoma, i la seva seqüència conté sis exons que poden donar lloc fins a 21 transcrits diferents per splicing alternatiu, coneguts com a actines β. En congruència amb aquesta complexitat, també els seus productes tenen localitzacions i formen part de processos molt diferents (citoesquelet, complex NuA4 histona-aciltransferasa, nucli cel·lular) i pel mateix també se li ha associat al mecanisme de gran quantitat de processos patològics (carcinomes, distonia juvenil, mecanismes d'infeccions, malformacions en el sistema nerviós i invasivitat de neoplasmas, entre altres)[111] s'ha trobat una nova forma d'actina, l'actina κ, que sembla substituir l'actina β en processos tumorals.[112]

Fins al moment s'han pogut detectar tres processos patològics que es deuen a una alteració directa de la seqüència d'un gen:
ACTG1 és el locus que codifica la proteïna de l'actina γ citosòlica responsable de la formació de microfilaments del citoesquelet. Conté 6 exons, donant lloc a 22 mRNAs diferents, fet que produeix 4 isoformes completes, possiblement expressades d'una forma depenent de teixit. També té dos promotors alternatius.[117] S'ha vist que les seqüències traduïdes d'aquest locus i el de l'actina β són més semblants del que s'esperava, suggerint una seqüència ancestral comuna que va patir duplicació i conversió gènica.[118]
Des del punt de vista patològic, ha estat associat a processos com l'amiloïdosi, la retinitis pigmentosa, mecanismes d'infecció, malalties renals i diverses pèrdues auditives congènites.[117]
Relacionades amb sis mutacions puntuals autosòmiques-dominants en la seqüència, es troben diverses formes de pèrdues d'audició, especialment la sensorineural tipus 20/26. Sembla que afecten de forma específica als estereocilis de les cèl·lules ciliades de l'òrgan de Corti. L'actina β és la proteïna més abundant en els teixits humans, però no en les cèl·lules ciliades, la qual cosa explicaria la localització de la patologia. D'altra banda, sembla que la major part d'aquestes mutacions afecten zones d'unió amb altres proteïnes, especialment l'actomiosina.[25] Alguns experiments suggereixen que el mecanisme patogènic d'aquest tipus de sordesa és perquè l'actina F seria més sensible de l'habitual a la cofilina.[119]
D'altra banda, encara que no es té constància de cap cas, se sap que l'actina γ també s'expressa en el múscul esquelètic, i encara que en quantitats molt petites, els models animals han mostrat que la seva absència podria donar lloc a miopaties.[120]
Alguns agents infecciosos utilitzen l'actina, especialment la citoplasmàtica, en el seu cicle de vida. En bacteris bàsicament existeixen dues formes:
A més de l'exemple citat anteriorment, en els passos inicials de la internalització d'alguns virus, notablement el VIH, s'estimula la polimerització de l'actina, per exemple inactivant la cofil·lina.[125]
En els processos d'invasió de les cèl·lules canceroses, les protrusions basades en actina exerceixen un paper encara no determinat.[126]
El citoesquelet eucariota mostra alguns components de gran semblança al llarg de l'escala filogenètica, especialment l'actina i la tubulina. Per exemple, la proteïna codificada pel gen ACTG2 d'humans posseeix una equivalència absoluta amb els ortòlegs presents en rata i ratolí, tot i que a nivell de nucleòtids la identitat disminueix al 92%.[127] Tanmateix, sí que hi ha grans diferències amb els equivalents en procariotes (FtsZ i MreB), que, al seu torn, presenten una identitat de seqüència d'entre un 40-50% entre les diferents espècies de bacteris i arqueus. Alguns autors suggereixen que la proteïna ancestral que va donar lloc al model bàsic d'actina eucariota s'assembla a les proteïnes del citoesquelet bacterià presents actualment.[128]

Alguns autors ressalten que l'actina, la tubulina i les histones, un tipus de proteïnes implicades en l'estabilització i regulació de l'ADN, presenten similituds en la seva capacitat d'unir nucleòtids i en el seu funcionament basat en l'aprofitament del moviment brownià, més encara, suggereixen que tots ells podrien derivar d'un ancestre comú,[129] per tant, els mecanismes evolutius van diversificar la proteïna ancestral en les variants avui presents, conservant, entre d'altres, les actines com a molècules eficaces per abordar processos biològics antics i essencials, com l'endocitosi.[130]
Si bé els bacteris no tenen un citoesquelet comparable en complexitat al dels eucariotes, s'han descrit proteïnes d'alta similitud amb els monòmers i polímers d'actina. La proteïna MreB de bacteris polimeritza en filaments prims, no helicoidals i, rarament, en estructures helicoidals semblants a l'actina F.[16] Més encara, la seva estructura cristal·lina és molt semblant a l'actina G (quant a conformació tridimensional), i fins i tot hi ha equivalències entre els protofilaments de MreB i l'actina F. El citoesquelet bacterià també posseeix entre els seus components les proteïnes FtsZ, semblants a la tubulina.[131]
Per tant, els bacteris posseeixen un citoesquelet amb elements homòlegs a l'actina (per exemple, MreB, PARM, i MamK), si bé la seqüència aminoacídica d'aquestes proteïnes divergeix de les presents en cèl·lules animals. Tanmateix, MreB i PARM posseeixen una alta similitud estructural amb l'actina eucariota. Els microfilaments, altament dinàmics, generats mitjançant agregació de MreB i PARM són essencials per a la viabilitat cel·lular i participen en la morfogènesi de la cèl·lula, segregació del genòfor i polaritat cel·lular. PARM, un homòleg de l'actina codificada en un plasmidi, intervé en la gestió de l'ADN plasmídic.[132]
L'aprofitament de l'actina en els laboratoris de ciència i tecnologia deriven de la seva participació com riel de motors moleculars com la miosina (ja sigui en el múscul com a fora d'ell), i de la seva presència necessària per al funcionament cel·lular. Quant a la clínica, atès que algunes variants anòmales de l'actina estan relacionats amb l'aparició de patologies, la seva detecció és un criteri de diagnòstic.
Seamless Wikipedia browsing. On steroids.
Every time you click a link to Wikipedia, Wiktionary or Wikiquote in your browser's search results, it will show the modern Wikiwand interface.
Wikiwand extension is a five stars, simple, with minimum permission required to keep your browsing private, safe and transparent.