热门问题
时间线
聊天
视角
氫氣
来自维基百科,自由的百科全书
Remove ads
氫氣是氫元素標準狀況下以氣態形式存在的物質,化學式為H2,由兩個氫原子構成,又稱分子氫。氫氣是最輕的氣體,可用於氣球填充中,但後來因其浮力而使用的氫氣被逐漸替換為危險性較小的不可燃氣體氦氣。氫氣也曾用於肉製品的保鮮。氫氣的英語hydrogen來自希臘語的ὕδωρ(水)和γεννᾰν(產生),即產生水的物質;而中文氫氣來自「輕氣」。
Remove ads
歷史
最先記錄氫氣製備的科學家是帕拉塞爾斯,他將硫酸倒至鐵粉上發現了這種氣體,但當時他並不知道實驗中放出的氣體的具體性質。後來,英國科學家亨利·卡文迪什用不同的金屬重複了帕拉塞爾斯的實驗,發現產生的氣體和空氣不同,其密度小且可燃,他稱這種氣體為「可燃性空氣」,並發現其燃燒生成水。法國化學家拉瓦節確認了卡文迪什的發現,提出用「氫氣」(hydrogène)一詞來取代「可燃性空氣」。
結構
氫氣分子由兩個氫原子透過一個σ鍵組成,鍵長約74.14 pm。基態之氫氣分子的σ鍵由兩個氫原子分別貢獻一個1s軌態的電子參與鍵結,並形成σ軌態。而氫分子以及其陽離子(H2+陽離子)因為結構簡單,而成為科學家在研究化學鍵本質時所用的重要對象。早在量子力學發展成熟整整半個世紀以前,詹姆斯·克拉克·麥克斯韋就觀察到了氫氣分子的量子效應。他注意到,H2的熱容量在低於室溫的溫度下,開始偏離雙原子氣體的性質,在極低溫下更像單原子氣體。根據量子理論,這一現象源自於分子旋轉能級之間的間距。在質量尤其低的H2分子中,能級之間的間距特別大。在低溫下,較大的能級間距使得熱量無法均分到分子的旋轉運動上。由更重的原子所組成的雙原子氣體會有較小的能級間距,所以在低溫下不呈現這種現象。[2]
氫氣分子在哈密頓算符中可以表示為:
-
- ,
其中M為質子的質量、m為電子的質量、為原子核的座標、為電子的座標。
Remove ads

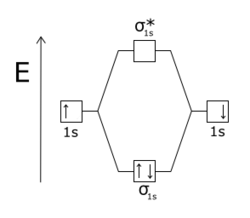
氫氣分子是最小、結構最簡單的分子,由兩個氫原子透過一個σ鍵組成,鍵長約74.14 pm。由於每個氫原子都有1個1s軌態電子,因此,2個氫原子各用一個1s軌態的電子參與鍵結。在分子軌態圖中,其可以表示如右圖,其中左側和右側為原本的原子軌態、中間是鍵結後對應的分子軌態、左側坐標軸的縱軸代表軌態的能量、並用箭頭表示該軌態中的電子,箭頭方向表示電子自旋的方向。
當2個s軌態端對端重疊後,所形成的分子軌態為σ軌態,當電子填入氫氣分子的σ軌態時,電子出現機率最高之處位在兩個氫原子核中心連線中間的位置。
相反的,兩個1s軌態也有可能是以反向的方式結合,其所形成的波則互相干涉抵消,而形成反鍵軌態,稱為σ*軌態,電子填入σ*軌態時,電子出現在兩個氫原子核中心連線中間位置的機率降為0,因此形成一個波節。σ*軌態的能量比σ軌態高,因此在基態的情況下,電子填入氫氣分子的分子軌態時,不會優先填到這個軌態。
在分子軌態理論中,氫氣的電子排佈為1σg2,其鍵級為(2-0)/2 = 1。其光電子譜在16至18eV之間有一組多重峰[3]。
電子填入氫氣分子的分子軌態時會先從低能量的σ軌態開始填,而σ軌態可以容納2個電子,氫氣分子共有兩個電子,因此電子在基態的氫氣分子將會填滿σ軌態。[4]
Remove ads
雙原子氫分子有兩個原子核相對自旋不同的自旋異構體。[5]其中正氫的兩個質子自旋平行,形成三重態,分子自旋量子數為1;仲氫的兩個質子自旋反平行,形成單重態,分子自旋量子數為0。在標準溫度和壓強下,氫氣含74.87%正氫和25.13%仲氫。[6]正氫和仲氫的平衡比例受溫度影響,但由於正氫屬於激發態,而非穩定態,所以無法純化分離出來。在極低溫度下,處於平衡狀態的氫幾乎完全由仲氫組成,如在25K下仲氫的含量為99.01%;隨着溫度的升高,正氫和仲氫的平衡比例趨向於3:1。[7]純正氫在液態和氣態時的熱力屬性與混合態截然不同,這是因為兩者在旋轉熱容上有很大的差異。[8]其他含氫分子和官能基也有正、仲之分,例如水和亞甲基,但它們在熱力屬性上的差別極小。[9]
在沒有催化劑的情況下,正氫和仲氫之間的轉換速率隨着溫度的升高而增加,所以急速冷卻的氫會含有高比例的正氫,且這些正氫會非常緩慢地轉變為仲氫。[10]氫在冷卻後的正、仲比例對液氫的製備和儲存十分重要:正氫向仲氫的轉化是一個放熱過程,其產生的熱量足以使一部份液氫蒸發並流失出去。在氫冷卻過程中協助正、仲氫轉化的催化劑有:三氧化二鐵、活性炭、鉑石棉、稀土金屬、鈾化合物、 三氧化二鉻及某些鎳化合物等等[11][12]。
Remove ads
製備

在實驗室里,氫可以通過活潑金屬和稀酸反應,或者兩性金屬和鹼的溶液反應得到。[13]
Remove ads
對水進行電解.淡水.鹽水.海水.處理過的污水,搭配相對的觸媒電極片,都能電解出氫氣,以很容易地製成氫氣。[13]當低電壓的電流通過水的時候,氧氣會在陽極積累,而氫氣則在陰極積累。在製備氫氣作儲存之用時,陰極的材料一般選用鉑等惰性金屬,以避免與氫氣發生反應。如果製成的氫氣須要當場用來燃燒,則氧氣可助燃,所以陽極也應該用惰性金屬作為材料。理論上的最大能源效率,即產出的氫氣所含潛在能量佔投入電能的比例,為80%至94%。[14]
用鋁鎵合金製成的顆粒,加入水中,會產生氫氣。這一反應也會產生氧化鋁,但用於防止顆粒表面形成氧化層、成本較高的鎵在反應之後可以回收再用。這一反應有潛力成為氫能經濟的基礎,因為氫氣可以在現場生成,無須運輸。[15]
Remove ads
在眾多氫氣製備方法中,經濟效益最高的是從碳氫化合物中提取出氫氣。商業上,一般是對天然氣進行蒸汽重整來大規模生產氫氣。[16]在高溫下(1000–1400K,700–1100°C,1300–2000°F),水蒸汽和甲烷會發生反應,產生一氧化碳和氫氣:
以上的反應在低壓進行時效率更高,但卻通常在高壓下進行(2.0MPa,20atm,600inHg),因為高壓氫氣是市場上最為普及,且變壓吸附純化系統更適合在高壓下工作。由於反應所產生的一氧化碳-氫氣混合物經常直接用於生產甲醇及其他相關的化合物,所以也稱為合成氣。甲烷以外的碳氫化合物也可以用來製造合成氣,但產物比例可能會有所不同。在缺水的情況下,焦炭就會形成,影響合成氣的產量:
因此,在進行蒸汽重整過程時,通常應注入過量的蒸汽。利用水氣轉移反應,並以氧化鐵作為催化劑,可從蒸汽中提取出更多的氫氣。蒸汽重整也是二氧化碳的一大工業來源:[16]
氫氣的其他生產方法還包括,碳氫化合物的部份氧化反應:[17]
以及對煤炭反應的碳產物進行以上的轉移反應:[16]
氫氣在生產後,有時會在同一道工業程序中直接被使用,期間不經分離。在用於生產氨的哈柏法中,氫氣是從天然氣中提取出來的。[18]對鹽水進行電解,在產生氯氣的同時,也會生成氫氣作為副產品。[19]
Remove ads
化學性質

氫氣的燃點雖然高達攝氏573.6度,由於氫氣的密度低,只要吸收一點熱量,就能瞬間達到燃燒所需要的溫度,不過非發煙式且低於573.6°C的高溫不會使氫氣燃燒,所以說氫氣只是閃火點低 而氫氣在普通條件下是動力學穩定的,如和氧氣混合併無明顯反應,但其混合物在火花的引發下會發生連鎖反應並爆炸。[13]
氫氣和鹵素也能直接反應,反應的劇烈程度隨着鹵素的活潑性的升高而加劇,如氫氣和氯氣反應可由光或熱引發,而和氟氣在黑暗處接觸即可爆炸:[20]
除了非金屬外,活潑金屬(如鈉、鈣、鈾等)也能和氫氣反應,生成氫化物:[20]
Remove ads
氫氣可以將活動性順序表中錳及錳之後的元素的氧化物還原為單質,對於變價金屬也可以得到部分還原的物質,以氧化鐵為例,被氫氣還原在325 °C以下得到的是四氧化三鐵,在此溫度之上得到金屬鐵:[20]
金屬鹽也可以被氫氣還原,較為容易被還原的有氯化鈀等物質,在溶液中即可反應:[20]
H2可以直接作為配體,和金屬形成配合物。例如氯化氫化雙(dppe)鐵和氟硼酸鈉在氫氣氛圍中反應,可以得到H2配合物:[21]
不飽和烴如烯烴或炔烴可以和氫氣發生加成反應得到相應的烷烴,這一反應通常由鎳、鉑催化劑催化;如果要完成部分氫化,可以採用林德拉催化劑,如毒化的Pd-CaCO3。[22]
- CH3CH2C≡CCH2CH3 + H2 —Lindlar cat.→ CH3CH2CH=CHCH2CH3
芳香烴作為不飽和烴的一種,也能和氫氣發生加成反應[23],如果使用釕系催化劑,可以使反應停留在環己烯一步上:[24]
- C6H6 + 3 H2 —Ni→ C6H12
- C6H6 + 2 H2 —Ru cat.→ C6H10
應用
石油和化學工業都需要大量的氫氣,其中以化石燃料加工及經哈勃法生產氨為主要應用。在石油化工廠中須消耗氫氣的過程有:加氫脫烷基反應、加氫脫硫反應和裂化反應等。氫氣可以用來對非飽和脂肪和油類進行氫化,增加飽和程度(如固體植物牛油),也可以用於生產甲醇和氫氯酸。氫氣可以對金屬礦物進行還原。[25]
氫氣極易溶於許多稀土金屬和過渡金屬之中,[26]同時也可溶於納米晶態和非晶態金屬。[27]氫氣在金屬中的可溶性受到了晶格局部變形和雜質的影響。[28]利用這一屬性,可將氫氣在高溫鈀圓盤上通過,提高氫氣的純度。不過,氫氣在金屬中的溶解會導致氫脆現象,[29]使運輸管和儲存罐的設計更為複雜。[30]
除了用在化學反應中以外,氫氣在物理學和工程學上也有廣泛的應用。它在一些焊接方法中可用作保護氣體,例如原子氫焊接法。[31][32]氫氣的分子質量很低,因此它密度低,熱容量和熱導率亦為所有氣體中最高,很適合用作發電機的轉子冷卻劑。液氫可用於低溫物理學中,例如對超導現象的研究。[33]
氫氣和氮氣混合後稱為合成氣體,可以作為示蹤氣體,用於探測微小的漏氣點,在汽車、化學、發電、航空航天和電信等工業中都有應用的空間。[34]氫氣在許多國家屬於合法的食物添加劑(E 949),可以用來探測包裝有無洩漏,以及防止食物氧化。[35]
氫可以用來飽和無定形碳和無定性矽的斷鍵(懸鍵),使物質屬性變得更加穩定。[36]氫在各種氧化物材料中可以作為電子供體,包括:ZnO、[37][38]SnO2、CdO、MgO、[39]ZrO2、HfO2、La2O3、Y2O3、TiO2、SrTiO3、LaAlO3、SiO2、Al2O3、ZrSiO4、HfSiO4和SrZrO3等。[40]
氘和氚同位素也有其各自的特殊應用。氘可用於核聚變反應中,也可用作核裂變反應的中子減速劑。[41]化學和生物學都會利用氘化合物來研究各種化學反應的動力學同位素效應。[42]核反應堆所產生的氚可以用來製造氫彈,[43]在生物科學中用作同位素標識,[44]以及在發光顏料中作為輻射源。[45]
1990年國際實用溫標(ITS-90)把氫在平衡態下的三相點溫度定義為13.8033 K,從而為開爾文溫標定下了國際標準。[46]

氫本身並不是一種能源資源。[47]但氫的質量密度很低,稍高於空氣密度的四分之一,所以歷史上有氣球和飛艇都曾經用氫氣來提供升力。[48]但1937年的興登堡號空難造成36人死亡後,氫氣在載人飛艇及氣球填充上的應用已被較穩定的氦氣所完全取代。[49]
利用氘或氚同位素來進行核聚變發電的技術,目前還遠沒有達到發展成熟的階段。[50]雖然太陽的能量來自於氫的核聚變反應,但要在地球上穩定控制這一過程卻是極為困難的。[51]用太陽能、電能或生物過程產生單質氫所需要的能量,比氫燃燒後所得的能量要高,所以氫只能是一種能量載體,就像電池一樣。氫可以取自甲烷等化石燃料,但這些燃料都屬於不可再生資源。[47]
液氮和壓縮氫氣的單位體積所含能量密度比傳統燃料低得多,但單位質量所含能量密度卻更加高。[47]氫氣被認為有潛力成為一種常用的能源載體,作為新的經濟基礎。[52]舉例來說,在從化石燃料提取氫氣的同時,可以對二氧化碳進行收集及封存。[53]汽車在燃燒氫氣時的污染較低,除一些氮氧化物以外,[54]不會排放任何的碳。[53]燃料電池將氫氣和氧氣轉化為電力,效率比內燃機更高。[55]然而,要從現狀完全轉變到氫經濟,則需要龐大的基建成本。[56]
2007年,太田成男發表了一項關於氫氣可在醫療上扮演抗氧化劑角色的研究,其中指出氫氣可選擇性地減少具細胞毒性之氧自由基[57]。但並無廣泛承認的實驗論證其為一種標準化的療法,而有人以此行醫,造成拖延疾病最終致死的案例[58]。多地行政部門指出,類似於「氫氣機」、「水素水」等氫氣療法相關的產品並非合法醫療器材,亦不具醫療效果而屬於欺詐產品[59][60][61]。
在食品生產業,氫氣也用於氫化處理過程。
參考文獻
參見
Wikiwand - on
Seamless Wikipedia browsing. On steroids.
Remove ads









![{\displaystyle {\mathrm {Zn} \ {}+{}\mathrm {H} {\vphantom {A}}_{\smash[{t}]{2}}\mathrm {SO} {\vphantom {A}}_{\smash[{t}]{4}}{}\mathrel {\longrightarrow } {}\mathrm {ZnSO} {\vphantom {A}}_{\smash[{t}]{4}}\ {}+{}\mathrm {H} {\vphantom {A}}_{\smash[{t}]{2}}\uparrow }}](http://wikimedia.org/api/rest_v1/media/math/render/svg/36faa8819177bc1af2e81d286f9e2f258b3b1237)
![{\displaystyle {2\,\mathrm {Al} \ {}+{}2\,\mathrm {NaOH} \ {}+{}6\,\mathrm {H} {\vphantom {A}}_{\smash[{t}]{2}}\mathrm {O} {}\mathrel {\longrightarrow } {}2\,\mathrm {Na} [\mathrm {Al} (\mathrm {OH} ){\vphantom {A}}_{\smash[{t}]{4}}]\ {}+{}3\,\mathrm {H} {\vphantom {A}}_{\smash[{t}]{2}}\uparrow }}](http://wikimedia.org/api/rest_v1/media/math/render/svg/9e0dbf83798b839cd7fbe65ccb044241052282d0)
![{\displaystyle {2\,\mathrm {H} {\vphantom {A}}_{\smash[{t}]{2}}\mathrm {O} {}\mathrel {\longrightarrow } {}2\,\mathrm {H} {\vphantom {A}}_{\smash[{t}]{2}}\uparrow {}+{}\mathrm {O} {\vphantom {A}}_{\smash[{t}]{2}}\uparrow }}](http://wikimedia.org/api/rest_v1/media/math/render/svg/2f22d432b56dd6f981b0a73906085cbc25c2cefc)
![{\displaystyle {\mathrm {CH} {\vphantom {A}}_{\smash[{t}]{4}}{}+{}\mathrm {H} {\vphantom {A}}_{\smash[{t}]{2}}\mathrm {O} {}\mathrel {\longrightarrow } {}\mathrm {CO} {}+{}3\,\mathrm {H} {\vphantom {A}}_{\smash[{t}]{2}}}}](http://wikimedia.org/api/rest_v1/media/math/render/svg/a3670cacd0f919c7c0b8e0b02c958deb310d4123)
![{\displaystyle {\mathrm {CH} {\vphantom {A}}_{\smash[{t}]{4}}{}\mathrel {\longrightarrow } {}\mathrm {C} {}+{}2\,\mathrm {H} {\vphantom {A}}_{\smash[{t}]{2}}}}](http://wikimedia.org/api/rest_v1/media/math/render/svg/0c45966ca83758e10980ede773c1a05658b466d4)
![{\displaystyle {\mathrm {CO} {}+{}\mathrm {H} {\vphantom {A}}_{\smash[{t}]{2}}\mathrm {O} {}\mathrel {\longrightarrow } {}\mathrm {CO} {\vphantom {A}}_{\smash[{t}]{2}}{}+{}\mathrm {H} {\vphantom {A}}_{\smash[{t}]{2}}}}](http://wikimedia.org/api/rest_v1/media/math/render/svg/a47dc7e3d179ae46ed9c47b8efc1f7bf0d7ba8b2)
![{\displaystyle {2\,\mathrm {CH} {\vphantom {A}}_{\smash[{t}]{4}}{}+{}\mathrm {O} {\vphantom {A}}_{\smash[{t}]{2}}{}\mathrel {\longrightarrow } {}2\,\mathrm {CO} {}+{}4\,\mathrm {H} {\vphantom {A}}_{\smash[{t}]{2}}}}](http://wikimedia.org/api/rest_v1/media/math/render/svg/e337666dbc40849a21b727c440e3736fc48a9440)
![{\displaystyle {\mathrm {C} {}+{}\mathrm {H} {\vphantom {A}}_{\smash[{t}]{2}}\mathrm {O} {}\mathrel {\longrightarrow } {}\mathrm {CO} {}+{}\mathrm {H} {\vphantom {A}}_{\smash[{t}]{2}}}}](http://wikimedia.org/api/rest_v1/media/math/render/svg/b73c88bff71d875989005163007c840f203d015a)
![{\displaystyle {2\,\mathrm {H} {\vphantom {A}}_{\smash[{t}]{2}}{}+{}\mathrm {O} {\vphantom {A}}_{\smash[{t}]{2}}{}\mathrel {\longrightarrow } {}2\,\mathrm {H} {\vphantom {A}}_{\smash[{t}]{2}}\mathrm {O} }}](http://wikimedia.org/api/rest_v1/media/math/render/svg/d4979e42bb665ad651b59baf94fc6fce589c68b4)
![{\displaystyle {\mathrm {H} {\vphantom {A}}_{\smash[{t}]{2}}{}+{}\mathrm {Cl} {\vphantom {A}}_{\smash[{t}]{2}}{}\mathrel {\longrightarrow } {}2\,\mathrm {HCl} }}](http://wikimedia.org/api/rest_v1/media/math/render/svg/ea85b635ad6336a4de31289c9475603016d966bd)
![{\displaystyle {\mathrm {H} {\vphantom {A}}_{\smash[{t}]{2}}{}+{}\mathrm {F} {\vphantom {A}}_{\smash[{t}]{2}}{}\mathrel {\longrightarrow } {}2\,\mathrm {HF} }}](http://wikimedia.org/api/rest_v1/media/math/render/svg/a99f1a9dfde878ccad68123eb6530fa3f292a779)
![{\displaystyle {\mathrm {Ca} {}+{}\mathrm {H} {\vphantom {A}}_{\smash[{t}]{2}}{}\mathrel {\longrightarrow } {}\mathrm {CaH} {\vphantom {A}}_{\smash[{t}]{2}}}}](http://wikimedia.org/api/rest_v1/media/math/render/svg/b6f557755b4fbd780777fcd4932c50756bbedc55)
![{\displaystyle {3\,\mathrm {Fe} {\vphantom {A}}_{\smash[{t}]{2}}\mathrm {O} {\vphantom {A}}_{\smash[{t}]{3}}{}+{}\mathrm {H} {\vphantom {A}}_{\smash[{t}]{2}}{}\mathrel {\longrightarrow } {}2\,\mathrm {Fe} {\vphantom {A}}_{\smash[{t}]{3}}\mathrm {O} {\vphantom {A}}_{\smash[{t}]{4}}{}+{}\mathrm {H} {\vphantom {A}}_{\smash[{t}]{2}}\mathrm {O} }}](http://wikimedia.org/api/rest_v1/media/math/render/svg/022c4a850c4e8b05562695dfe7e934ce6b414d79)
![{\displaystyle {\mathrm {Fe} {\vphantom {A}}_{\smash[{t}]{2}}\mathrm {O} {\vphantom {A}}_{\smash[{t}]{3}}{}+{}3\,\mathrm {H} {\vphantom {A}}_{\smash[{t}]{2}}{}\mathrel {\longrightarrow } {}2\,\mathrm {Fe} {}+{}3\,\mathrm {H} {\vphantom {A}}_{\smash[{t}]{2}}\mathrm {O} }}](http://wikimedia.org/api/rest_v1/media/math/render/svg/d4e61105e17e81dbf48890f493e8ca4869273f2f)
![{\displaystyle {\mathrm {PdCl} {\vphantom {A}}_{\smash[{t}]{2}}{\mskip {2mu}}(\mathrm {aq} ){}+{}\mathrm {H} {\vphantom {A}}_{\smash[{t}]{2}}{}\mathrel {\longrightarrow } {}\mathrm {Pd} \downarrow {}{}+{}2\,\mathrm {HCl} }}](http://wikimedia.org/api/rest_v1/media/math/render/svg/4342457a604572b648ebb098eb431f55580c6bc9)
![{\displaystyle {\mathrm {HFeCl} (\mathrm {dppe} ){\vphantom {A}}_{\smash[{t}]{2}}{}+{}\mathrm {NaBF} {\vphantom {A}}_{\smash[{t}]{4}}{}+{}\mathrm {H} {\vphantom {A}}_{\smash[{t}]{2}}{}\mathrel {\longrightarrow } {}[\mathrm {HFe} (\mathrm {H} {\vphantom {A}}_{\smash[{t}]{2}})(\mathrm {dppe} ){\vphantom {A}}_{\smash[{t}]{2}}]\mathrm {BF} {\vphantom {A}}_{\smash[{t}]{4}}{}+{}\mathrm {NaCl} }}](http://wikimedia.org/api/rest_v1/media/math/render/svg/44273609f6e129615885cf86e2b5eae542421457)