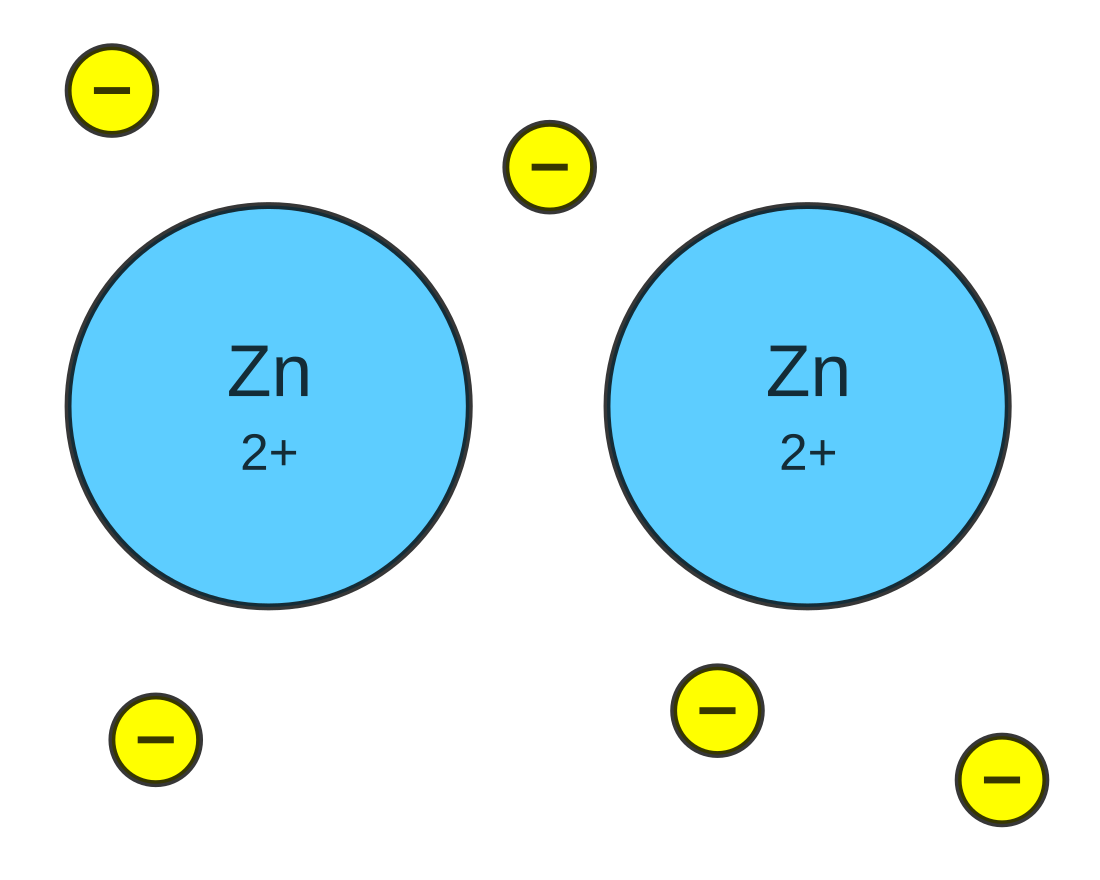
金屬鍵
来自维基百科,自由的百科全书
金屬鍵是化學鍵中的一種,主要在金屬中存在,一些原子簇化合物中也存在金屬鍵。游離域電子及排列成晶格狀的金屬離子之間的靜電吸引力組合而成。由於電子的自由運動,金屬鍵沒有固定的方向,因而是非極性鍵。

金屬鍵決定了金屬許多物理特性,如強度、可塑性、延展性、傳導熱量、導電性、不透明度和光澤[1][2][3][4]。例如一般金屬的熔點、沸點隨金屬鍵的強度而升高。離子半徑越小,金屬鍵越強。
金屬之間的鍵結除了金屬鍵以外,也有其他的鍵結方式,甚至是單質也不例外。例如元素態的鎵在固態及液態下有共價的原子對鍵結,這些原子對形成晶格,和其他的金屬仍以金屬鍵鍵結。另一個金屬-金屬共價鍵的例子是多原子汞陽離子Hg2+
2。
歷史
當化學納入科學體系後,人們發現週期表中大部份的元素是金屬,也可以描述金屬和酸反應形成的鹽類。隨着電化學的發展,知道金屬在溶液中一般會形成帶正電的離子,而金屬的氧化反應可以用電化學的方式來描述。當時的金屬模型常會用許多正電荷的離子,被一大群帶負電的電子包圍來表示。
隨着量子力學的發展,上述的模型也變成用自由電子模型來表示,甚至更擴展到近自由電子近似。這兩種模型中,電子描述成通過固體晶格的氣體,其能量是各向同性的,是依動量向量k量值的平方而決定,而不是依其方向來決定。在三維的k空間中,最高填滿能量的點形成的集合(費米面)必定是一球體。在近自由電子近似中,類似箱子的布里淵區,反映因為晶格來產生的週期性勢能變化,略微影響其各向同性。
金屬鍵的本質
以下二種現象的結合產生了金屬鍵:離域電子以及遠多於離域電子數量的離域能階,後者也稱為缺電子(electron deficiency)。
金屬簇中的金屬芳香性是另一個離域電子的例子。這種情形下多半會是三維的。金屬將離域原則發揮到極致,可以說一個金屬晶體就表示成一個分子,而其中所有傳導帶的電子都是離域電子,在三維空間中自由移動。這代表在一塊金屬內無法再區分個別的分子,金屬鍵既不是分子間的鍵結,也不是分子內的鍵結,也許用「非分子」鍵結來描述會比較合適。金屬鍵大部份都是非極性的,因為若金屬中沒有雜質,都由同一種原子組成,其電負度都相同,就算是在合金裏,參與鍵結的元素其電負度的差異也很小,因此金屬鍵可以算是非常離域的共價鍵,以這個觀點來看,金屬鍵根本不是另外一種新的鍵結,而金屬鍵也只能描述在凝聚態(結晶固態、玻璃態及液態)中的原子鍵結。相反的,金屬蒸氣一般會有明顯的原子性(例如汞),有時也會以傳統的共價鍵鍵結,形成分子(例如Na2)。
s層及p層電子的離域效果最為明顯。例如銫的電子離域效果很強,電子其實脫離了銫原子,形成氣體,但是被拘束在銫金屬表面的附近。因此對於銫而言,由Cs+離子和帶負電的電子氣體鍵結來描述也不算非常不精確[5]。其他原子的電子比較不自由,仍然會受到金屬原子的勢能所影響,有時勢能影響還相當的強。因此需要一些更複雜的量子力學處理(緊束縛近似),其中原子會視為是電中性的,像是苯裏面的碳原子。d層電子及f層電子完全沒有離域效果,尤其是f層電子更為明顯,因此可以維持其自旋的不成對電子,也讓這些金屬帶有磁性。
金屬原子在其價殼層中的電子較少,因此這此原子是缺電子元素,原子間的電子分享不會改變此一情形:可用的能階仍然遠少於分享的電子。因此滿足導電性的二個要求:電子有高度離域性,以及部份填滿的能階。這類的電子可以輕易的從一個能階移動到另一個略為不同的能階。電子不只是離域,也形成了滲透晶格的電子海,而當存在外部電場時,大量電子也可以在晶格之間移動。在沒有外在電場時,電子會自由的往任何方向移動。在有外在電場時,外在電場會略為改變其能階的狀態,因此會產生不同的波矢,往某個方向移動的電子會比其他方向多,形成電流。
傳導電子可自由移動的特點也讓各層金屬原子可以進行相對位移,但仍維持金屬鍵的特性。以局部來說,金屬鍵很容易就會破壞,之後又會建立新的金屬鍵,這個過程對共享的金屬鍵不會造成太大的影響。這就是金屬其延展性的原因。這個特性對於純元素格外的明顯,但是在溶解其他物質的情形,晶格中的缺陷會讓金屬的硬性提高。例如金在沒有雜質(24克拉)時是非常軟的,因此珠寶上的金一般會是18克拉或是更低純度的合金。
金屬一般而言也是良好的傳熱體,不過這個現象只有一部份是因傳導電子的的影響。原子集合性的振動(稱為聲子)會在固體之中像波一樣的移動,這是金屬傳熱的主要原因。
不過像鑽石之類的物質也會傳熱,但不導電。鑽石不導電不是因為鑽石中的電子沒有離域特性,而是因為鑽石沒有缺電子的特性。 缺電子特性是金屬鍵和其他傳統的共價鍵最為不同的地方。因此較好定義金屬鍵的定義是「金屬鍵是缺電子,且電子高度離域的共價鍵」.
金屬鍵半徑
金屬鍵半徑(Metallic radius)定義為金屬晶格內,相鄰金屬離子之間距離的一半。金屬鍵半徑和金屬原子的特性有關,也和環境有關,環境因素中最重要的是配位數,而配位數會受到溫度及壓力所影響。
在比較金屬鍵半徑的週期趨勢時,一般會套用所謂的戈德施密特校正(Goldschmidt correction),將金屬鍵半徑轉換為在12配位數下的半徑。因為金屬鍵配位數最高,金屬鍵半徑也會越大,較低配位數的校正會乘以一個0到1之間的數值x。配位數為4時,x = 0.88;配位數為6時,x = 0.96;配位數為8時,x = 0.97。此校正方式是得名於找到上述數值的維克多·戈德施密特[6]。
金屬鍵半徑會依照通則的週期性趨勢:在同一週期內,半徑會因為有效核電荷(不會受價電子數量增加所影響)增加而減少。在同一族內,半徑會因為主量子數的增加而增加。在第三週期及第四週期之間會出現鑭系收縮,鑭系元素相較於上一週期的元素,其半徑增加不多,原因是因為f軌域電子屏蔽效應不完全所影響。
金屬鍵的強度
金屬原子之間有很強的吸引力,因此需要許多能量才能克服此吸力。許多金屬元素的沸點很高,像鎢(5828 K)就格外的高。不過12族元素:鋅、鎘及汞可能是例外。其電子組態結束在...ns2,因為空的np軌域的能階較大,其組態很接近稀有氣體組態。因此這類的金屬容易揮發,不宜在超高真空的系統下使用。
其他的金屬原子鍵結非常強,甚至連融化成液體的金屬也不例外,例如鎵。鎵的熔點只比室溫高一點點,放在手上就會溶化,但其沸點和銅差不多。熔融態的鎵由於其金屬鍵,是很不容易揮發的液體。
液態金屬中的強鍵結表明了金屬鍵中的能量和金屬鍵結的方向關係不大,這種缺乏鍵結方向性的特點是因為電子離域化所造成的,和一般共價鍵有方向性的鏈結相反。金屬鍵中的能量主要可以表示為金屬原子周圍電子數量的函數,就如同嵌入式原子模型[7]。因此金屬會有較簡單、緊密堆積的晶體結構,如FCC,BCC和HCP等。
若是液態金屬的冷卻率夠高,且其中有適當的合金成份,金屬鍵甚至可以形成類似玻璃結構的非晶態金屬。
許多的生物化學都和金屬離子和生物分子中的微弱交互作用有關。這類交互作用及衍生的構象改變可以用雙極化干涉測量法來量測。
溶解度及化合物的形成
金屬不溶於水及有機溶劑,不過和水或有機溶劑反應時,會生成可溶的產物。一般來說金屬和水(或有機溶劑)會形成氧化還原反應,破壞金屬原子最外層的電子,因此破壞其金屬鍵。不過金屬在維持其金屬鍵特性的情形下,也溶解和其他物質。例如金很容易被汞溶解,即使在室溫下也是如此。在固態金屬中,若二個金屬的結構相同,也可以有很高的溶解度,其至完全的固體溶解性(例如金和銀形成的合金琥珀金)。不過,兩種金屬也可能會產生結構和這兩種金屬完全不同的產生,可以稱為是金屬互化物,不過因為金屬鍵的材料多半沒有分子的結構,道爾頓的定比定律也不適用,多半其化學計量比會在一定範圍內。針對這類的物質,較理想的作法是不使用「純物質」或是「溶質」之類的概念,改用物質的相來描述。近來這類的研究比較多是冶金學的主題,而不是化學的主題,不過這兩個領域有一些部份的重疊。
定域化及金屬簇
複雜化合物中的金屬鍵不一定會對其中所有的組成元素平均分配。有可能其中有些元素完全沒有參與金屬鍵,傳導電子在這些元素附近的流動就好像流經島嶼或是大石頭的河流一樣。也可以觀察哪些元素有參與金屬鍵,例如量測在X射線光電子能譜學(XPS)光譜中的核心水平,若有元素參與金屬鍵,其峰值會有傾斜的情形。
有些金屬間化合物(例如會形成原子簇的)有類似分子的性質,這些化合物比較常在化學中進行討論,而不是在冶金學中討論。這些原子簇的形成可以視為是將缺電子的鍵結轉變為更定域化(localized)的鍵結。氫氣是這種凝聚形式的極端例子,在高壓下氫是一種金屬,木星內部就有許多的金屬氫,而因為重力本身形成很高的壓力。不過在低壓下,其鍵結定域化,變成為一般的共價鍵,而且定域化非常完全,因此產生了(一般更為熟悉的)H2氣體。另一個類似的例子是硼,相較於碳,硼是電子缺乏的元素,不會形成金屬。不過硼有些複雜的結構,例如二十面體的B12原子簇。電荷密度波也是和這個相關的現象。
這些現象和原子彼此接近或是遠離的運動有關,可以詮釋成材料中電子及振動狀態(聲子)的耦合。一般認為另一種電子-聲子交互作用造成了在超低溫下很不一様的結果,也就是超導現象。定域鍵中會形成電子對,讓電荷載流子無法遷移,超導現象中恰好相反,生成的庫柏對在移動時不會遇到任何的阻力。
光學性質
大量移動電荷載體的存在也造成金屬獨特的光學性質。此性質無法用傳統共價鍵中個別電子的狀態來理解,只能將許多的電子視為整體才能理解。
光是電場及磁場的組合,電場常常可以激發金屬鍵中的電子,使其產生彈性的響應。因此,光子無法穿透到金屬的內部,多半會被反射,光子會被反彈出來,不過有些也會被吸收。這對所有可見光譜下的光子都成立,因此金屬常常會是銀白色或是灰白色,而且會有特殊的反射,即為金屬光澤。光反射及吸收的比例決定了金屬會偏銀色或是偏灰色。不過其儘管表面失澤可能會掩蓋這種觀察。銀是高導電性的金屬,也是最白的幾種金屬中的一個。
不過也有些金屬不是銀灰色的,最著名的是紅色的銅以及黃色的金。其顏色的原因是因為可激發金屬電子,使其有響應的頻率有其上限,稱為等離子頻率。在等離子頻率時,自由電子氣體中和頻率相依的介電函數會由負(反射)變成正(穿透),因此金屬表面不會反射高頻率的光子,也不會影響金屬的的顏色。有些材料(像氧化銦錫)是金屬導體(其實是簡併半導體),但在紅外線下有反射作用[8],因此氧化銦錫在可見光下是透明的,但在紅外線下則可作為反射鏡。
銀的上限頻率在遠紫外線區,但銅和金的上限頻率接近可見光區,因此這兩種金屬會有特殊的顏色。在金屬表面有一種共振效應稱為表面等離子共振,這是傳導電子的集體振盪,像是電子海上的漣漪。而且,就算光子有足夠的能量可以激發電子,一般也沒有足夠的動量造成表面的漣漪。因此,很難在大塊金屬上激發等離子體激元(plasmons),這也是金和銅雖然有一些顏色,但其光澤仍類似其他金屬的原因。不過奈米黃金中的金屬鍵只局限在小的金屬顆粒中,避免等離子體激元的共振波逃脫,因此動量選擇規則已不存在,等離子體激元共振會對綠色強烈的吸收,因此會有漂亮的紫紅色。這種顏色的強度比一般靠個別電子及其能階的染料強度要高幾個量級。
相關條目
參考資料
Wikiwand - on
Seamless Wikipedia browsing. On steroids.