Loading AI tools
З Вікіпедії, вільної енциклопедії
Ферме́нти, або ензи́ми — органічні каталізатори білкової або РНК природи, що утворюються в живих організмах. Прискорюють біохімічні реакції як in vivo, так і in vitro. Можуть мати від одного до кількох поліпептидних ланцюгів — субодиниць з високою молекулярною масою (від десятка тисяч до кількох мільйонів).
| Ферменти | |
 | |
| Молекулярна функція | каталіз[1] |
|---|---|
| | |
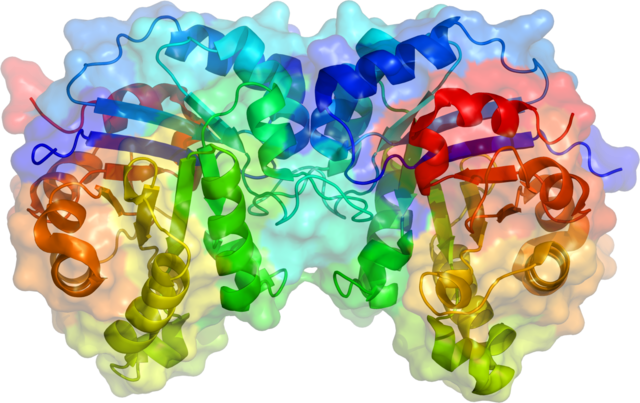
За хімічним складом ферменти можуть належати до простих чи складних білків. В останньому випадку молекула складається з білкової частини (апоферменту) та сполуки небілкової природи (кофактору). У білковій частині ферменту каталітичні функції виконують відносно невеликі ділянки молекули — активні центри, які визначають специфічність хімічної реакції, що каталізується цим ферментом. Активний центр являє собою поєднання певних амінокислот, які можуть знаходитись у поліпептидному ланцюгу як поруч, так і в різних його частинах. Якщо амінокислоти просторово віддалені одна від одної, формування активного центру відбувається шляхом згортання молекули ферменту в глобулярну структуру. Крім активного центру деякі ферменти мають алостеричний центр, який регулює роботу активного центру.
За характером каталізованих реакцій розрізняють оксидоредуктази, трансферази, гідролази, ліази, ізомерази, лігази.
Біохімічні реакції відбуваються за участю ферментів за нормального тиску, температури, у слабокислому, нейтральному чи слаболужному середовищі. Ферментативна реакція також може регулюватися іншими молекулами, як білкової природи, так й іншими — активаторами та інгібіторами.
Ферменти РНК-природи називають рибозимами і їх вважають первісною формою ферментів, які були замінені білковими ферментами в процесі еволюції.
Терміни «фермент» і «ензим» можна використовувати як синоніми. Але наука про ферменти називається ензимологією, а не ферментологією (ймовірно щоб не змішувати корені слів латинської і грецької мов).

Термін «фермент» ввів у XVII столітті хімік Ян ван Гельмонт для опису механізмів травлення. Наприкінці XVIII — на початку XIX століття вже було відомо, що м'ясо перетравлюється шлунковим соком, а крохмаль перетворюється на цукор під дією слини. Проте механізм цих явищ був ще невідомий[2]. У XIX столітті Луї Пастер, вивчаючи перетворення вуглеводів в етиловий спирт під дією дріжджів, дійшов висновку, що цей процес (бродіння) каталізується якоюсь «життєвою силою», що знаходиться в дріжджових клітинах.
Понад сто років тому терміни «фермент» і «ензим» відображали різні погляди Луї Пастера, з одного боку, та Марселена Бертло і Юстуса фон Лібіха, з іншого, в теоретичній суперечці про природу спиртового бродіння. Власне «ферментами» (від лат. fermentum — «закваска») називали «організовані ферменти» (тобто саме живі мікроорганізми), а термін «ензим» (від грец. ἐν- — «в-» і ζύμη — «дріжджі», «закваска») ввів 1876 року Віллі Кюне для «неорганізованих ферментів», що секретуються клітинами, наприклад, до шлунку (пепсин) або кишки (трипсин, амілаза). Через два роки по смерті Пастера (1897) Едуард Бухнер опублікував роботу «Спиртове бродіння без дріжджових клітин», в якій експериментально показав, що екстракт клітин дріжджів здійснює спиртове бродіння так само, як і незруйновані дріжджові клітини[3]. 1907 року за цю роботу він був удостоєний Нобелівської премії. 1926 року американський біохімік Джеймс Самнер вперше виділив фермент у кристалічній формі (уреазу), довівши таким чином білкову природу ферментів. 1946 року «За отримання в чистому вигляді ферментів і вірусних білків» отримав половину Нобелівської премії з хімії. Іншу половину отримали Вендел Стенлі і Джон Нортроп. Останній у 1930 році виділив у кристалічному вигляді протеолітичний фермент пепсин, а у 1932 — трипсин.
Ферменти є біологічними каталізаторами, вони наявні в усіх живих клітинах і сприяють перетворенню одних речовин (субстратів) на інші (продукти). Ферменти виступають каталізаторами практично в усіх біохімічних реакціях, що відбуваються в живих організмах — ними прискорюється близько 4000 окремих біореакцій[4]. Ферменти відіграють надзвичайно важливу роль у всіх процесах життєдіяльності, скеровуючи та регулюючи обмін речовин організму. Для ферментів характерним є те, що їхній синтез та каталітична активність контролюється на генетичному рівні, а також за участю низькомолекулярних сполук-субстратів або продуктів реакції[5]. Інша особливість ферментів — надзвичайно висока активність в порівнянні з неорганічними каталізаторами: деякі ферменти пришвидшують біохімічні реакції у мільйони разів.
Подібно до всіх каталізаторів, ферменти прискорюють як пряму, так і зворотну реакцію, знижуючи енергію активації процесу. Хімічна рівновага при цьому не зсувається ні в прямий, ні в зворотний бік. Відмінність ферментів від небілкових каталізаторів полягає у їхній високій специфічності — константа дисоціації деяких субстратів з білком-ферментом може досягати менш ніж 10−10 моль/л.
Ферменти широко використовуються і в народному господарстві — у харчовій, текстильній, фармацевтичній промисловості.
За типом реакцій, що каталізують, ферменти поділяються на 6 класів згідно з ієрархічною класифікацією ферментів (КФ або EC — Enzyme Commission code). Класифікацію запропонував Міжнародний союз біохімії і молекулярної біології (International Union of Biochemistry and Molecular Biology [Архівовано 28 квітня 2013 у WebCite]). Кожен клас містить підкласи, так що фермент описується сукупністю чотирьох чисел, розділених крапками. Наприклад, пепсин має код КФ 3.4.23.1. Перше число описує клас реакцій, що каталізує фермент:[6]
Ферменти є каталізаторами, тому вони прискорюють як пряму, так і зворотну реакції, тому, наприклад, ліази здатні каталізувати і зворотну реакцію — приєднання по подвійних зв'язках. Тим не менш напрямок реакції може залучати кілька субстратів і бути таким, що зворотна реакція практично не відбувається.
Зазвичай фермент іменують за типом реакції, яку він каталізує, додаючи суфікс -аза до назви субстрату (наприклад лактаза — фермент, що бере участь в перетворенні лактози). Таким чином, у різних ферментів, що виконують одну функцію, буде однакова назва. Такі ферменти розрізняють по інших властивостях, наприклад, по оптимальному pH (лужна фосфатаза) або локалізації в клітині (мембранна аденозинтрифосфатаза).

Найпростішим і найпоширенішим описом кінетики односубстратних ферментативних реакцій є рівняння Міхаеліса — Ментен.
На сьогоднішній момент описано і кілька складніших типів кінетики ферментів. Наприклад, якщо реакція вимагає кількох молекул субстрату або різних субстратів, часто реакція протікає через утворення третинного комплексу. Для дії багатьох ферментів також типове утворення перехідних комплексів (станів), що описується «механізмом пінг-понг».
Для оцінки діяльності ферментів використовують поняття молекулярної активності, питомої активності ферменту та умовної одиниці. Молекулярна активність — це число молекул субстрату, що зазнали хімічних змін за одну хвилину в стандартних умовах проведення реакції (тобто за оптимальної температури і pH), в перерахунку на одиницю маси ферменту. Питома активність ферменту — це число одиниць ферменту в перерахунку на один міліграм маси каталізованого білка чи субстрату. Умовна одиниця — це така кількість ферменту, яка каталізує хімічне перетворення одного мікромоля субстрату за одну хвилину в стандартних умовах проведення реакції.
За правилом Вант-Гоффа при кожному підвищенні температури на 10 °C швидкість ферментативних реакцій зростає у 1,5—3 рази, однак ця закономірність працює лише до досягнення температурного оптимуму, притаманного тому чи іншому ферменту (у більшості ензимів він досить низький). Після того, як температура перевищить температурний оптимум, швидкість ферментативної реакції зростає непропорційно або взагалі зменшується внаслідок зміни природної структури білка.
Активність ферментів визначається їхньою тривимірною структурою[7].
Як і всі білки, ферменти синтезуються у вигляді лінійного ланцюга амінокислот, який згортається певним чином. Кожна послідовність амінокислот згортається особливим чином, і молекула (білкова глобула), що утворюється, набуває унікальних властивостей. Декілька білкових ланцюжків можуть об'єднуватися у білковий комплекс. Найбільші рівні структури білків — третинна та четвертинна структури — руйнуються при нагріванні або під дією деяких хімічних речовин.
Щоб каталізувати реакцію, фермент повинен зв'язатися з одним або кількома субстратами. Білковий ланцюжок ферменту згортається таким чином, що на поверхні глобули утворюється щілина або западина, до якої приєднуються молекули субстрату. Ця область називається ділянкою (сайтом) зв'язування субстрату. Зазвичай вона збігається з активним центром ферменту або знаходиться поблизу від нього. Деякі ферменти містять також ділянки зв'язування кофакторів або іонів металів.
У деяких ферментів присутні також ділянки зв'язування малих молекул, що не беруть безпосередньої участі в реакції і часто, але не обов'язково, є субстратами або продуктами метаболічного шляху, в який входить фермент. Вони зменшують або збільшують активність ферменту, що створює можливість для зворотного зв'язку або регуляції роботи ферменту.
Для активних центрів деяких ферментів характерне явище кооперативності.
Ферменти зазвичай проявляють високу специфічність по відношенню до своїх субстратів. Це досягається частковою комплементарністю форми, розподілу зарядів і гідрофобних областей на молекулі субстрату і в ділянці зв'язування субстрату на ферменті. Ферменти демонструють високий рівень стереоспецифічності (просторової специфічності), регіоселективності (специфічності орієнтації) і хемоселективності (специфічності до хімічних груп).


У 1890 році Герман Еміль Фішер припустив, що специфічність ферментів визначається точною відповідністю форми ферменту і субстрату[8]. Таке припущення називається моделлю «ключ-замок». Фермент з'єднується із субстратом з утворенням короткоживучого фермент-субстратного комплексу. Проте, хоча ця модель пояснює високу специфічність ферментів, вона не пояснює явища стабілізації перехідного стану, яке спостерігають на практиці.
У 1958 році американський дослідник Деніел Кошланд запропонував модифікацію моделі «ключ-замок»[9]. Ферменти, переважно, — не жорсткі, а гнучкі молекули. Активний центр ферменту може змінити конформацію після зв'язування з ним субстрату. Бічні групи амінокислот активного центру займають таке положення, яке дозволяє ферменту виконувати свою каталітичну функцію. В деяких випадках молекула субстрату також міняє конформацію після скріплення в активному центрі. На відміну від моделі «ключ-замок», модель індукованої відповідності пояснює не тільки специфічність ферментів, але і стабілізацію перехідного стану.
Багато ферментів після синтезу білкового ланцюга зазнають модифікацій, без яких фермент не проявляє свою активність повною мірою; такі модифікації називаються посттрансляційними. Один з найпоширеніших типів посттрансляційних модифікацій — приєднання хімічних груп до бічних залишків поліпептидного ланцюжка. Наприклад, приєднання фосфатної групи називається фосфорилюванням, воно каталізується ферментом кіназою. Багато ферментів ядерних організмів глікозовані, тобто модифіковані олігомерами вуглеводної природи.
Ще один поширений тип посттранляційних модифікацій — розщеплення поліпептідного ланцюжка. Наприклад, хімотрипсин (протеаза, що бере участь в травленні), утворюється при відщепленні поліпептидної ділянки з хімотрипсиногена. Хімотрипсиноген є неактивним попередником хімотрипсина і синтезується в підшлунковій залозі. Неактивна форма транспортується до шлунку, де перетворюється на хімотрипсин. Такий механізм необхідний для того, щоб уникнути пошкодження підшлункової залози та інших тканин до надходження ферменту в шлунок. Неактивний попередник ферменту називають також «зімогеном».
Одна з його функцій полягає в забезпеченні найсприятливішого для реакції взаєморозташування реактантів шляхом орієнтації їх за допомогою нековалентних взаємодій з бічними ланцюгами амінокислотних залишків ферменту. Активний центр сприяє зниженню енергії активації реакції, що відбувається на ньому.
Деякі ферменти виконують каталітичну функцію самі собою, без додаткових компонентів. Проте є ферменти, яким для здійснення каталізу необхідні компоненти небілкової природи. Кофактори можуть бути як неорганічними молекулами (іони металів, залізо-сірчані кластери тощо), так і органічними (наприклад, флавін або гем). З поміж металів найчастіше кофакторами виступають іони натрію, калію, кальцію, марганцю, кобальту, магнію, крім них також поширений такий неорганічний кофактор як аніон хлору. Іони металів не тільки забезпечують саму можливість ферментативної реакції, а й пришвидшують її, тобто одночасно виступають як активатори ферментів. Органічні кофактори, які постійно (назавжди) зв'язані з ферментом, називають також простетичними групами. Кофактори органічної природи, що здатні відділятися від ферменту, називають коферментами. Багато коферментів є похідними вітамінів, до таких, наприклад, належать НАД і НАДФ (похідні вітаміну PP), флавін (похідний вітаміну B2), а вітамін B6 як кофермент і сам бере участь в реакціях переамінування й декарбоксилювання.
Фермент, який вимагає наявності кофактора для здійснення каталітичної активності, але не зв'язаний з ним, називається апофермент. Апофермент в комплексі з кофактором називаються голоферментом. Більшість кофакторів пов'язана з ферментом нековалентними, але досить міцними взаємодіями. Є і такі простетичні групи, що зв'язані з ферментом ковалентно, наприклад, тіамінпірофосфат в складі ферменту піруватдегідрогенази.
Речовини, що уповільнюють швидкість ферментативних реакцій, називають інгібіторами ферментів. Механізм їхньої дії часто полягає в блокуванні активного центру ферменту. Серед найактивніших інгібіторів такого типу — іони срібла, ртуті, свинцю, які пригнічують діяльність багатьох ензимів різних груп. Інший механізм інгібіції полягає в тому, що молекула інгібітора за своєю будовою виявляється схожою на молекулу субстрату. Наприклад, інгібітором сукцинатдегідрогенази є малеїнова кислота, чиї молекули подібні до молекул бурштинової кислоти, яку цей фермент окислює. В деяких випадках інгібітором може бути та ж сама речовина, що й активатор.
Seamless Wikipedia browsing. On steroids.
Every time you click a link to Wikipedia, Wiktionary or Wikiquote in your browser's search results, it will show the modern Wikiwand interface.
Wikiwand extension is a five stars, simple, with minimum permission required to keep your browsing private, safe and transparent.