Tautoméry sú štruktúrne izoméry (konštitučné izoméry) chemických zlúčenín, ktoré môžu voľne prechádzať z jedného na druhý.[1][2][3][4][5][6] Táto reakcia je zvyčajne výsledkom presunu protónu (vodíkového katiónu).[6] Tento dej je dôležitý napríklad v chovaní aminokyselín alebo nukleových kyselín, základných výstavbových molekúl živých systémov.

Chemická reakcia, pri ktorej sa premieňa jeden tautomér na druhý, sa nazýva tautomerizácia. Tento koncept sa nazýva tautoméria. Zriedka sa nazýva dezmotropia (kedy sú oba tautoméry stabilné a možno ich vyizolovať z roztoku).[7] Kedysi sa nazývala i alelotropia.[8]
Tautoméria by nemala byť zamieňaná s rezonančnými štruktúrami. Tautoméry sú odlišné zlúčeniny, ktoré možno identifikovať podľa rôznych vlastností (napríklad spektroskopických).[9] Naproti tomu rezonančné štruktúry umožňujú vysvetliť chovanie či vlastnosti molekúl, ale neexistujú ako samostatné molekuly.
Príklady

Tautoméria je všadeprítomná v organickej chémii. Zvyčajne je asociovaná s polárnymi molekulami a iónmi obsahujúcimi funkčné skupiny, ktoré sú aspoň slabo kyslé. Tautoméry existujú väčšinou v pároch, čo znamená, že sa protón presúva medzi dvoma miestami v molekule. Typicky je to zmena spojená s pohybom dvojitej väzby: H−X−Y=Z ⇌ X=Y−Z−H. Bežné páry tautomérov zahŕňajú:[6][10]
- ketón – enol: O=C−C−H ⇌ H−O−C=C , takzvaná keto-enol tautoméria (alebo oxo-enolová)
- imín – enamín: N=C−C−H ⇌ H−N−C=C
- kyanamid – karbodiimid
- guanidín – guanidín - guanidín: guanidínová skupina má uhlíkový atóm, na ktorý sú naviazané tri dusíkové skupiny - umožňuje teda presun v troch rôznych orientáciách
- amid – imidol: H−N−C=O ⇌ N=C−O−H (imidol vzniká napríklad pri hydrolýze nitrilov)
- imín – imín: R1R2C(=NCHR3R4) ⇌ (R1R2CHN=)CR3R4, napríklad pri enzýmových reakciách s pyridoxalfosfátom
- nitro – aci-nitro (nitrónová kyselina): RR'HC–N+(=O)(O–) ⇌ RR'C=N+(O–)(OH)
- nitrózo – oxim (nazývaná i nitrózová – izonitrózová[11]): H−C−N=O ⇌ C=N−O−H
- ketén – ynol: H−C=C=O ⇌ C≡C−O−H, reakcie sa účastní trojitá väzba
- fosfát – fosfonát: P(OR)2(OH) ⇌ HP(OR)2(=O), zmena trojväzbového fosforu na päťväzbový
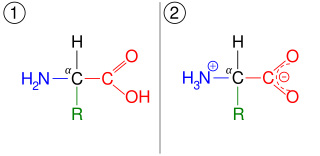
- aminokyselina – karboxylát amónny: H2N−CH2−COOH ⇌ H3N+
−CH2−CO−
2, reakcia je bežná pre aminokyseliny (základné stavebné bloky bielkovín). Protón sa presúva o viac ako dva atómy ďalej, čím vzniká zwitterión namiesto presunu dvojitej väzby
Druhy tautomérie

Dve špecifické podkategórie tautomerizácie sú:
- Anulárna tautomerizácia je druh prototropickej tautomérie, počas ktorej sa môže protón nachádzať na viacerých pozíciach v heterocyklickom systéme, ako je napríklad 1H- a 3H-imidazol, 1H-, 2H- a 4H-1,2,4-triazol, a 1H- a 2H-izoindol.[12] Tento typ tautomérie je dôležitý napríklad u aminokyseliny histidínu.
- Tautoméria, pri ktorej je pohyb protónu spojený so zmenou tvaru molekuly z reťazca na kruh. Príkladom je napríklad zmena tvaru cukrov z otvoreného reťazca na hemiacetálový kruh, typická pre pyranózy a furanózy. Táto tautoméria by sa dala zapísať ako H−O ⋅ C=O ⇌ O−C−O−H, pričom "⋅" znázorňuje miesto, kde sa v procese vytvorí nová väzba.
Tautomerizácia môže všeobecne byť katalyzovaná:
- kyselinou, pozostávajúc z krokov: protonácia, vytvorenie delokalizovaného katiónu a deprotonácia na inom mieste vedľa katiónu
- bázou (zásadou), pozostávajúc z krokov: deprotonácia, vytvorenie delokalizovaného aniónu (napr. enolátu) a protonácia na inom mieste vedľa aniónu

Prototropia
Prototropia je reakcia, počas ktorej sa presúva protón, a je to najbežnejší druh tautomérie.[13][14] Prototropická tautoméria sa dá považovať za časť acidobázického chovania látok. Tieto tautoméry sú sadami izomérnych protónovaných štruktúr s rovnakým sumárnym vzorcom a celkovým nábojom.
Ako prototropia sa môže označovať i presun protónu v rámci štruktúry smerom k stabilnejšej molekule, napríklad ak vzniká konjugovaný systém:[5]
- CH2=C(CH3)-CH2-CHO → CH3-C(CH3)=CH2-CHO
Valenčná tautoméria
Valenčná tautoméria je druhu tautomérie, pri ktorej sa rýchlo tvorí a zaníka obyčajna alebo dvojitá väzba, a to bez zmeny polohy atómov alebo skupín.[15] Je odlišná od prototropickej tautomérie a spočíva v rýchlej reorganizácii elektrónov tvoriacich väzby.

Párom valenčných tautomérov so vzorcom C6H6O sú oxepin a benzénoxid.[15][16]
Iné príklady tohto typu tautomérie je možné vidieť napríklad u bullvalénu a u otvorených či cyklických foriem niektorých heterocyklov, ako sú azidy a tetrazoly.[17]
Valenčné tautoméry vyžadujú zmenu v molekulárnej geometrii a nemali by sa zamienať s rezonančnými štruktúrami.
Referencie
Zdroj
Wikiwand in your browser!
Seamless Wikipedia browsing. On steroids.
Every time you click a link to Wikipedia, Wiktionary or Wikiquote in your browser's search results, it will show the modern Wikiwand interface.
Wikiwand extension is a five stars, simple, with minimum permission required to keep your browsing private, safe and transparent.
