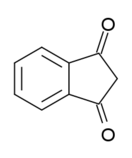
Индандион
химическое соединение Из Википедии, свободной энциклопедии
Индан-1,3-дион — органическое вещество, представитель ненасыщенных транс-фиксированных β-дикетонов. В кристаллическом виде бесцветное или желтоватое и существует в форме именно дикетона. В водном же растворе частично енолизирован. Значительный вклад в развитие химии индандиона и его производных внёс профессор РТУ Г. Я. Ванаг — основатель рижской школы химиков-органиков.
| Индан-1,3-дион | |||
|---|---|---|---|
| |||
| Общие | |||
| Систематическое наименование |
Индан-1,3-дион 1,3-индандион |
||
| Традиционные названия |
Индандион 1,3-дикетогидринден |
||
| Хим. формула | C9H6O2 | ||
| Физические свойства | |||
| Состояние | бесцветное или желтоватое твёрдое | ||
| Молярная масса | 146.14 г/моль | ||
| Плотность | 1,37 [1] | ||
| Термические свойства | |||
| Температура | |||
| • плавления | 129—130 (или 132[2]) | ||
| Энтальпия | |||
| • образования | (для газа) -165,0 ± 2,6 кДж/моль | ||
| Удельная теплота испарения | (пересчитано из значения ниже) 0,497 Дж/кг | ||
| Удельная теплота плавления | 17,2 кДж/моль[3] | ||
| Давление пара | |||
| Химические свойства | |||
| Константа диссоциации кислоты | 7,4 | ||
| Растворимость | |||
| • в воде | небольшая | ||
| Классификация | |||
| Рег. номер CAS | 606-23-5 | ||
| PubChem | 11815 | ||
| Рег. номер EINECS | 210-109-7 | ||
| SMILES | |||
| InChI | |||
| ChEBI | 78877 | ||
| ChemSpider | 11322 | ||
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |||
| Медиафайлы на Викискладе | |||
Особенности строения
Енольная форма характеризуется сопряжением связей и отрицательным частичным зарядом на 2-м атоме углерода и том атоме кислорода, который не связан с водородом (то есть, любой из двух). Анион же индандиона — это сопряжённая 6π-электронная система, отрицательный заряд делокализирован. Согласно приблизительным расчётам по методу МО Хюккеля (для такой системы транс-фиксированного дикетона вообще) наибольшая электронная плотность после обоих атомов кислорода находится опять-таки на 2-м атоме углерода. Это обуславливает многие его химические свойства.
Получение
Индандион получают кислым гидролизом и одновременным декарбоксилированием натриевой соли 2-алкоксикарбонилиндан-1,3-диона (обычно этокси-) при повышенной температуре.
Саму же соль получают сложноэфирной конденсацией алкилацетата и диалкилфталата (обычно этилацетата и диэтил- или диметилфталата).
При окислении же индана такими реагентами, как пероксид водорода или трет-бутилгидропероксид, в качестве основного продукта получают индан-1-он, индандион получается лишь как примесь.[4]
Химические свойства
Суммиров вкратце
Перспектива
Индан-1,3-дион является очень сильным C-нуклеофилом.
Специфические реакции
- Самоконденсация происходит весьма легко с образованием биндона — специфического реагента на первичные амины.

Общие для дикетонов свойства
- Енолизация — в воде pKE = 5,6, это соответствует двум процентам енола. Надо помнить, что в разных растворителях KE может быть разная ввиду различных эффектов сольватирования для OH- и CH-кислот. Как обычно, транс-фиксированные дикетоны с пятичленным циклом менее енолизированны, чем подобные соединения с шестичленным циклом.

- Электрофильное присоединение — получаются продукты как C-, так и O-присоединения. Это, однако, зависит также от растворителя и концентрации веществ. Реакция происходит с енольной формой или анионом. Например, при бромировании можно получить в зависимости от стехиометрии 2-броминдан-1,3-дион или 2,2-диброминдан-1,3-дион.[5]

- Очень характерна реакция нитрования — проходит легко с образованием 2-нитроиндандиона — сильной кислоты. C-электрофилы обычно реагируют с анионом дикетона. Продукты реакции с альдегидами — обычно бис-продукты.
- В качестве примера ацилирования можно привести реакцию с 1,1-дифенилацетоном, которой можно получить родентицид 2-дифенилацетилиндан-1,3-дион (дифацинон или дифенадион).[6]

- В качестве других электрофильных реакций присоединения можно упомянуть галогенирование другими реагентами, сульфирование, азосочетание, нитрозирование.
Этот раздел нужно дополнить. |
- Восстановление амальгамой цинка по Клемменсену приводит к индану, побочным же продуктом является инден.[7]

- Равно и каталитическое ионное гидрирование (триэтилсиланом и трифторуксусной кислотой) приводит к индану.[8]
- Зато, восстанавливая селективным восстановителем боргидридом натрия (в присутствии палладиевого катализатора), получают 3-гидрокси-1-инданон; при дальнейшем восстановлении — соответственно, индан-1,3-диол.[9]

- Сходным образом и цинковая пыль в ледяной уксусной кислоте реагирует с образованием 3-гидрокси-1-инданона.[10]
- Гомолитические реакции — при взаимодействии индандиона с активными свободными радикалами, а также при окислении анионов образуются стабилизированные делокализацией радикалы, тут же вступающие в дальнейшие реакции, как, например, с алкадиенами, алкинами и друг с другом (димеризация). Особенно стабильны радикалы 2-арилпроизводных индандиона.
- Частным случаем является окисление индандиона в нингидрин с помощью NBS и диметилсульфоксида. Те же реагенты помогают получить нингидрин из 1-инданона и 2-инданона.[11]

Применение
Производные индандиона — биндон, 2-нитроиндандион, нингидрин — используют в аналитической химии. Есть производные, которые, возможно, будут использоваться в фотонике (ведутся исследования).[12] Некоторые производные являются препаратами, понижающими свёртываемость крови (антикоагулянты). В медицине, в частности, применяют арилпроизводные (фенилин — 2-фенилиндан-1,3-дион и омефин — 2-гидроксиметил-2-фенилиндан-1,3-дион). В качестве родентицида (крысиного яда) применяют ратиндан (2-дифенилацетилиндан-1,3-дион); нужно, однако, помнить, что этот способ травли крыс весьма жесток — крыса, ввиду своего образа жизни часто получающая небольшие царапины, истекает кровью и погибает от её потери.
Литература
- Нейланд О. Я. Органическая химия: Учеб. для хим. спец. вузов. Москва: Высшая школа, 1990.— с. 481—490.
- Valters, Raimonds. Organiskā ķīmija (speckurss). Lekciju konspekts. Rīga: RTU izdevniecība, 2009.— 114 lpp. (латыш.)
Примечания
Wikiwand - on
Seamless Wikipedia browsing. On steroids.