Loading AI tools
związek chemiczny Z Wikipedii, wolnej encyklopedii
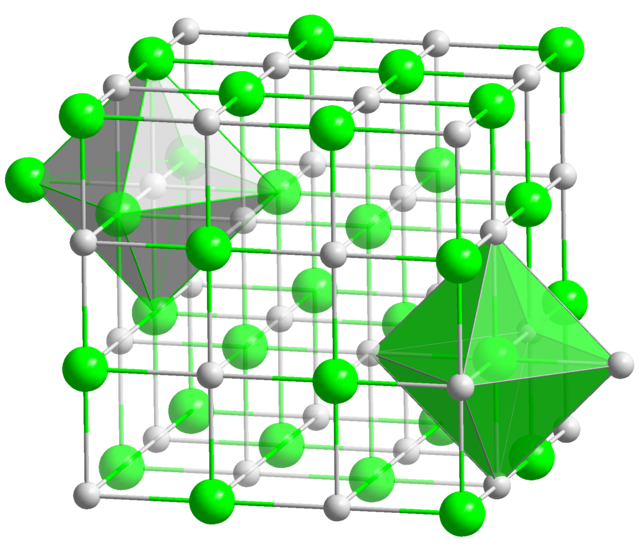
Tlenek magnezu (magnezja palona), MgO – nieorganiczny związek chemiczny z grupy tlenków zasadowych zawierający magnez na II stopniu utlenienia.
| |||||||||||||||||||||||||||||||
 | |||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||
| Ogólne informacje | |||||||||||||||||||||||||||||||
| Wzór sumaryczny |
MgO | ||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Masa molowa |
40,30 g/mol | ||||||||||||||||||||||||||||||
| Wygląd |
biały proszek | ||||||||||||||||||||||||||||||
| Minerały | |||||||||||||||||||||||||||||||
| Identyfikacja | |||||||||||||||||||||||||||||||
| Numer CAS | |||||||||||||||||||||||||||||||
| PubChem | |||||||||||||||||||||||||||||||
| DrugBank | |||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||
| Podobne związki | |||||||||||||||||||||||||||||||
| Podobne związki | |||||||||||||||||||||||||||||||
| Jeżeli nie podano inaczej, dane dotyczą stanu standardowego (25 °C, 1000 hPa) | |||||||||||||||||||||||||||||||
Związek ten w temperaturze pokojowej jest białą substancją krystaliczną. Otrzymany w temperaturze do 900 °C nazywany jest magnezją kaustyczną kalcynowaną[5] i łatwo ulega reakcjom, np. roztwarza się w kwasach. W przeciwieństwie do CaO z zimną wodą reaguje bardzo powoli[6][7], jednak po podgrzaniu reakcja staje się szybka[7]. Produktem jest wodorotlenek magnezu, Mg(OH)
2[6][7]. Po wyprażeniu w temp. 1700–2000 °C lub wyższej tworzy tzw. magnezję spiekaną (znaną też jako magnezja całkowicie wypalona[5][8]), która ze względu na bardzo małą powierzchnię właściwą jest niereaktywna[9]. Po stopieniu magnezji (tt. >2800 °C) w łuku elektrycznym i zestaleniu otrzymuje się magnezję topioną[9][5], o jeszcze mniejszej reaktywności; jest ona praktycznie odporna na warunki atmosferyczne[9].
Tlenek magnezu występuje w przyrodzie jako minerał peryklaz.
Stosowany jest do wyrobu cementów, odlewów, naczyń ognioodpornych, tygli. Ma również zastosowanie w medycynie jako lek na nadkwasotę i zatrucia. W fotografii służy do zobojętniania emulsji fotograficznej.
Tlenek magnezu na skalę przemysłową otrzymuje się[9]:
W procesach tych MgO wytwarza się podobnie jak z wody morskiej. Chlorek magnezu można poddać też pirohydrolizie, umieszczając go w strumieniu przegrzanej pary wodnej o temp. 300–1000 °C:
Na skalę laboratoryjną MgO można otrzymać poprzez utlenianie lub spalanie magnezu[10]:
Inne metody to rozkład termiczny Mg(OH)
2 lub niektórych soli magnezu (MgCO
3[7], Mg(NO
3)
2, MgSO
4)[10].
Seamless Wikipedia browsing. On steroids.
Every time you click a link to Wikipedia, Wiktionary or Wikiquote in your browser's search results, it will show the modern Wikiwand interface.
Wikiwand extension is a five stars, simple, with minimum permission required to keep your browsing private, safe and transparent.