രാസസംയുക്തം From Wikipedia, the free encyclopedia
സ്ഥിരതയില്ലാത്ത ഒരു അകാർബണിക സയനൈഡ് സംയുക്തമാണ് അമോണിയം സയനൈഡ് (Ammonium cyanide). ഇതിന്റെ തന്മാത്രാ സൂത്രം NH4CN.
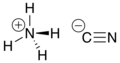 | |||
| |||
| Identifiers | |||
|---|---|---|---|
3D model (JSmol) |
|||
| ChemSpider | |||
PubChem CID |
|||
CompTox Dashboard (EPA) |
|||
| InChI | |||
| SMILES | |||
| Properties | |||
| തന്മാത്രാ വാക്യം | |||
| Molar mass | 0 g mol−1 | ||
| Appearance | colourless crystalline solid | ||
| സാന്ദ്രത | 1.02 g/cm3 | ||
| ക്വഥനാങ്കം | |||
| very soluble | |||
| Solubility | very soluble in alcohol | ||
| Related compounds | |||
| Other anions | Ammonium hydroxide Ammonium azide Ammonium nitrate | ||
| Other cations | Sodium cyanide Potassium cyanide | ||
Except where otherwise noted, data are given for materials in their standard state (at 25 °C [77 °F], 100 kPa).
| |||
കാർബണിക പദാർത്ഥങ്ങൾ നിർമ്മിക്കാനാണ് അമോണിയം സയനൈഡ് പൊതുവേ ഉപയോഗിക്കുന്നത്. അസ്ഥിര സംയുക്തമായതിനാൽ, വ്യവസായിക ആവശ്യങ്ങൾക്കായി കയറ്റുമതി ചെയ്യാറില്ല.
താഴ്ന്ന താപനിലയിൽ, ഹൈഡ്രജൻ സയനൈഡ് ജലീയ അമോണിയയുമായി ബബ്ബ്ളിംഗ് നടത്തി അമോണിയം സയനൈഡ് നിർമ്മിക്കാം
കാൽസ്യം സയനൈഡ്, അമോണിയം കാർബണേറ്റ് എന്നിവ തമ്മിൽ പ്രവർത്തിപ്പിച്ചും അമോണിയം സയനൈഡ് നിർമ്മിക്കാം
പൊട്ടാസ്യം സയനൈഡ് അല്ലെങ്കിൽ പൊട്ടാസ്യം ഫെറോസയനൈഡ് അമോണിയം ക്ലോറൈഡുമായി പ്രവർത്തിപ്പിച്ച് ലഭിക്കുന്ന വാതകം ഖരീഭവിപ്പിച്ച് അമോണിയം സയനൈഡ് ക്രിസ്റ്റൽ തയ്യാറാക്കാം.
അമോണിയം സയനൈഡ് വിഘടിച്ച് അമോണിയ, ഹൈഡ്രജൻ സയനൈഡ് എന്നിവയുണ്ടാകുന്നു.
ലോഹിയ ലവണങ്ങളുമായി പ്രവർത്തിക്കുന്നു. ഗ്ലയോക്സാലുമായി പ്രവർത്തിച്ച് ഗ്ലൈസീൻ (aminoacetic acid) ഉണ്ടാകുന്നു.
മാരക വിഷമാണ് അമോണിയം സയനൈഡ്. ശരീരത്തിലെത്തിയാൽ മരണം സംഭവിക്കാം. ലവണം വിഘടിച്ച് ഹൈഡ്രജൻ സയനൈഡ് ഉണ്ടാവുന്നതിനാൽ അതും കൈകാര്യം ചെയ്യുന്നത് അപകടമാണ്.
ഘടകങ്ങൾ: H 9.15%, C 27.23%, N 63.55%.
Seamless Wikipedia browsing. On steroids.
Every time you click a link to Wikipedia, Wiktionary or Wikiquote in your browser's search results, it will show the modern Wikiwand interface.
Wikiwand extension is a five stars, simple, with minimum permission required to keep your browsing private, safe and transparent.