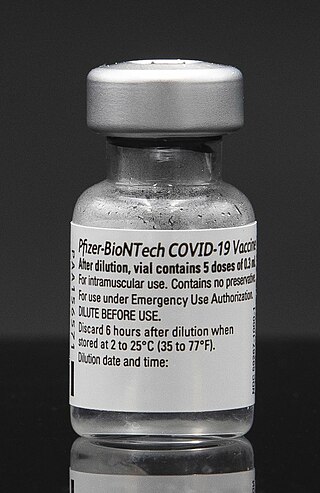
Vaccino anti COVID-19 Pfizer-BioNTech
Vaccino mRNA contro COVID-19 di BioNTech in collaborazione con Pfizer Da Wikipedia, l'enciclopedia libera
Il vaccino anti COVID-19 Pfizer-BioNTech, denominazione comune internazionale Tozinameran (nome durante la sperimentazione BNT162b2), commercializzato come Comirnaty, è un vaccino anti COVID-19 a mRNA sviluppato nel 2020 da BioNTech e Pfizer e somministrabile per iniezione intramuscolare.
| Tozinameran | |
|---|---|
 | |
| Nomi alternativi | |
| BNT162b2 Comirnaty | |
| Caratteristiche generali | |
| Numero CAS | |
| DrugBank | DBDB15696 |
| Dati farmacologici | |
| Categoria farmacoterapeutica | Vaccino |
| Modalità di somministrazione | Iniezione intramuscolare |
| Indicazioni di sicurezza | |
Il nome secondo la denominazione comune internazionale, al momento della messa in commercio del vaccino, è un pINN, cioè un nome proposto non ancora definitivamente approvato.[1]
La vaccinazione, possibile a tutti dal compimento del 5º compleanno, richiede principalmente due dosi somministrate a 21 giorni di distanza come minimo e 42 giorni di distanza come massimo.[2][3][4] In seguito, tra i 4 e i 6 mesi successivi, si può effettuare la terza dose (booster one) se si ha almeno dodici anni e successivamente i soggetti fragili e gli anziani anche un’ulteriore quarta (booster two) dopo un altro arco di tempo extramensile.
È stato preferito alla sua variante, BNT162b1, per gli studi clinici di fase II e III,[5] ed è in fase di valutazione intermedia nella fase III alla fine del 2021: il 18 novembre 2020 è stata pubblicata una prima valutazione relativa ai dati di fase,[6] ma lo studio e sperimentazione dureranno fino a gennaio 2023.[3]
Il 2 aprile 2021 le due società Pfizer e BioNTech hanno confermato in un comunicato congiunto, secondo quanto riporta la CNN, che dai test effettuati durante le sperimentazioni cliniche di Fase III, il vaccino da loro prodotto fornisce una protezione per almeno sei mesi dopo la somministrazione della seconda dose e ha un'efficacia del 100% contro la variante sudafricana del SARS-CoV-2 501.V2.[7]
La distribuzione e la conservazione di BNT162b2 è una sfida logistica globale, a causa della necessità di mantenere il vaccino a mRNA a temperature inferiori ai −70 °C fino a due ore prima delle vaccinazioni.[8] Il 26 marzo 2021 l'Agenzia europea per i medicinali ha espresso un parere positivo per consentire il trasporto e la conservazione delle fiale del vaccino BioNTech/Pfizer a temperature comprese tra -25 °C e -15 °C per un periodo una tantum di due settimane.[9]
Caratteristiche
Riepilogo
Prospettiva
La tecnologia di BioNTech per il vaccino BNT162b2 si basa sull'uso dell'RNA che codifica parte della proteina spike sulla superficie del SARS-CoV-2, innescando una risposta immunitaria contro l'infezione da parte della proteina del virus.[10]
L'mRNA è modificato con nucleotidi per codificare una forma mutata della proteina spike ed è incapsulato in nanoparticelle liposomiali.[11]
La versione mutata della proteina spike contiene due sostituzioni di prolina (K986P, V987P) che le inducono ad adottare una forma che stimola gli anticorpi neutralizzanti.[11][12]
In seguito all'esito degli studi sull'efficacia, il vaccino di Pfizer-BioNTech è risultato avere una efficacia pari al 95% nel prevenire le infezioni sintomatiche da COVID-19.[13] Il 95% di riduzione si riferisce alla differenza tra i 162 casi che si sono avuti nel gruppo dei 18 325 che hanno ricevuto il placebo e i soli 8 casi che si sono avuti nei 18 198 che hanno ricevuto il vaccino.[14] L'efficacia nel prevenire il contagio e l'infezione è risultata pari al 80%.[15] Per avere un caso sintomatico dopo la vaccinazione, il vaccino deve fallire sia nella prevenzione dell'infezione che nella prevenzione della malattia sintomatica pertanto nei modelli matematici utilizzati per stimare l'effetto della vaccinazioni di massa, l'efficacia complessiva è pari al 75%.[16]
Storia
Riepilogo
Prospettiva
BioNTech è lo sviluppatore originale della tecnologia vaccinale, mentre Pfizer fornisce la logistica, finanzia e supervisiona gli studi clinici, ed è il partner di produzione di Comirnaty in tutto il mondo, con l'eccezione della Cina dove la licenza è stata acquistata da Fosun.[2][17]
Pfizer ha indicato a novembre 2020 che 50 milioni di dosi potrebbero essere disponibili negli Stati Uniti entro la fine del 2020, con circa 1,3 miliardi di dosi entro la metà del 2021.[4] Pfizer ha accordi di acquisto per circa 3 miliardi di dollari per la fornitura di un vaccino autorizzato negli Stati Uniti, nell'Unione europea, nel Regno Unito, in Giappone, Canada e Perù.[8] Il 21 aprile 2021 il quotidiano catalano La Vanguardia ha pubblicato in esclusiva la versione integrale del contratto siglato tra Pfizer e Commissione UE. Il documento firmato dettaglia le possibili responsabilità dell'azienda nel caso in cui il prodotto causi danni a terzi. Il testo chiarisce che ogni responsabilità è nelle mani della Commissione europea e dei Paesi membri. L'azienda farmaceutica è responsabile per qualsiasi guasto che potrebbe essere registrato nella produzione del vaccino, ma dalla consegna ai Paesi membri la multinazionale non è responsabile, né dovrà affrontare alcun risarcimento. Né lei, né alcuno dei suoi direttori o dipendenti, né quelli di alcuno dei suoi partner.[18]
Nel settembre 2021 l'Istituto Spallanzani di Roma ha pubblicato uno studio finanziato dal ministero della salute sulla caratterizzazione virologica e sierologica delle infezioni da SARS-CoV-2 diagnosticate dopo la vaccinazione con mRNA BNT162b2.[19]
L'11 ottobre 2022 Janine Small, presidente dei mercati internazionali sviluppati per Pfizer, ha ammesso davanti al Parlamento europeo a Bruxelles che, durante lo sviluppo del vaccino, non sono stati effettuati test per verificare quanto le persone vaccinate potevano trasmettere il virus prima della sua immissione sul mercato.[20][21]
Si tratta del farmaco più venduto al mondo nel 2021.[22]
Composizione
Flaconcino multidose contenente 6 dosi da 0,3 mL. Una dose contiene 30 microgrammi di RNA messaggero (mRNA).[23]
Elenco degli eccipienti:
- ((4-idrossibutil)azanediil)bis(esano-6,1-diil)bis(2-esildecanoato) (ALC-0315)
- 2-[(polietilenglicole)-2000]-N,N-ditetradecilacetammide (ALC-0159)
- 1,2-distearoil-sn-glicero-3-fosfocolina (DSPC)
- Colesterolo
- Potassio cloruro
- Potassio diidrogeno fosfato
- Sodio cloruro
- Fosfato disodico diidrato
- Saccarosio
- Acqua per preparazioni iniettabili
- sodio idrossido (per aggiustamento del pH)
- acido cloridrico (per aggiustamento del pH)[24]
Posologia
Soggetti di età pari o superiore a 12 anni. Il vaccino viene somministrato per via intramuscolare dopo diluizione come ciclo di tre dosi (da 0,3 mL ciascuna).[24]
Per soggetti di età pari o superiori a 5 anni e fino a 11 anni, il vaccino viene somministrato per via intramuscolare dopo diluizione come ciclo di due dosi (da 0,1 mL ciascuna).
Non sono disponibili dati sull'intercambiabilità di Comirnaty con altri vaccini anti-COVID-19 per completare il ciclo di vaccinazione. I soggetti che hanno ricevuto una dose di Comirnaty devono ricevere una seconda dose di Comirnaty per completare il ciclo di vaccinazione.[25]
Effetti collaterali
Riepilogo
Prospettiva
Le reazioni più frequentemente segnalate sono rappresentate da febbre, dolore in sede di iniezione, stanchezza/astenia, brividi e malessere generale. Seguono in ordine di frequenza le patologie del sistema nervoso, prevalentemente costituite da cefalea, parestesie agli arti e sonnolenza, e le patologie del sistema muscolo-scheletrico e del tessuto connettivo, soprattutto mialgie, artralgie e dolore muscoloscheletrico. Più raramente sono stati riportati sospetti eventi avversi relativi alla classe organo-sistemica delle patologie gastro-intestinali e delle patologie del sistema emolinfopoietico, prevalentemente rappresentati da linfoadenopatia. Fra le reazioni avverse segnalate con frequenza molto rara rientrano tachicardia e paralisi del nervo facciale.[26]
Nel gennaio 2021 viene riportata la notizia di alcune morti di anziani, avvenute in Norvegia dopo la somministrazione del vaccino Comirnaty. Secondo il Folkehelseinstituttet (Istituto nazionale di sanità pubblica), anche reazioni comuni ai vaccini, come febbre e nausea, potrebbero contribuire a un peggioramento clinico o a un esito fatale tra i pazienti anziani più fragili.[27][28]
Il 19 luglio 2021 l'AIFA pubblica una nota informativa di aggiornamento importante sul rischio di miocardite e di pericardite osservati dopo la vaccinazione con i vaccini mRNA anti COVID-19 Comirnaty e Spikevax. I casi si sono verificati entro 14 giorni successivi alla vaccinazione, dopo la seconda dose e principalmente nei giovani di sesso maschile. Fino al 31 maggio 2021, nello Spazio economico europeo (SEE), si sono verificati 145 casi di miocardite tra i soggetti che hanno ricevuto Comirnaty e 19 casi tra i soggetti che hanno ricevuto Spikevax. Inoltre, si sono verificati 138 casi di pericardite a seguito dell'uso di Comirnaty e 19 casi a seguito dell'uso di Spikevax. Si stima che circa 177 milioni di dosi di Comirnaty e 20 milioni di dosi di Spikevax siano state somministrate nello Spazio economico europeo fino al 31 maggio 2021. L'incidenza è pertanto inferiore a un caso su un milione (basandosi sulla farmacovigilanza passiva).[29] Al 3 settembre 2021, il Vaccine Adverse Event Reporting System segnala 2 053 casi di miocardite negli Stati Uniti in un totale di 212 320 000 somministrazioni, dimostrando invece un'incidenza di almeno un caso su 103 000.[30][31]
L'11 agosto 2021 l'EMA pubblica uno studio di sicurezza su nuove segnalazioni per potenziali effetti collaterali collegabili alla vaccinazione relative all'eritema multiforme, la valutazione segue un piccolo numero di casi segnalati dopo l'iniezione al sistema EudraVigilance. Altre segnalazioni vengono esaminate riguardo alla glomerulonefrite (infiammazione dei minuscoli filtri nei reni) e alla sindrome nefrosica (malattia renale che porta a perdere troppe proteine nelle urine).[32]
Il 16 agosto 2021 è stato pubblicato il primo caso di sindrome di Stevens-Johnson / necrolisi epidermica tossica in seguito alla somministrazione del vaccino Pfizer anti COVID-19.[33]
Il 6 ottobre l'EMA ha riferito tra le reazioni avverse per il vaccino Comirnaty di Pfizer anche i casi di parestesie. In particolare, come scritto nella scheda redatta dal Comitato di valutazione rischi per la farmacovigilanza (PRAC) sono stati segnalati quasi 22 000 casi di parestesie e ipoestesie su circa 1 220 000 000 dosi somministrate nel mondo.[34]
Al 9 aprile 2022 la banca dati europea delle segnalazioni di sospette reazioni avverse ai farmaci segnala 892.579 sospetti eventi avversi, il 70,8% delle reazioni è riferita a individui di sesso femminile. I principali Paesi europei con il più alto numero di casi segnalati dopo la somministrazione del vaccino sono: Germania 166.621, Paesi Bassi 117.281, Francia 101.115, Italia 84.119, Austria 54.439, Spagna 36.845, Svezia 20.819, Norvegia 17.554, Danimarca 15.298 e Portogallo 12.369.[35] Al 1º aprile 2022, il VAERS segnala 149.248 eventi avversi gravi.[36]
L'8 novembre 2021 la rivista scientifica Circulation pubblica il risultato di uno studio evidenziando che i vaccini a mRNA hanno aumentato notevolmente markers di infiammazione sull'endotelio e l'infiltrazione di cellule T del muscolo cardiaco e possono spiegare l'aumento della trombosi, cardiomiopatie e altri eventi vascolari successivi alla vaccinazione, in un gruppo di pazienti gia' sotto osservazione dagli Autori. Lo studio precisa anche l'assenza di un gruppo di controllo.[37]
Il 10 novembre 2021 le autorità di Taiwan hanno deciso di sospendere la somministrazione della seconda dose del vaccino Pfizer-BioNTech per la popolazione di età 12-17 anni a causa di possibili rischi di infiammazione cardiaca.[38][39][40]
Il 18 novembre 2021 il Journal of Endocrinological Investigation pubblica lo studio di una tiroidite silente e della malattia di Graves successivi alla vaccinazione.[41]
Il 27 novembre 2021 il Dermatology Online Journal pubblica lo studio di una reazione lupus erimatoso cutaneo sviluppatasi due mesi e mezzo dopo la seconda dose del vaccino.[42]
Il 16 dicembre 2021 la rivista AACE Clinical Case Reports pubblica lo studio di due pazienti con evidenza sintomatica di tiroidite subacuta successiva alla vaccinazione.[43]
Il 1º febbraio 2022 la rivista The Lancet pubblica lo studio di diversi ricoveri ospedalieri con evidenza sintomatica di herpes zoster successiva alla vaccinazione.[44]
Nel febbraio 2022 l'AIFA pubblica il rapporto annuale sulla sicurezza dei vaccini anti-COVID-19.[45]
Il 24 marzo 2022 il BMC Oral Health pubblica lo studio di quattro casi di eritema multiforme orale sviluppatasi dopo la vaccinazione.[46]
Note
Altri progetti
Collegamenti esterni
Wikiwand - on
Seamless Wikipedia browsing. On steroids.