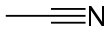Loading AI tools
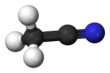
Asetonitril adalah senyawa kimia dengan rumus CH3CN. Senyawa ini berupa cairan tidak berwarna, merupakan nitril organik yang paling sederhana (hidrogen sianida lebih sederhana, tetapi anion sianida tidak digolongkan sebagai organik). Senyawa ini terutama diproduksi sebagai produk samping dari pembuatan akrilonitril. Senyawa ini digunakan sebagai pelarut polar aprotik dalam sintesis organik dan pemurnian butadiena.[5]
| |||
| |||
| Nama | |||
|---|---|---|---|
| Nama IUPAC (preferensi)
Acetonitrile[1] | |||
| Nama IUPAC (sistematis)
Ethanenitrile[1] | |||
| Nama lain | |||
| Penanda | |||
Model 3D (JSmol) |
|||
| 3DMet | {{{3DMet}}} | ||
| Referensi Beilstein | 741857 | ||
| ChEBI | |||
| ChEMBL | |||
| ChemSpider | |||
| Nomor EC | |||
| Referensi Gmelin | 895 | ||
| MeSH | acetonitrile | ||
PubChem CID |
|||
| Nomor RTECS | {{{value}}} | ||
| UNII | |||
| Nomor UN | 1648 | ||
CompTox Dashboard (EPA) |
|||
| |||
| |||
| Sifat | |||
| C2H3N | |||
| Massa molar | 41,05 g·mol−1 | ||
| Penampilan | Cairan tak berwarna | ||
| Densitas | 0.786 g mL−1 | ||
| Titik lebur | −46 hingga −44 °C; −51 hingga −47 °F; 227 hingga 229 K | ||
| Titik didih | 3.271 hingga 3.279 °C; 5.920 hingga 5.934 °F; 3.544 hingga 3.552 K | ||
| Larut | |||
| log P | −0.334 | ||
| Tekanan uap | 9.71 kPa (at 20.0 °C) | ||
| kH | 530 μmol Pa−1 kg−1 | ||
| Keasaman (pKa) | 25 | ||
| Kebasaan (pKb) | −11 | ||
| λmaks | 195 nm | ||
| Absorbansi | ≤0.10 | ||
| Indeks bias (nD) | 1.344 | ||
| Termokimia | |||
| Kapasitas kalor (C) | 91.69 J K−1 mol−1 | ||
| Entropi molar standar (S |
149.62 J K−1 mol−1 | ||
| Entalpi pembentukan standar (ΔfH |
40.16–40.96 kJ mol−1 | ||
| Entalpi pembakaran standar ΔcH |
−1256.03–−1256.63 kJ mol−1 | ||
| Bahaya | |||
| Piktogram GHS |   | ||
| Keterangan bahaya GHS | {{{value}}} | ||
| H225, H302, H312, H319, H332 | |||
| P210, P280, P305+351+338 | |||
| Titik nyala | 20 °C (68 °F; 293 K) | ||
| 5.230 °C (9.450 °F; 5.500 K) | |||
| Ambang ledakan | 4.4–16.0% | ||
| Dosis atau konsentrasi letal (LD, LC): | |||
LD50 (dosis median) |
| ||
LC50 (konsentrasi median) |
5655 ppm (guinea pig, 4 hr) 2828 ppm (rabbit, 4 hr) 53,000 ppm (rat, 30 min) 7500 ppm (rat, 8 hr) 2693 ppm (mouse, 1 hr)[3] | ||
LCLo (terendah tercatat) |
16,000 ppm (dog, 4 hr)[3] | ||
| Batas imbas kesehatan AS (NIOSH): | |||
PEL (yang diperbolehkan) |
TWA 40 ppm (70 mg/m3)[4] | ||
REL (yang direkomendasikan) |
TWA 20 ppm (34 mg/m3)[4] | ||
IDLH (langsung berbahaya) |
500 ppm[4] | ||
| Senyawa terkait | |||
Related alkananitril |
| ||
Senyawa terkait |
DBNPA | ||
Kecuali dinyatakan lain, data di atas berlaku pada suhu dan tekanan standar (25 °C [77 °F], 100 kPa). | |||
| Referensi | |||
Di laboratorium, senyawa ini ini digunakan sebagai pelarut dengan polaritas medium yang larut dalam air dan pelarut organik, namun tidak pada hidrokarbon jenuh. Senyawa ini memiliki nilai konstanta dielektrik tinggi yaitu 38.8. Dengan momen dipol 3.92 D,[6] asetonitril melarutkan berbagai macam senyawa ion dan nonpolar dan berguna sebagai fase gerak pada HPLC dan LC-MS. Rangka N-C-C linear dengan jarak C-N pendek 1.16 Å.[7]
Asetonitril pertama kali dibuat pada tahun 1847 oleh ahli kimia Prancis Jean-Baptiste Dumas.[8]
Asetonitril digunakan terutama sebagai pelarut dalam pemurnian butadiena di kilang. Secara khusus, asetonitril diumpankan ke bagian atas kolom distilasi yang diisi dengan hidrokarbon seperti butadiena dan selagi asetonitril melalui kolom, asetonitril menyerap butadiena yang diumpankan dari bagian bawah menara ke menara pemisahan kedua. Panas ini kemudian digunakan di menara pemisahan untuk memisahkan butadiena.
Senyawa ini banyak digunakan dalam aplikasi baterai karena dielektrik konstan yang tinggi dan kemampuannya melarutkan elektrolit. Untuk alasan yang sama senyawa ini menjadi pelarut yang populer dalam voltametri siklik.
Sintesis organik
Asetonitril umum digunakan dalam sintesis organik[9] dalam berbagai bahan kimia, termasuk asetamidin hidroklorida, tiamin, dan asam α-naftalenaasetik.[10] Reaksi dengan sianogen klorida menghasilkan malononitril.[5]
Ligan dalam kimia koordinasi
Dalam kimia anorganik, asetonitril digunakan sebagai pelarut dan mudah menggantikan ligan. Misalnya, PdCl2(CH3CN)2 ini dibuat dengan memanaskan suspensi (polimer) paladium klorida dalam asetonitril:
- PdCl2 + 2 CH3CN → PdCl2(CH3CN)2
Kompleks terkait adalah [Cu(MeCN)4]+. Gugus CH
3CN pada kompleks dengan cepat digantikan oleh ligan lainnya.
Toksisitas
Asetonitril cukup beracun pada dosis kecil.[10][11] Senyawa ini dapat dimetabolisme menjadi hidrogen sianida, yang merupakan sumber utama efek racun.[12][13][14] Pada umumnya timbulnya efek toksik tertunda karena ada waktu yang diperlukan bagi tubuh untuk memetabolisme asetonitril menjadi sianida (umumnya sekitar 2-12 jam).[10]
Wikiwand in your browser!
Seamless Wikipedia browsing. On steroids.
Every time you click a link to Wikipedia, Wiktionary or Wikiquote in your browser's search results, it will show the modern Wikiwand interface.
Wikiwand extension is a five stars, simple, with minimum permission required to keep your browsing private, safe and transparent.