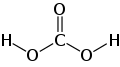
Asam karbonat
senyawa kimia Dari Wikipedia, ensiklopedia bebas
Asam karbonat adalah asam organik dengan rumus kimia H2CO3. Asam karbonat termasuk asam lemah. Dalam fisiologi, asam karbonat digambarkan sebagai asam volatil atau asam pernapasan, karena senyawa ini adalah satu-satunya asam yang diekskresikan sebagai gas oleh paru-paru.[2] Senyawa ini memainkan peran penting dalam sistem penyangga bikarbonat untuk mempertahankan homeostasis asam-basa.
| |||
| Nama | |||
|---|---|---|---|
| Nama IUPAC
Asam karbonat[1] | |||
| Nama lain
Larutan karbon dioksida; Dihidrogen karbonat; asam udara; asam hidroksimetanoat | |||
| Penanda | |||
Model 3D (JSmol) |
|||
| 3DMet | {{{3DMet}}} | ||
| ChEBI | |||
| ChEMBL | |||
| ChemSpider | |||
| Nomor EC | |||
| KEGG | |||
| Nomor RTECS | {{{value}}} | ||
CompTox Dashboard (EPA) |
|||
| |||
| |||
| Sifat | |||
| H2CO3 | |||
| Massa molar | 62.03 g/mol | ||
| Densitas | 1.668 g/cm3 | ||
| Hadir hanya dalam larutan | |||
| Keasaman (pKa) | 3.6 (pKa1 for H2CO3 only), 6.3 (pKa1 including CO2(aq)), 10.32 (pKa2) | ||
Kecuali dinyatakan lain, data di atas berlaku pada suhu dan tekanan standar (25 °C [77 °F], 100 kPa). | |||
| verifikasi (apa ini ?) | |||
| Referensi | |||
Sudah lama diyakini bahwa asam karbonat tidak dapat hadir sebagai senyawa murninya. Namun, pada tahun 1991 dilaporkan bahwa para ilmuwan NASA telah berhasil membuat sampel H2CO3 padat.[3]
Kesetimbangan reaksi kimia
Ketika karbon dioksida (CO2) larut dalam air (H2O) maka akan menghasilkan asam karbonat:[4]
- CO2 + H2O
 H2CO3.
H2CO3.
Asam karbonat bisa berubah menjadi ion bikarbonat (HCO3-) dan atom hidrogen.
Keasaman
Ringkasan
Perspektif
Asam karbonat adalah asam karboksilat dengan gugus hidroksil sebagai substituen. Senyawa ini juga merupakan asam poliprotik - khususnya diprotik, artinya senyawa ini memiliki dua proton yang dapat terlepas dari molekul induknya. Sehingga, terdapat dua konstanta disosiasi, yang pertama adalah untuk disosiasi menjadi ion bikarbonat (juga disebut hidrogen karbonat) HCO3−:
- Ka1 = 2.5×10−4;[4] pKa1 = 3.6 pada 25 °C.
Harus diperhatikan saat mengutip dan menggunakan konstanta disosiasi pertama asam karbonat. Dalam larutan air, asam karbonat ada dalam kesetimbangan dengan karbon dioksida, dan konsentrasi H2CO3 auh lebih rendah daripada konsentrasi CO2. Dalam banyak analisis, H2CO3 memasukkan CO2 terlarut (dirujuk sebagai CO2(aq)), H2CO3* digunakan untuk mewakili kedua spesi saat menulis persamaan kesetimbangan kimia berair. Persamaan dapat ditulis ulang sebagai berikut:[4]
- H2CO3*
 HCO3− + H+
HCO3− + H+ - Ka(app) = 4.47×10−7; pK(app) = 6.35 pada 25 °C dan kekuatan ionik = 0.0.
Peranan asam karbonat dalam darah
Asam karbonat merupakan langkah intermediat dalam transpor CO2 ke luar dari tubuh melalui pertukaran gas secara pernapasan. Reaksi hidrasi CO2 umumnya sangat lambat tanpa adanya katalis, tetapi sel darah merah mengandung enzim karbonik anhidrase, yang dapat meningkatkan laju reaksi serta mendisosiasi ion hidrogen (H+) dari asam karbonat yang terbentuk, menghasilkan bikarbonat (HCO3−) yang larut dalam plasma darah. Reaksi yang terkatalisasi ini berbalik di paru-paru, di mana bikarbonat diubah kembali menjadi CO2 sehingga gas ini dapat dibuang ke luar. Keseimbangan ini berperan penting sebagai suatu larutan penyangga atau buffer dalam darah mamalia.[5] Sebuah laporan teori pada tahun 2016 menunjukkan bahwa asam karbonat dapat memainkan peran penting dalam melindungi berbagai basa nitrogen dalam serum darah.[6]
Lihat pula
- Air berkarbonasi (minuman ringan)
- Karbon dioksida
- Dihidroksimetilidena (asam karbonat)
- Asam nonvolatil
- Pengasaman laut
Referensi
Bacaan lebih lanjut
Pranala luar
Wikiwand - on
Seamless Wikipedia browsing. On steroids.