kémiai vegyület From Wikipedia, the free encyclopedia
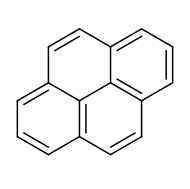
A pirén lapos policiklusos aromás szénhidrogén (PAH) 4 kondenzált benzolgyűrűvel. Képlete C16H10. E sárgászöld szilárd anyag a legkisebb perikondenzált (1-nél több oldalon kondenzált gyűrűs) PAH. A pirén szerves vegyületek részleges égésekor keletkezik.[6]
| Pirén | |||
 | |||
 | |||
 | |||
| Más nevek | Benzo[def]fenantrén | ||
| Kémiai azonosítók | |||
|---|---|---|---|
| CAS-szám | 129-00-0 | ||
| PubChem | 31423 | ||
| ChemSpider | 29153 | ||
| KEGG | C14335 | ||
| ChEBI | 39106 | ||
| RTECS szám | UR2450000 | ||
| |||
| |||
| InChIKey | BBEAQIROQSPTKN-UHFFFAOYSA-N | ||
| Beilstein | 1307225 | ||
| Gmelin | 84203 | ||
| UNII | 9E0T7WFW93 | ||
| ChEMBL | 279564 | ||
| Kémiai és fizikai tulajdonságok | |||
| Kémiai képlet | C16H10 | ||
| Moláris tömeg | 202,25 g/mol | ||
| Megjelenés | színtelen szilárd anyag (sárga szennyeződések gyakoriak sok mintában) | ||
| Sűrűség | 1,271 g/cm3[1] | ||
| Olvadáspont | 150,62 °C | ||
| Forráspont | 394 °C | ||
| Oldhatóság (vízben) | 0,049 mg/l (0 °C) 0,139 mg/l (25 °C) 2,31 mg/l (75 °C)[2] | ||
| Tiltott sáv | 2.02 eV[3] | ||
| Mágneses szuszceptibilitás | -147·10−6 cm3/mol[4] | ||
| Megoszlási hányados | 5.08[5] | ||
| Kristályszerkezet | |||
| Kristályszerkezet | Monoklin | ||
| Tércsoport | P21/a | ||
| Rácsállandó | a = 13,64 Å, b = 9,25 Å, c = 8,47 Å | ||
| Rácsállandó-szög | α = 90°, β = 100,28°, γ = 90° | ||
| Termokémia | |||
| Std. képződési entalpia ΔfH | 125,5 kJ·mol−1 | ||
| Standard moláris entrópia S | 224,9 J·mol−1·K−1 | ||
| Hőkapacitás, C | 229,7 J/(K·mol) | ||
| Veszélyek | |||
| Főbb veszélyek | irritáló | ||
| NFPA 704 | |||
| Lobbanáspont | nem gyúlékony | ||
| Ha másként nem jelöljük, az adatok az anyag standardállapotára (100 kPa) és 25 °C-os hőmérsékletre vonatkoznak. | |||
A pirént először kőszénkátrányból izolálták, ahol 2 tömegszázalékig fordul elő. Perikondenzált PAH-ként sokkal jobban rezonanciastabilizált az 5 tagú gyűrűs izomerjénél, a fluoranténnél. Így sok égés mellékterméke. Az autók átlagosan mintegy 1 μg-ot termelnek kilométerenként.[7]
Kromáttal való oxidációjakor perinaftenon, majd naftalin-1,4,5,8-tetrakarbonsav keletkezik. Számos hidrogénezésre képes, és eltérő szelektivitással hajlamos halogénezésre, Diels–Alder-reakciókra és nitrálásra.[7] Az egyik 3-as szénatomon brómozható.[8]
Nátriummal redukálva gyökaniont ad. Ebből sok π-arénkomplex állítható elő.[9]
Pirénből és származékaiból festékek és festékprekurzorok, például piranin és naftalin-1,4,5,8-tetrakarbonsav állíthatók elő. Erős UV-Vis-abszorpciója van három 330 nm-nél lévő sávnál diklórmetánban. Az emisszió az abszorpcióhoz közel van, de 375 nm-nél.[10] A jelek oldószerenként eltérnek. Származékaik is hasznos molekuláris indikátorok fluoreszcenciaspektroszkópiához, nagy kvantumhozamuk és hosszú életük (0,65, illetve 410 ns etanolban 293 K-en). A pirén volt az első molekula, melynél excimereket figyeltek meg.[11] Ez az excimer 450 nm-nél jelenik meg. Theodor Förster számolt be róla 1954-ben.[12]
A pirén fluoreszcencia-emissziós spektruma érzékeny az oldószer polaritására, így a pirén használható oldószerkörnyezetek meghatározására, mivel a gerjesztett állapota az alapállapottal szemben nem síkalkatú. Egyes emissziós sávok érintetlenek, mások intenzitása eltér az oldószerrel való kölcsönhatás ereje miatt.

A pirének erős elektrondonorok, és számos anyaggal együtt elektrondonor-akceptor rendszert alkotnak, melyek energiaátalakításra és fényfelhasználásra használhatók.[10]
Bár nem benzopiréneknél kevésbé mérgező, állatkísérletek szerint a pirén mérgező a vesékre és a májra. A pirén a halak és az algák életműködéseit befolyásolja.[14][15][16][17]
Biológiai bomlását nagymértékben vizsgálták. Ez két CH=CH kötés hidroxilezésével kezdődik.[18] Sertéskísérletek alapján az 1-hidroxipirén a szájon át adott pirén metabolitja.[19]
Seamless Wikipedia browsing. On steroids.
Every time you click a link to Wikipedia, Wiktionary or Wikiquote in your browser's search results, it will show the modern Wikiwand interface.
Wikiwand extension is a five stars, simple, with minimum permission required to keep your browsing private, safe and transparent.