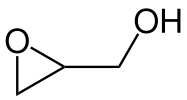
Epoxidok
From Wikipedia, the free encyclopedia
Az epoxidok háromtagú gyűrűs éterek. A molekula alakja közelítőleg egyenlő oldalú háromszög, ami jelentős gyűrűfeszültséget okoz, ezért az epoxidok erősen, más étereknél sokkal inkább reaktívak. Számos alkalmazásuk miatt nagy mennyiségben gyártják őket. A kisebb molekulatömegű epoxidok általában apoláris, színtelen, gyakran illékony vegyületek.[1]

Nevezéktanuk
Az epoxid funkciós csoportot tartalmazó vegyületeket lehet epoxi, epoxid, oxirán vagy etoxilin névvel nevezni. Az egyszerű epoxidokat gyakran oxidoknak nevezik. Az etilén (C2H4) epoxidját így etilén-oxidnak (C2H4O) nevezik. Számos vegyületnek hétköznapi neve van, az etilén-oxidot például „oxiránnak” hívják. Némelyik névben szerepel az epoxid funkciós csoportra utalás, ilyen például az 1,2-epoxiheptán, melyet más néven 1,2-heptén-oxidnak is neveznek.
Az epoxidból gyártott polimert epoxinak nevezik, de ezekben az anyagokban nincs epoxidcsoport (leszámítva a műgyanta gyártása közben esetleg el nem reagált néhány visszamaradó csoport).
Előállítása
Az iparilag legjelentősebb epoxidok az etilén- és propilén-oxid, ezekből évente mintegy 15, illetve 3 millió tonnát állítanak elő.[2]
Alkének heterogén katalitikus oxidációja
Az etilén oxigénnel történő epoxidálása az alább egyenlet szerint játszódik le:
- 7 H2C=CH2 + 6 O2 → 6 C2H4O + 2 CO2 + 2 H2O
Az alkének közvetlen oxigénnel történő reakciója csak ennek az epoxidnak az előállítására használható fel. A reakcióhoz többnyire módosított heterogén ezüst katalizátort használnak.[3] Más alkének, köztük a propilén sem reagál hasznosítható mértékben, bár TS-1 hordozós Au katalizátorok képesek a propilén szelektív epoxidálására.[4]
Olefinek oxidációja szerves peroxidokkal és fémkatalizátorokkal
Az etilén-oxid kivételével az epoxidokat alkének peroxidtartalmú reagensekkel történő kezelésével állítják elő, melyek egyetlen oxigénatomot adnak le. A szerves peroxidok hajlamosak a spontán bomlásra vagy akár öngyulladásra, ezért ezek a reakciók nagy elővigyázatosságot igényelnek.
A fémkomplexek hasznos katalizátorai a hidrogén-peroxiddal és alkil-hidroperoxidokkal történő epoxidálási reakcióknak. Az elektrofilebb peroxikarbonsavak fémkatalizátorok alkalmazása nélkül epoxiddá konvertálják az alkéneket. Speciális esetekben más peroxid tartalmú reagenseket, például dimetil-dioxiránt alkalmaznak. A reakciómechanizmus és a kiindulási alkén geometriájától függően cisz és/vagy transz epoxid diasztereomerek keletkezhetnek. Ha a kiindulási anyagban más sztereocentrumok is vannak, akkor ezek is befolyásolhatják az epoxidálás sztereokémiáját. A fémkatalizált epoxidálási reakciókat elsőként terc-butil-hidroperoxiddal (TBHP) vizsgálták.[5] A TBHP fémmel (M) történő kapcsolódása hozza létre az MOOR csoportot tartalmazó aktív peroxi komplexet, amely aztán az alkénre átvisz egy O centrumot.[6]
A propilén-oxid propilénből történő előállítására szerves peroxidokat használnak. A reakcióhoz katalizátor is szükséges. Oxigénforrásként t-butil-hidroperoxid és etillbenzol-hidroperoxid is szolgálhat.[7]
Olefinek peroxidálása peroxikarbonsavakkal
Jellemzően laboratóriumi célra a Prilezhaev-reakció használatos,[8][9] melynek során az alként peroxisavval, például m-CPBA-val oxidálják. Példaként álljon itt a sztirol-oxid előállítása sztirol perbenzoesavval történő epoxidálásával:[10]
A reakció az ún. „pillangó mechanizmus” szerint játszódik le.[11] A peroxid elektrofil és az alkén nukleofil között koncertikus reakció játszódik le (a lenti mechanizmusban a számok az egyszerűség kedvéért szerepelnek). A pillangó mechanizmus biztosítja az O−O szigma csillag pálya ideális pozícióját a C−C π-elektronok támadásához.[12] <--Because two bonds are broken and formed to the epoxide oxygen, this is formally an example of a coarctate transition state.-->
A katalitikus enantioszelektív opixidáláshoz, mint amilyen a Sharpless-epoxidálás és a Jacobsen-epoxidálás epoxidation, hidroperoxidokat is használnak. A Shi-epoxidálással együtt ezek a reakciók hasznosak királis epoxidok enantioszelektív szintéziséhez. Oxaziridin reagensek is felhasználhatók epoxidok alkénekből történő készítéséhez.
Homogén katalitikus aszimmetrikus epoxidálás
Királis epoxidokból gyakran lehet enantioszelektíven nyerni prokirális alkénekből. Sok fémkomplex aktív katalizátora e reakcióknak, de a legfontosabbak a titán, vanádium és molibdén komplexei.[13][14]
A Sharpless-epoxidálás az egyik legfőbb enantioszelektív kémiai reakció. Felhasználásával primer és szekunder allil-alkoholokból állítanak elő 2,3-epoxialkoholokat.[15][16]

Intramolekuláris SN2 szubsztitúció
Ebben az eljárásban dehidrohalogénezés történik. Maga a módszer a Williamson-féle éterszintézis egyik változata, melynek során egy alkoxidion intramolekulárisan lép egy klór helyébe. A kiindulási anyagokat halohidrinnek nevezzük.[18] A világ propilén-oxid termelésének nagy részét ezzel az eljárással állítják elő, propilén-klórhidrinből kiindulva.
Az intramolekuláris epoxid képződés a Darzens-reakció egyik kulcslépése.
A Johnson–Corey–Csajkovszkij-reakció során karbonilcsoportból és szulfónium ilidből képződik epoxid. Ebben a reakcióban klorid helyett szulfónium a távozó csoport.
Nukleofil epoxidálás
Elektronban szegény olefineket, például enonokat és akrilszármazékokat nukleofil oxigénvegyületekkel, például peroxidokkal lehet epoxidálni. A reakció mechanizmusa két lépéses. Első lépésben az oxigén nukleofil konjugált addícióval stabilizált karbaniont alakít ki, majd ez a karbanion ugyanezt az oxigénatomot megtámadva kiszorítja arról a távozó csoportot, ezzel bezárva az epoxidgyűrűt.
Bioszintézis
A természetben az epoxidok ritkán fordulnak elő. Keletkezési módjuk többnyire az alkénekre citokróm P450 hatására bekövetkező oxigéntranszfer.[19] (De lásd még a rövid életű, jelátvivő molekula szerepet betöltő epoxieikozatriénsavakat[20] és a hasonló epoxidokozapentaénsavakat és epoxieikozatetraénsavakat is.)
Reakcióik
Az epoxidok reakciókészségét a gyűrűnyitási reakciók uralják – az epoxidok erős elektrofilek. Ebben a reakcióban alkoholok, víz, aminok, tiolok és számos más reagens is lehet a nukleofil. Ez a reakció az alapja az epoxi ragasztóknak és a glikolok gyártásának. Savas körülmény között a nukleofil támadásának helyét mind a sztérikus hatások (mint normálisan az SN2 reakcióknál), mind a karbokation stabilitása (mint normálisan az SN1 reakcióknál) befolyásolja. Az epoxidok savkatalizált hidrolízise glikol terméket eredményez. A hidrolízis során a vízmolekula nukleofil addícióval lép be az epoxidba. Bázikus körülmények között – összhangban az SN2 folyamat normál menetével – a nukleofil a legkevésbé szubsztituált szénatomon támad. Tiokarbamiddal reagáltatva az epoxidokból szulfidok keletkeznek, ezek neve tiirán.
Az epoxidok polimerizációja poliétert eredményez, például etilén-oxidból polietilén-glikol, más néven polietilén-oxid keletkezik.
Az epoxidok gyűrű bővülési reakciói is ismertek, ilyen például a szén-dioxid beékelődése, melynek révén gyűrűs karbonátok keletkeznek.
Egyéb reakciók
- Az epoxidok lítium-alumínium-hidriddel vagy alumínium-hidriddel történő redukciója a megfelelő alkoholt eredményezi.[21] A redukció a hidridion (H−) nukleofil addíciójának következménye.
- Az epoxidok reduktív hasítása β-lítioalkoxidokat ad.[22]
- Volfrám-hexakloriddal és n-butillítiummal redukálva a megfelelő alkén keletkezik:[23]
Felhasználásuk
Példák epoxidokra
Az etilén-oxidot széles körben használják detergensek és felületaktív anyagok – etoxilálással történő – gyártására. Hidrolízisével etilénglikol nyerhető.
Az epoxidok és aminok közötti reakció az alapja az epoxi ragasztók és szerkezeti anyagok előállításának. Gyakran használt amin térhálósító a trietilén-tetramin (TETA).
Hivatkozások
Fordítás
Wikiwand - on
Seamless Wikipedia browsing. On steroids.