Un solvant est une substance, liquide ou supercritique à sa température d'utilisation, qui a la propriété de dissoudre, de diluer ou d'extraire d’autres substances sans les modifier chimiquement et sans lui-même se modifier. Les solvants sont utilisés dans des secteurs très diversifiés tels que le dégraissage, les peintures, les encres, la détergence, la synthèse organique, et représentent des quantités considérables en ce qui concerne le tonnage et le chiffre d'affaires.
En Suisse romande et en Belgique, on utilise le terme anglais thinner pour les solvants organiques destinés à la dilution des peintures.
L'eau est le solvant le plus courant, la solution étant alors qualifiée de solution aqueuse.
Généralités
Le terme « solvant organique » se réfère aux solvants qui sont des composés organiques qui contiennent des atomes de carbone. Habituellement, les solvants ont un point de fusion faible et s'évaporent facilement. Les solvants permettent de dissoudre les réactifs et d'amener les réactifs en contact. Ils ne réagissent pas chimiquement avec le composé dissous : ils sont inertes. Les solvants peuvent aussi être utilisés pour extraire les composés solubles d'un mélange, l'exemple le plus commun étant l'infusion de thé dans de l'eau chaude. Les solvants sont souvent des liquides transparents avec une odeur caractéristique. La concentration d'une solution est la quantité de soluté dans un certain volume de solvant.
Pour les solutions liquides (phase uniforme liquide contenant plusieurs espèces chimiques), si l'une des espèces est très largement majoritaire (au moins un facteur 100), on l'appelle le « solvant ». C'est le cas de l'eau pour les solutions aqueuses (par exemple une solution aqueuse de sulfate de cuivre : l'eau est le solvant et les ions sulfate et cuivre(II) les solutés).
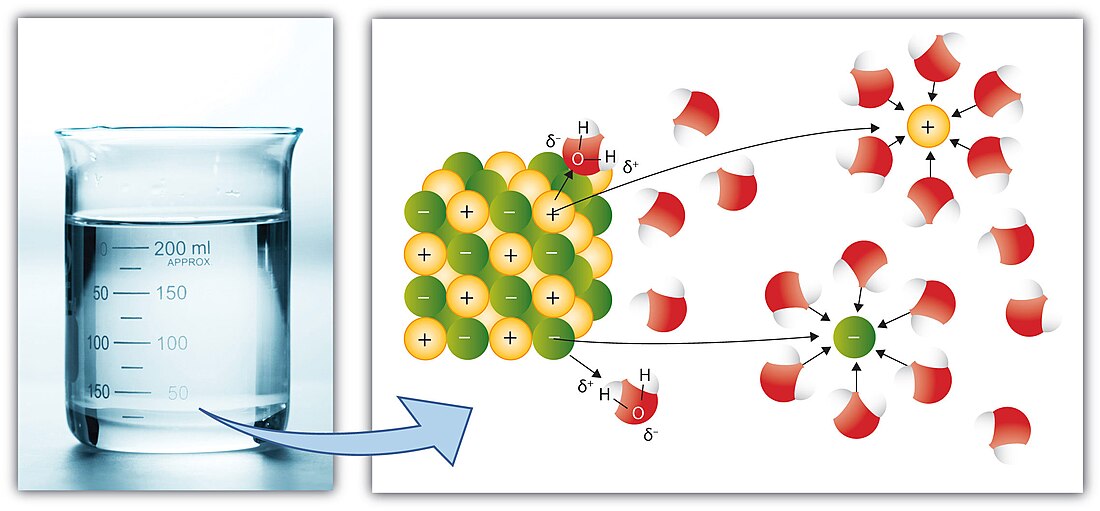
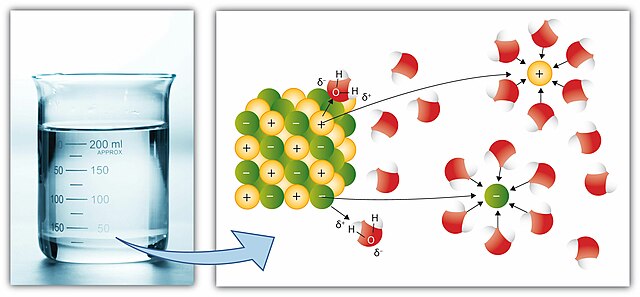
En règle générale, les atomes ou molécules de même nature s'assemblent pour former un liquide ou un solide (un cristal ou un solide amorphe). Dans le cas d'une solution, le solvant empêche les atomes ou molécules de s'assembler, il les disperse. Dans le cas de l'eau, cela se produit selon deux phénomènes :
- une diminution des interactions électriques (forces de van der Waals) : l'eau a une permittivité électrique d'environ 80, ce qui signifie qu'elle divise les forces de Coulomb par 80 ;
- une solvatation (pour l'eau une hydratation) : si les molécules du solvant sont polaires, elles peuvent entourer les espèces dissoutes et former un « bouclier ».
Classification
Il existe de nombreuses classifications des solvants : en fonction de la nature chimique du composé, de sa polarité, de ses propriétés physico-chimiques[1], de son secteur d'utilisation, de sa toxicité, de son origine (pétrolière ou agrosourcée), etc.
Selon leur polarité
- Les solvants polaires :
- Les solvants protiques polaires (appelés aussi solvants protogènes) possèdent un ou plusieurs atomes d'hydrogène susceptibles de former des liaisons hydrogène. Exemples : eau, méthanol, éthanol.
- Les solvants polaires aprotiques possèdent un moment dipolaire non nul et sont dénués d'atomes d'hydrogène susceptibles de former des liaisons hydrogène. Exemples : acétonitrile (CH3CN), diméthylsulfoxyde (DMSO, (CH3)2SO), tétrahydrofurane (THF, C4H8O).
- Les solvants apolaires aprotiques possèdent un moment dipolaire permanent nul. Par exemple, les hydrocarbures : benzène, alcanes linéaires, ramifiés ou cycliques, alcènes.
Le tableau suivant compare ces différentes familles[2] :
| Solvants | Constante diélectrique | Moment dipolaire | Atomes d'hydrogène | Liaisons hydrogène | Pouvoir ionisant | Pouvoir de solvatation | Effet sur les réactions organiques |
|---|---|---|---|---|---|---|---|
| Aprotiques apolaires | Faible | Faible | Tous sont liés à des atomes de carbone | Non | Faible | Faible | |
| Aprotiques polaires | Élevée | Élevée | Tous sont liés à des atomes de carbone | Accepteur uniquement | Solvatent très bien les cations et peu les anions | Favorisent les mécanismes SN2 par rapport au SN1 et favorisent la substitution par rapport à l’élimination | |
| Protiques polaires | Élevée | Élevée | Au moins un est lié à un hétéroatome | Accepteur et donneur | Élevé | Élevé | Favorisent les mécanismes SN1 par rapport au SN2 |
Selon leur nature chimique
Les solvants inorganiques ne contiennent pas d'atomes de carbone. L'eau, les solutions aqueuses contenant des additifs (tensioactifs, solution tampon...), l'acide sulfurique concentré, l'ammoniaque sont des solvants inorganiques classiques.
Les solvants organiques contiennent des atomes de carbone. Ils sont classés en trois familles :
- solvants hydrocarbonés :
- aliphatiques : alcanes, alcènes,
- aromatiques : benzène, toluène, xylène ;
- solvants oxygénés :
- solvants halogénés : hydrocarbures halogénés (fluorés, chlorés, bromés ou iodés) : perchloroéthylène, trichloréthylène, dichlorométhane, chloroforme, tétrachlorométhane.
Selon leur charge
Espèces non ioniques : la majorité des solvants actuels sont des espèces non ioniques.
Espèces ioniques : tandis que la plupart des solvants sont de nature moléculaire (formés d'une seule espèce neutre), il existe une nouvelle classe de solvants, appelés liquides ioniques, constitués d'anions et de cations. Les liquides ioniques sont des sels fondus possédant un point de fusion inférieur à 100 °C et une tension de vapeur quasiment nulle (ils sont non-volatils). Ils constituent une alternative de plus en plus sérieuse aux solvants moléculaires classiques et sont désormais très utilisés en électrochimie. De nombreuses recherches actuelles s'intéressent à leur utilisation pour la séparation des métaux radioactifs et pourraient aboutir à des solutions particulièrement écologiques pour le retraitement des déchets radioactifs.
Selon leur origine
Il est important de préciser que l'origine du solvant n'a pas de conséquence sur sa toxicité ; un solvant agrosourcé peut être néfaste pour l'homme ou l'environnement (cas du furfural).
Les solvants pétrochimiques proviennent du pétrole et donc de la pétrochimie. La plupart des solvants actuellement utilisés sont d'origine pétrochimique (hexane, benzène, acétate d'éthyle, dichlorométhane).
Les solvants agrosourcés (appelés aussi biosolvants) proviennent de la valorisation de la biomasse végétale (bois, sucre, huiles végétales, huiles essentielles). Les exemples les plus connus sont les alcools (méthanol, éthanol, etc.), le furfural, le glycérol ou encore des esters comme le lactate d'éthyle.
Propriétés physiques de solvants communs
Les solvants les plus couramment utilisés peuvent être caractérisés par les propriétés physiques suivantes : point de fusion, point d'ébullition, pression de vapeur saturante, solubilité dans l'eau, miscibilité avec d'autres solvants, constante diélectrique, densité, viscosité, pouvoir solvant (indice kauri-butanol et point d'aniline), paramètres de solubilité d'Hansen (en).
Les solvants ci-dessous sont groupés en solvants apolaires, polaires aprotiques et polaires protiques, classés par polarité croissante.
| Solvant | Formule chimique | Point d'ébullition[3] |
Constante diélectrique[4] |
Masse volumique (g/ml) |
Moment dipolaire (D) |
|---|---|---|---|---|---|
| Solvants apolaires | |||||
| Pentane | CH3-CH2-CH2-CH2-CH3 | 36 °C | 1,84 | 0,626 | 0,00 |
| Cyclopentane | C5H10 | 40 °C | 1,97 | 0,751 | 0,00 |
| Hexane | CH3-CH2-CH2-CH2-CH2-CH3 | 69 °C | 1,88 | 0,655 | 0,00 |
| Cyclohexane | C6H12 | 80,75 °C | 2,02 | 0,7786 | 0,00 |
| Benzène | C6H6 | 80 °C | 2,3 | 0,879 | 0,00 |
| Toluène | C6H5-CH3 | 111 °C | 2,4 | 0,867 | 0,36 |
| 1,4-Dioxane | /-CH2-CH2-O-CH2-CH2-O-\ | 101 °C | 2,3 | 1,033 | 0,45 |
| Chloroforme | CHCl3 | 61 °C | 4,8 | 1,48 | 1,04 |
| Éther diéthylique | CH3CH2-O-CH2-CH3 | 35 °C | 4,3 | 0,713 | 1,15 |
| Solvants polaires aprotiques | |||||
| Dichlorométhane (DCM) | CH2Cl2 | 40 °C | 9,1 | 1,326 | 1,60 |
| Tétrahydrofurane (THF) | /-CH2-CH2-O-CH2-CH2-\ | 66 °C | 7,5 | 0,886 | 1,75 |
| Acétate d'éthyle | CH3-C(=O)-O-CH2-CH3 | 77 °C | 6,0 | 0,894 | 1,78 |
| Acétone | CH3-C(=O)-CH3 | 56 °C | 21 | 0,786 | 2,88 |
| N,N-Diméthylformamide (DMF) | H-C(=O)N(CH3)2 | 153 °C | 38 | 0,944 | 3,82 |
| Acétonitrile (MeCN) | CH3-C≡N | 82 °C | 37 | 0,786 | 3,92 |
| Diméthylsulfoxyde (DMSO) | CH3-S(=O)-CH3 | 189 °C | 47 | 1,092 | 3,96 |
| Carbonate de propylène | C4H6O3 | 240 °C | 64,0 | 1,205 | 4,9 |
| Solvants polaires protiques | |||||
| Acide formique | H-C(=O)OH | 101 °C | 58 | 1,21 | 1,41 |
| Butan-1-ol | CH3-CH2-CH2-CH2-OH | 118 °C | 18 | 0,810 | 1,63 |
| Isopropanol (IPA) | CH3-CH(-OH)-CH3 | 82 °C | 18 | 0,785 | 1,66 |
| Propan-1-ol | CH3-CH2-CH2-OH | 97 °C | 20 | 0,803 | 1,68 |
| Éthanol | CH3-CH2-OH | 79 °C | 24 | 0,789 | 1,69 |
| Méthanol | CH3-OH | 65 °C | 33 | 0,791 | 1,70 |
| Acide acétique | CH3-C(=O)OH | 118 °C | 6,2 | 1,049 | 1,74 |
| Eau | H-O-H | 100 °C | 80 | 1,000 | 1,85 |
Dissolution
Dissolution acide
La dissolution peut se faire par réaction chimique entre des espèces du solvant (en général des ions) et le solide. Le cas le plus fréquent est celui de la dissolution par un acide : les protons H+ (ou dans l'eau, les ions oxonium H3O+) provoquent une oxydation du solide 2M + 2H+ → 2M+ + H2 (l'atome de solide M cède un électron à l'ion H+ qui peut alors former une molécule de dihydrogène), l'ion M+ étant alors soluble dans le solvant.
Dissolution dans un verre
À haute température (au-delà de 2 000 °C), le verre (dioxyde de silicium SiO2) est liquide. On peut donc y dissoudre un certain nombre de produits qui sont, eux, solides à cette température.
On peut aussi dissoudre les solides dans d'autres types de verre, par exemple le métaborate de lithium ou le tétraborate de lithium, utilisés pour diluer les matériaux à analyser en spectrométrie de fluorescence X (technique de préparation dite de la « perle fondue »).
Bien qu'ayant lieu à haute température et avec un solvant différent, le principe est similaire à la dissolution dans l'eau (dispersion solvatation, dissolution acide).
Solvants alternatifs
Plusieurs raisons (telles que la raréfaction des ressources pétrolières, la réglementation de plus en plus stricte sur l'utilisation de composés volatils, toxiques ou reprotoxiques) incitent les industriels et académiques à se tourner vers de nouveaux solvants alternatifs, souvent appelés « solvants verts »[5]. Il n'existe pas de définition officielle d'un solvant vert mais plusieurs définitions peuvent être mentionnées : l'adjectif « vert » peut faire référence aux 12 principes de la chimie verte[6] dans le cas où le solvant rempli un ou plusieurs de ces principes (synthèse avec économie d'atomes, issu de matières premières renouvelables...). Cependant, le terme « solvant vert » peut être employé dans différents cas, comme dans le cas où le solvant n'est pas toxique, ou bien qu'il est biodégradable ou encore qu'il provient de ressources renouvelables. Ainsi, le terme « vert » peut correspondre à différentes définitions. C'est pourquoi différentes familles de solvants sont qualifiées de « solvants verts » : les solvants agrosourcés[7], les liquides ioniques, les fluides supercritiques, les polymères liquides.
Les solvants agrosourcés sont, comme leur nom l'indique, issus d'agro-synthons (petites molécules d'origine renouvelable pouvant être obtenues à partir de cellulose, d'hémicellulose, de lignine, d'huile végétale, etc.) Le glycérol et le lactate d'éthyle sont deux exemples représentatifs de cette famille de solvants. Leur origine non pétrolière les classe parmi les solvants verts.
Les liquides ioniques sont classés parmi les solvants verts du fait de leur non volatilité. Cependant, de nombreux doutes subsistent sur la toxicité de ces composés. Les liquides ioniques les plus étudiés sont les dérivés imidazolium, mais leur toxicité prouvée tend les académiques à se tourner vers des structures moins toxiques pouvant même parfois être issues de ressources renouvelables. C'est par exemple le cas de l'acétate de choline.
Les fluides supercritiques sont classés parmi les solvants verts car ils sont inertes. L'exemple le plus utilisé est le CO2 supercritique. L'inconvénient de cet exemple est lié aux risques que présentent les installations industrielles mettant en œuvre des fluides supercritiques (sous pression).
Les polymères liquides sont aussi cités parmi les solvants verts du fait de leur non volatilité et, pour certains, de leur biocompatibilité. Les polyéthylène glycols, notés PEG, font partie de cette famille.
Utilisations
Les solvants servent comme :
- milieux réactionnels ;
- en synthèse organique, les solvants classiques sont, entre autres, l'acétone, l'éther de pétrole, le cyclohexane, le dioxane, le dichlorométhane ;
- agents d'extraction et de séparation analytique ou préparative ;
- diluants, par exemple en peinture ;
- agents de nettoyage ;
- dégraissants, par exemple le perchloroéthylène qui est utilisé pour le nettoyage à sec. Voir aussi Bain à ultrasons ;
- support pour le conditionnement, le transport et la mise en œuvre de cosmétiques, peintures et encres.
- fabrication du vernis à ongles
Toxicité
De nombreux solvants présentent des risques pour la santé, ce qui est d'autant plus inquiétant qu'en 2003, 14,7 % de la population salariée était exposée à des solvants (contre 12,3 % en 1994 ; études INRS) ; il n'est pas nécessaire de travailler dans une usine chimique pour être en contact avec des solvants toxiques, les professionnels de la peinture, de la plasturgie, de l'imprimerie, du nettoyage, du funéraire, de la blanchisserie, etc. subissent aussi leurs effets néfastes.
Plusieurs types d'éthers de glycol ont été ainsi mis en cause dans des cas de cancers graves ; neuf ont été classés reprotoxiques (dangereux pour les fœtus des femmes enceintes).
Enfin, de nombreux composés chimiques ont fait l'objet d'études faibles avant leur mise sur le marché et les risques réels qu'ils nous font courir sont mal connus. D'où l'importance du projet européen REACH qui pourrait obliger les industriels à mieux tester leurs produits, et l'importance du travail des comités d'hygiène (CHSCT en France) sur ces questions dans le cadre de l'entreprise. L'air des habitations peut aussi receler de nombreux solvants (issus des colles, peintures et vernis, mais aussi des produits d'entretien), d'où la recommandation d'aérer chaque pièce au moins 10 minutes chaque jour.
Notes et références
Voir aussi
Wikiwand in your browser!
Seamless Wikipedia browsing. On steroids.
Every time you click a link to Wikipedia, Wiktionary or Wikiquote in your browser's search results, it will show the modern Wikiwand interface.
Wikiwand extension is a five stars, simple, with minimum permission required to keep your browsing private, safe and transparent.