هورمون شادی From Wikipedia, the free encyclopedia
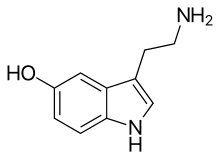
سروتونین (به انگلیسی: Serotonin) یا هیدروکسیتریپتامین نوعی انتقالدهندههای عصبی از نوع مونوآمینه اسید بیوژنیک است. به لحاظ زیستشیمی از مشتقات تریپتوفان میباشد. سروتونین بهطور اهم در دستگاه گوارش، پلاکتها و سیستم عصبی مرکزی حیوانات و همینطور انسان یافت شدهاست. این ماده نزد افکار عمومی بهعنوان جاریکنندهٔ «احساس خوب» شناخته شدهاست.
 | |
| دادههای بالینی | |
|---|---|
| نامهای دیگر | 5-HT, 5-Hydroxytryptamine, Enteramine, Thrombocytin, ۳-(β-Aminoethyl)-5-hydroxyindole, Thrombotonin |
| دادههای فیزیولوژیک | |
| بافتهای منبع | هسته رافه، enterochromaffin cells |
| بافتهای هدف | system-wide |
| گیرندهها | 5-HT1, 5-HT2, 5-HT3, 5-HT4, 5-HT5, 5-HT6, 5-HT7 |
| آگونیستها | Indirectly: بازدارندههای بازجذب سروتونینs, بازدارندههای مونوآمین اکسیدازs |
| پیشماده | ۵-هیدروکسی تریپتوفان |
| بیوسنتز | Aromatic L-amino acid decarboxylase |
| متابولیسم | مونوآمین اکسیداز |
| شناسهها | |
| |
| شمارهٔ سیایاس | |
| پابکم CID | |
| IUPHAR/BPS | |
| کماسپایدر | |
| KEGG | |
| لیگاند بانک داده پروتئین | |
| CompTox Dashboard (EPA) | |
| ECHA InfoCard | 100.000.054 |
| سروتونین | |
|---|---|
 | |
 | |
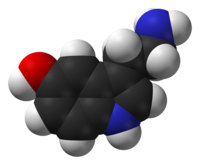 | |
5-Hydroxytryptamine or | |
دیگر نامها 5-Hydroxytryptamine 5-HT Enteramine; Thrombocytin 3-(β-Aminoethyl)-5-hydroxyindole Thrombotonin | |
| شناساگرها | |
| شماره ثبت سیایاس | ۵۰-۶۷-۹ |
| پابکم | ۵۲۰۲ |
| کماسپایدر | ۵۰۱۳ |
| UNII | 333DO1RDJY |
| KEGG | C00780 |
| MeSH | Serotonin |
| ChEBI | CHEBI:28790 |
| ChEMBL | CHEMBL۳۹ |
| IUPHAR ligand | 5 |
| جیمول-تصاویر سه بعدی | Image 1 |
| |
| |
| خصوصیات | |
| فرمول مولکولی | C10H12N2O |
| جرم مولی | 176.215 g/mol |
| شکل ظاهری | White powder |
| دمای ذوب | ۱۲۱–۱۲۲°C (ligroin)[1] |
| دمای جوش | ۴۱۶ ±۳۰٫۰°C (at 760 Torr)[2] |
| انحلالپذیری در آب | slightly soluble |
| گشتاور دوقطبی | 2.98 D |
| خطرات | |
| MSDS | External MSDS |
| LD50 | 750 mg/kg (subcutaneous, rat),[3] 4500 mg/kg (intraperitoneal, rat),[4] 60 mg/kg (oral, rat) |
| به استثنای جایی که اشاره شدهاست در غیر این صورت، دادهها برای مواد به وضعیت استانداردشان داده شدهاند (در 25 °C (۷۷ °F)، ۱۰۰ kPa) | |
| | |
| Infobox references | |
|
| |
تقریباً ۹۰٪ از سروتونین موجود در بدن انسان، در سلولهای انتروکرومافین که بهصورت پراکنده در غشای دستگاه گوارش موجود اند متمرکز است. و در آنجا موجب تنظیم تحرکات روده میگردد. مقادیر کمتری از سروتونین، با شبکهٔ عصبی سروتونرژیک سیستم اعصاب مرکزی سنتز شده، و کارکردهای گوناگونی مییابد، این کارکردها شامل: تنظیم در حالات روانی، اشتها و خواب میگردد. سروتونین همچنین دارای عملکردهای شناختی، مانند تأثیرات بر حافظه و یادگیری نیز میباشد. مدولاسیون سروتونین در سیناپسها بهعنوان عملکرد اصلی برای چندین کلاس مختلف از، داروهای ضدافسردگی شناخته شدهاست.
سروتونین ترشحشده از، سلولهای انتروکرومافین دستگاه گوارش درنهایت به یاختههای خونی راه پیدا کرده، و در آنجا فعالانه توسط پلاکتها، حمل شده و جاسازی میگردد. آنها سروتونین را در هنگام لخته شدن آزاد میکنند، که با ایجاد انقباض در عملیات هموستازی (خون ایستی)، و انعقاد خون نقشآفرینی کند. سروتونین همچنین، بهعنوان بهبود دهنده آسیبها، بهعنوان یکی از فاکتورهای رشد در برخی از سلولها شناسایی شدهاست.
سوختوساز سروتونین بهطور عمده توسط کبد صورت میپذیرد. این سوختوساز در ابتدا با اکسایش توسط مونوآمین اکسیداز monoamine axidaze با آلدهید میانجامد، سپس 5-HIAA از اکسایش دهیدروژناز آلدهید (Aldehyde dehydrogenases) با 5-HIAA ایندول استیک اسید منشعب میشود، که توسط کلیهها قابل دفع است. نوعی از تومور با نام کارسینوید در اثر عدم توازن ممکن است، مقادیر انبوهی سروتونین در بدن ترشح کند، که به این حالت سندرم کارسینوید گفته میشود. و باعث بروز عوارضی مانند: برافروختگی، اسهال و مشکلات قلبی میشود که به دلیل تأثیر سروتونین، بر ماهیچه قلب (میوکارد) شخص مبتلا دچار ضربان بیشتر از حد عضله میوکارد شده، و ممکن است دریچه سهلختی (تریکاسپید) قلبش دچار آسیب شود.
همینطور که سروتونین در حیوانات نیز دارای کارکردهایی است، سروتونین، در قارچها و گیاهان نیز یافت شده است. سروتونین، در نیش حشرات و خارهای گیاهان به عنوان عامل ایجادکننده درد حضور دارد، به همان شکل که درد از عوارض تزریق مستقیم سروتونین نیز میباشد. سروتونین، توسط آمیبهای تک سلولی بیماریزا نیز تولید میشود که در رودهها باعث بروز اسهال میشود. موارد بیشماری از حضور سروتونین در دانهها و میوهها مشاهده شده، که در دستگاه گوارش کمک به دفع دانه از دستگاه گوارش کند.
سروتونین، انتقال دهنده عصبیای است، که در تمام جانداران شاخه دوسوئیان (Bilateria) یافت میشود، که در آنان عملکردی به عنوان، واسط برای تحرکات روده، و همینطور عامل ادراک موجودات نسبت به موجودیت منابع زیستی میباشد. در موجوداتی با ساختار زیستی سادهتر همچون، بی مهرگان، منابع معنی سادهتری فقط به معنای موجود بودن غذا دارد. در موجوداتی پیشرفتهتر به مانند: بندپایان و مهرهداران، تعریف منابع میتواند شامل مفاهیم گستردهتری مانند، برتریهای اجتماعی نیز باشد. در پاسخ به ادراک جاندار نسبت به کمبود، یا فراوانی منابع رشد، تولید مثل یا روحیه او میتواند ارتقا یا تنزل بیابد. این شاید آن چیزی باشد که تعیینکننده این است که، چه میزانی از سروتونین میبایستی دفع یا جذب شود.
گیرندههای 5HT، گیرندههای سروتونین در غشای سلولی سلولهای عصبی، و انواع دیگر سلول در جانداراناند، و به عنوان، یک کانال یونی دریچه-لیگاندی درونزاد، برای تأثیرات سروتونین و طیف گستردهای از داروها و روانگردانهای توهمزا، واسطهگری میکنند. به استثنای گیرندهٔ 5HT3 که دروازه لیگاندی کانال یونی است، همه گیرندههای 5HT از شاخه گیرندههای «هفت مارپیچ غشاءگذر (Heptahelical Receptors)» هستند، که سیستم پیامرسانی ثانویه درون سلولی را فعال میکند.
| گیرنده | Ki nM | عملکرد گیرنده |
|---|---|---|
| 5-HT1 receptor family signals via Gi/o inhibition of adenylyl cyclase. | ||
| 5-HT1A | ۳٫۱۷ | حافظه (آگونیستها↓); یادگیری (آگونیستها↓); اضطراب (آگونیستها↓); افسردگی (آگونیستها↓); نشانههای مثبت، منفی و شناختی بیماری شیزوفرنی (تعدادی از آگونیستها↓); بیحسی نسبت به درد (آگونیستها↑); پرخاشگری (آگونیستها↓); آزادسازی دوپامین در پوسته لوب پیشانی مغز (آگونیستها↑); آزادسازی سروتنین و سنتز آن (آگونیستها↓) |
| 5-HT1B | ۴٫۳۲ | انقباض عروق (آگونیستها↑); پرخاشگری (آگونیستها↓); توده استخوانی (↓). Serotonin autoreceptor. |
| 5-HT1D | ۵٫۰۳ | انقباض عروق (آگونیستها↑) |
| 5-HT1E | ۷٫۵۳ | |
| 5-HT1F | ۱۰ | |
| 5-HT2 receptor family signals via Gs activation of phospholipase C. | ||
| 5-HT2A | ۱۱/۵۵ | Psychedelia (آگونیستها↑; آنتاگونیستها↑); افسردگی (آگونیستها& آنتاگونیستها↓); اضطراب (آنتاگونیستها↓); نشانگان مثبت و منفی شیزوفرنی (آنتاگونیستها↓); آزادسازی نوراپینفرین از هستهٔ لوکوس سرلیوس (آنتاگونیستها↑); آزادسازی گلوتامات از قشر مغز در لوب پیشانی |
| 5-HT2B | ۸٫۷۱ | عملکرد قلبی عروقی (اثر آگونیستها بر افزایش خطر پرفشاری ریوی) |
| 5-HT2C | ۵٫۰۲ | آزادسازی دوپامین در مسیرهای دوپامینرژیک (آگونیست↓); آزادسازی استیل کولین در قشر لوب پیشانی مغز (آگونیستها↑); اشتها (آگونیستها↓); تأثیرات ضد جنون (آگونیستها↑); تأثیرات ضدافسردگی (آگونیستها& آنتاگونیستها↑) |
| Other 5-HT receptors | ||
| 5-HT3 | ? | تهوع و استفراغ (آگونیستها↑); اضطراب (آنتاگونیستها↑) |
| 5-HT4 | ۱۲۵/۸۹ | حرکت دادن غذا در دستگاه گوارش (آگونیستها↑); حافظه و یادگیری (آگونیستها↑); تأثیرات ضدافسردگی (آگونیستها↑). سیگنالینگ از طریق Gαq با فعال کردن آدنیلات سیکلاز. |
| 5-HT5A | ۲۵۱/۲ | اندوزش خاطرات.<سیگنالینگ Gi/o با محدود کردن آدنیلات سیکلاز |
| 5-HT7 | ۹۸/۴۱ | شناخت (آنتاگونیستها↑); تأثیرات ضدافسردگی (آگونیستها و آنتاگونیستها↑). Gs با سیگنالینگ به وسیله آدنیلات سیکلاز عمل میکند. |
| 5-HT7 | ۸٫۱۱ | شناخت (آنتاگونیستها↑); تأثیرات ضدافسردگی (آنتاگونیستها↑). Gs با سیگنالینگ به وسیله آدنیلات سیکلاز عمل میکند. |
عملکرد سروتونین، به عنوان یک انتقال دهنده عصبی به همان نسبتی که ساده به نظر میرسد، پیچیده است. به عنوان مثال، در نوعی کرم لولهای با نام «سی. الگانس» که از باکتریها تغذیه میکند، سروتونین در پاسخ به یک اتفاق مثبت، مثلاً یافت شدن منبع غذایی جدید، یا در جنس نر به دلیل یافت جنس ماده آماده جفتگیری آزاد میشود. زمانی که یک کرم سیر حضور باکتریها را از طریق حواس پوسته خود احساس کند، دوپامین آزاد شده موجب آرام شدن او میشود، ولی در صورت گرسنه بودنش، سروتونین نیز آزاد میشود، که این نیز خود موجب بیشتر آرام شدنش میشود، و به این ترتیب این مکانیسم، باعث بیشتر شدن مدت زمان حضور جاندار در محیط حاوی غذا میشود. در این زمان عین حال سروتونین باعث تحرک بیشتر ماهیچه های مربوط به غذا خوردن میشود، در حالی که، اکتاپامین درست برعکس تأثیر سرکوبکننده بر آنها خواهد داشت. سروتونین بر سلولهای حساس به سروتونین منتشر شده، که کارشان کنترل ادراک جاندار از میزان وفور منابع غذایی اطراف است. وقتی بوی غذا به مشام انسان میرسد، دوپامین آزاد میشود، تا به افزایش اشتها بینجامد. اما برخلاف کرمها، سروتونین باعث تشدید رفتارهای پیشینیانه در گونهٔ انسان نمیشود، در ازای آن، سروتونین آزاد میشود. درحالی که مصرف سروتونین، باعث فعال شدن گیرندههای 5-HT2C بر سلولهای تولیدکننده دوپامین میشود. این عمل، موجب توقف آزاد شدن دوپامین توسط آنها میشود، و به این ترتیب سروتونین اشتها را کم میکند. به این ترتیب، داروهایی که باعث مسدود شدن گیرندههای 5-HT2C میگردند، مخصوصاً در اشخاصی که دارای تعداد کمی از گیرندهها باشند. وضعیتهای گیرندههای 5-HT2C در هیپوکامپوس از ساعت زیستی بدن تبعیت میکند، درست با آزاد شدن سروتونین در هستههای ونترومدیال (ventromedial nucleus) در هیپوتالاموس، که برنامهریزی شده تا بیشترین سطح ترشح را در صبحگاه داشته باشد، درست زمانی که انگیزه برای خوردن در بالاترین سطح ممکن است. سروتونین در سیری نقش دارد.[5] آگونیستهای سروتونین، مصرفِ غذای موشها را کم میکنند. سیرکنندگی سروتونین سه خصوصیت مهم دارد:[6]
در انسانها، اگونیستهای سروتونین (برای مثال، فنفلورامین، دکسفنفلورامین، فلوکستین)، گرسنگی، خوردن و وزن را کم میکنند.[7]
از سروتونین در درمانِ چاقی نیز استفاده میشود.[8] سروتونین، در دستگاه گوارش از سلولهای انتروکرومافین در پاسخ به ورود غذا آزاد میشود. افزایش ترشح سروتونین موجب تهوع و اسهال میشود.
در انسان سطح سروتونین تحت تأثیر رژیم غذایی است. هر افزایشی در نسبت تریپتوفان بر فنیلآلانین و لوسین سطح سروتونین را افزایش خواهد داد. میوههایی با این نسبت بالا شامل خرما، اسفناج و موز میباشند. مطالعات همینطور نشان میدهند که، رژیمهایی غنی از کربوهیدرات که حاوی مقادیر کمتری پروتئین باشند، موجب افزایش ترشح انسولین میشود، که خود با کمک در رقابت آمینو اسیدی باعث بالاتر رفتن سطح سروتونین میشود. اما، ترشح انسولین به میزان زیاد و در مدت طولانی ممکن است، باعث فعال شدن مقاومت انسولینی، چاقی مفرط یا دیابت نوع دوم شود که بالطبع کاهش سطح سروتونین در پی خواهد داشت. ماهیچهها، دوازده گونه از سیزده گروه آمینو اسید را استفاده میکنند (غیر از تریپتوفان)، که این به اشخاص با بدنهایی عضلانی اجازه تولید مقادیر بیشتری سروتونین را میدهد.
سلولهای انتروکرومافین در تمامی سطح رودهها گسترده شدهاند، و درآنجا در پاسخ به حضور غذا در مجرا، سروتونین ترشح میکنند. این امر به رودهها قابلیت انقباض بخشیده است که ماحصل آن مدیریت غذا در رودههاست. سروتونین مازاد توسط پلاکتهای موجود در شبکه مویرگهای اطراف و احاطهکننده رودهها جذب میگردد. اگر مادهای ناخوشآیند در غدا موجود باشد، انتروکرومافینها مقادیر بیشتری سروتونین ترشح میکنند تا به رودهها تحرک بیشتری ببخشند، و به این ترتیب با ایجاد اسهال رودهها را از مواد مضر خالی کنند. اگر سرعت ترشح سروتونین بالاتر از سرعت جذب آن توسط پلاکتهای خون باشد، سطح سروتونین آزاد در خون بالا میرود. این امر موجب فعال شدن گیرندههای 5HT3 در پیاز مغز شده که فرمان به استفراغ میدهند. سلولهای انتروکرومافین نه فقط نسبت به غذای مسموم، بلکه نسبت به پرتودرمانی و شیمیدرمانی هم واکنش نشان میدهند. داروهایی که موجب مسدود شدن 5HT3 بشوند، بسیار در کنترل تهوع و استفراغ ناشی از شیمیدرمانی علیه سرطانها مؤثرند و جزئی از استانداردهای اصلی استفاده از آنها پذیرفته شدهاند.
میزان غذایی که جانداران بهدست میآورند تنها به فاکتور فراوانی غذا بستگی ندارد، بلکه به توان جاندار در رقابت با دیگران نیز وابسته است. این حقیقت به ویژه در جانورانی که دارای نوع زندگی گروهی میباشند، صدق میکند، جایی که اعضای قویتر ممکن است، دست به سرقت جانداران ضعیفتر بزنند. (این به این معنی نیست که جانداران ضد اجتماعی که نیازهای دیگر همگونانشان مورد توجهشان نیست، غذای یکدیگر را نمیدزدند). سروتونین فقط عاملی دخیل در ادراک نسبت به فراوانی غذا نیست، بلکه با فاکتور مرتبه اجتماعی نیز مرتبط است.
هنگامی که به یک لابستر سروتونین تزریق شود، رفتارهای اجتماعی آلفا (رده مدیریت گروه) از او سر میزند، در حالی که ترشح اکتاپامین، باعث بروز رفتارهای سلطه پذیرانهای از او میشود. یک خارچنگ سراسیمه شده، ممکن است با دمزنی (caridoid escape reaction) از مهلکه بگریزد، و تأثیر سروتونین بر این رفتار عمیقاً به جایگاه اجتماعی او مرتبط است. سروتونین از فرار اعضای تابع (subordinates) گروه از مهلکه جلوگیری کرده، اما در صورتی که این عضو از اعضای غالب یا برعکس، از اعضای مطرود باشد، انگیزهٔ فرار را تشدید میکند. دلیل این واکنش اجتماعی تفاوت نسبت در گیرندههای سروتونین (5HT) است، که تأثیر مستقیم بر پاسخ جنگ و گریز (Fight or Flight response) دارد، تأثیر در گروه سلطه پذیر بیشتر بر گیرندههای 5HT1 است در حالی که در گروه سلطه جوها غلبه با گیرندههای 5HT2 است.
در انسانها سطح فعالیت گیرندههای 5HT1A در مغز ارتباط معکوس با رفتار تهاجمی از خود نشان میدهد، و یک جهش ژنتیک در ژنی که حاوی کد 5HT2A است احتمال خودکشی را در آن ژنوتیپ افزایش میدهد. سروتونین در مغز پس از استفاده معمولاً معدوم نمیشود، بلکه توسط نورونهای سرتونرژیک و توسط گیرندههای سروتونین در پوسته سلول جمعآوری میشود. مطالعات به دست آوردهاند که نزدیک به ده درصد از کل اختلالات در اضطرابهای خلقی مربوطند به این توضیح که کجا، کی و چه تعداد از انتقالدهندههای سروتونین اعزام یا جایگذاری شوند.|
در کرم لولهای سی. الگانس (C. elegans)، تقلیل مصنوعی سروتونین، یا افزایش اکتاپامین اشاره به رفتار عمومی نسبت به کمبود غذا میکند. سی. الگانس بیش از پیش فعال میشود، و جفتگیری و تخمگذاری محدود میشود، در حالی که برعکس این حالت اتفاق میافتد وقتی که سروتونین افزایش یابد، و اکتاپامین کاهش بیابد. سروتونین برای رفتار طبیعی کرم لولهای نر، و تمایلش برای ترک غذا و جستجوی جنس ماده لزوم دارد. سیگنالینگ سروتونرژیک عموماً باعث ایجاد وفقپذیری این کرم با تغییرات سریع در محیطهایی با سیگنالینگهای شبهانسولین، و فاکتورهای رشد بتا میشود، که وفقپذیریهای بلند مدت را کنترل میکنند.
در تحقیقی که در ۱۹۹۹ توسط محقق ایتالیایی marazziti et al صورت پذیرفت. گروهی زن ومرد که در ۶ ماه گذشته عاشق شده بودند، و گروهی دیگر از بیماران مبتلا به بیماری وسواس بیاختیار OCD هر دو گروه بهطور چشمگیری دارای سطح پایینتری از سروتنین نسبت به گروه معیار داشتند. محققان پس از بررسی میزان سروتنین در خون نسبت به بررسی میزان سروتنین در مغز پرداختند، و کاهش سروتنین به همراه افزایش سطح دوپامین و نورآدرنالین را از جمله تغیرات شیمیایی مغز حین ادراک تجربه و احساس عشق در انسان معرفی کردهاند. به گفته دکتر هلن فیشر (Helen fisher)، انسانشناس دانشگاه روتگر نیوجرسی که با گروهی از دانشمندان، طی تحقیقات دامنهداری در دهٔ هشتاد در زمینه عشق و اسکن مغزی عاشقان انجام دادند، مهمترین هدف این تغییرات هورمونی هدایت انسان به سوی انجام وظیفهٔ ژنتیک خود یعنی جفتگیری و تولید مثل است. او از عشق به عنوان دام تولید مثل در انسان یاد میکند. در تحقیق دیگری که به روی موشها انجام شده، ضعف سروتنین موجب تغییر رجحان و تغییر در انتخاب جنسیت جفت اعلام شده است. در مردان، سروتینی که به همراه مواد دیگری در هنگام فرایند انزال در هیپوتالاموس مغز ترشح میشود، به روشنی تأثیر مهارکنندهٔ میل جنسی، پس از پایان عمل جنسی را دارد. به همین ترتیب که داروهای مهارکنندهٔ بازجذبش باعث عوارضی همچون کاهش لیبیدو یا اختلال نعوظ میشوند. در زنان استروژن باعث افزایش تراکم سایتهای ناقل سروتونین در جلو مغز است. اهمیت این عمل استروژن که باعث عملکرد ترانسپورتر سروتونین میباشد، نقشی کلیدی در سیگنالینگ سروتونین در زنان گزارش شده است، که در اختلالات خلقی (حتی در دورهٔ قاعدگی) دخیل است. امروزه ۷٫۱ میلیون آمریکایی از SSRIها برای مقابله با افسردگی، استرس، ماتمزدگی و نامیدی از تراژدی عشق استفاده میکنند، که باعث رفع حالت vegetative و بهبود آسیبهای وارده به هیپوکامپ به دلیل اضطرابهای طولانی مدت میشود. بهطور تخمینی ۷۰٪ از مصرفکنندگان عوارضی را در حوزه اختلالات جنسی تجربه میکنند. اثر این داروها از سوی روانشناسان به صورت «کاهش احساس» بیان شده است.
سروتونین به عنوان عاملی مرتبط با تنظیم عمر، یادگیری، و حافظه شناسایی شده است. شواهد اولیه از مطالعه طول عمر در سی. الگانس به دست آمده. در فاز اولیه گذر عمر، سطح سروتونین افزایش مییابد که طبعات آن افزایش رفتار پرانرژی و تقویت حافظه اجتماعی میباشد. تأثیری که توسط جهشها یا داروها (همچون میانسرین و متیتپین) با محدود کردن گیرندههای سروتونین قابل ترمیم است. مشاهدات در تضاد با این فرضیه که سطح سروتونین به مرور گذران عمر در پستانداران و انسانها پایین میآید نیست، با توجه به اینکه این پایین آمدن سطح در آنان دیرتر اتفاق میافتد.
در موشها و انسانها مشاهده شده که، تغییر در سیگنالینگ و سطوح سروتونین موجب تنظیماتی در توده استخوانی میباشد. موشهایی با فقر سروتنینی در مغز دچار کمتراکمی استخوان (Osteopenia) بودهاند، در حالی که موشهایی با فقر سروتونین در روده دچار تراکم استخوان بالا بودند. در انسانها سطحی بالا از سروتونینِ موجود در خون به عنوان نشانی پیشگویانه از پوکی استخوان یافت شده است. سروتونین همچنین، هرچند در سطوح خیلی پایین، اما دارای قابلیت سنتز شدن در سلولهای استخوانی است؛ و به این شکل تأثیر مثبت خود بر استخوانها را از طریق سه گیرنده مختلف روا میدارد. از طریق گیرندهٔ HTR1B، به صورت منفی بر توده استخوانی تأثیر میگذارد، در حالی که تأثیرات مثبت آن از طریق گیرندههای HTR2B و HTR2C صورت میگیرد. این یک ایجاد تعادل بسیار ظریف بین وظیفهٔ فیزیولوژیک سروتونینِ روده، و آسیبشناسی آن است. بر اساس جزئیات یک تحقیق، افزایش در مقدار سروتونین خارج سلولی باعث مجموعه پیچیدهای از رلههای سیگنالی در استئوبلاستها شده که، Fox1/Creb و ATF4 به اوج میرسد. این مطالعات افق جدیدی از تحقیقات دربارهٔ متابولیسم استخوانی گشودهاند؛ که بهطور بالقوه راههایی برای درمان بیماریهای مربوط به استخوان خواهند بود.
از آنجا که سروتونین، حاوی پیام در دسترس بودن مواد غذایی است، پس حقیقت تأثیرگذاری آن بر رشد اندامها شگفت زدهمان نخواهد کرد؛ مطالعات بسیاری بر انسانها و جانوران نشان میدهد، که تغذیه در سنین پایینتر زندگی میتواند بر دوره بزرگسالی تأثیرگذار باشد، مسائلی همچون فربگی بدن، چربی خون، فشار خون، تصلب شریانها، رفتارها، یادگیری و طول عمر. آزمایشهایی به روی جوندگان عیان میکند، که در معرض مهارکنندههای بازجذب سروتونین (SSRIs) قرار گرفتن در سنین پایین باعث تغییرات پایداری در سیستم انتقال سروتونین در مغز شده که در تغییرات رفتاری حاصل میشوند، و داروهای ضد افسردگی بازگشتهاند. در مقایسه موشها تحت شرایط عادی و موشهای آزمایشگاهی تغییر ژنتیک یافته با ضعف در انتقال دهندههای سروتونین، دانشمندان نشان دادند، که واکنشهای احساسی عادی در بزرگسالی، مانند وقفه پیش از فرار یا تمایل به کشف محیطهای جدید ارتباط مستقیم با انتقال دهندههای فعال سروتونین در دوره نوزادی دارد.
در مگس سرکه، که انسولین هم تنظیمکننده قند خون است، و هم فاکتور رشد، نورونهای سرتونرژیک با تأثیرگذاری بر ترشح انسولین در اندازه بدن تأثیرگذار است. سروتونین همینطور به عنوان فعالکننده رفتار ازدحامی (Swarm Behaviour)، در ملخها هنگام پدیده آفت ملخها (Locust) است. در انسانها اگرچه انسولین تنظیمکننده قند خون و فاکتور رشد شبه انسولین (IGF) تنظیمکننده رشد است، سروتونین کنترلکننده آزاد شدن هر دو هورمون است، پس از آنجا که سروتنین ترشح انسولین از سلولهای بتا در پانکراس را محدود کرده، و مهارکنندههای بازجذب سروتنین باعث کاهش رشد جنینی میشوند. سروتنین انسان همینطور میتواند مستقیماً به عنوان فاکتور رشد عمل کند. آسیب کبدی باعث افزایش بیان ژنی گیرندههای 5HT2A و 5HT2B میشود، سپس سروتونین حاضر در خون باعث تحریک رشد سلولی بری بازسازی آسیب کبدی میگردد. همچنین گیرندههای 5HT2B باعث فعال شدن اساستئوسیت میشوند، که خاصیت استخوانسازی دارد، هرچند که سروتنین همچنین از طریق 5HT1B باعث ایجاد محدودیت برای استئوبلاست میگردد.
سروتین در ادامه، از طریق مکانیسم عامل تحریک و برانگیختگی سنتز نیتریک اکساید درونرگی است، از طریق مکانیسم وساطت گیرنده 5HT1B، فسفورولاسیون P44/P42 میتوژن-اکتیویتید، پروتئین کیناز در کشت میکروسکپی سلولهای آئورت. در خون، سروتنین توسط پلاکتها از پلاسما جذب شده و ذخیره میشود؛ و به مجردی که پلاکت به بافتی صدمه دیده برخورد کند، به عنوان تنگکننده عروق فعال میشود، و همینطور به عنوان فیبروسیت میتوزی (فاکتور رشد) برای کمک به بهبود ناحیه صدمه دیده.
برخی داروهای سرتونرژیک آگونیست، باعث بروز فیبروسیس در هر جایی از بدن میشوند، به ویژه در سندرم فیبروز ریتروپریتونن، و همینطور فیبروز دریچه قلبی. در گذشته سه گروه از داروهای سرتونرژیک بهطور اپیدمیک با این سندرومها مرتبط بودند. آنها داروهای تنگکننده عروق سرتونرژیک ضد میگرن (ergotamine و methaysergide)، داروهای سرتونرژیک مهارکننده اشتها (fenfluramine, chlorphentermine و aminorex) و مخصوصاً آگونیستهای ضد پارکینسون دوپامینرژیک، که گیرندههای 5HT2B را هم تحریک مینمودند بودند، به علاوهٔ perlgolide و cabergoline ونه lisuride. همانند fenfluramine پس از اینکه بسیاری موارد آماری رو به رشد از سندرومهای یادشده در مصرفکنندگان مشاهده شد، بعضی از این داروها از بازار جمعآوری شدند. به عنوان مثال میتوان به pergolide اشاره کرد، که مصرف آن از سال ۲۰۰۳ که در ارتباط با فیبروز قلبی شناخته شد مصرفش بسیار کاهش یافت. دو تحقیق مستقل که در انگلستان منتشر شدند دلالت کردند بر اینکه، این دارو به همراه داروی cabergoline باعث بروز نارسایی دریچه قلب میشوند. در نتیجه سازمان غذا و داروی آمریکا در سال ۲۰۰۷ دستور به جمعآوریشان از بازار داد. از آن رو که cabergoline در آمریکا هرگز برای درمان پارکینسون تأیید نشده بود، به دلیل کاربردش برای درمان Hyperprolactinaemia در بازار باقی ماند، زیرا که دوز مورد مصرف در درمان آن از دوز مورد نیاز در درمان پارکینسون بسیار پایینتر بوده و این، خطر بروز نارسایی قلبی را کاهش میدهد.
از آن رو که سروتنین از شاخصهای انعقاد خون است، افزایش ناگهانی و بسیارش در سطوح محیطی، باعث درد میگردد. دلیل اینکه زنبورهای وحشی و عقربهای دثاستاکر در زهر نیش خود سروتنین دارند، شاید همین عاملیت دردزایی سروتنین برای افزایش درد نیششان در حیوانات بزرگتر باشد. این سروتنین موجود، در هنگام شکار در جانداران کوچکتر به دلیل خاصیت انعقاد خون، باعث مرگ شکار خواهد شد. سروتنین به صورت طبیعی در، سم وزغهای سمی نیز یافت میشود.
در آزمایشگاه کرمهای سی. الگانسی که با تغییرات ژنتیکی دچار ضعف سروتونین شده بودند، از لحاظ تولید مثل، طول عمر بیشتری یافتند، فربه تر شدند، و در بعضی مواقع دورههای از توقیف در مرحله میانآسایی را به نمایش بگذارند.
سروتونین در پستانداران توسط دو نوع مختلف از تریپتوفان هیدروکسیلازها ساخته میشود: TPH1 سروتونین را در غده صنوبری مغز و سلولهای انتروکرومافین تولید شده، و در حالی که TPH2 در هسته رافی و شبکه آورباخ ساخته میشود. موشهای تغییر ژنتیک یافته با فقر TPH1، در همان اعوان دچار ضعف روزافزون قلبی میشوند، پوستی رنگپریده و مشکلات تنفسی دارند، و خیلی زود خسته میشوند، و در انتها به دلیل نارسایی قلبی میمیرند. موشهای تغییر ژنتیک یافته با فقر TPH2 وقتی که متولد میشوند، طبیعی هستند، اما بعد از سه روز به نظر کوچکتر و ضعیف تر هستند، و با پوستی نرمتر از باقی خویشانشان به نظر میرسند.
در انسانها، سیگنالینگ معیوب سروتنین در مغز ممکن است، دلیل اصلی سندرم مرگ ناگهانی در نوزادان (SIDS) باشد. محققان ایتالیایی با بررسی موشی با ژن دستکاری شده با سطوح کمتری از انتقال دهنده عصبی سروتنین، متوجه مشکلات نمونه در تعداد ضربات قلب و دیگر علائم سندرم SIDS انسان، و دیگر گونههای نوزادان جانداران در او شدند. پژوهشگران اینک باور دارند که، سطوح پایینتر از سروتونین در ساقهٔ مغز جانداران، که وظیفهاش کنترل تنفس و ضربان قلب است، باعث این عارضهٔ مرگ ناگهانی است، این نتیجهگیری در سال ۲۰۰۸ شد. اگر نورونهایی که سروتنین میسازند (نورونهای سروتونرژیک) در نوزادان غیرعادی عمل کنند، آنها در خطر سندروم مرگ ناگهانی نوزادان (SIDS) قرار میگیرند.
تحقیقاتی که در دانشگاه راکفلر صورت پذیرفته نشان میدهد، در هر دو گروه، بیمارانی که از افسردگی رنج میبردند و موشهایی با همان گونه از بیماری، سطح پروتئین p11 تنزل کرده است؛ این پروتئین مرتبط با نوروترنسمیترهای سروتونین در مغز است.
این نورترانسمیتر هرچند هورمون نیست، اما بانام هورمون خلقوخو نیز شناخته میشود. در بیشتر افراد، روزهداری و رژیمهای شدید غذایی باعث واکنشهای رفتاری همراه با خشم یا اضطراب میگردد.[9][10][11]
نورونهای موجود در هسته رافی (Raphe Nuclei)، منابع اصلی آزادسازی سروتونین در مغز میباشند. هفت یا هشت هسته رافی وجود دارند، که همه آنها در میان مرکز ساقه مغز و به دور ساخت شبکهای جای گرفتهاند (برخی دانشمندان گروههایی از هستهها را به عنوان یک هسته دستهبندی کردهاند). آکسونهای نورونهای هستههای رافی از سیستم انتقالات عصبی، تقریباً به همه جای سیستم مرکزی عصبی میرسند. آکسونهای این نورونها در قسمتهای پایینی هستههای رافی در مخچه و طناب نخاعی پایان مییابند، در حالی که آکسونهای هستههای رافی بالاتر در کل مغز پخش میشوند.
سروتونین در فضای مابین نورونها آزاد میشود، تا با منتشر شدنش در یک شکاف به نسبت وسیع (بیش از ۲۰ میکرومیلیمتر) گیرندههای 5HT را که در دندریتها، پریکاریونها (سوماً، جسم سلولی نورونها)، ترمینالهای پریسمپاتیک (سیناپسها) نورونهای مجاور را فعال کند.
فرایند سروتونرژیک عمدتاً توسط بازجذب 5HT از سیناپس پایان میپذیرد. این عملیات از طریق یک مونوآمینه انتقال دهندهٔ مشخص، با نام SERT (Serotonin Transporter) روی نورون پاراسمپاتیک صورت میپذیرد. عوامل متعددی توانایی محدود کردن 5HT از بازجذب را دارند، شامل اکستازی (MDMA)، آمفتامین، کوکائین، دکسترومتروفان (نوعی شربت سینه)، ضد افسردگیهای سه حلقهای (Tricyclic Antidepressants)، و محدودکنندههای بازجذب انتخابی سروتونین (SSRIs). تحقیق جالب توجهای که در دانشگاه واشینگتن در سال ۲۰۰۶ انجام شده نوع جدیدی انتقال دهنده مونوآمینه با نام PMAT (Plasma Membrane Monoamine Transporter) را معرفی میکند، که مسئولیت محاسبه درصد قابل ملاحظهای از ترخیص 5HT را دارد. در تضاد با SERT با پیوستگی بالا، PMAT با اینکه به عنوان انتقال دهندهای با پیوستگی پایین شناسایی شده، اما قابلیت حمل مقادیر بیشتری سروتنین را دارد، و راندمانش در سیستمهای بیان همپیوندی (Heterologous Expression Systems) به شدت با SERT قابل مقایسه است.
سروتنین، میتواند از طریق یک فرایند غیرگیرندهای اقدام به سیگنالینگ کند، که این کارکرد سروتونیلاسیون نامیده میشود؛ و طی آن سروتنین پروتئینها را تغییر میدهد. این اتفاق پیش زمینهٔ تأثیر سروتونین بر سلولهای پلاکت شکل (ترومبیسیت) است، که آن هم مرتبط با تغییرات سیگنالی آنزیمی با نام GTPase است، که باعث آزاد شدن محتوای وزیکول از طریق برونرانی (Exocytosis) میشود. تأثیر سروتنین به روی نرمی عروقی در «تونوس ماهیچه اسکلتی» بستگی به سروتونیلاسیون پروتئینهای در ارتباط با دستگاه انقباضی سلولهای ماهیچه دارد.
در جانداران از جمله انسان، سروتنین از آمینواسید ال-تریپتوفان و از طریق مسیر متابولیک شامل آنزیمهای تریپتوفان هیدرولاز (TPH) و آمینواسید دکربوکسیلاز (Aromatic L-amino acid decarboxylase - DDC) سنتز میشود؛ که در این میان نقش عملکرد واکنش TPH به عنوان عامل توقفگاهی برای محدودکننده سرعت در مسیر است. مشخص شده که TPH در دو نوع، نوع TPH1 در بسیاری از بافتها و نوع TPH2 که یک ایزوفرم مخصوص عصبی است وجود دارد.
سروتونین در آزمایشگاه به وسیلهٔ niger Aspergillus و Psilocybe coprophila از تریپتوفان قابل تجزیه است. فاز اول به 5-hydroxytryptophan نیازمند خواباندن تریپتوفان در آب به مدت ۷روز است، سپس ترکیب کردن با HCI یا اسید مناسب دیگری، در حدی که pH آن به ۳ برسد، و سپس اضافه کردن NaOH به شکلی که pH طی مدت یک ساعت به ۱۳ برسد. در این فاز نقش کاتالیست بر عهده قارچ Asperigillus niger است. فاز دوم سنتز خود تریپتوفان از 5-hydroxytryptophan میانجی، به اضافه کردن اتانول و آب و انتظار به مدت ۳۰ روز نیاز دارد. دو مرحله بعدی آن همانند دو مرحله انتهایی در فاز اول است، اضافه کردن HCI و رسیدن به pH ۳، اضافه کردن NaOH و رساندن pH به شیوه بسیار معمولی به ۱۳ در مدت یک ساعت، که کاتالیزور این واکنش هم قارچ coprophila خواهد بود.
سروتنینی که خوراکی مصرف شود، توان رسیدن به مسیرهای سرتونرژیک سیستم مرکزی عصبی را ندارد، زیرا قابل گذر از سد خونی مغز (BBB) نیست. اما تریپتوفان و متابولیت آن یعنی 5HTP که سروتونین از آن سنتز میشود میتوانند و از سد خونی مغز میگذرند. این عوامل در مکملهای غذایی موجودند و میتوانند عوامل سرتونرژیک تأثیرگذاری باشند. یکی از محصولات مشتق سروتنین 5-Hydroxyindoleacetic acid (5-HIAA) است که از ادرار دفع میشود. سروتنین و 5HIAA گاهی به مقادیر شدیداً زیادی در بعضی موارد توسط تومورها و سرطانهای خاصی تولید میشوند و سطح این مواد در ادرار را میتوان برای شناسایی این تومورها مورد آزمایش قرار داد.
ظاهراً کاهش سطح سروتونین مغز از علل اصلی افسردگی است، لذا داروهای ضدافسردگی متعدد بر این اساس ساخته شدهاند مانند: لیگاندهای گیرنده 5HT1، لیگاندهای گیرنده 5HT2، لیگاندهای 5-HT3 گیرنده، 5-HT4 گیرنده، 5-HT5A گیرنده، 5-HT6 گیرنده، 5-HT7 گیرنده، مهارکنندههای بازجذب سروتونین و مهارکنندههای آنزیم MAO (آنزیم تخریبکننده سروتونین در مغز). از معروفترین داروهای افسردگی این گروهها فلوکسیتین، سرترالین، فلووکسامین و سلژلین هستند. چندین رده از داروها و روانگردانها سیستم 5HT را هدف قرار میدهند، شامل بعضی داروهای ضد افسردگی (Antidepressants)، داروهای ضد روانپریشی (Antipsychotics)، داروهای ضد اضطراب (Antianxiety)، داروهای ضد تهوع (Antiemetic)، داروهای ضد میگرن (Antimigraine)، و همچنین روانگردانهایی همچون Empathogen-Entactogen (Psychoactive Drugs) و مواد سایکدلیک (Psychedelic).
مواد سایکدلیک مانند Psilocin، DMT، mescaline، الاسدی، قارچ سایلوسایبین و آگونیستها عمدتاً بر گیرندههای 5HT2A/2C تأثیرگذارند. Empathogen-Entactogen MDMA سروتونین را از وزیکول سیناپس آزاد میکند.
بیماران افسرده، میزان کمتری از متابولیتهای سروتونین در مایع مغزی نخاعی و بافت مغزی دارند. داروهایی که سطح سروتونین را مورد تغییر قرار میدهند، در درمان افسردگی، اختلال اضطراب فراگیر (GAD) و فوبیای اضطراب اجتماعی (SAD) کاربرد دارند. مهارکنندههای مونوآمینه اکسیداز (MAOIs) از تجزیه انتقال دهندههای عصبی مونوآمینه از جمله، سروتونین جلوگیری میکنند، و از این رو باعث تجمع انتقال دهندهها در مغز میگردند. درمان با MAOI مرتبط با بسیاری از اختلالات دارویی است، و این ریسک بیشتر برای بیمارانیست، که همزمان در اثر مصرف غذای حاوی تیرامین بالا در خطر فشار خون بالای اورژانسی قرار میگیرند، یا در اثر اختلال با برخی داروهای خاص دیگر. بعضی از داروها که مهارکننده بازجذب سروتونین هستند، باعث وقفهٔ بیشترش در شکاف سیناپسی میشوند. ضدافسردگیهای سه حلقهای (TCAs) هم بازجذب سروتنین را مهار میکنند، و هم بازجذب نوراپینفرین را. مهارکنندههای جدید بازجذب انتخابی سروتنین (SSRIs) عوارض کمتری دارند، و کمتر در تداخل عملکرد با دیگر داروها قرار میگیرند. کاهش حجم توده استخوانی در سالمندان و خطر بروز استئوپروسیس (پوکی استخوان) از عوارضیست، که بروز آن جدیداً مشاهده شده است، هرچند هنوز به درستی مشخص نیست این عارضه به دلیل تأثیر مهارکنندهها بر تولید سروتونین در سیستم تولید سروتونین جانبی است، یا بر اثر تأثیرش بر روده، یا مغز. داروهای مهارکنندههای مشخصی سطح کمتری از سروتونین را در پی مصرف طولانی مدت، برخلاف سطح بالای سروتونین در ابتدای مصرف نشان دادهاند. این قضیه عطف به معاینات از گروهی انتخابی از بیمارانیست، که مزایای مهارکنندهها برایشان پس از مصرف طولانی مدت کاهش یافته است. این مسئله در بیش از ۷۰٪ از موارد با تعویض دارو حل خواهد شد.
تیانپتین داروی جدید ضدافسردگی، یک «تقویت» کننده بازجذب انتخابی سروتونین است، که دارای اثراتی بر بهبود خلق و خو است. این شاهدی بر این نظریه است، که سروتونین به احتمال بسیار زیاد به جای اینکه طور مستقیم سطوح خلق و خوی را تعیین کند، برای تنظیم میزان یا شدت حالات روحی استفاده میشود. در واقع، کدهای ژن 5HTTLPR برای تعداد انتقال دهندههای سروتونین در مغز، با افزایش مقدار بیشتر آن، باعث کاهش مدت زمان و شدت سیگنالینگ سروتونرژیک میشوند. پلیمورفیسم 5HTTLPR که باعث تشکیل انتقال دهندههای بیشتر سروتونین میشود، دلیل اصلی مقاومت در برابر افسردگی و اضطراب است؛ بنابراین، افزایش سطح سروتونین خارج سلولی ممکن است با افزایش عواطف همراه شود، چه از نوع مثبت و چه از نوع منفی.
اگرچه هراسها (Phobia) و افسردگیها (Depression) ممکن است در اثر تأثیر داروهای تأثیرگذار بر سروتونین تضعیف شوند، اما این، غیر از تغییری در ادراک شان از محیط، به معنی بهبود در وضعیت اشخاص نیست. گاهی سطح پایینی از سروتونین حتی ممکن است مزایایی داشته باشد، برای مثال در بازی اولتیماتوم*، بازیگرانی با سطح عادی از سروتنین بیشتر متمایل به پذیرش پیشنهادهای غیرعادلانه بودند، تا شرکت کنندگانی که سطح سروتنینشان به صورت مصنوعی مورد تنزل قرار گرفته بود. (اولتیماتوم نوعی بازی در رده «اقتصاد تجربی» میان شرکت کنندگان است که به صورت تقسیم هرمی پول میانشان به صورت میپذیرد، بررسی تئوری و کنشهای متقابل در این بازی بسیار مورد توجه روانشناسان، جامعهشناسان و نورواکونومیستها قرار گرفته است)
سطوح به شدت بالای سروتنین میتواند باعث وضعیتی به نام سندروم سروتنین، که بسیار سمی و به صورت بالقوهای مرگبار است شود. در عمل، رسیدن به این چنین سطوحی مسمومیتآور از سروتنین در پی مصرف بیش از حد فقط یک دارو (Overdose) غیرممکن است، اما در پی ترکیب و تداخل چند دارو مانند مهارکنندههای انتخابی بازجذب (SSRIs)، و مهارکنندههای مونوآمینه اکسیدازها (MOAIs) اتفاق میافتد. شدت علائم و نشانههای سندرم سروتونین در طیفی بیش از متفاوت گسترده است، و اشکال خفیفتر آن حتی ممکن است در سطوحی غیررسمی برآورد شوند.
بعضی از آنتاگونیستهای 5-HT3، مانند انداسترون (Ondansetron)، گرانیسترون (Granisetron)، تروپیسترون (Tropisetron) عاملهای ضد تهوع مهم میباشند. آنها مخصوصاً در درمان حالت تهوع و استفراغی که در حین شیمی درمانی ضد سرطان با داروهای سایتوتوکسیک (Cytotoxicity) روی میدهند استفاده میشوند.
سروتنین توسط گونههای متعددی از ارگانیسمهای تک سلولی با اهداف مختلفی استفاده شده است. سمی بودن مهارکنندههای سروتنین برای جلبکها به اثبات رسیده است. آمیب نتاموبیا هیستولیتیکا (E. histolytica) که نوعی انگل گوارشیست، و توانایی ترشح سروتنین دارد، باعث اسهال ترشحی مزمن در بعضی مبتلایان میشود. بیماران آلوده به این انگل گوارشی سطح بالایی از سروتنین پلاسما پیدا میکنند، که پس از رفع عفونت برطرف میشود. آمیب ئی. هیستولیتیکا همچنین در اثر وجود سروتنین بدخیمتر شده است، و این به این معنی است که نتاموبیا نه فقط با ترشح سروتنین که منجر به اسهال میزبان شود به توسعه خود کمک میکند، بلکه از آن برای تنظیم رفتار خود بر اساس حجم جمعیتی، پدیدهای که Quorum sensing (QS) نام دارد نیز استفاده میکنند. بیرون از بدن میزبان، حجم جمعیتی این آمیب و همینطور غلظت سروتنین کم است. سروتنین کم به آمیبها پیام میدهد که آنها بیرون از بدن میزبان هستند و به همین دلیل آنها کمتر آزارگر(virulent) هستند، تا از اتلاف انرژی جلوگیری کنند. آنها وقتی به میزبان جدید وارد شوند، شروع به تقسیم سلولی در رودهها میکنند و با افزایش غلظت سروتنین وارد مرحله آزارگری میشوند.
در دانههایی که در حال خشک شدن، ترشح سروتنین راهی برای خلاص شدن از شر تولید آمونیاک سمی است. آمونیاک در قسمت ایندول ال-تریپتوفان جمعآوری و ذخیره شده، که سپس به وسیله تریپتوفان دیکربوکسلاز کربوکسیل زدایی شده، و سپس توسط سیتوکروم پی۴۵۰ مونوکسیژینایز، هیدروکسیلات شده و سروتونین به دست میدهد. اما، از آنجا که سروتنین وظیفهاش ابزار تنظیمات در دستگاه گوارش است، ممکن است که تولیدش توسط گیاهان و وجودش در میوهها، راهی برای تسریع روند عبور دانههایشان از دستگاه گوارش حیوانات باشد، دقیقاً به همان روشی که بسیاری از دانهها و گیاهان که به عنوان ملین شناخته شدهاند، کارکرد دارند. سروتنین در قارچهایی در سردهٔ (Genus) پانائیلوس (Panaeolus) وجود دارد.
وجود مادهای در خون که رگهای خونی را منقبض میکند، در اواسط قرن پیشین توسط کارل لودویگ پیشنهاد شده بود. دانشمند ایتالیایی به نام ویتوریو ارسپامر در ۱۹۳۵ مادهای را از سلولهای انتروکرومافین جدا کرد که موجب انقباض رودهها میشدند. هرچند که عدهای باور داشتند، که خاصیت این ماده جدید به دلیل حاوی آدرنالین بودن آن است؛ اما ارسپامر دو سال بعد نشان داد که این ماده نوعی آمینهٔ پیشتر ناشناخته است، که او نام آن را اینترامینه نامید.
در سال ۱۹۴۸ موریس راپورت، آردا گرین و ایروین پیج از کلینیک کلیولند ترکیبی با خاصیت منقبضکنندگی رگها در پلاسمای خون یافتند، و از آنجا که این ماده عامل مؤثر در پلاسما (Serum) خون برای ایجاد ضرباهنگ و وضعیت (tone) آوندها بود، نام آن را Serotonin گذاشتند. در ۱۹۵۲ پس از اینکه مشخص شد که، اینترامینه همان سروتنین است، و پس از اینکه طیف گستردهای از دیگر تأثیرات ماده مشخص شد، اصطلاح 5-HT که مخفف نام مناسب شیمیاییاش (5-hydroxytryptamine) بود، برای ذکر در زمینههای داروشناسی مورد ترجیح قرار گرفت. نامهای معادل برای نام این ماده شامل اسامیای همچون 5-hydroxytriptamine, thrombotin, enteramin, substance DS, and ۳-(β-Aminoethyl)-5-hydroxyindole. میباشند. در سال ۱۹۵۳ ایروین پیج و بتی تواروگ سروتنین را در دستگاه مرکزی عصبی نیز کشف کردند.
در دهه پنجاه میلادی، برای اولین بار داروهای مهارکننده بازجذب سروتنین در بیمارستان Munsterlingen در سوئیس در تلاش برای یافت دارویی برای درمان اسکیزوفرنی آزمایش شدند، هر چند که ایدهٔ آنها مبنی بر تلاش برای مهار بازجذب سروتنین تا دهه شصت ارائه نشد، و در طول این دهه تلاشهای جدی برای تولید داروهایی با عوارض کمتری صورت پذیرفت. در سال ۱۹۷۴ نتایج پژوهشهای شرکت الی لیلی و دیوید تی ونگ دربارهٔ دارویی که بعدها فلوکسیتین نام گرفت، در مجله لایف ساینس منتشر، و در سال ۱۹۷۷ به عنوان اولین داروی مهارکننده بازجذب سروتنین برای اخذ مجوز به سازمان غذا و دارو ارائه شد. فلوکسیتین در سال ۸–۱۹۸۷ پس از اخذ مجوز نهایی آن سازمان در سال اول ورود به بازار با نام تجاری پروزاک (لینک ویدئو) به فروش ۳۵۰ میلیون دلاری رسید، هر چند که بعدها آنها اعتراف کردند، که اولین داروی مهارکننده باز جذب سروتنین داروی زیملیدین (Zimelidine) بوده است که به وسیله دانشمند سوئدی آروید کارلسون توسعه یافته، و در سال ۱۹۸۴ به بازار عرضه شده بود. تا سال ۱۹۹۰ این مهارکنندهٔ بازجذب سروتنین تبدیل به عنوان محبوبترین داروهای ضد افسردگی در بین پزشکان و بیماران، با بیش از ششصد و پنجاه هزار نسخهٔ تجویز یا تمدید شده، به رکورد فروش یک میلیارد دلاری دست یافت. در سال ۲۰۰۵ فلوکسیتین، تبدیل به تجویز شدهترین دارو در بازار داروی ایالات متحده شد و در سال ۲۰۱۱ به فروش تقریباً ۱۲ میلیاردی در بازار آمریکا رسید، کما اینکه پیشبینی شده در نبود درمانهای جایگزین، این فروش به بیش از ۱۳ میلیارد دلار در سال ۲۰۱۸ برسد.
علیرغم وجود میلیونها نفر از مصرفکنندگان SSRIها که این داروها را پس از ربعی از قرن استفاده به عنوان منجیان زندگی خود شناخته و سپاس گفتهاند، از همان اعوان انتقادات بسیار گزندهای، چه در زمینههای پزشکی و داروشناسی، و چه در زمینههای دیگر مثلاً از سوی جامعهشناسان از این دارو مطرح شده است. در سال ۱۹۹۳ پیتر دی کرامر در کتاب خود با نام «گوش فرادادن به پروزاک» با مصطلح کردن اصطلاح روان داروشناسی آرایشی (Cosmetic psychopharmacology) نوع نگرش به اختلالات روحی، و دارو درمانی را از منظر دیدگاههای اخلاقی، روانشناسانه، جامعهشناسانه، فلسفی و پزشکی به بوتهٔ نقد گذاشت. امروزه، علیرغم میلیونها نسخهای که حاوی تجویز داروهای مهارکنندههای سروتنین بوده است، و علیرغم تمامی تاییدیهها، هنوز در مورد نحوه عملکرد آنها میان دانشمندان اختلاف نظر وجود دارد؛ زیرا که علیرغم همه پژوهشهای انجام شده، دانش بشر دربارهٔ این هورمون بسیار مهم، تقریباً هنوز در حد هیچ است.
Seamless Wikipedia browsing. On steroids.
Every time you click a link to Wikipedia, Wiktionary or Wikiquote in your browser's search results, it will show the modern Wikiwand interface.
Wikiwand extension is a five stars, simple, with minimum permission required to keep your browsing private, safe and transparent.