Η 1-πενταναμίνη ή 1-αμινοπεντάνιο ή πεντυλαμίνη ή αμυλαμίνη ή μονοπεντυλαμίνη (ΜPeΑ: MonoPentylAmine) ή 1-αζεξάνιο είναι η πρωτοταγής αμίνη με σύντομο συντακτικό τύπο CH3CH2CH2CH2CH2NH2. Χρησιμοποιείται ως διαλύτης, ως μια πρώτη ύλη για την παραγωγή μιας ποικιλίας άλλων χημικών ενώσεων, που περιλαμβάνουν βερνίκια, γαλακτωματοποιητές, φαρμακευτικά προϊόντα[1], καθώς και ως ένα αρωματικό μέσο[2].
Γρήγορες Πληροφορίες Γενικά, Χημικά αναγνωριστικά ...
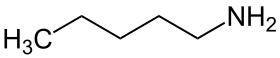
| 1-πενταναμίνη |
 |
| Γενικά |
| Όνομα IUPAC | 1-πενταναμίνη |
| Άλλες ονομασίες | Πεντυλαμίνη
Μονοπεντυλαμίνη
Αμυλαμίνη
1-αμινοπεντάνιο
1-αζεξάνιο |
| Χημικά αναγνωριστικά |
| Χημικός τύπος | C5H13N |
| Μοριακή μάζα | 87,16 amu |
Σύντομος
συντακτικός τύπος | CH3CH2CH2CH2CH2NH2 |
| Συντομογραφίες | BuCH2NH2
MPeA |
| Αριθμός CAS | 110-58-7 |
| SMILES | CCCCCN |
| InChI | 1S/C5H13N/c1-2-3-4-5-6/h2-6H2,1H3 |
| Αριθμός EINECS | 203-780-2 |
| Αριθμός RTECS | SC0300000 |
| Αριθμός UN | 1106 |
| PubChem CID | 8060 |
| ChemSpider ID | 7769 |
| Ισομέρεια |
| Ισομερή θέσης | 17 |
| Φυσικές ιδιότητες |
| Σημείο τήξης | -55 °C |
| Σημείο βρασμού | 94-110 °C |
| Πυκνότητα | 752 kg/m3 |
Διαλυτότητα
στο νερό | Αναμείξιμη |
Δείκτης διάθλασης ,
nD | 1,411 |
| Εμφάνιση | Υγρό |
| Χημικές ιδιότητες |
Ελάχιστη θερμοκρασία
ανάφλεξης | 1 °C |
| Επικινδυνότητα |
|
  |
| Εύφλεκτη (F) και διαβρωτική (C). |
| Φράσεις κινδύνου | R11, R20/21/22, R34 |
| Φράσεις ασφαλείας | S16, S26, S33, S36/37/39, S45 |
| LD50 | 470 mg/kg |
| Εκτός αν σημειώνεται διαφορετικά, τα δεδομένα αφορούν υλικά υπό κανονικές συνθήκες περιβάλλοντος (25°C, 100 kPa). |
Κλείσιμο
Με βάση το χημικό της τύπο, C5H13N, έχει τα ακόλουθα 16 ισομερή θέσης:
- 2-πενταναμίνη ή 1-μεθυλοβουτυλαμίνη, με σύντομο συντακτικό τύπο CH3(CH2)2CH(ΝH2)CH3, σε δύο (2) οπτικά ισομερή.
- 3-πενταναμίνη ή (αιθυλοπροπυλ)αμίνη, με σύντομο συντακτικό τύπο (CH3CH2)2CHΝH2.
- 2-μεθυλο-1-βουταναμίνη ή 2-μεθυλοβουτυλαμίνη, με σύντομο συντακτικό τύπο CH3CH2CH(CH3)CH2ΝH2, σε δύο (2) οπτικά ισομερή.
- 3-μεθυλο-1-βουταναμίνη ή 3-μεθυλοβουτυλαμίνη, με σύντομο συντακτικό τύπο (CH3)2CH(CH2)2ΝH2.
- 2-μεθυλο-2-βουταναμίνη ή (1,1-διμεθυλοπροπυλ)αμίνη, με σύντομο συντακτικό τύπο CH3CH2C(ΝH2)(CH3)2.
- 3-μεθυλο-2-βουταναμίνη ή (1,2-διμεθυλοπροπυλ)αμίνη, με σύντομο συντακτικό τύπο (CH3)2CHCH(CH3)ΝH2, σε δύο (2) οπτικά ισομερή.
- διμεθυλοπροπαναμίνη ή νεοπεντυλαμίνη, με σύντομο συντακτικό τύπο (CH3)3CCH2ΝH2.
- N-μεθυλο-1-βουταναμίνη ή βουτυλομεθυλαμίνη, με σύντομο συντακτικό τύπο CH3(CH2)3ΝHCH3.
- N-μεθυλο-2-βουταναμίνη ή δευτεροταγής βουτυλομεθυλαμίνη, με σύντομο συντακτικό τύπο CH3CH2CH(CH3)ΝHCH3, σε δύο (2) οπτικά ισομερή.
- 2,N-διμεθυλο-1-προπαναμίνη ή ισοβουτυλομεθυλαμίνη, με σύντομο συντακτικό τύπο (CH3)2CHCH2ΝHCH3.
- 2,N-διμεθυλο-2-προπαναμίνη ή μεθυλοτριτοταγής βουτυλαμίνη, (CH3)3CΝHCH3.
- N-αιθυλο-1-προπαναμίνη ή αιθυλοπροπυλαμίνη, με σύντομο συντακτικό τύπο CH3(CH2)2ΝHCH2CH3.
- Ν-αιθυλο-2-προπαναμίνη ή αιθυλισοπροπυλαμίνη, με σύντομο συντακτικό τύπο (CH3)2CHΝHCH2CH3.
- N,N-διμεθυλο-1-προπαναμίνη ή διμεθυλοπροπυλαμίνη, με σύντομο συντακτικό τύπο CH3(CH2)2Ν(CH3)2.
- N,N-διμεθυλο-2-προπαναμίνη ή διμεθυλισοπροπυλαμίνη, με σύντομο συντακτικό τύπο (CH3)2CHΝ(CH3)2.
- Ν-αιθυλο-N-μεθυλαιθαναμίνη ή διαιθυλομεθυλαμίνη, με σύντομο συντακτικό τύπο (CH3CH2)2NCH3.
Η ονομασία «1-πενταναμίνη» προέρχεται από την ονοματολογία κατά IUPAC. Συγκεκριμένα, το πρόθεμα «πεντα-» δηλώνει την παρουσία πέντε (5) ατόμων άνθρακα ανά μόριο της ένωσης, το ενδιάμεσο «-αν-» δείχνει την παρουσία μόνο απλών δεσμών μεταξύ ατόμων άνθρακα στο μόριο και η κατάληξη «-αμίνη» φανερώνει ότι περιέχει μια αμινομάδα ως κύρια χαρακτηριστική ομάδα. Ο αριθμός θέσης «1-» δηλώνει τη θέση του ατόμου άνθρακα με το οποίο ενώνεται η αμινομάδα, ώστε να διαχωρίζονται τα ισομερή θέσης.
Η δομή της μπορεί να βρεθεί αν αντικατασταθεί ένα άτομο υδρογόνου από ένα μόριο αμμωνίας με πεντύλιο.
Περισσότερες πληροφορίες Δεσμός, τύπος δεσμού ...
| Δεσμοί[3] |
| Δεσμός | τύπος δεσμού | ηλεκτρονική δομή | Μήκος δεσμού | Ιονισμός |
| C-H | σ | 2sp3-1s | 109 pm | 3% C- H+ |
| C-C | σ | 2sp3-2sp3 | 154 pm | |
| C-N | σ | 2sp3-2sp3 | 152 pm | 6% C+ Ν- |
| Ν-H | σ | 2sp3-1s | 101,7 pm | 17% N- H+ |
Κατανομή φορτίων
σε ουδέτερο μόριο |
| N | -0,40 |
| C#5 | -0,09 |
| C#2-#4 | -0,06 |
| C#1 | 0,00 |
| H(CH2) | +0,03 |
| H(NH2) | +0,17 |
|
Κλείσιμο
Με 1-πεντανόλη και χλωριούχο αμμώνιο
Η 1-πενταμίνη παράγεται συνήθως με επίδραση χλωριούχου αμμωνίου (NH4Cl) σε 1-πεντανόλη (CH3CH2CH2CH2CH2OH) με την παρουσία τριχλωριούχου σιδήρου ως καταλύτη[4]:
![{\displaystyle \mathrm {CH_{3}CH_{2}CH_{2}CH_{2}CH_{2}OH+NH_{4}Cl{\xrightarrow[{-H_{2}O}]{FeCl_{3}}}CH_{3}CH_{2}CH_{2}CH_{2}CH_{2}NH_{3}Cl{\xrightarrow {NaOH}}CH_{3}CH_{2}CH_{2}CH_{2}CH_{2}NH_{2}+NaCl+H_{2}O} }](//wikimedia.org/api/rest_v1/media/math/render/svg/42767160e1e7e42ead0b02669af61811aff7b529)
- Συμπαρασκευάζονται διπεντυλαμίνη και τριπεντυλαμίνη. Η χημική κινητική καθορίζει την τελική αναλογία αυτών των προϊόντων.
Με χλωριούχο αμμώνιο και πεντανάλη
Με επίδραση χλωριούχου αμμωνίου (NH4Cl) σε πεντανάλη (CH3CH2CH2CH2CHO) παράγεται αρχικά υδροχλωρική 1-πεντανιμίνη (CH3CH2CH2CH2CH=NH2Cl) και έπειτα υδροχλωρική 1-πενταναμίνη. Η τελευταία με υδροξείδιο του νατρίου (NaOH) δείνει καθαρή 1-πενταναμίνη[4]:
![{\displaystyle \mathrm {NH_{4}Cl+CH_{3}CH_{2}CH_{2}CH_{2}CHO{\xrightarrow {}}CH_{3}CH_{2}CH_{2}CH_{2}CH=NH_{2}Cl+H_{2}O{\xrightarrow[{-CH_{3}CH_{2}CH_{2}CH_{2}COOH}]{+CH_{3}CH_{2}CH_{2}CH_{2}CHO}}CH_{3}CH_{2}CH_{2}CH_{2}CH_{2}NH_{3}Cl{\xrightarrow {+NaOH}}CH_{3}CH_{2}CH_{2}CH_{2}CH_{2}NH_{2}+NaCl+H_{2}O} }](//wikimedia.org/api/rest_v1/media/math/render/svg/296b3d4c6b6c16b4113489ed280e6e8cf7e36502)
- Μια παραλλαγή της παραπάνω είναι η επίδραση αμμωνίας σε πεντνάλη, που δίνει 1-πεντανιμίνη, και στη συνέχεια υδρογόνωση της τελευταίας, 1-πενταναμίνη:

Με αμμωνία και πεντυλαλογονίδιο
Με επίδραση αμμωνίας (NH3) σε πεντυλαλογονίδιο (CH3CH2CH2CH2CH2X, μέθοδος Hofmann)[5]:

- Συμπαρασκευάζονται διπεντυλαμίνη και τριπεντυλαμίνη. Η χημική κινητική καθορίζει την τελική αναλογία αυτών των προϊόντων.
Με πεντυλίωση φθαλιμιδικού καλίου
Με πεντυλίωση φθαλιμιδικού καλίου (σύνθεση Gabriel)[6]:
Με αναγωγή αζωτούχων ενώσεων
1. Με αναγωγή 1-νιτροπεντανίου (CH3CH2CH2CH2CH2NO2)[7]:

2. Με αναγωγή πεντανονιτρίλιου (CH3CH2CH2CH2CN)[8]

3. Με αναγωγή 1-πεντανιμίνης (CH3CH2CH2CH2CH=NH)[9]:

Με αποικοδόμηση εξαναμιδίου
Με αποικοδόμηση εξαναμιδίου (CH3CH2CH2CH2CH2CONH2, μετάθεση Hofmann)[10]:

- Το BrOK παράγεται επιτόπου («in citu») με την αντίδραση:

Με χλωραμίνη σε πεντυλομαγνησιοαλογονίδιο
Με επίδραση χλωραμίνης (NH2Cl) σε πεντυλομαγνησιοαλογονίδιο (CH3CH2CH2CH2CH2MgX)[11]:

Με κυκλοπροσθήκη αμμωνίας σε αιθυλοκυκλοπροπάνιο
Με κυκλοπροσθήκη αμμωνίας (NH3) σε αιθυλοκυκλοπροπάνιο , παράγεται 1-πενταναμίνη[12]:


Με κυκλοπροσθήκη αμμωνίας σε μεθυλοκυκλοβουτάνιο
Με κυκλοπροσθήκη αμμωνίας (NH3) σε μεθυλοκυκλοβουτάνιο, παράγεται 1-πενταναμίνη[12]:


Με κυκλοπροσθήκη υδρογόνου αε 2-αιθυλοκυκλοπροπαναμίνη
Με κυκλοπροσθήκη υδρογόνου (H2) σε 2-αιθυλοκυκλοπροπαναμίνη, παράγεται 1-πενταναμίνη[12]:
![{\displaystyle \mathrm {CH_{3}CH_{2}(CH_{2}CH_{2}CH(NH_{2})]+H_{2}{\xrightarrow {Pt}}CH_{3}CH_{2}CH_{2}CH_{2}CH_{2}NH_{2}} }](//wikimedia.org/api/rest_v1/media/math/render/svg/d7f275809ee720e236ebac09bbc6bb01e7776c38)
Με κυκλοπροσθήκη υδρογόνου αε 2-μεθυλοκυκλοβουταναμίνη
Με κυκλοπροσθήκη υδρογόνου (H2) σε 2-μεθυλοκυκλοβουταναμίνη, παράγεται 1-πενταναμίνη[12]:
![{\displaystyle \mathrm {CH_{3}(CH_{2}CH_{2}CH_{2}CH(NH_{2})]+H_{2}{\xrightarrow {Pt}}CH_{3}CH_{2}CH_{2}CH_{2}CH_{2}NH_{2}} }](//wikimedia.org/api/rest_v1/media/math/render/svg/6e9b82ba4d20cd233279f054d2b63313a5e92034)
Με κυκλοπροσθήκη υδρογόνου αε 2-προπυλαζιριδίνη
Με κυκλοπροσθήκη υδρογόνου (H2) σε 2-προπυλαζιριδίνη, παράγεται 1-πενταναμίνη[12]:

Με κυκλοπροσθήκη υδρογόνου αε 2-αιθυλαζετιδίνη
Με κυκλοπροσθήκη υδρογόνου (H2) σε 2-αιθυλαζετιδίνη, παράγεται 1-πενταναμίνη[12]:

Συμπεριφορά βάσης
Παράγει άλατα με οξέα. Π.χ.:

Αλκυλίωση
Αντιδρά με αλκυλαλογονίδια (RX), παράγοντας δευτεροταγείς αμίνες:

Ακυλίωση
Αντιδρά με ακυλαλογονίδια (RCOX), παράγοντας δευτεροταγή αμίδια:

Ιμίνες
Με καρβονυλικές ενώσεις δίνει ιμίνες. Π.χ. με αλδεΰδες (RCHO):

Οξείδωση
Οξείδώνεται με υπεροξείδιο του υδρογόνου (H2O2) παράγοντας 1-νιτροπεντάνιο:

Προσθήκη
1. Προσθήκη σε διπλούς δεσμούς. Π.χ. με αιθένιο δίνει N-αιθυλο-1-πενταναμίνη:

2. Προσθήκη σε τριπλούς δεσμούς.. Π.χ. με αιθίνιο δίνει αρχικά N-πεντυλαιθεναμίνη, και στη συνέχεια την ταυτομερή της N-πεντυλαιθανιμίνη:

3. Προσθήκη σε συζυγείς διπλούς δεσμούς. Π.χ. με 1,3-βουταδιένιο δίνει N-πεντυλο-1-βουτεν-2-αμίνη:

4. Κυκλοπροσθήκη σε ενώσεις με τριμελείς ή τετραμελείς ισοκυκλικούς δακτυλίους. Π.χ. με κυκλοπροπάνιο δίνει Ν-προπυλο-1-πενταναμίνη:


5. Κυκλοπροσθήκη σε ενώσεις με τριμελείς ή τετραμελείς ετεροκυκλικούς δακτυλίους. Π.χ. με εποξυαιθάνιο δίνει 2-πεντυλαμιναιθανόλη[13]:


Παρεμβολή καρβενίων
- Τα καρβένια μπορούν παρεμβληθούν στους δεσμούς C-Η και N-H. Π.χ. με μεθυλένιο έχουμε[14]:

- Η αντίδραση είναι ελάχιστα εκλεκτική και αυτό σημαίνει ότι κατά προσέγγιση έχουμε:
- 1. Παρεμβολή στους τρεις (3) δεσμούς CH2-H. Παράγεται 1-εξαναμίνη.
- 2. Παρεμβολή στους δυο (2) δεσμούς C#1H-H. Παράγεται 2-εξαναμίνη.
- 3. Παρεμβολή στους δυο (2) δεσμούς C#2H-H. Παράγεται 2-μεθυλο-1-πενταναμίνη.
- 4. Παρεμβολή στους δυο (2) δεσμούς C#3H-H. Παράγεται 3-μεθυλο-1-πενταναμίνη.
- 5. Παρεμβολή στους δυο (2) δεσμούς C#4H-H. Παράγεται 4-μεθυλο-1-πενταναμίνη.
- 6. Παρεμβολή στους δυο (2) δεσμούς ΝH-H: 2. Παράγεται N-μεθυλο-1-πενταναμίνη.
Προκύπτει επομένως μίγμα 1-εξαναμίνης ~23%, 2-εξαναμίνης ~15%, 2-μεθυλο-1-πενταναμίνης ~15, 3-μεθυλο-1-πενταναμίνης ~15%%, 4-μεθυλο-1-πενταναμίνης ~15% και Ν-μεθυλο-1-πενταναμίνης ~15%.
Flick, Ernest W. (1998). Industrial Solvents Handbook (5th ed. έκδοση). Park Ridge, NJ: William Andrew. σελ. 695. ISBN 0-8155-1413-1. Τα δεδομένα προέρχονται εν μέρει από το «Table of periodic properties of thw Ellements», Sagrent-Welch Scientidic Company και Ασκήσεις και προβλήματα Οργανικής Χημείας Ν. Α. Πετάση 1982, Σελ. 34. Οι ηλεκτραρνητικότητες κατά Pauling, από τις οποίες υπολογίστηκε ο ιονισμός, προέρχονται από τους πίνακες δεδομένων των χημικών στοιχείων άνθρακας, υδρογόνο, οξυγόνο και άζωτο. Ασκήσεις και προβλήματα Οργανικής Χημείας Ν. Α. Πετάση 1982, σελ.243, §10.2Α.
Ασκήσεις και προβλήματα Οργανικής Χημείας Ν. Α. Πετάση 1982, σελ.243, §10.2Β.
Ασκήσεις και προβλήματα Οργανικής Χημείας Ν. Α. Πετάση 1982, σελ.243, §10.2B2α και σελ. 247, §10.6.4α.
Ασκήσεις και προβλήματα Οργανικής Χημείας Ν. Α. Πετάση 1982, σελ.243, §10.2B2γ.
Ασκήσεις και προβλήματα Οργανικής Χημείας Ν. Α. Πετάση 1982, σελ.243, §10.2B2δ.
Ασκήσεις και προβλήματα Οργανικής Χημείας Ν. Α. Πετάση 1982, σελ.243, §10.2B3.
Ασκήσεις και προβλήματα Οργανικής Χημείας Ν. Α. Πετάση 1982, σελ.243, §10.2Γ3.
Ν. Αλεξάνδρου, Α. Βάρβογλη, Δ. Νικολαΐδη: Χημεία Ετεροχημικών Ενώσεων, Θεσσαλονίκη 1985, §2.1., σελ. 16-17, εφαρμογή γενικής αντίδρασης για Nu = CH3CH2CH2CH2CH2NH.
Ασκήσεις και προβλήματα Οργανικής Χημείας Ν. Α. Πετάση 1982, σελ. 155, §6.7.3.
- SCHAUM'S OUTLINE SERIES, «ΟΡΓΑΝΙΚΗ ΧΗΜΕΙΑ», Μτφ. Α. Βάρβογλη, 1999
- «Ασκήσεις και προβλήματα Οργανικής Χημείας» Ν. Α. Πετάση 1982
- Αναστάσιου Βάρβογλη, «Χημεία Οργανικών Ενώσεων», Παρατηρητής, Θεσσαλονίκη 1991
- Καραγκιοζίδη Σ. Πολυχρόνη, «Ονοματολογία Οργανικών Ενώσεων στα Ελληνικά & Αγγλικά» Β΄ ΈκδοσηΘεσσαλονίκη 1991
- Νικολάου Ε. Αλεξάνδρου, «Γενική Οργανική Χημεία», Εκδόσεις Ζήτη, Θεσσαλονίκη 1985
- Δημητρίου Ν. Νικολαΐδη, «Ειδικά Μαθήματα Οργανικής Χημείας», ΑΠΘ, θεσσαλονίκη 1983
- Νικολάου Ε. Αλεξάνδρου, Αναστάσιου Βάρβογλη, Φαίδωνα Χατζημηχαλάκη, «Εργαστηριακός Οδηγός», Εκδόσεις Ζήτη, Θεσσαλονίκη 1986
- Νικολάου Ε. Αλεξάνδρου, Αναστάσιου Βάρβογλη, Δημητρίου Ν. Νικολαΐδη: «Χημεία Ετεροκυκλικών Ενώσεων», Εκδόσεις Ζήτη, Θεσσαλονίκη 1985



![{\displaystyle \mathrm {CH_{3}CH_{2}CH_{2}CH_{2}CH_{2}OH+NH_{4}Cl{\xrightarrow[{-H_{2}O}]{FeCl_{3}}}CH_{3}CH_{2}CH_{2}CH_{2}CH_{2}NH_{3}Cl{\xrightarrow {NaOH}}CH_{3}CH_{2}CH_{2}CH_{2}CH_{2}NH_{2}+NaCl+H_{2}O} }](http://wikimedia.org/api/rest_v1/media/math/render/svg/42767160e1e7e42ead0b02669af61811aff7b529)
![{\displaystyle \mathrm {NH_{4}Cl+CH_{3}CH_{2}CH_{2}CH_{2}CHO{\xrightarrow {}}CH_{3}CH_{2}CH_{2}CH_{2}CH=NH_{2}Cl+H_{2}O{\xrightarrow[{-CH_{3}CH_{2}CH_{2}CH_{2}COOH}]{+CH_{3}CH_{2}CH_{2}CH_{2}CHO}}CH_{3}CH_{2}CH_{2}CH_{2}CH_{2}NH_{3}Cl{\xrightarrow {+NaOH}}CH_{3}CH_{2}CH_{2}CH_{2}CH_{2}NH_{2}+NaCl+H_{2}O} }](http://wikimedia.org/api/rest_v1/media/math/render/svg/296b3d4c6b6c16b4113489ed280e6e8cf7e36502)



![{\displaystyle \mathrm {+CH_{3}CH_{2}CH_{2}CH_{2}CH_{2}X{\xrightarrow[{+2H_{2}O}]{H^{+}}}CH_{3}CH_{2}CH_{2}CH_{2}CH_{2}NH_{2}+} }](http://wikimedia.org/api/rest_v1/media/math/render/svg/9da814096d3d9315b5552468e2034faeadeba3ab)








![{\displaystyle \mathrm {CH_{3}CH_{2}(CH_{2}CH_{2}CH(NH_{2})]+H_{2}{\xrightarrow {Pt}}CH_{3}CH_{2}CH_{2}CH_{2}CH_{2}NH_{2}} }](http://wikimedia.org/api/rest_v1/media/math/render/svg/d7f275809ee720e236ebac09bbc6bb01e7776c38)
![{\displaystyle \mathrm {CH_{3}(CH_{2}CH_{2}CH_{2}CH(NH_{2})]+H_{2}{\xrightarrow {Pt}}CH_{3}CH_{2}CH_{2}CH_{2}CH_{2}NH_{2}} }](http://wikimedia.org/api/rest_v1/media/math/render/svg/6e9b82ba4d20cd233279f054d2b63313a5e92034)












