Loading AI tools
chemische Verbindung Aus Wikipedia, der freien Enzyklopädie
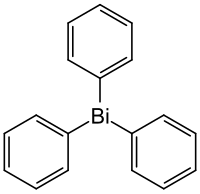
Triphenylbismutan ist eine metallorganische Verbindung des Bismuts, welches als Reagenz in der organischen Synthese angewendet wird. Es ist hinsichtlich der Molmasse die schwerste und letzte bekannte Triphenylverbindung in der Stickstoffgruppe des Periodensystems mit den weiteren Vertretern Triphenylamin, Triphenylphosphin, Triphenylarsin und Triphenylstibin. Bei schwereren Elementen in der Stickstoffgruppe sind mit dem Pentaphenylarsoran, dem Pentaphenylstiboran und dem Pentaphenylbismoran auch fünffach substituierte Vertreter bekannt.[6]
| Strukturformel | |||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
 | |||||||||||||||||||
| Allgemeines | |||||||||||||||||||
| Name | Triphenylbismutan | ||||||||||||||||||
| Andere Namen |
| ||||||||||||||||||
| Summenformel | C18H15Bi | ||||||||||||||||||
| Kurzbeschreibung |
weißer Feststoff[1] | ||||||||||||||||||
| Externe Identifikatoren/Datenbanken | |||||||||||||||||||
| |||||||||||||||||||
| Eigenschaften | |||||||||||||||||||
| Molare Masse | 440,31 g·mol−1 | ||||||||||||||||||
| Aggregatzustand |
fest | ||||||||||||||||||
| Dichte | |||||||||||||||||||
| Schmelzpunkt | |||||||||||||||||||
| Siedepunkt |
242 °C (14 Torr)[2] | ||||||||||||||||||
| Löslichkeit |
| ||||||||||||||||||
| Sicherheitshinweise | |||||||||||||||||||
| |||||||||||||||||||
| Toxikologische Daten | |||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen (0 °C, 1000 hPa). | |||||||||||||||||||
Die Synthese von Triphenylbismutan erfolgt durch die Umsetzung von Bismut(III)-chlorid mit Phenylmagnesiumbromid in einem etherischen Lösungsmittel.[4][7]
Analog gelingt die Synthese auch mit der Verwendung von Phenyllithium.[8]
Triphenylbismutan ist ein weißer kristalliner Feststoff[1], der bei 77,6 °C schmilzt.[4] Wichtige thermodynamische Daten sind:
Triphenylbismutan ist gegenüber dem pyrophoren Trimethylbismutan luftbeständig und hydrolysestabil. Eine Oxidation zur entsprechenden Bismutoxyverbindung Ph3Bi=O erfordert starke Oxidationsmittel wie Kaliumpermanganat oder Wasserstoffperoxid.[6]
Mit Chloriden reagiert es unter Bildung von Diphenylbismutchlorid und Phenylmetallchloriden.[9]
Mit Interhalogenverbindungen oder Halogen-Pseudohalogenverbindungen bildet sich Diphenylbismuthalogenid / -pseudohalogenid.[9]
Eine oxidative Chlorierung mittels Sulfurylchlorid führt zur fünfwertigen Bismutverbindung Triphenylbismutdichlorid. Ein anschließender Halogenaustausch mit einem Grignardreagenz bzw. Phenylmagnesiumhalogenid ergibt das Pentaphenylbismoran[6], welches als violetter Feststoff isoliert werden kann.[10]
Triphenylbismutan und Pentaphenylbismoran ergeben über einen Phenylgruppentransfer das entsprechende Tetraphenylbismutoniumsalz.[10][11]
In der organischen Synthese wird es als Reagenz für Glycolspaltungsreaktionen und zur Phenylierung von Alkoholen und Aminen verwendet. Photochemisch können Phenylradikalreaktionen induziert werden.[4]
Seamless Wikipedia browsing. On steroids.
Every time you click a link to Wikipedia, Wiktionary or Wikiquote in your browser's search results, it will show the modern Wikiwand interface.
Wikiwand extension is a five stars, simple, with minimum permission required to keep your browsing private, safe and transparent.