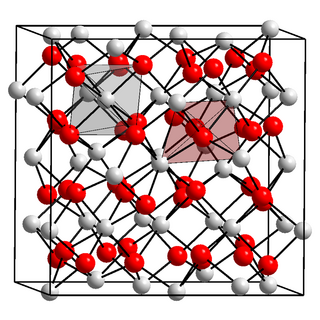
Mangan(III)-oxid
chemische Verbindung Aus Wikipedia, der freien Enzyklopädie
Mangan(III)-oxid ist ein Oxid des Mangans. In der Natur ist Mangan(III)-oxid als seltenes Mineral Bixbyit-(Mn) bekannt.
| Kristallstruktur | ||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
 | ||||||||||||||||
| _ Mn3+ _ O2− | ||||||||||||||||
| Allgemeines | ||||||||||||||||
| Name | Mangan(III)-oxid | |||||||||||||||
| Andere Namen |
| |||||||||||||||
| Verhältnisformel | Mn2O3 | |||||||||||||||
| Kurzbeschreibung |
schwarzer geruchloser Feststoff[1] | |||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||
| ||||||||||||||||
| Eigenschaften | ||||||||||||||||
| Molare Masse | 157,88 g·mol−1 | |||||||||||||||
| Aggregatzustand |
fest[1] | |||||||||||||||
| Dichte |
4,50 g·cm−3[1] | |||||||||||||||
| Schmelzpunkt | ||||||||||||||||
| Löslichkeit |
nahezu unlöslich in Wasser[1] | |||||||||||||||
| Sicherheitshinweise | ||||||||||||||||
| ||||||||||||||||
| MAK |
0,5 mg·m−3[1] | |||||||||||||||
| Toxikologische Daten | ||||||||||||||||
| Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen (0 °C, 1000 hPa). | ||||||||||||||||
Gewinnung und Darstellung
Zusammenfassung
Kontext
Es entsteht zum Beispiel in Zink-Braunstein-Zellen bei deren Entladung:
Mangan(III)-oxid entsteht auch bei der Zersetzung von Mangan(IV)-oxid (MnO2 bei Temperaturen über 535 °C).
Bei der Umsetzung einer Lösung von Mangansulfat-Tetrahydrat mit Wasserstoffperoxid und Ammoniak bei Raumtemperatur erhält man γ-MnO(OH) (Manganit). Aus diesem kann durch vorsichtige Entwässerung im Vakuum bei 250 °C γ-Mangan(III)-oxid erhalten werden.[2]
Eigenschaften
Mangan(III)-oxid ist ein nicht brennbarer schwarzer geruchloser Feststoff, der praktisch unlöslich in Wasser ist. Er zersetzt sich bei Erhitzung über 940 °C.[1] Das in der Natur nicht vorkommende γ-Mn2O3 besitzt eine tetragonale Kristallstruktur mit der Raumgruppe I41/amd (Nr. 141) (a = 577 pm, c = 944 pm).[2][3] Es wandelt sich bei 500 °C in 48 Stunden, bei Raumtemperatur in einem Jahr in die α-Form um. Diese hat bei Temperaturen über 29 °C eine kubische Bixbyit-Struktur mit der Raumgruppe Ia3 (Nr. 206) und darunter eine orthorhombische Struktur mit der Raumgruppe Pcab (Nr. 61, Stellung 2).[4][5] Bei höheren Drücken existieren auch noch andere Modifikationen. So besitzt das bei Drücken über 28 GPa synthetisierbare δ-Mn2O3 eine Kristallstruktur vom CaIrO3-Typ mit der Raumgruppe Cmcm (Nr. 63), ε-Mn2O3 eine Kristallstruktur vom Korund-Typ mit der Raumgruppe R3 (Nr. 148) und ζ-Mn2O3 eine verzerrte trikline Doppelperovskit-Struktur mit der Raumgruppe F1 (Nr. 2, Stellung 5)[6][7].
Verwendung
Mangan(III)-oxid wird als Ausgangsstoff zur Herstellung von Lithiummangan(III,IV)-oxid LiMn2O4 (Kathodenmaterial von Lithium-Ionen-Akkus) und als Pigment in Farbstoffen (färbt Glas z. B. braun) verwendet. Das Mischoxid mit Yttrium und Indium ergibt ein brillantes blaues Pigment, das YInMn-Blau. Die allgemeine Formel lautet YIn1-xMnxO3[8] Ist kein Mangan enthalten, ist das Oxid farblos, ist kein Indium enthalten, ist es schwarz.
Einzelnachweise
Wikiwand - on
Seamless Wikipedia browsing. On steroids.