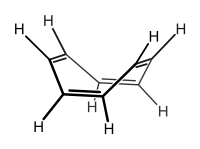
Cyclooctatetraen
ungesättigte cyclische organische Verbindung, Zwischenprodukt Aus Wikipedia, der freien Enzyklopädie
Cyclooctatetraen (COT) ist eine organisch-chemische Verbindung aus der Gruppe der cyclischen Kohlenwasserstoffe. Die Verbindung mit der Summenformel C8H8 besitzt vier konjugierte C=C-Doppelbindungen.
| Strukturformel | ||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
 | ||||||||||||||||
| Allgemeines | ||||||||||||||||
| Name | Cyclooctatetraen | |||||||||||||||
| Andere Namen |
| |||||||||||||||
| Summenformel | C8H8 | |||||||||||||||
| Kurzbeschreibung |
gelbe Flüssigkeit[1] | |||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||
| ||||||||||||||||
| Eigenschaften | ||||||||||||||||
| Molare Masse | 104,15 g·mol−1 | |||||||||||||||
| Aggregatzustand |
flüssig | |||||||||||||||
| Dichte |
0,93 g·cm−3[1] | |||||||||||||||
| Schmelzpunkt | ||||||||||||||||
| Siedepunkt |
142–143 °C[1] | |||||||||||||||
| Dampfdruck | ||||||||||||||||
| Löslichkeit | ||||||||||||||||
| Brechungsindex |
1,5381 (20 °C)[3] | |||||||||||||||
| Sicherheitshinweise | ||||||||||||||||
| ||||||||||||||||
| Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen (0 °C, 1000 hPa). Brechungsindex: Na-D-Linie, 20 °C | ||||||||||||||||
Im Gegensatz zu Benzol (C6H6) zählt COT nicht zu den aromatischen Kohlenwasserstoffen, da es aufgrund der Anzahl seiner π-Elektronen nicht der Hückel-Regel entspricht und auch nicht planar ist, sondern Wannenform aufweist.
Somit ist Cyclooctatetraen weder ein Aromat, noch ein Antiaromat.[4] Durch die fehlende aromatische Stabilisierung ist es eher den gewöhnlichen Polyenen vergleichbar, allerdings aufgrund der durch die Ringspannung verursachten Bindungswinkeldeformation von erhöhter Reaktivität.
Das wannenförmige COT-Molekül kann als Chelatligand – ähnlich wie 1,5-Cyclooctadien (COD) – Metallkomplexe bilden. Durch die Aufnahme von zwei Elektronen, z. B. durch Übertragung von einem Metall, wird aus dem COT das planare, aromatische Cyclooctatetraenyl-Anion C8H82− mit zehn π-Elektronen und erfüllt damit die Hückel-Regel. Ein bekanntes Beispiel für einen Komplex mit planaren Cyclooctatetraenyl-Liganden ist das Uranocen.
Vorkommen
COT wurde in Tabakrauch nachgewiesen.[5]
Darstellung
- COT wurde erstmals 1905 von Richard Willstätter aus Pseudopelletierin synthetisiert.[6]
- Die gängigste Synthese von COT erfolgt nach einem katalytischen Verfahren von Walter Reppe durch Cyclotetramerisierung von Ethin.[7]
Eigenschaften
Durch Erhitzen von Cyclooctatetraen 1 auf 100 °C erhält man ein Gemisch der beiden dimeren C16H16-Verbindungen 2 und 3. Das Dimer 2 (Schmelzpunkt 53 °C) entsteht durch eine Diels-Alder-Reaktion zweier Moleküle Cyclooctatetraen (1). Diese Reaktion ist bei hoher Temperatur teilweise reversibel. In einem zweiten Schritt lagert sich 2 in das Dimer 3 (Schmelzpunkt 76 °C) um.[9]
Aus der pentacyclischen Verbindung 3, die ein Homotropiliden-Strukturelement aufweist, erhält man durch UV-Bestrahlung unter Abspaltung von Benzol 5 den C10H10-Kohlenwasserstoff Bullvalen 4.[10]
Cyclooctatetraen findet Verwendung bei der Synthese von Korksäure und Cyclooctan.[11]
Einzelnachweise
Wikiwand - on
Seamless Wikipedia browsing. On steroids.