Loading AI tools
chemische Verbindung Aus Wikipedia, der freien Enzyklopädie
Vinylchlorid (Chlorethen, auch Monochlorethen oder – eigentlich veraltet – Monochlorethylen), abgekürzt VC, ist ein farbloses, brennbares, narkotisierendes Gas mit in hoher Konzentration leicht süßlichem, chlorartigem Geruch.[2] Es ist die Grundsubstanz zur Herstellung von Polyvinylchlorid (PVC). Vinylchlorid wurde von Henri Victor Regnault entdeckt.
| Strukturformel | ||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
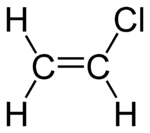 | ||||||||||||||||
| Allgemeines | ||||||||||||||||
| Name | Vinylchlorid | |||||||||||||||
| Andere Namen | ||||||||||||||||
| Summenformel | C2H3Cl | |||||||||||||||
| Kurzbeschreibung |
farb- und geruchsloses Gas[2] | |||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||
| ||||||||||||||||
| Eigenschaften | ||||||||||||||||
| Molare Masse | 62,5 g·mol−1 | |||||||||||||||
| Aggregatzustand |
gasförmig | |||||||||||||||
| Dichte |
2,86 kg·m−3 (0 °C und 1,013 bar)[2] | |||||||||||||||
| Schmelzpunkt | ||||||||||||||||
| Siedepunkt |
−13,4 °C[2] | |||||||||||||||
| Dampfdruck | ||||||||||||||||
| Löslichkeit |
| |||||||||||||||
| Dipolmoment | ||||||||||||||||
| Brechungsindex |
1,3700 (20 °C)[5] | |||||||||||||||
| Sicherheitshinweise | ||||||||||||||||
| ||||||||||||||||
| MAK | ||||||||||||||||
| Toxikologische Daten | ||||||||||||||||
| Thermodynamische Eigenschaften | ||||||||||||||||
| ΔHf0 | ||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen (0 °C, 1000 hPa). Brechungsindex: Na-D-Linie, 20 °C | ||||||||||||||||
Um 1830 erhielt Henri Victor Regnault Vinylchlorid durch Dehydrohalogenierung von 1,2-Dichlorethan mit alkoholischem Kaliumcarbonat, das auch beim thermischen Cracken derselben Verbindung entsteht (Ernst Biltz, 1902).[10]
Das erste Verfahren zur technischen Herstellung von Vinylchlorid das von der Chemischen Fabrik Griesheim-Elektron entwickelt wurde geht auf eine 1912 patentierte Synthese von Fritz Klatte zurück.[11] Danach wird Acetylen mit Chlorwasserstoff im Rahmen einer Hydrochlorierung bei Temperaturen von 140–200 °C unter Normaldruck an Quecksilber(II)-chlorid-Katalysatoren, welche auf Aktivkohle geträgert sind, umgesetzt.[12]

Die gesamte Reaktion läuft in der Gasphase ab und wird in Rohrbündelreaktoren, welche die exotherme Reaktion (ΔHR= −98,8 kJ·mol−1) mithilfe eines Ölkreislaufes kühlen, durchgeführt.[13] Der Acetylenumsatz ist mit 96–97 % nahezu quantitativ und die Vinylchlorid-Selektivität beträgt 98–99 %. Das Verfahren verläuft im Allgemeinen sehr selektiv und ist apparativ wenig aufwendig.[12]
Die Verwendung von Acetylen als Rohstoff für die industrielle Vinylchlorid-Produktion hat in den letzten Jahrzehnten stark an Bedeutung verloren. Die hohen Selbstkosten des Acetylens im Gegensatz zu preiswerteren und besser verfügbaren Rohstoffen auf Basis petrochemischer Erzeugung, vor allem Ethen, führten dazu, dass bis zur Jahrtausendwende lediglich noch 5 % des Vinylchlorids auf Basis von Acetylen hergestellt wurden.
In den letzten Jahren hat sich die Situation erneut stark verändert. Heute werden wieder nahezu 23 % des Vinylchlorids aus Acetylen hergestellt.[14] Dies lässt sich dadurch erklären, dass vor allem in Regionen, in denen Acetylen als Rohstoff noch preiswert zur Verfügung steht und die Gewinnung ebenfalls billig ablaufen kann, die momentane Vinylchlorid-Synthese auf Basis von Acetylen (häufig auch in gekoppelten Prozessen mit der EDC-Route) erfolgt. Besonders in China und Südafrika – beides Gebiete, die noch über große Kohle- und Steinsalzvorkommen verfügen und geringe Nebenkosten (z. B. Strom) haben – ist dieses Verfahren noch rentabel.[12][15]
Bei der modernen Herstellung von Vinylchlorid wird in einem ersten Schritt aus Ethen und Chlor durch so genannte „Direktchlorierung“ 1,2-Dichlorethan erzeugt.[16]
Weit verbreitet ist auch die Darstellung mittels Oxychlorierung von Ethen mit Chlorwasserstoff und Sauerstoff.[16]
In einem nachgeschalteten Schritt wird das 1,2-Dichlorethan unter Abspaltung von Chlorwasserstoff zu Vinylchlorid umgesetzt.[16][17]
Im Jahr 2010 wurden weltweit ca. 35 Millionen Tonnen an Vinylchlorid verbraucht.
Vinylchlorid ist leicht entflammbar (Zündtemperatur 435 °C). Bei einem Volumenanteil von 3,8 bis 31 Prozent in Luft ist es explosiv. Vinylchlorid kondensiert bei −13,9 °C und erstarrt bei −154 °C.
Vinylchlorid polymerisiert bei Einwirkung von Licht, Luft und Wärme zu Polyvinylchlorid. Die Polymerisationswärme beträgt −71 kJ·mol−1 bzw. −1135 kJ·kg−1.[18]
Verbrennungsprodukte von Vinylchlorid an der Luft sind Kohlendioxid und Chlorwasserstoff, wobei unter Sauerstoffmangel Spuren von Phosgen entstehen können. Bei durch Chlorid sensibilisierten Oxidationsreaktionen können aus Vinylchlorid Monochloracetaldehyd und Kohlenmonoxid entstehen.[10]
Vinylchlorid löst sich fast unbegrenzt in organischen Lösungsmitteln, aber nur wenig in Wasser.
Der Hauptverwendungszweck von Vinylchlorid ist die Herstellung von Polyvinylchlorid (2004 rund 38 Millionen Tonnen).[19] Dies geschieht mittels radikalischer Polymerisation.
Vinylchlorid wird als Zwischenprodukt bei der Herstellung von 1,1,1- und 1,1,2-Trichlorethan eingesetzt.[10]
Früher wurde Vinylchlorid auch unter diversen Namen als Kühlmittel verwendet.[20]
In ihren Air Quality Guidelines for Europe[21] geht die WHO davon aus, dass die in westeuropäischen Ländern generell vorhandene, durchschnittliche Luftkonzentration zwischen 0,1 und 0,5 μg/m3 liegt. In der Nachbarschaft von Vinylchlorid- und Polyvinylchlorid-Anlagen können die 24-Stunden-Konzentrationen 100 μg/m3 überschreiten. In Entfernungen von über einem Kilometer zur Anlage liegen sie üblicherweise unter 10 μg/m3. VC zersetzt sich an der Luft und hat eine Halbwertszeit von 20 Stunden. Die WHO geht davon aus, dass bei einer lebenslangen Exposition mit 1 μg/m3 das Krebsrisiko bei 1 zu 1 Million liegt.
1974 lag in der Bundesrepublik Deutschland die Emission von Vinylchlorid bei der Herstellung von PVC zwischen 15 und 55 kg pro Tonne produziertem PVC, konnte aber bereits zwei Jahre später auf Werte zwischen 8 und 20 kg pro Tonne produziertem PVC gesenkt werden.[22]
Bei einem Chemieunfall in Bitterfeld kam es am 11. Juli 1968 im Elektrochemischen Kombinat Bitterfeld bei der PVC-Produktion zu einem Entweichen von Vinylchlorid, das in der Folge eine Explosion auslöste, bei der 42 Menschen starben und über 270 verletzt wurden.
Am 3. Februar 2023 entgleisten beim Eisenbahnunfall von East Palestine mehrere Waggons mit Gefahrgütern, darunter Vinylchlorid. Ein Teil der Chemikalien entzündete sich und explodierte, der andere Teil wurde kontrolliert abgebrannt. Anwohner berichteten von Umweltbelastungen und Vergiftungserscheinungen.[23] Auch ein Fischsterben der örtlichen Gewässer wurde berichtet. Dabei ist noch unklar, welche der Chemikalien dies verursacht haben.[24][25][26]
Vinylchlorid wurde lange Zeit lediglich als betäubend und augenreizend eingestuft. Die toxischen Eigenschaften für den Menschen wurden erstmals in den 1960er Jahren erkannt. Erst Anfang der 1970er Jahre wurde das klinische Bild der Vinylchlorid-Krankheit erkannt. Leber, Speiseröhre und Milz sowie die Durchblutung der Hand, die Handknochen und die Haut sind hiervon betroffen.
Exposition mit Vinylchlorid ist ätiopathogenetisch als Ursache der idiopathischen Akroosteolyse (Black-Nail-Syndrom) und des Raynaud-Syndroms beschrieben worden.
Hans Popper (1903–1988) machte die wichtige Beobachtung, dass die berufliche Exposition gegenüber Vinylchlorid hepatotoxisch ist und häufig zum Auftreten eines hepatischen Angiosarkoms führt.[27] Es wurde als krebserzeugend eingestuft und kann beispielsweise Hämangioendothelsarkome der Leber verursachen.[28]
Die Grenzwerte für die maximale Vinylchlorid-Konzentration am Arbeitsplatz wurden laufend herabgesetzt: 1966 betrug der MAK-Wert 500 ppm, 1971 100 ppm und 1974 50 ppm. Wegen der inzwischen erwiesenen Karzinogenität kann heute kein MAK-Grenzwert festgelegt werden.
Bei der Handhabung sind als Schutzmaßnahmen Atemschutz und Vollschutz notwendig. Die Lagerung erfolgt in Druckdosen und -zylindern.
Bei der Exposition mit Vinylchlorid können Thiodiglycolsäure und Carbocystein als Metaboliten im Urin nachgewiesen werden.[29][30]
Der verbindliche Arbeitsplatzgrenzwert für Vinylchlorid in der Europäischen Union ist 3 ppm bzw. 7,77 mg·m−3 (Richtlinie 2004/37/EG).[2][31] Der Arbeitsplatzgrenzwert nach TRGS 900 liegt momentan in Deutschland für Vinylchlorid bei 1 ppm (2,6 mg/m³).[32] Vinylchlorid ist als krebserzeugend der Kategorie K1 (Stoffe, die beim Menschen bekanntermaßen krebserzeugend wirken) eingestuft.
Seamless Wikipedia browsing. On steroids.
Every time you click a link to Wikipedia, Wiktionary or Wikiquote in your browser's search results, it will show the modern Wikiwand interface.
Wikiwand extension is a five stars, simple, with minimum permission required to keep your browsing private, safe and transparent.