Loading AI tools
Organische Stoffgruppe Aus Wikipedia, der freien Enzyklopädie
Sulfinsäuren sind eine Klasse von chemischen Verbindungen mit organisch gebundenem Schwefel und Sauerstoff der allgemeinen Struktur R–S(=O)–OH, dabei ist R ein Alkyl- oder Arylrest. Die Grundsubstanz Sulfinsäure besitzt die Struktur H–S(=O)–OH und ist tautomer zur Sulfoxylsäure.[1] Die Salze der Sulfinsäuren sind die Sulfinate.
| Sulfinsäure und Sulfinate |
|---|
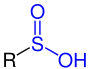 Sulfinsäure |
 Sulfinate |
| R ist eine Organylgruppe. Die funktionelle Gruppe ist blau markiert. |
Sulfinsäuren, die als Zwischenstufe bei der Oxidation von Thiolen auftreten, können nicht isoliert werden. Zugänglich sind Sulfinsäuren durch
Grignard-Reaktion, in der ein metallorganisches Reagenz mit Schwefeldioxid reagiert
oder durch Reduktion von Sulfonylchloriden mittels Zinkstaub.[2]
Sulfinsäureester lassen sich gut herstellen durch Reaktion von Disulfiden mit N-Bromsuccinimid in Gegenwart des esterbildenden Alkohols. Die Reaktion mit primären Alkoholen gelingt gut, bei sekundären Alkoholen wirkt sich ein Zusatz einer kleinen Menge an Kaliumcarbonat günstig aus. Dichlormethan kann als Cosolvens dienen. Alkohole, die mit dem Halogenierungsmittel direkt reagieren, sind für diese Methode ungeeignet.[3] Die benötigten symmetrischen Disulfide lassen sich bequem durch oxidative Kupplung von Thiolen mit Luftsauerstoff herstellen.[4]
Die niedermolekularen Vertreter sind viskose Öle, die höheren Homologen sind kristalline Stoffe, die meisten sind gut wasserlöslich. Viele Sulfinsäuren sind instabil. Alle Sulfinsäuren werden von Luftsauerstoff zu Sulfonsäuren oxidiert. Auch unter Luftausschluss disproportionieren sie allmählich.[5]
Sulfinsäuren sind mittelstarke Säuren (pKS ≈ 2–3[2]) und bilden stabile Salze, die Sulfinsäuresalze.[6] Weitere stabile Derivate sind beispielsweise die als cyclische Ester aufzufassenden Sultine.
Eine Behandlung mit Reduktionsmitteln wie nascierendem Wasserstoff – etwa aus Zink und Salzsäure – führt zu Thiolen:[2]
Mit Halogenalkanen reagieren die Sulfinsäuresalze zu Sulfonen:[7]
Bei der Reaktion mit Thionylchlorid entstehen aus Sulfinsäuren die Sulfinsäurehalogenide (Sulfinylhalogenide); diese sehr reaktiven Substanzen können – z. B. durch Einwirkung von Triethylamin – zu ketenanalogen Sulfinen (nach IUPAC Thioaldehydoxide und Thioketonoxide) umgesetzt werden:[6]
Reaktive Aromaten lassen sich nach Art der Friedel-Crafts-Reaktion sulfinylieren. Sulfinsäurester sind geeignet, die empfindlicheren Sulfinylchloride in der Friedel-Crafts-Sulfinylierung zu ersetzen. Die Reaktion vollzieht sich unter milden Bedingungen.[8]
Seamless Wikipedia browsing. On steroids.
Every time you click a link to Wikipedia, Wiktionary or Wikiquote in your browser's search results, it will show the modern Wikiwand interface.
Wikiwand extension is a five stars, simple, with minimum permission required to keep your browsing private, safe and transparent.